一测多评法同时测定降脂减肥保健品中儿茶素类活性成分的含量Δ
2017-07-25谢静韦杰周璐炜何金莲王乾龙杜蕾蕾成都医学院药学院成都60083中国科学院成都生物研究所湖州生物资源利用与开发创新中心浙江湖州33000成都中医药大学药学院成都637
谢静,韦杰,周璐炜,何金莲,王乾龙,杜蕾蕾(.成都医学院药学院,成都60083;.中国科学院成都生物研究所湖州生物资源利用与开发创新中心,浙江湖州33000;3.成都中医药大学药学院,成都637)
·药物分析与检定·
一测多评法同时测定降脂减肥保健品中儿茶素类活性成分的含量Δ
谢静1*,韦杰1,周璐炜1,何金莲1,王乾龙2,杜蕾蕾3#(1.成都医学院药学院,成都610083;2.中国科学院成都生物研究所湖州生物资源利用与开发创新中心,浙江湖州313000;3.成都中医药大学药学院,成都611137)
目的:建立同时测定减肥降脂保健品中儿茶素类活性成分含量的方法。方法:采用高效液相色谱法,以表没食子基儿茶素没食子酸酯(EGCG)为内标,计算其与没食子儿茶素(EGC)、儿茶素(C)、表儿茶素(EC)、没食子基儿茶素没食子酸酯(GCG)和没食子酰表儿茶素(ECG)的相对校正因子(RCF),通过RCF计算样品中EGC、C、EC、GCG、ECG的含量,以外标法测定的EGC、C、EC、GCG和ECG含量作实测值;采用向量夹角余弦法评估实测值与计算值之间的相似性。结果:EGC、C、EC、EGCG、GCG、ECG检测质量浓度线性范围分别为0.006 5~0.130 5mg/m L(r=0.999 8)、0.000 5~0.010 7mg/m L(r=0.999 7)、0.002 0~0.040 0 mg/m L(r=0.999 9)、0.015 3~0.305 3mg/m L(r=0.999 8)、0.000 8~0.015 5mg/m L(r=0.999 8)、0.004 0~0.079 2mg/m L(r=0.999 9);精密度、稳定性、重复性试验的RSD<2.0%;加样回收率分别为95.07%~100.35%(RSD=1.94%,n=6)、95.24%~101.87%(RSD=2.79%,n=6)、96.08%~103.86%(RSD=3.01%,n=6)、97.51%~101.06%(RSD=1.45%,n=6)、96.01%~101.66%(RSD=2.27%,n=6)、96.20%~102.89%(RSD=2.71%,n=6)。实测值与计算值差异无统计学意义(P>0.05)。结论:该方法操作简便,精密度、稳定性、重复性好,可用于减肥降脂保健品中儿茶素类活性成分的含量测定。
减肥;保健品;儿茶素;一测多评法;高效液相色谱法
以儿茶素成分为主的茶多酚提取物对人体健康有积极影响[1],尤其是其具有降糖降脂等多种活性,常作为降脂减肥的功能原料用于保健品中[2]。目前,对含茶多酚保健品的质控方法仍以比色法测定为主[3]。虽然有较多文献报道用高效液相色谱法(HPLC)外标法测定药材及其制剂中儿茶素成分的含量[4-5],但由于儿茶素类多为成对光学异构体,纯化困难,价格较昂贵,从而导致文献所报道的外标法在生产和检验实际工作中应用有限。近年来提出的一测多评法可克服此不足[6]。一测多评法通过测定1个成分(对照品供应充足、易得者)与其他组分(对照品难供应、昂贵者)之间的相对校正因子(RCF),而实现多个成分的同时测定。一测多评法已收录入2015年版《中国药典》并应用于多种药材中有效成分的定量分析[7],本研究即基于一测多评建立的技术指南[8],建立了以表没食子基儿茶素没食子酸酯(Epigallocatechin gallate,EGCG)为内标,同时测定含表没食子儿茶素(Epigallocatechin,EGC)、儿茶素(Catechin,C)、表儿茶素(Epicatechin,EC)、没食子基儿茶素没食子酸酯(Gallocatechin gallate,GCG)、没食子酰表儿茶素(Epicatechin gallate,ECG)含量的一测多评法,用于保健品中6种儿茶素成分的质量评价与控制。
1 材料
1.1 仪器
LC-2010型HPLC仪,含LC-20AD二元高压泵、DGU-20A3R自动脱气机、SIL-20A自动进样器、MSDM 20A二极管阵列检测器(日本Shimadzu公司);KH5200B型超声波清洗器(昆山禾创超声仪器有限公司,功率:200W,频率:40 kHz);GA110型电子分析天平(美国Ohaus公司)。
1.2 药品与试剂
某减肥胶囊(A公司,批号:150921,规格:0.30 g/粒,无茶多酚标示量);某减肥胶囊(B公司,批号:612165005,规格:0.45 g/粒,茶多酚标示量:14.1%);某减肥胶囊(C公司,批号:20160407,规格:0.40 g/粒,茶多酚标示量:3.67%);某减肥茶(D公司,批号:150502,规格:2 g/袋,茶多酚标示量:5.0%);某左旋多酚片(E公司,批号:151001,规格:0.80 g/片,茶多酚标示量:4.04%),上述5批样品编号为S1~S5;EGC对照品(批号:PS14110601)、C对照品(批号:PS15042901)、EGCG对照品(批号:PS15042701)、EC对照品(批号:PS15050901)、GCG对照品(批号:PS14102902)、ECG对照品(批号:PS1410202)均购自成都普思生物科技股份有限公司,纯度均>98.5%;乙腈为色谱纯,其余试剂均为分析纯,水为纯化水。
2 方法与结果
2.1 基本原理
化合物的量与其检测器响应值在一定线性范围内成正比(f=A/C)。在多成分同时分析时,通过选取其中一种成分为内标物,建立该成分与其他成分之间的RCF(fkm):
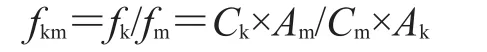
其中,Ck、Cm分别为内标物、待测物的浓度,Ak、Am分别为内标物、待测物的检测器响应值。通过RCF,计算出样品中其他待测成分的含量:

2.2 色谱条件与系统适用性试验
色谱柱:Wonda CractODS-2(250mm×4.6mm,5 μm);流动相:0.5%乙酸溶液(A)-乙腈(B),梯度洗脱(0~40m in,10%→30%B);流速:1.0m L/m in;检测波长:280 nm;柱温:35℃;进样量:10μL。在上述色谱条件下,理论板数以EGCG峰计不少于10 000;各成分基线分离良好,分离度>1.5,详见图1。
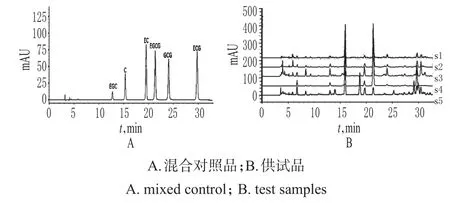
图1 高效液相色谱图Fig 1 HPLC chromatogram s
2.3 溶液的制备
2.3.1 对照品溶液分别取待测成分对照品各适量,加50%甲醇溶液制成EGC、C、EC、EGCG、GCG、ECG质量浓度分别为6.2、5.1、9.5、5.8、4.9、4.7mg/m L的单一对照品溶液。
2.3.2 供试品溶液取样品(胶囊取内容物、片剂粉碎、袋泡茶直接取样)200mg,精密称定,置于50m L量瓶中,加50%甲醇溶液45m L,超声提取15m in,静置至室温,加50%甲醇溶液定容,经0.45μm微孔滤膜滤过,取续滤液,即得。
2.4 线性关系考察
将“2.3.1”项下EGC、C、EC、EGCG、GCG、ECG对照品溶液以10∶1∶2∶25∶1.5∶8(V/V/V/V/V/V)的比例混合,得工作溶液Ⅰ(EGC、C、EC、EGCG、GCG、ECG质量浓度分别为0.130 5、0.010 7、0.040 0、0.305 3、0.015 5、0.079 2mg/m L),加50%甲醇溶液逐级稀释得工作溶液Ⅱ~Ⅴ。精密量取上述工作溶液Ⅰ~Ⅴ各10μL,按“2.2”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,μg/m L)为横坐标、峰面积(y)为纵坐标进行线性回归,得回归方程与线性范围,详见表1。

表1 回归方程与线性范围Tab 1 Regression equationsand linear ranges
2.5 精密度试验
取“2.3.2”项下供试品溶液(编号:S2)适量,按“2.2”项下色谱条件连续进样测定6次,记录峰面积。结果,EGC、C、EC、EGCG、GCG和ECG峰面积的RSD分别为0.55%、0.76%、0.47%、0.39%、0.51%、0.36%(n=6),表明方法精密度良好。
2.6 稳定性试验
取“2.3.2”项下供试品溶液(编号:S2)适量,分别于室温下放置0、4、8、12、16 h时按“2.2”项下色谱条件进样测定,记录峰面积。结果,EGC、C、EC、EGCG、GCG和ECG峰面积的RSD分别为1.02%、0.87%、1.15%、1.33%、0.79%、1.26%(n=5),表明供试品溶液室温放置16 h内基本稳定。
2.7 重复性试验
精密称取同一批样品(编号:S2)适量,按“2.3.2”项下方法制备供试品溶液,共6份,再按“2.2”项下色谱条件进样测定,记录峰面积。结果,EGC、C、EC、EGCG、GCG和ECG峰面积的RSD分别为1.83%、1.45%、1.92%、1.76%、2.06%、1.13%(n=6),表明本方法重复性良好。
2.8 加样回收率试验
取已知含量样品(编号:S2)适量,共6份,分别加入一定质量的待测成分对照品,按“2.3.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
2.9 RCF的计算
以EGCG为内标,按“2.1”项下公式计算,结合“2.4”项下系列混合对照品溶液所得峰面积数据,计算EGCG对EGC、C、EC、GCG和ECG的RCF。结果,EGCG对EGC、C、EC、GCG和ECG的RCF分别为0.54、0.35、0.41、0.89、0.60。
2.10 一测多评法的系统应用性考察
2.10.1 不同流速考察精密量取“2.4”项下工作溶液Ⅰ适量,分别考察0.8、1.0、1.3m L/m in的流速对RCF的影响,结果,EGCG对EGC、C、EC、GCG和ECG RCF的RSD分别为1.63%、1.39%、2.11%、2.53%、1.96%(n=3),表明流速对RCF无显著影响。
2.10.2 不同柱温考察精密量取“2.4”项下工作溶液Ⅰ适量,分别考察柱温为25、35、40℃对RCF的影响。结果,EGCG对EGC、C、EC、GCG和ECG RCF的RSD分别为1.05%、1.21%、1.73%、2.06%、1.64%(n=3),表明柱温对RCF无显著影响。
2.10.3 不同进样量考察精密量取“2.4”项下工作溶液Ⅰ5、10、20μL,考察不同进样量对RCF的影响。结果,EGCG对EGC、C、EC、GCG和ECG RCF的RSD分别为1.21%、1.29%、1.43%、1.81%、1.67%(n=3),表明进样量对RCF无显著影响。
2.11 样品含量测定

表2 加样回收率试验结果(n=6)Tab 2 Resultsof recovery tests(n=6)
取5批样品各适量,分别按“2.3.2”项下方法制备供试品溶液,再按“2.2”项下色谱条件进样测定,记录峰面积并计算样品含量,计算EGC、C、EC、GCG和ECG的实测值和计算值之间的夹角余弦值[9],结果见表3(表中ES为实测值,QAMS为计算值,Cir为夹角余弦值)。结果表明,两种方法所得含量差异无统计学意义(P>0.05)。
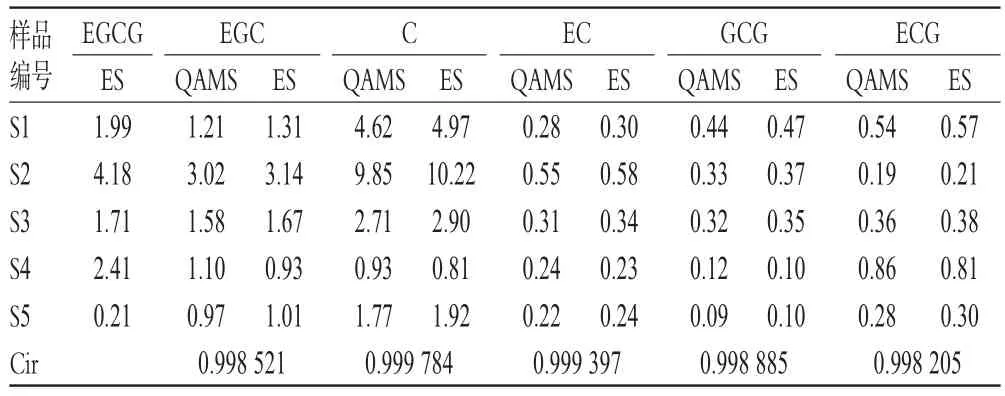
表3 样品含量测定结果(n=3,%)Tab 3 Results of contents determ ination of sam p les(n=3,%)
3 讨论
本研究针对添加茶多酚的降脂减肥保健品中的儿茶素类成分进行定量分析,对一测多评法的技术适用性和实践可行性进行了充分的探讨。结果表明,一测多评法计算出的结果与常规外标法测得的结果之间具有较高的相似度,表明一测多评法可实现以较易获得的、便宜的EGCG为内标,通过确定RCF计算其余5种儿茶素的含量,实现多指标质量评价;而且一测多评法具有实验室间差别小的特点,方法成功建立后,可以在不同部门、不同单位之间直接使用,适合于药品生产企业及监管部门等的大批量常规检测。
[1]赵振军,刘宗岸,仓梅琴,等.茶多酚及儿茶素对人体健康的影响[J].福建茶叶,2006,39(1):38-41.
[2]李学鸣,孟宪军,彭杰.茶多酚降低小鼠营养性肥胖的效果[J].沈阳农业大学学报,2009,40(5):612-614.
[3]丁友昌.分光光度法测定茶多酚保健品中茶多酚[J].中国公共卫生,1998,14(9):573-575.
[4]袁和军,邱明丰.茶多酚检测方法综述[J].北方药学,2013,10(11):11-13.
[5]刘振,余梦瑶,胡丹,等.好易升颗粒剂的含量测定及稳定性研究[J].华西药学杂志,2016,31(4):422-425.
[6]左岚,孟胜男.一测多评法在中药药物分析中的应用进展[J].中国药房,2016,27(18):2589-2591.
[7]徐彦,刘圆,吕露阳,等.一测多评法测定卷叶贝母中生物碱类成分含量[J].天然产物研究与开发,2012,24(11):1513-1515.
[8]王智民,钱忠直,张启伟,等.一测多评法建立的技术指南[J].中国中药杂志,2011,36(6):657-659.
[9]王龙星,肖红斌,梁鑫淼,等.一种评价中药色谱指纹谱相似性的新方法:向量夹角法[J].药学学报,2002,37(9):713-715.
ContentsDeterm ination of Catechins Active Components in Lipid-lowering Slimm ing Health Productsby Quantitative AnalysisofMulti-Componentsvia Single Marker
XIE Jing1,WEI Jie1,ZHOU Luwei1,HE Jinlian1,WANG Q ianlong2,DU Leilei3(1.College of Pharmacy,Chengdu Medical College,Chengdu 610083,China;2.Huzhou Center for Biological Resources Utilization and Innovation,Chengdu Institute of Biology,Chinese Academy of Sciences,Zhejiang Huzhou 313000,China;3.College of Pharmacy,Chengdu University of TCM,Chengdu 611137,China)
OBJECTIVE:To establish the method for contents determ ination of catechins active components in lipid-lowering slimm ing health products.METHODS:HPLC method was adopted.Using epigallocatechin gallate(EGCG)as a reference,relative correction factor(RCF)of EGCG to gallocatechin(EGC),catechin(C),epicatechin(EC),gallocatechin gallate(GCG)and galloylepicatechin(ECG)were calculated.The contents of EGC,C,EC,GCG and ECG in 5 batches of samples were calculated through RCF.The contents of EGC,C,EC,GCG and ECG determ ined by external standard method were used asmeasured value. The sim ilarity of the value determ ined by external standard method w ith the value calculated by quantitative analysis ofmulti-components via single marker method(QAMS)was evaluated w ith vector included angle cosinemethod.RESULTS:The linear ranges of EGCG,EGC,C,EC,GCG and ECG were 0.006 5-0.130 5 mg/m L(r=0.999 8)、0.000 5-0.010 7 mg/m L(r=0.999 7)、0.002 0-0.040 0 mg/m L(r=0.999 9)、0.015 3-0.305 3 mg/m L(r=0.999 8)、0.000 8-0.015 5 mg/m L(r=0.999 8)、0.004 0-0.079 2 mg/m L(r=0.999 9);RSDs of precision,stability and reproducibility testswere all lower than 2.0%.The recoverieswere 95.07%-100.35%(RSD=1.94%,n=6)、95.24%-101.87%(RSD=2.79%,n=6)、96.08%-103.86%(RSD=3.01%,n=6)、97.51%-101.06%(RSD=1.45%,n=6)、96.01%-101.66%(RSD=2.27%,n=6)、96.20%-102.89%(RSD=2.71%,n=6),respectively.There was no significant difference between measured value and calculated value.CONCLUSIONS:The method is simple,precise,stable and reproducible,and can be used for contents determ ination of catechinsactive components in lipid-lowering slimm ing health products.
Sli mm ing;Health products;Catechins;Quantitative analysis ofmulti-components via singlemarkermethod;HPLC
R 917
A
1001-0408(2017)18-2529-04
2016-07-23
2016-10-08)
(编辑:张静)
国家自然科学基金资助项目(No.81503361);四川省教育厅科研计划项目(No.16ZA0299)
*讲师。研究方向:天然产物活性成分。电话:028-62308658。E-mail:aggie-xj@163.com
#通信作者:讲师。研究方向:天然药物质量标准。电话:028-85224504。E-mail:934534055@qq.com
DOI10.6039/j.issn.1001-0408.2017.18.23
