pH及共存金属离子对生物质炭吸附铅稳定性的影响①
2017-07-21刘荣琴钱林波晏井春胡钦红陈梦舫
刘荣琴,钱林波,晏井春,韩 璐,胡钦红,陈梦舫*
pH及共存金属离子对生物质炭吸附铅稳定性的影响①
刘荣琴1, 2,钱林波2,晏井春2,韩 璐2,胡钦红1*,陈梦舫2*
(1 中国地质大学(武汉)环境学院,武汉 430074;2 中国科学院土壤环境与污染修复重点实验室(南京土壤研究所),南京 210008)
生物质炭对重金属吸附性能的稳定性是评价生物质炭修复效果的重要指标。本文研究了不同pH、金属离子Cd和Al存在下,Pb在不同炭化温度(100℃、400℃、700℃)生物质炭上的脱附性能及脱附过程。结果表明,pH越低,Pb的脱附率越大。其主要是由于H+的竞争效应,以及生物质炭表面官能团的质子化,促进了Pb的重新活化。在Cd和Al共存时,Pb的脱附率进一步增加。当pH = 3.5时,Cd和Al的存在分别使Pb从CM100、CM400和ZKZ700上的脱附率提高了13.9%、1.0%、3.4% 和26.8%、13.0%、11.3%。这主要归因于多金属的水解使得更多的H+得以释放,进而促进了Pb的脱附。Pb在生物质炭上的脱附率随脱附时间的延长而不断增加,反应前4 h,脱附率迅速增加并均已达最大脱附率的70%,4 h后脱附速率减慢。Pb的脱附动力学符合伪一级动力学模型及颗粒内扩散模型(前4 h)。当Cd和Al存在时,解吸液对Cd、Al易解吸态的优先脱附降低了Pb的脱附速率并延长了其脱附所达平衡的时间。
生物质炭;吸附稳定性;pH;共存离子
生物质炭(Biochar)是生物质(木材、枯枝落叶、秸秆、家畜粪便等)在缺氧或无氧条件下低温(<700℃)裂解制备而成的富碳固体[1–3]。因其具有孔隙结构发达、比表面积大、官能团及矿物组分丰富等独特的物理化学性质,而表现出高效的吸附性能,在污染土壤修复中具有巨大的潜力,被认为是一种新型的环境修复材料[4–7]。
随着我国工业化的快速发展,重金属铅(Pb)已逐渐成为威胁人类健康的一大重要因素。土壤中的Pb主要通过食物链或直接通过人的口部摄入和皮肤接触等途径进入人体。人体中过量的Pb可影响神经、造血、消化、泌尿、生殖和发育、心血管、内分泌、免疫、骨骼等系统和器官。由于儿童自身的行为特点和生理特征,Pb对儿童的危害更是高于成人。我国儿童受Pb的暴露概率平均为33.8%[8],远高于美国及其他发达国家。因此,开展土壤Pb污染治理和修复工作是一项十分紧迫而艰巨的任务。近年来很多学者研究发现生物质炭能够有效吸附土壤中的Pb,降低其在土壤中的活性和生物有效性。目前生物质炭对Pb的吸附机理主要包括:①与含氧官能团发生离子交换或络合作用[9–10];②与无机组分发生沉淀作用[11–12];③C=C的π键作用[13–14]。此外,牛粪生物质炭中含磷矿物对Pb的去除起到了至关重要的作用[15–16]。
然而生物质炭对Pb的吸附,主要是将Pb以更稳定的形式存在于土壤中,降低其在土壤中的移动性,却无法把Pb从土壤中彻底去除。因此生物质炭吸附Pb的长期稳定性是应用于Pb污染土壤修复的关键。目前对生物质炭的研究大多仍集中在吸附效果和初步的吸附机理方面,对于其吸附Pb的稳定性研究较少。现实环境中土壤Pb污染常伴有一种或多种金属的存在[17],例如在有色金属的冶炼过程中出现的Pb、Cd复合污染,该共存离子会影响生物质炭与Pb的结合能力[18];此外受金属污染的土壤大多呈酸性,酸性环境又会进一步促进有毒金属的活化,如当土壤的pH<5.5时,大量铝离子(Al)开始分解释放[19],因而酸性环境以及共存离子均会影响生物质炭对Pb的固持效果。
因此本文选择不同炭化温度的生物质炭,通过批量脱附试验探讨不同pH、共存金属离子Cd和Al对生物质炭吸附Pb稳定性的影响以及Pb在生物质炭上的脱附过程,为准确评估生物质炭修复重金属污染土壤时重金属的迁移转化行为提供理论依据,为利用生物质炭钝化重金属离子实现土壤污染缓解提供技术支撑。
1 材料与方法
1.1 供试材料
供试材料选择了具有代表性的12种实验室生物质炭以及12种商业生物质炭。通过对这24种不同类型生物质炭的预实验,最终选定2种实验室生物质炭和1种商业生物质炭。其中实验室生物质炭为牛粪生物质炭,原料选自安徽安庆[20],取回后经烘干和粉碎装入棕色瓶中备用。商业生物质炭为毛竹生物质炭(ZKZ700),制备温度700℃,购自浙江泽可生物科技有限公司。3种生物质炭的相关性质见表1。
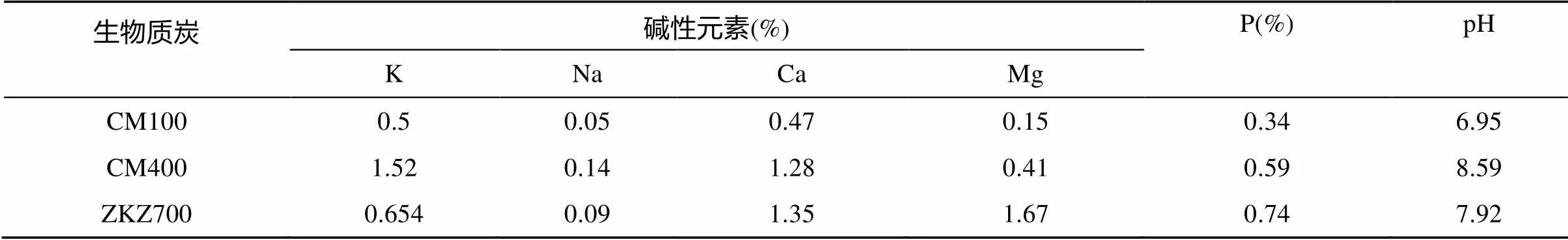
表1 生物质炭的相关性质
1.2 生物质炭的制备
实验室生物质炭的制备采用限氧裂解法[21]。将晒干后的牛粪用自来水清洗2遍,去除表面粉尘,后放入烘箱中烘干。之后用粉碎机粉碎,并研磨过100目筛。过筛得到的牛粪生物质装于棕色瓶中,贴好标签待用。称取过筛后的生物质颗粒于250 ml坩埚中,压实(约100 g),盖上盖子,放置于马弗炉中以5℃/min的升温速率置于一定温度(100℃、400℃),保持热解温度6 h。炭化样品待冷却至室温后取出,用研钵磨细过100目筛,得到牛粪生物质炭样品,置于棕色瓶中备用,分别标记为CM100、CM400(CM代表牛粪,其后数字代表炭化温度)。
将制备好的生物质炭按原吸附实验的固液比 (8 mg/40 ml)批量制取被重金属吸附的生物质炭,以备用于重金属的脱附研究。具体方法如下:取1 g生物质炭于5 L烧杯中,加入5 L PbCl2初始浓度为100 μmol/L的CaCl2背景溶液(CaCl2浓度0.5 mmol/L,模拟土壤离子环境)。调节溶液初始pH为4.0(防止Pb的氢氧化物沉淀)。固液混合后,机械搅拌24 h(我们的吸附动力学实验表明,反应已在24 h时达到了平衡),抽滤,烘干并研磨,获得被单金属Pb吸附的生物质炭,置于10 ml玻璃管中备用,并依次标记为CM100、CM400和ZKZ700。制备Pb-Cd及Pb-Al共吸附的生物质炭方法与单金属Pb方法相同,生物质炭吸附PbCl2与CdCl2的共存溶液(浓度均为100 μmol/L),吸附后的生物质炭标记为CM100-Cd、CM400-Cd及ZKZ700-Cd;生物质炭吸附PbCl2与AlCl3的共存溶液(浓度均为100 μmol/L),最终的生物质炭标记为CM100-Al、CM400-Al及ZKZ700-Al。
1.3 脱附批实验
脱附率大小用于表征生物质炭对Pb吸附稳定性的强弱,脱附率越大说明在对应环境条件下易脱附态Pb的比重越大,即Pb的吸附稳定性越差;脱附率越小说明在对应环境条件下不易脱附态Pb的比重越大,即Pb的吸附稳定性越强。因此通过脱附实验对生物质炭吸附稳定性进行研究。脱附实验采用批处理方法,包括Pb单金属体系和Pb-Cd、Pb-Al共存体系中,pH对金属脱附的影响实验和脱附动力学实验。试剂添加量均为2 mg生物质炭/40 ml解吸液。解吸液采用浓度比为3︰2的H2SO4、HNO3配制的模拟酸雨溶液[22]。在pH影响实验中,共设pH为3.5、4.0、4.5、5.0及5.5的5组点。将试剂按比例混合后加入50 ml聚乙烯离心管中,在(25±0.5)℃、150 r/min条件下振荡24 h(脱附24 h达平衡)。取10 ml上清液,过0.45 μm水相滤膜,取一定量滤液用0.2% 盐酸稀释,用原子吸收光谱仪测定金属离子浓度。脱附动力学实验步骤同pH影响实验,以生物质炭脱附效果明显的解吸液做脱附动力学分析。实验拟定的动力学取样时间点为0、1、2、4、8、12、24 h。脱附实验设置仅加解吸液样品的对照空白,以扣除解吸液溶出的影响,每组处理设2个平行,取平均值进行分析。
1.4 数据计算与分析
1) 数据计算重金属在生物质炭上的脱附量(D)可用差减法计算,脱附率 (d,%) 为脱附量与吸附量的比值,计算公式如下:
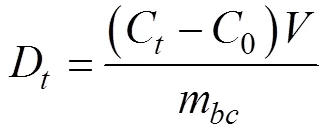
(2)
式中:D为时刻重金属的脱附量(mg/g);0为未添加生物质炭时解吸液中重金属的浓度(mg/L);C为时刻溶液中重金属的浓度(mg/L);为解吸液体积(L);m为不同炭化温度生物质炭的质量(g);d为时刻金属的脱附率(%);为生物质炭对重金属的最大吸附量(mg/g)。
2) 数据分析用伪一级动力学、伪二级动力学及颗粒内扩散模型对动力学数据进行拟合分析,从而对其脱附机理进行阐述。
伪一级动力学:
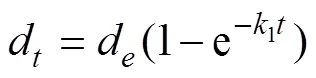
伪二级动力学:
(4)
颗粒内扩散模型:
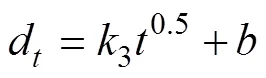
式中:d与d分别是时刻及平衡时刻重金属的脱附率;1与2分别是伪一级、伪二级动力学速率常数(h–1),3为扩散速率常数(h–0.5);为颗粒内扩散模型方程的直线截距。
伪一级动力学方程引入平衡脱附量,适合描述以快速脱附为主导、慢速脱附极弱的理想表面单分子层脱附过程;伪二级动力学模型包含了脱附的所有过程,如液膜扩散、颗粒内扩散和表面吸附等,用于描述吸附质的吸附能力与吸附位点有关的脱附过程;颗粒内扩散模型考虑了分子扩散和相分配等因素,适合描述吸附质在颗粒内的扩散过程,是最常见的表征吸附过程与机制的模型[23]。
2 结果与讨论
2.1 pH对生物质炭吸附Pb稳定性的影响
2.1.1 pH对Pb脱附的影响 Pb在生物质炭上的脱附率与pH之间的关系见图1。如图1A所示,当溶液pH为5.5和5.0时,CM100、CM400、ZKZ700均未发现Pb的脱附;而当pH减小到4.5时,CM100和CM400开始出现Pb的脱附,脱附率分别为6.5%、3.9%;当pH为4.0时,脱附率进一步增加,Pb在CM100、CM400和ZKZ700上的脱附率分别为30.2%、18.1% 和17.5%;而当pH减小到3.5时,各生物质炭上Pb的脱附率达最大,分别为51.2%、45.3% 和37.4%。在相同pH条件下,Pb在不同炭化温度生物质炭上的脱附能力也存在明显的差异,如在平衡时Pb的脱附率大小顺序为CM100 > CM400 > ZKZ700,这可能与生物质炭的孔隙发育有关。生物质炭具有多孔性特征,且随着炭化温度的升高其孔隙不断发育。在低温阶段(<100℃),各孔基本未通;继续升温至400℃生物质炭热解成片状堆叠,开始形成微孔;最后到700℃时,微孔进一步增加[24]。吸附于生物质炭表面孔隙上的Pb易被解吸,而吸附于内部孔隙上的Pb更稳定,不易被解吸[25]。此外,生物质炭表面的有机组分和无机矿物组分与Pb的结合力不同,也会影响Pb的脱附过程[26–27]。Pb在生物质炭上的脱附率随pH的减小而增大的主要原因可能有以下两个方面:①在较强的酸性条件下,H+对Pb的竞争效应增强,Pb与生物质炭表面活性位点的亲和力被改变,导致Pb与生物质炭之间的吸附平衡被破坏;②对于生物质炭来说,在较低的pH条件下其表面的官能团被质子化[28–30],可供Pb吸附的活性位点减少,而当溶液pH升高时,官能团被质子化的作用减弱,Pb与生物质炭的静电斥力也随之减小。此外,在低pH条件下,生物质炭对溶液pH的缓冲性能减弱(图1B),较酸的溶液体系会促使Pb的脱附。孙良臣等[31]在研究改性碳黑对Cu2+和Cd2+的吸附稳定性时,也发现pH影响较大,重金属在吸附剂上的脱附率会随pH的增大而迅速减小。因此,当生物质炭应用于Pb污染土壤修复时,环境酸性越强易解吸态的Pb比重越大,生物质炭对Pb吸附性能稳定性越差。
2.1.2 Cd/Al存在时pH对Pb脱附的影响 在Cd/Al存在的条件下,生物质炭上Pb的脱附与pH之间的关系见图2。如图2A所示,当pH为5.5、5.0时,与单金属Pb体系相同,CM100-Cd、CM400-Cd和ZKZ700- Cd均未发现Pb的脱附;当pH减小到4.5时,CM100- Cd和CM400-Cd开始出现Pb的脱附,且Pb的脱附率较单金属Pb体系有少量增加;在pH为4.0时,Pb的脱附率进一步增加,发生在CM400-Cd和ZKZ700- Cd上的脱附率较单金属Pb体系分别增加了1.3% 和3.6%;而当pH为3.5时,Pb的脱附率则显著增加,尤其是在CM100-Cd和ZKZ700-Cd上,Pb的脱附率较单金属Pb体系分别提高了13.9% 和3.4%。可见Cd的存在促进了Pb的脱附。在相同pH条件下,各生物质炭上Pb的脱附受Cd存在的影响程度也存在差异,CM100受影响最大,ZKZ700其次,CM400最弱。Cd的存在促进Pb脱附的主要原因可能有两方面:①在双金属体系中,两种金属的水解会释放出更多的H+(图2B),图1A结果表明溶液pH越低,Pb的脱附越明显;②金属的相互作用促进了Pb的脱附,因为物理化学性质相似的重金属作用方式和途径相似,在生物质炭表面结合位点的竞争会影响金属共存时的相互作用。Xu等[32]和Qian等[33]在研究生物质炭对重金属的去除时发现各重金属之间存在着竞争作用,该作用改变了生物质炭对目标污染物的吸附特性。
与Cd相比,Al的存在使Pb的脱附更明显,生物质炭对Pb的吸附稳定性更差(图2C)。当pH为5.5时,依旧未发现Pb的脱附;当pH减小到5.0时,CM100-Al上出现少量Pb的脱附;在pH减小到4.5时,Pb的脱附率较单金属体系迅速增加,在CM100- Al、CM400-Al和ZKZ700-Al上,Pb的脱附率分别增加了13.1%、7.2% 和6.7%;在pH为4.0时,Pb的脱附率进一步增加,发生在CM100-Al、CM400-Al和ZKZ700-Al上的脱附率分别较单金属Pb体系增加了13.5%、11.3% 和9.0%;而当pH为3.5时,各生物质炭上Pb的脱附率增加到最大,分别较单金属Pb体系增加了26.8%、13.0% 和11.3%。在相同pH条件下,各生物质炭上Pb的脱附受Al存在的影响程度不同,其中CM100受影响最大,CM400其次,ZKZ700最弱。Al较Cd对Pb脱附有更强的促进作用,主要有两方面原因:①生物质炭对Al的亲和力较Cd强(在初始pH均为4.0时,CM100、CM400和ZKZ700对Al的最大吸附量分别为12.00、39.00、14.53 mg/g,而对Cd的最大吸附量为0、3.82、6.35 mg/g),说明Al较Cd有更强的竞争吸附能力,对生物质炭吸附Pb也会产生更强的抑制作用;②Al的致酸效应,对比图2B与2D,Al的存在降低了溶液体系中的pH,进一步促进了Pb的脱附。
2.1.3 pH对Cd/Al脱附的影响 为进一步探讨共存离子Cd/Al对Pb脱附的影响,研究了Pb-Cd和Pb-Al金属共存体系中,Cd和Al的脱附情况。Cd的脱附与pH之间的关系见图3A,发现仅CM400-Cd存在Cd的脱附,与Pb的脱附现象相似,pH越小,Cd的脱附越多。在Pb-Cd共存体系中,解吸液对吸附于CM400-Cd上易解吸态Cd的脱附一定程度上缓解了多金属水解过程中释放的H+对Pb的竞争强度,进一步解释了在Pb-Cd共存体系中,CM400较其他两种生物质炭表现出对Pb更稳定的吸附性能。
Al的脱附情况与pH之间的关系见图3B。pH对Al脱附影响的整体趋势与Pb相同。当溶液pH为5.5和5.0时,CM100-Al、CM400-Al、ZKZ700-Al均未出现脱附;当pH减小到4.5时,开始出现脱附,脱附率分别为6.4%、8.5% 和6.6%;当pH减小到4.0时,脱附率进一步增加,其脱附率分别为19.4%、18.9% 和22.6%;而在pH为3.5时,各生物质炭上Al的脱附率达最大,分别为35.5%、28.1% 和65.6%。数据表明,在相同pH条件下,ZKZ700-Al上Al的脱附最显著,说明解吸液对吸附于ZKZ700上易解吸态Al的脱附更大程度上缓解了金属共存体系中H+对Pb的竞争强度,也进一步印证了当Al存在时,ZKZ700上Pb的脱附受影响程度最小。
2.2 Pb的脱附动力学
2.2.1 Pb的脱附动力学 以脱附现象最明显的解吸液(pH = 3.5)作Pb脱附动力学研究。Pb的脱附动力学见图4。如图4A所示,Pb的脱附率随脱附时间的延长而不断增加,且随着时间的延长溶液反应后的pH不断增大(图4B)。Pb从生物质炭上脱附的整个过程可分为快速反应和慢速反应两个阶段。在脱附开始的4 h内,脱附率迅速增加,CM100、CM400和ZKZ700对Pb的脱附率已分别达各自最大脱附率的93.7%、77.9%和100%;4 h后,脱附率缓慢增加,逐渐达到脱附平衡,各生物质炭在平衡时的脱附率分别为83.6%、67.5% 和57.2%。脱附动力学曲线的快速反应阶段对应于静电吸附态Pb的脱附,慢速反应阶段主要对应于专性吸附态Pb的脱附[34]。对比3种生物质炭上Pb的脱附速率,Pb在ZKZ700上脱附最快,CM100其次,CM400最慢。
Pb在生物质炭上的脱附过程可通过伪一级、伪二级动力学及颗粒内扩散模型进行拟合,用相关系数2作为综合判断的指标,拟合参数列于表2。如表2所示,伪一级动力学模型拟合最好,其绝对系数2最高,且与实测数据点符合程度最好,说明Pb的脱附属于单层快速脱附。从表2可知,不同生物质炭的1值存在明显的差异,表明不同炭化温度的生物质炭上Pb的脱附速率不同。根据伪一级动力学拟合结果,Pb的脱附速率顺序为ZKZ700(2.24 h–1)> CM100(1.81 h–1)> CM400(0.53 h–1);脱附达平衡时,CM100、CM400和ZKZ700上Pb的脱附率分别为77.74%,66.34% 和57.37%。颗粒内扩散模型能较好地拟合Pb在0 ~ 4 h的脱附情况,证明了颗粒扩散对Pb的脱附起着至关重要的作用。截距可表示生物质炭边界层厚度,值越大则说明边界层对脱附的影响越大[35–36]。
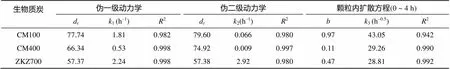
表2 脱附Pb的伪一级、伪二级和颗粒内扩散动力学模型拟合参数
2.2.2 Cd/Al存在时Pb的脱附动力学 在Cd/Al存在的条件下,Pb的脱附动力学见图5。如图5A所示,当Cd存在时,反应1 h,Pb在CM100-Cd和ZKZ700-Cd上的脱附率较单一Pb金属体系分别减少了13.9% 和5.4%,表明Cd的存在降低了Pb的脱附速率。可能原因是在反应初始阶段,解吸液对Cd的优先脱附降低了Pb的脱附速率。而CM400-Cd对Pb的脱附率则有所增大,反应1 h,Pb的脱附率较单一Pb金属体系增加了3.0%。
Al的存在降低了Pb的脱附速率(图5C),并延长了脱附所达平衡的时间。反应1 h,CM100-Al、CM400-Al和ZKZ700-Al对Pb的脱附率较单一Pb金属体系减少了21.0%、3.6% 和8.5%;随后的23 h,Pb的脱附率不断增加,且在24 h脱附率仍保持上升趋势,说明Pb的脱附平衡时间延长。在Pb-Cd和Pb- Al共存体系中,Pb的脱附动力学均不符合伪一级、伪二级动力学及颗粒内扩散模型,说明该体系下Pb脱附的复杂性,以及生物质炭对Pb吸附的不稳定性。
2.2.3 Cd/Al的脱附动力学 Cd和Al在生物质炭上的脱附动力学见图6。如图6A所示,CM400-Cd上Cd的脱附速率较Pb低,反应1 h,Cd的脱附率仅达最大脱附率的21.5%(Pb为44.2%)。解吸液会首先脱附生物质炭作用力较弱的组分,因此共吸附于生物质炭表面的Cd与Pb组分会相互竞争,Cd的脱附速率进而会影响着Pb的脱附速率,只有当Cd的脱附达到平衡时Pb的脱附才能达到平衡。如图6B所示,Al的脱附较Pb的脱附速率慢且到达平衡所需的时间长。与Cd相同,Al脱附的同时会制约着Pb的脱附。当吸附于生物质炭表面的Al脱附未达到平衡状态时,解吸液仍会对易解吸态Pb进行脱附,进一步解释了Al的存在延长了Pb达脱附平衡的时间。
3 结论
Pb在生物质炭上的脱附率随着pH的减小而逐渐增大,表明当生物质炭应用于重金属污染土壤修复时,各pH条件下H+对重金属的竞争作用程度不同,即各pH条件下可能重新活化的重金属有所差别,因而生物质炭对目标污染物的吸附稳定性强烈受环境pH变化的影响。试验发现在相同pH条件下,炭化温度越高的生物质炭对Pb吸附稳定性越好,Pb在各生物质炭上的脱附率大小顺序为CM100 > CM400 > ZKZ700,这可能与生物质炭的孔隙发育、表面的有机组分和无机矿物组分有关。共存离子Cd/Al会促进Pb的脱附,同时Al的存在对Pb的脱附影响更加明显。
Pb的脱附率随脱附时间的延长而不断增加,且整个脱附过程可分为快速反应和慢速反应两个阶段。反应前4 h,各生物质炭上Pb的脱附率均达最大脱附率的70%。3种生物质炭上Pb的脱附快慢顺序为ZKZ700> CM100> CM400。Pb的脱附行为符合伪一级动力学模型和颗粒内扩散模型(前4 h)。解吸液对Cd、Al易解吸态的优先脱附降低了Pb的脱附速率并延长了其脱附所达平衡的时间。
[1] Liu W J, Jiang H, Yu H Q. Development of biochar-based functional materials: Toward a sustainable platform carbon material[J]. Chemical Reviews, 2015, 115(22): 12251– 12285
[2] Sohi S P, Krull E, Lopez-Capel E, et al. A review of biochar and its use and function in soil[J]. Advances in Agronomy, 2010, 105: 47–82
[3] Chan K Y, Van Zwieten L, Meszaros I, et al. Agronomic values of greenwaste biochar as a soil amendment[J]. Australian Journal of Soil Research, 2007, 45(8): 629–634
[4] Han L, Xue S, Zhao S C, et al. Biochar supported nanoscale iron particles for the efficient removal of methyl orange dye in aqueous solutions[J]. PloS One, 2015, 10(7). DOI: 10.1371/journal.pone.0132067
[5] Moon D H, Park J W, Chang Y Y, et al. Immobilization of lead in contaminated firing range soil using biochar[J]. Environmental Science and Pollution Research, 2013, 20(12): 8464–8471
[6] Tan X F, Liu Y G, Zeng G M, et al. Application of biochar for the removal of pollutants from aqueous solutions[J]. Chemosphere, 2015, 125: 70–85
[7] 谢祖彬, 刘琦, 许燕萍, 等. 生物炭研究进展及其研究方向[J]. 土壤, 2011, 43(6): 857–861
[8] Venegas A, Rigol A, Vidal M. Viability of organic wastes and biochars as amendments for the remediation of heavy metal-contaminated soils[J]. Chemosphere, 2015, 119: 190–198
[9] Lu H L, Zhang W H, Yang Y X, et al. Relative distribution of Pb2+sorption mechanisms by sludge-derived biochar[J]. Water Research, 2012, 46(3): 854–862
[10] Cao X D, Ma L N, Gao B, et al. Dairy-manure derived biochar effectively sorbs lead and atrazine[J]. Environmental Science and Technology, 2009, 43(9): 3285–3291
[11] Mohan D, Pittman C U, Bricka M, et al. Sorption of arsenic, cadmium, and lead by chars produced from fast pyrolysis of wood and bark during bio-oil production[J]. Journal of Colloid and Interface Science, 2007, 310(1): 57–73
[12] Inyang M D, Gao B, Yao Y, et al. Removal of heavy metals from aqueous solution by biochars derived from anaerobically digested biomass[J]. Bioresource Technology, 2012, 110: 50–56
[13] Swiatkowski A, Pakula M, Biniak S, et al. Influence of the surface chemistry of modified activated carbon on its electrochemical behaviour in the presence of lead (II) ions[J]. Carbon, 2004, 42(15): 3057–3069
[14] Uchimiya M, Lima I M, Klasson K T, et al. Immobilization of heavy metal ions (Cu-II, Cd-II, Ni-II, and Pb-II) by broiler litter-derived biochars in water and soil[J]. Journal of Agricultural and Food Chemistry, 2010, 58(9): 5538–5544
[15] Mohan D, Kumar H, Sarswat A, et al. Cadmium and lead remediation using magnetic oak wood and oak bark fast pyrolysis bio-chars[J]. Chemical Engineering Journal, 2014, 236: 513–528
[16] Uchimiya M. Influence of pH, ionic strength, and multidentate ligand on the interaction of Cd-II with biochars[J]. ACS Sustainable Chemical and Engineering, 2014, 2(8): 2019–2027
[17] Teng Y G, Wu J, Lu S J, et al. Soil and soil environmental quality monitoring in China: A review[J]. Environment International, 2014, 69: 77–199
[18] 郑振华, 周培疆, 吴振斌. 复合污染研究的新进展[J]. 应用生态学报, 2001, 12(3): 469–473
[19] Exley C. Reflections upon and recent insight into the mechanism of formation of hydroxyaluminosilicates and the therapeutic potential of silicic acid[J]. Coordination Chemistry Reviews, 2012, 245(1–2): 82–88
[20] Qian L B, Chen B L. Dual role of biochars as adsorbents for aluminum: The effects of oxygen-containing organic components and the scattering of silicate particles[J]. Environment Science and Technology, 2013, 47: 8759–8768
[21] Chen B L, Zhou D D, Zhu L Z. Transitional adsorption and partition of nonpolar and polar aromatic contaminants by biochars of pine needles with different pyrolytic temperature[J]. Environmental Science and Technology, 2008, 42(14): 5137–5143
[22] Cao Y Z, Wang S Y, Zhang G, et al. Chemical characteristics of wet precipitation at an urban site of Guangzhou, South China[J]. Atmospheric Research, 2009, 94(3): 462–469
[23] Foo K Y, Hameed B H. Utilization of oil palm biodiesel solid residue as renewable sources for preparation of granular activated carbon by microwave induced KOH activation[J]. Bioresource Technology, 2013, 130: 696–702
[24] 周丹丹. 生物碳质对有机污染物的吸附作用及机理调控[D]. 杭州: 浙江大学, 2008
[25] 毛世慧, 郭新超, 周岩梅, 等. 四氯联苯在草木灰上的吸附/解吸特征及吸附动力学研究[J]. 环境科学与技术, 2013, 36(6): 42–46
[26] 甘复兴, 汪的华, 邹津耘. 界面缓蚀剂的吸附稳定性[J]. 电化学, 1999, 5(2): 52–41
[27] 孙良臣. 重金属污染土壤原位钝化稳定性研究[D]. 济南: 山东师范大学, 2015
[28] Ofomaja A E, Unuabonah E I, Oladoja N A. Competitive modeling for the biosorptive removal of copper and lead ions from aqueous solution by Mansonia wood sawdust[J]. Bioresource Technology, 2010, 101(11): 3844–3852
[29] Chen Z M, Xiao X, Chen B L, et al. Quantification of chemical states, dissociation constants and contents of oxygen-containing groups on the surface of biochars produced at different temperatures[J]. Environmental Science and Technology, 2015, 49(1): 309–317
[30] Qian L B, Zhang W Y, Yan J C, et al. Effective removal of heavy metal by biochar colloids under different pyrolysis temperatures[J]. Bioresource Technology, 2013, 206: 217–224
[31] 孙良臣, 成杰民. Cu2+和Cd2+在改性纳米碳黑和钠基膨润土上的吸附稳定性及其影响因素[J]. 山东化工, 2015, 44(2): 16–20
[32] Xu X Y, Cao X D, Zhao L. Comparison of rice husk- and dairy manure-derived biochars for simultaneously removing heavy metals from aqueous solutions: Role of mineral components in biochars[J]. Chemosphere, 2013, 92(8): 955–961
[33] Qian L B, Chen M F, Chen B L. Competitive adsorption of cadmium and aluminum onto fresh and oxidized biochars during aging processes[J]. Journal of Soils and Sediments, 2015, 15(5): 1130–1138
[34] 郭观林, 周启星. 重金属镉在黑土和棕壤中的解吸行为比较[J]. 环境科学, 2006, 27(5): 1013–1019
[35] Wang Z Y, Liu G C, Zheng H, et al. Investigating the mechanisms of biochar’s removal of lead from solution[J]. Bioresource Technology, 2015, 177: 308–317
[36] 张默, 贾明云, 卞永荣,等. 不同温度玉米秸秆生物炭对萘的吸附动力学特征与机理[J]. 土壤学报, 2015, 52(5): 1106–1115
Effects of Coexisting Metal Ions and pH on Adsorption Stability of Lead on Biochars
LIU Rongqin1,2, QIAN Linbo2, YAN Jingchun2, HAN Lu2, HU Qinhong1*, CHEN Mengfang2*
(1 School of Environmental Studies, China University of Geosciences, Wuhan 430074, China; 2 Key Laboratory of Soil Environment and Pollution Remediation, Institute of Soil Science, Chinese Academy of Sciences, Nanjing 210008, China)
The stability of adsorbed heavy metals onto biochars is one of the most important factors to evaluate the biochar’s remediation performance. In this study, the effects of pH and coexisting ions Cd/Al on Pb desorption were investigated. It was found that Pb desorption increased with the decrease of pH which was mainly due to the competing effect of H+and the protonation of functional groups which promoted the activation of Pb. However, with the presence of Cd/Al, the desorption efficiencies of Pb were further promoted. At pH 3.5, apromotion effect was observed from the presence of Cd, with Pb desorption efficiencies increasing by 13.9%, 1.0%, 3.4% for CM100, CM400 and ZKZ700, respectively; the increases were even stronger for Al at 26.8%, 13.0% and 11.3%. The more metal hydrolyzed, the more release of H+, which helped to activate more Pb from the surface of biochars. The desorption efficiencies of Pb increased with the increasing contact time. During the first 4 h, Pb was quickly desorbed from biochars to account for 70% of their maximum Pb desorption. However, the rate of Pb desorption gradually decreased during the next 20 hours. Desorption of Pb from biochars followed the pseudo-first order kinetic model and the intraparticle diffusion model during the first 4 h. The presence of Cd/Al and preferential desorption of these coexisting ions reduced Pb desorption rate and extended the time to reach equilibrium.
Biochar; Adsorption stability; pH; Coexisting ions
10.13758/j.cnki.tr.2017.03.007
X53
A
江苏省自然科学基金项目(SBK2015041561)、国家自然科学基金项目(21507138,51309214,41471404)、南京土壤研究所“一三五”计划和领域前沿项目(ISSASIP1656)和中国科学院科技服务网络计划项目(STS, KFJ-EW-STS-091)资助。
(water19049@gmail.com;mfchen@issas.ac.cn)
刘荣琴(1990—),女,江苏泰州人,硕士研究生,主要从事污染场地土壤及地下水修复研究。E-mail: rqliu@issas.ac.cn
