磁性氯甲基聚苯乙烯微球固相萃取-气相色谱-串联质谱法测定环境水样中7种硝基苯类化合物
2017-07-20董云渊陈林吉叶学敏曹小吉
董云渊,陈林吉,叶学敏,曹小吉*
(1.浙江工业大学化学工程学院,杭州310014;2.浙江工业大学分析测试中心,杭州310014)
磁性氯甲基聚苯乙烯微球固相萃取-气相色谱-串联质谱法测定环境水样中7种硝基苯类化合物
董云渊1,陈林吉2,叶学敏1,曹小吉2*
(1.浙江工业大学化学工程学院,杭州310014;2.浙江工业大学分析测试中心,杭州310014)
采用磁性氯甲基聚苯乙烯微球(CMPNs)固相萃取-气相色谱-串联质谱法测定环境水样中7种硝基苯类化合物(NBs)的含量。优化的试验条件如下:①萃取剂为CMPNs材料;②CMPNs的用量为15.0 mg;③萃取时间为4 min;④氯化钠的加入量为340 g·L-1;⑤洗脱剂丙酮的用量为3 mL;⑥洗脱时间为1 min。气相色谱分离用HP-INNOWAX色谱柱,质谱分析采用全扫描和选择离子监测模式。7种NBs的质量浓度均在0.2~4.0μg·L-1内与其峰面积呈线性关系,方法的检出限(3S/N)在0.006~0.022μg·L-1之间。7种NBs测定值的相对标准偏差(n=6)在0.30%~5.3%之间。方法用于环境水样的分析,回收率在72.4%~113%之间。
气相色谱-串联质谱法;CMPNs;固相萃取;环境水样;NBs
硝基苯类化合物(NBs)是硝基芳香族化合物的总称,被广泛用于染料、农药、炸药、造纸和纺织等工业[1]。然而该类化合物属于高毒有机污染物,且易在环境中累积,其在工业生产中往往会因为转化不彻底而形成残留,并随废水一起排放到环境中,进而对地表水和地下水造成污染。我国现有的硝基苯限量标准(GB 22573-2008)[2]中规定农田灌溉用水中硝基苯的质量浓度不得超过2 mg·L-1。硝基苯在环境水样中残留量低,且存在复杂基体的干扰,在分析前需要对其进行富集和净化[3-15]。
目前分析环境水样中NBs的前处理方法主要有液液萃取(LLE)[5]、固相萃取(SPE)[6-10]、液相微萃取(LPME)[11-14]和单滴微萃取(SDME)[15-16]等。然而,这些方法操作繁琐复杂,需要消耗大量的时间或使用有毒有机溶剂。近年来,磁性固相萃取技术越来越广泛地用于环境样本中痕量污染物的富集和净化。离子液体物理修饰的磁性石墨烯可用于环境水样中5种NBs的超声辅助磁性固相萃取,但该萃取方法存在上样量较小,离子液体不能回收利用等缺点[17]。有文献报道采用一步细乳聚合法制备磁性氯甲基聚苯乙烯微球(CMPNs)[18],所制得疏水的磁性纳米微球表面的氯甲基聚苯乙烯层容易通过π-π作用吸附芳香类化合物,已用于水样中邻苯二甲酸酯的磁性固相萃取[19],并取得了较好的萃取效果,而将该材料用于环境水样中NBs的磁性固相萃取(MSPE)还未见报道。本工作以CMPNs为磁性固相萃取的磁性吸附剂,在超声辅助下,通过对CMPNs用量、超声萃取时间和洗脱溶剂用量等影响磁性固相萃取效率的相关因素进行系统优化,结合气相色谱-串联质谱法(GC-MS/MS),建立了一种简便快速、绿色环保的筛查环境水样中痕量NBs的分析方法。
1 试验部分
1.1 仪器与试剂
Agilent7890A-7000B型气相色谱三重四极杆质谱仪,CTC多功能自动进样器;Milli-Q型超纯水纯化系统。
7种NBs的标准储备溶液:均为100 mg·L-1。
7种NBs的标准溶液:均为10 mg·L-1,4℃避光保存,使用时根据需要用丙酮逐级稀释成不同浓度的混合标准溶液系列。
甲醇、丙酮为色谱纯;试验用水为超纯水(电阻率18 MΩ·cm)。
1.2 仪器工作条件
1)色谱条件HP-INNOWAX色谱柱(60 m× 0.25 mm,0.25μm);载气为氦气,流量1 mL· min-1;进样方式为不分流进样,进样量1μL,进样口温度240℃。程序升温:初始温度50℃,保持2 min;以20℃·min-1速率升温至240℃,保持5 min。
2)质谱条件电子轰击电离源(EI),电离能量70 eV;离子源温度230℃,传输杆温度250℃;质量扫描范围m/z 30~650;碰撞气为氮气,流量1.5 mL·min-1。
1.3 试验方法
1.3.1 CMPNs的合成
CMPNs采用一步细乳聚合法制备[18]。
1.3.2 磁性固相萃取过程
称取CMPNs 15.0 mg,依次用甲醇3 mL和水3 mL浸泡2 min活化。在一定量的加标水样中加入氯化钠34 g,溶解定容至100 mL,再向其中加入上述活化后的CMPNs,超声萃取4 min后经外加磁场分离,接着用3 mL丙酮对磁性吸附剂材料上的NBs超声洗脱1 min,收集洗脱液,常温下氮吹至1 mL以下。最后用丙酮定容至1 mL,过0.22μm尼龙滤膜后,按仪器工作条件进行测定。
2 结果与讨论
2.1 NBs在CMPNs上的吸附等温线
吸附等温线对了解NBs在CMPNs表面的吸附性能非常重要。15.0 mg的CMPNs被用来吸附100 mL水中不同质量浓度的7种NBs。NBs在CMPNs上的吸附等温线见图1。
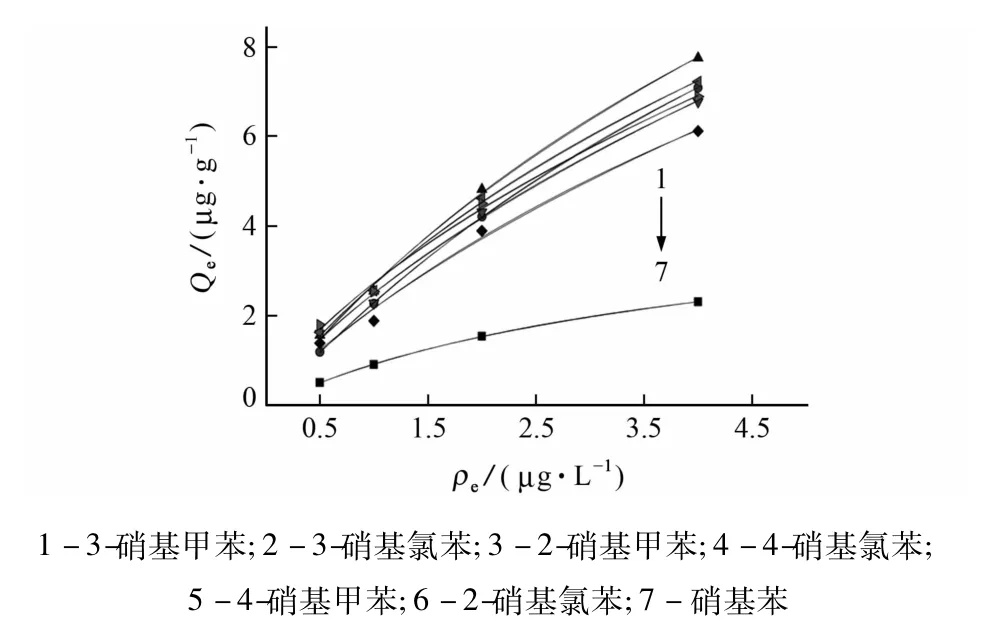
图1 NBs在CMPNs上的吸附等温线Fig.1 Adsorption isotherms of NBs on CMPNs
平衡吸附量(Qe)与平衡浓度(ρe)的定量关系符合Langmuir等温吸附模型,由吸附等温式可得硝基苯饱和吸附量为4 723 ng·g-1,其余6种NBs饱和吸附量在14 024~23 578 ng·g-1之间。由图1可知:NBs的质量浓度增大到4μg·L-1时,CMPNs对它们的吸附仍未达到饱和[19]。
2.2 磁性固相萃取条件的选择
为了获得CMPNs对NBs的最佳萃取效率,试验分别对影响萃取过程的主要因素如萃取剂种类、盐的用量、磁性萃取材料用量、萃取时间、洗脱溶剂体积、洗脱时间等因素进行了考察。试验考察过程的加标水样质量浓度为1μg·L-1。
2.2.1 萃取剂
试验考察了二氧化硅包覆四氧化三铁钠米微球材料(Fe3O4@SiO2)、乙烯基硅烷修饰的Fe3O4@ SiO2、聚合离子液体修饰的Fe3O4@SiO2、NMPNs、羧化Fe3O4@SiO2和氨化Fe3O4·SiO2等6种不同磁性材料作为萃取剂时对NBs的萃取效率,结果发现,CMPNs明显优于其他5种材料。推测原因是其他5种磁性材料与NBs之间基本不存在π-π相互作用,而CMPNs表面含有大量苯环结构,能通过ππ相互作用吸附NBs。试验选择CMPNs作为萃取剂。
2.2.2 萃取剂的用量
试验考察了CMPNs的用量为5.0,10.0,15.0,20.0 mg时对萃取效率的影响,结果见图2。

图2 CMPNs磁性材料的用量对萃取效率的影响Fig.2 Effect of amount of CMPNs magnetic material on extraction efficiency
由图2可知:当CMPNs的用量为15.0 mg时,萃取率达到最大值。试验选择CMPNs的用量为15.0 mg。
2.2.3 萃取时间
试验考察了萃取时间依次为4,8,12,16 min时对萃取率的影响,结果表明:随着萃取时间的延长,萃取率基本没有变化。试验选择萃取时间为4 min。
2.2.4 盐的用量
试验考察了氯化钠的加入量为0,150,250, 340 g·L-1(盐的用量再多会导致氯化钠析出)时对萃取率的影响。结果发现:随着氯化钠加入量的增加,萃取率有明显的改善;当氯化钠量的加入量为340 g·L-1时,萃取效果最好,可能是盐析效应,即氯化钠的加入降低了硝基苯在水中的溶解度。试验选择氯化钠的加入量为340 g·L-1。
2.2.5 洗脱剂用量和洗脱时间
试验以丙酮为洗脱剂,考察了丙酮用量依次为1,2,3,4 mL时对萃取率的影响。结果表明:当丙酮的用量为1,2 mL时,萃取率很低;当丙酮的用量为3 mL时,萃取率达到最大;继续增大丙酮用量,萃取率基本不变。
试验进一步考察了洗脱时间依次为0,1,2,3,4 min时对萃取率的影响.结果表明:随洗脱时间的延长,萃取率逐渐变大;当洗脱时间为1 min时,萃取效果最佳;继续延长洗脱时间,萃取率略有降低。试验选择洗脱时间为1 min。
2.3 标准曲线与检出限
按试验方法对7种NBs混合标准溶液系列进行测定,并绘制标准曲线,结果表明:7种NBs的质量浓度均在0.2~4.0μg·L-1内与其对应的色谱峰面积呈线性关系,其线性回归方程、相关系数、检出限(3S/N)和测定下限(10S/N)见表1。

表1 线性参数、检出限与测定下限Tab.1 Linearity parameters,detection limits and lower limits of determination
由表1可知:检出限在0.006~0.022μg·L-1之间,测定下限在0.020~0.067μg·L-1之间。
2.4 精密度试验
按试验方法测定7种NBs混合标准溶液,平行测定6次。结果表明:硝基苯、2-硝基甲苯、3-硝基甲苯、4-硝基甲苯、3-硝基氯苯、4-硝基氯苯、2-硝基氯苯的相对标准偏差依次为4.6%,0.30%,3.5%,4.2%,5.3%,0.70%,0.40%,方法重现性良好。
2.5 方法的比对
将试验方法与文献报道的LLE、SPE[6]、SDME[13]、LPME[14]、IL-Fe3O4@G-MSPE[17]中的方法进行比较,比对结果见表2。试验所用的方法只需15 mg的萃取材料,超声萃取4 min,3 mL丙酮超声洗脱1 min即可完成磁性固相萃取过程,获得更低的检出限,大大减少了样品前处理时间及有机溶剂的用量。
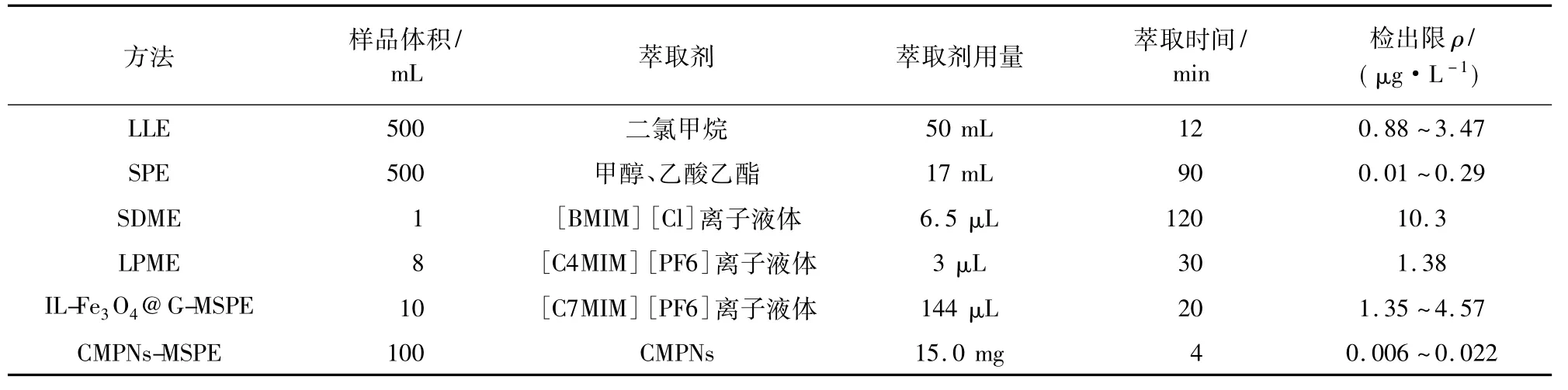
表2 方法样品处理和检出限的比对Tab.2 Comparison of sample treatments and detection limits of the proposed method with the other methods
2.6 样品分析
按试验方法对钱塘江流域3座大桥采集的水样进行分析,其结果见表3。其中“-”表示未检出。
由表3可知:仅桥3水样中检测到4-硝基氯苯,其余所得水样中未检出7种NBs,加标回收率在72.4%~113%之间,方法可以满足于环境水样中NBs的分析要求。
本工作建立了同时测定环境水样中7种NBs的CMPNs-MSPE/GC-MS/MS分析方法,在优化条件下,CMPNs-MSPE快速富集了水样中的7种NBs,测定结果准确可靠。方法检出限低,且重复性较好。与传统方法相比,操作简单快速,有机溶剂用量少,符合绿色化学的要求,可应用于环境样品中NBs的快速筛查。

表3 样品分析结果Tab.3 Analytical results of the samples
[1]PARHAM H,SAEED S.Pre-concentration and determination of traces of nitrobenzene and 1,3-dinitrobenzene in water samples using anthracite adsorbent[J].J Ind Eng Chem,2014,20(3):1003-1009.
[2]GB 22573-2008灌溉水中氯苯、1,2-二氯苯、1,4-二氯苯、硝基苯限量[S].
[3]WU L J,SONG C M,ZHAO Y,et al.Determination of organochlorine pesticides in tea beverage by directly suspended droplet microextraction combined with GC-ECD[J].Food Anal Method,2015,8(1):147-153.
[4]CORTADA C,VIDAL L,CANALS A.Determination of nitroaromatic explosives in water samples by direct ultrasound-assisted dispersive liquid-liquid microextraction followed by gas chromatography-mass spectrometry[J].Talanta,2011,85(5):2546-2552.
[5]张营,郜炜,景逵,等.液液萃取-气相色谱法测定水中的硝基苯类化合物[J].辽宁大学学报(自然科学版),2010,37(3):282-284.
[6]刘宁.固相萃取-气相色谱法测定水中硝基苯类化合物的含量[J].山东化工,2012,41(5):48-51.
[7]PENG X T,XING Z,FENG Y Q.Preparation of phenothiazine bonded silica gel as sorbents of solid phase extraction and their application for determination of nitrobenzene compounds in environmental water by gas chromatography-mass spectrometry[J].J Chromatogr A,2011,1218:9314-9320.
[8]任朝兴,向统领,杨家欢.固相萃取-气相色谱/质谱法同时测定海水中9种硝基苯类化合物[J].海洋环境科学,2012,31(5):743-745.
[9]XIE F W,SHANG J J,GUO J Z,et al.Determination of seven nitrobenzene compounds in mainstream cigarette smoke with heart-cutting two-dimensional gas chromatography[J].J Chromatogr A,2012,50:387-392.
[10]任衍燕.固相萃取-气相色谱/质谱法测定水中硝基苯类化合物[J].城镇供水,2012(5):51-52.
[11]刁春鹏,赵汝松,柳仁民,等.分散液相微萃取-气相色谱/质谱快速分析水中的硝基苯类化合物[J].分析试验室,2009,28(6):9-12.
[12]翦英红,范宁伟,张德.分散液液微萃取高效液相色谱法测定环境水样中硝基苯[J].天津化工,2011,25 (1):51-53.
[13]沈彬,罗三姗,张占恩.液相微萃取-气相色谱/质谱测定水中硝基苯类化合物[J].分析科学学报,2007,23 (6):705-708.
[14]CHA D M,MA B.Determination of nitrobenzene in water using ionic liquid-based liquid-phase microextraction coupled with HPLC[J].American Laboratory,2009,41:12-15.
[15]YAO C,TWU P,ANDERSON J L.Headspace single drop microextraction using micellar ionic liquid extraction solvents[J].Chromatographia,2010,72:393-402.
[16]母应锋,杨丽莉,胡恩宇,等.一滴溶剂微萃取-毛细管气相色谱法分析水中的七种硝基苯类化合物[J].色谱,2007,25(6):876-880.
[17]CAO X J,SHEN L X,YE X M,et al.Ultrasound-assisted magnetic solid-phase extraction based ionic liquidcoated Fe3O4@graphene for the determination of nitrobenzene compounds in environmental water samples[J].Analyst,2014,139(8):1938-1944.
[18]ZHENG Z,WANG J L,ZHANG M,et al.Magnetic polystyrene nanosphere immobilized TEMPO:a readily prepared,highly reactive and recyclable polymer catalyst in the selective oxidation of alcohols[J].Chem Cat Chem,2013,5(1):307-312.
[19]CAO X J,KONG Q L,CAI R N,et al.Solid-phase extraction based on chloromethylated polystyrene magnetic nanospheres followed by gas chromatography with mass spectrometry to determine phthalate esters in beverages[J].J Sep Sci,2014,37(24):3677-3683.
GC-MS/MS Determination of 7 Nitrobenzenes in Environmental Water Samples with Solid Phase Extraction Based on Chloromethylated Magnetic Polystyrene Nanospheres
DONG Yunyuan1,CHEN Linji2,YE Xuemin1,CAO Xiaoji2*
(1.College of Chemical Engineering,Zhejiang University of Technology,Hangzhou 310014,China; 2.Research Center of Analysis and Measurement,Zhejiang University of Technology,Hangzhou 310014,China)
GC-MS/MS was applied to the determination of 7 nitrobenzenes in environmental water samples with solidphase extraction based on chloromethylated magnetic polystyrene nanospheres(CMPNs).The optimized conditions found were as follows:①extracting agent:CMPNs material;②amount of CMPNs:15.0 mg;③extraction time:4 min;④amount of NaCl:340 g·L-1;⑤amount of acetone(eluant):3 mL;⑥elution time:1 min.The HP-INNOWAX chromatographic column was used for GC separation,and the full-scanning mode and the selected ion monitoring mode were adopted in MS.Linear relationships between values of peak area and mass concentration ofthe 7 nitrobenzenes were kept in the same range of0.2-4.0μg·L-1,with detection limits(3S/N)in the range of0.006-0.022μg·L-1.Precision of the method was tested,and values of RSD(n=6)for 7 NBs found were in the range of 0.30%-5.3%.The proposed method was applied to the analysis of environmental water samples,giving values of recovery in the range of 72.4%-113%.
GC-MS/MS;CMPNs;solid phase extraction;environmental water sample;nitrobenzene
O657.63
A
1001-4020(2017)05-0497-05
10.11973/lhjy-hx201705001
2016-04-20
浙江省环保科研计划项目(2014A011);杭州市环境保护科技项目(2013HZHB002)
董云渊(1991-),男,浙江衢州人,硕士研究生,研究方向为分析化学
*通信联系人。xiaojicao@zjut.edu.cn
