零价铁活化过硫酸钠降解甲基橙
2017-07-18马国峰叶永庆张丽卓董世柱贺春林沈阳大学辽宁省先进材料制备技术重点实验室辽宁沈阳110044
马国峰, 叶永庆, 张丽卓, 董世柱, 贺春林(沈阳大学 辽宁省先进材料制备技术重点实验室, 辽宁 沈阳 110044)
零价铁活化过硫酸钠降解甲基橙
马国峰, 叶永庆, 张丽卓, 董世柱, 贺春林
(沈阳大学 辽宁省先进材料制备技术重点实验室, 辽宁 沈阳 110044)
利用零价铁活化过硫酸钠产生的硫酸根自由基作氧化剂降解偶氮染料甲基橙.研究了不同因素对目标污染物降解效率的影响,其中包括零价铁的加入量、过硫酸钠的浓度、温度、pH等.实验结果表明:当单独投加零价铁的甲基橙溶液,其甲基橙的降解率只有2.99%;而单独加入过硫酸钠时,降解率达到51.81%,在酸性和中性的条件下过硫酸钠都会发生水解,生成硫酸根基使溶液的氧化性增强,从而使甲基橙褪色.当pH值为3.0时、温度为30 ℃、铁的加入量为11.2 mg/L、过硫酸钠的浓度2.0 mol/L时,在60 min降解率达到最大约为94%.同时还比较了零价铁、过硫酸钠、温度和不同pH条件对甲基橙降解效率的影响大小,结果表明前30 min时温度和零价铁的量对降解的影响最大,其影响大小为:温度>铁的加入量>pH>过硫酸钠浓度.而在后30 min时,降解的速率缓慢,温度和pH成为主要影响因素,影响大小为:温度>pH>过硫酸钠浓度>铁的加入量.
零价铁; 活化; 过硫酸钠; 甲基橙; 降解率
偶氮染料含有偶氮基连接芳香基分子结构,是用于纺织印染行业的主要着色剂[1]从这些行业释放的污水含有各种高度着色的偶氮染料[2].如果污水处理的不适当,它会对水环境造成不良的影响[3-4].大多数的偶氮染料由于其复杂的结构和较好的稳定性而难以降解,因此,传统的生物处理工艺处理染料废水可能不再符合严格的污水排放标准[5-6].目前,物理化学脱色法被广泛使用,如Anouar[7]等利用活性炭的吸附作用处理偶氮类染料活性紫5废水.研究发现,室温、pH值为2的实验条件下,活性炭对10 mg/L活性紫5吸附处理10 min,偶氮类染料活性紫5 的脱色率达到98%.然而,化学污泥产生、吸附剂再生以及薄膜分离[8-9]等可能引发二次污染.


也可以由加热[19-21]、紫外线[22-23]、微波、超声波和强碱溶液的方式产生.
由于铁作为过渡金属催化剂在活化时相对无毒、廉价和方便操作等特点,用它活化过硫酸盐氧化污染物得到广泛研究.根据多种类型的铁的形态,发现零价铁作为催化剂活化过硫酸盐产生了良好的效果.
本实验以含有偶氮结构的甲基橙为研究目标,以此研究零价铁活化过硫酸钠降解甲基橙的影响因素,以期为进一步探索处理废水提供理论依据.
1 实验方法
铁屑(天津市科密欧试剂有限公司,分析纯);过硫酸钠(天津市大茂化学试剂厂,分析纯);750型紫外-可见分光光度计;PHS-25 pH计;恒温水浴锅;JJ-1电动搅拌器.
称取50 mg的甲基橙,放入烧杯中加入100 mL蒸馏水搅拌溶解,然后将溶液移到1 000 mL的容量瓶中用蒸馏水定容.
采用750型紫外-可见分光光度,以蒸馏水作为参照,于波长为473.2 nm处测定滤液的吸光度,通过标准曲线换算成C(甲基橙).甲基橙的去除率为
CE= (C0-Ct)/Ct×100%.
式中:CE为甲基橙的去除率,%;t为反应时间,min;C0和Ct分别为初始和t时刻的C(甲基橙),mol/L;pH值采用pH计测定.采用Excel 2010进行数据处理,采用Origin 8.6进行数据处理.
在研究实验前,分别取相应体积的甲基橙溶液置于恒温水浴锅中预热到30 ℃,粗调pH为弱酸性.每隔一段时间取样,加入甲醇终止反应,用0.45 μm滤膜过滤.
2 结果与讨论
2.1 空白实验
选取质量浓度为50 mg/L的甲基橙溶液,分别单独加入Fe和过硫酸钠进行空白实验,结果如图1所示.

图1 单独投放Fe和PDS时的空白对比实验
由图1可以看出单独加Fe或过硫酸钠有很大的区别.单独加入过硫酸钠时,甲基橙的去除率达到51.81%.这是因为在酸性或中性条件下过硫酸钠会水解产生硫酸根基,使得溶液的氧化能力增强,而碱性时过硫酸钠氧化水或氢氧根生成羟基基团,增加了氧化能力使甲基橙褪色.在酸度不高时,还会水解生成H2O2,使反应体系氧化能力增强.涉及的反应方程式如下:
单独加入零价铁时,甲基橙的去除率只有2.99%.由于铁具有还原性,所以直接将甲基橙的显色集团(非芳香性π键的类苯醌式结构)还原成芳香胺类化合物,破坏其π键共轭系统结构,进而被降解褪色.反应方程式如下:
2.2 Fe的量对降解甲基橙的影响
取质量浓度为50 mg/L的甲基橙溶液100 mL,加入浓度为2.0 mmol/L的过硫酸钠47.6 mg,Fe的加入量分别为每L 2.8、5.6、11.2、22.4和44.8 mg.研究Fe的用量对降解甲基橙的影响.

图2 Fe的加入量对降解甲基橙的影响
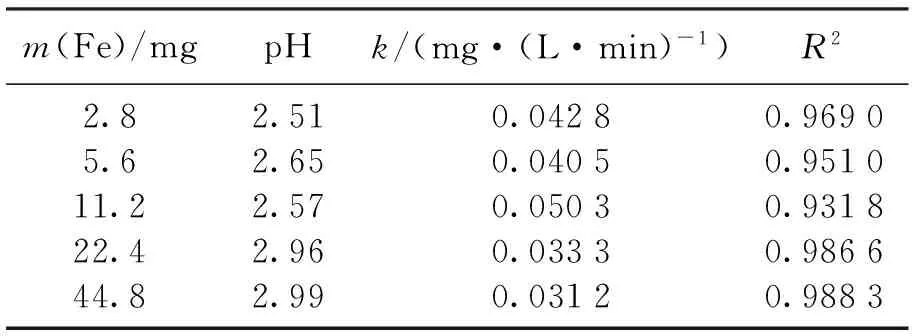
表1 在不同Fe量下pH值和反应动力学常数(k)的变化
由图2可见,当Fe的投入量为每L 11.2 mg时,甲基橙的降解率达到91.18%,达到最高.原因可能是二价铁与过硫酸钠初始反应过快,产生了大量的硫酸根基[24],消耗了二价铁,使降解率提高.但当加入铁的量为22.4 mg/L时其甲基橙的降解率为68.56%,反而低于初始加入的铁的量每L 2.8 mg的82.56%.根据曲线,前30 min时反应的速率几乎成直线,而后速率开始逐渐缓慢.甲基橙的降解率出现先增加后降低的现象.可能由于零价铁直接与过硫酸钠反应生成了硫酸根基.同时,发生自我淬灭[25];而溶液中过量的二价铁可以与硫酸根基生成沉淀降低硫酸根基的浓度,抑制了甲基橙的降解.涉及的反应方程式如下:
2.3 过硫酸钠的浓度对甲基橙降解的影响
取质量浓度为50 mg/L的甲基橙溶液100 mL,加入11.2 mg/L的Fe,分别加入0.5、1.0、2.0、4.0和8.0 mmol/L等不同浓度的过硫酸钠溶液.考察过硫酸钠的浓度对甲基橙降解的影响,结果如图3所示.

图3 过硫酸钠的浓度对甲基橙降解的影响

表2 在不同浓度过硫酸钠下pH值和反应动力学常数(k)的变化
图3可见,随着过硫酸钠浓度的增加,甲基橙的降解率也随之增加,分为快速和慢速两个阶段.当过硫酸钠的浓度为2.0 mmol/L时,甲基橙的降解率达到90%以上,但是当过硫酸钠浓度为4.0 mol/L时甲基橙的降解效率反而下降.由于过硫酸钠浓度的增加并没有使体系中去除率明显增加,可以知道投加铁的加入量有限是影响甲基橙降解的主要因素.从图4的曲线看,当过硫酸钠的浓度为2.0和8.0 mol/L时,过硫酸钠的质量浓度下降的最快,反应速率加快,而反应的量最多的是浓度为2.0 mol/L,为最佳浓度.从反应速率和相关系数表明:过硫酸盐的浓度对脱色的效果有很大的影响,其中脱色最好的浓度为2.0 mol/L时.

图4 过硫酸钠的质量浓度随时间的变化
2.4 pH对甲基橙降解的影响
取质量浓度为50 mg/L的甲基橙溶液100 mL,在加入11.2 mg零价铁和47.6 mg/L过硫酸钠的条件下,考察不同pH对甲基橙降解效果的影响,结果如图5所示.

图5 pH对甲基橙降解的影响Fig.5 Effect of pH on degradation of methyl orange

表3 在不同初始pH下pH值和反应动力学常数(k)的变化
如图5所示,当pH值为3.0的时候,甲基橙的去除率最高达到94.20%.随着pH值的升高,甲基橙的降解效率反而降低.说明在酸性条件下,零价铁会快速被酸化生成二价铁,加快和过硫酸钠的反应,进而产生大量过硫酸根基,使得反应速率加快.由表观反应速率k值可知,酸性条件使得反应的速率大大提高.同时酸性环境也会加快过硫酸钠的酸化,使体系中的硫酸根基增多,氧化性增强.而在碱性或中性条件,甲基橙的降解率下降可能是因为过量的二价铁发生水解生成沉淀[26],使得体系中的二价铁减少,阻碍了二价铁和过硫酸钠之间的反应,同时生成的沉淀对过硫酸钠的催化性较低,过硫酸根基的量减少,氧化性降低,所以不能继续降解甲基橙.涉及的反应方程式如下:
2.5 温度对甲基橙降解的影响
取质量浓度为50 mg/L的甲基橙溶液100 mL,在加入11.2 mg/L的Fe,47.6 mg/L的过硫酸钠,pH值为7.0的条件下,考察不同温度对甲基橙降解影响,结果如图6所示.

图6 温度对甲基橙降解的影响

表4 在不同温度下pH值和反应动力学常数(k)的变化
由图6可见,在一定的范围内,甲基橙的降解率会随着温度的升高而增加.原因是升高温度可以加快分子的运动,进而提高反应物分子间的碰撞速率,加快反应的进行[27],过硫酸盐产生的硫酸根基增加,降解的速率也随之增加.但当温度在30~40 ℃之间时,甲基橙的降解率并没有明显的提高.可能是因为反应物前期消耗的太快,随着反应物的减少,温度对反应的速率影响就不太大了.同时由于体系的反应已经达到了极限,温度的升高只会缩短反应的时间,并不会使体系中的降解率增加.由表格中的相关系数和速率可知,温度在30和40 ℃时的差别不是很大,说明单独热活化提高完全降解的程度不是很高. 反应方程式如下:
从上述的实验结果中选取最佳条件,将其进行对比,结果如图7所示.从图中可以看出反应初始时影响降解效率最大是铁的加入量和温度,但温度的影响并不太稳定,可能与环境的温度的影响有关,使溶液的温度下降,影响了反应的进行.而过硫酸钠和pH值在前30 min内对甲基橙的降解成线性,而后趋势开始减慢.零价铁量在30 min时速率也开始减慢.所以降解甲基橙最好的时间点是当时间在30 min时,影响最大的是温度.由于温度过高时,分子的运动速率加快,加快反应的进行,降解率提高.铁和过硫酸钠对甲基橙的降解效果相似,差别不大,且两者的量存在着一定的关系,过高过低都对降解效果有影响.通过对比发现前30 min时其影响大小为:温度>铁的加入量>pH>过硫酸钠浓度.而在后30 min时,降解的速率缓慢,温度和pH成为主要影响因素,影响大小为:温度>pH>过硫酸钠的浓度>铁的加入量.
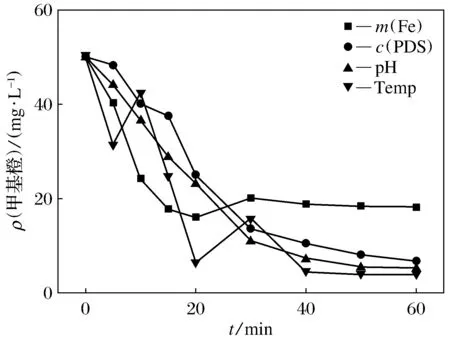
图7 不同条件对降解的影响Fig.7 Effect of different conditions on degradation
3 结 论
(1) 当溶液为弱酸性时、无活化的状态下,单独加11.2 mg/L零价铁时降解率只有2.99%;但当加入过硫酸钠的浓度2.0 mol/L时,其降解率达到51.81%.
(2) 零价铁的量、过硫酸钠浓度、pH和温度在反应的30 min内对甲基橙的降解有较大的影响.初期时,零价铁的量增加和温度的升高均能使甲基橙的去除率提高;pH较低时对降解的效率也有很大的影响.当pH=3时,在60 min时的降解效率达90%以上,当铁的加入量为11.2 mg/L时达到91.18%.原因是pH值较低时加快了活化的过程,使过硫酸根基的量增多,从而提高了甲基橙的降解率,所以升高过硫酸钠的浓度也会使降解的效果增加.
(3) 实验中甲基橙对的降解符合反应动力学,会产生大量过硫酸根基降解污染物.同时反应还研究了不同条件的影响大小,发现在前期时铁的加入量和温度的影响很大,反应后期pH的效果更加明显一些,而温度仍是主要因素.
(4) 最后发现:甲基橙溶液在反应温度为30 ℃、pH值为3.0、过硫酸钠浓度2.0 mol/L、零价铁加入量11.2 mg/L、质量浓度为50 mg/L的条件下降解的效果最好,降解率达94%.
[ 1 ] DURRUTY I,FASCE D,GONZLEZ J F,et al. A kinetic study of textile dyeing wastewater degradation by Penicillium chrysogenum[J]. Bioprocess and Biosystems Engineering, 2015,38(6):1-13.
[ 2 ] SUBRAMONIAN W,WU T Y. Effect of enhancers and inhibitors on photocatalytic sunlight treatment of methylene blue[J]. Water Air & Soil Pollution, 2014,225(4):1-15.
[ 3 ] 林茂森,王殿武,刘玉珍,等. 城市河流健康威胁与生态修复[J]. 沈阳大学学报(自然科学版), 2015(3):197-200. (LIN M S,WANG D W,LIU Y Z,et al. Urban river health and ecological restoration[J]. Journal of Shenyang University(Natural Science), 2015,27(3):197-200.)
[ 4 ] 周彦波,郭少鹏,鲁军,等. Fenton试剂氧化法深度处理含氰废水[J]. 沈阳大学学报(自然科学版), 2012,24(2):18-22. (ZHOU Y B,GUO S P,LU J,et al. Advanced treatment of cyanide wastewater using fenton reagent[J]. Journal of Shenyang University(Natural Science), 2012,24(2):18-22.)
[ 5 ] 俞洁,张海涛,陆泉芳,等. 坡缕石/聚乙二醇/丙烯酸水凝胶的表征及其对阳离子染料的吸附性能[J]. 化工进展, 2015,34(4):1115-1121. (YU J,ZHANG H T,LU Q F,et al. Characterization of palygorskite/poly(ethylene glycol)/acrylic acid hydrogel and its application as an adsorbent for cationic dyes[J]. Chemical Industry and Engineering Progress, 2015,34(4):1115-1121.)
[ 6 ] 汤善康,耿启金,刘刚,等. 光催化降解活性染料K-GL的动力学及其盐效应[J]. 化工进展, 2014,33(7):1908-1912. (TANG S K,GENG Q J,LIU G,et al. Investigation into salt effect and kinetics of photocatalytic degradation of reactive dye K-GL[J].Chemical Industry and Engineering Progress, 2014,33(7):1908-1912.)
[ 7 ] ANOUAR H,ELHOURCH A,ELKACEMI K,et al. Removal of violet 5R azo dye by adsorption on powdered activated carbon[J]. International Journal of Innovation and Applied Studies, 2014,9(3):1368-1372.
[ 8 ] CONG W,XIANG H,ZHANG G L. Dyeing wastewater treatment and reutilization through ultrafiltration and nanofihration integrated membrane processes[J]. Technology of Water Treatment, 2008,8(10):75-78.
[ 9 ] FERSI C,DHAHBI M. Treatment of textile plant effluent by ultrafiltration and/or nanofiltration for water reuse[J]. Desalination, 2008,222(1):263-271.
[10] XU X R,LI X Z. Degradation of azo dye orange G in aqueous solutions by persulfate with ferrous ion[J]. Separation & Purification Technology, 2010,72(1):105-111.
[11] TAN C,GAO N,DENG Y,et al. Heat-activated persulfate oxidation of diuron in water[J]. Chemical Engineering Journal, 2012,203(5):294-300.
[12] JIANG X,WU Y,WANG P,et al. Degradation of bisphenol A in aqueous solution by persulfate activated with ferrous ion[J]. Environmental Science and Pollution Research, 2013,20(7):49474953.
[13] PETERNEL I,KUSIC H,MARIN V,et al. UV-assisted persulfate oxidation: the influence of cation type in the persulfate salt on the degradation kinetics of an azo dye pollutant[J]. Reaction Kinetics, Mechanisms and Catalysis, 2013,108(1):17-39.
[14] ANIPSITAKIS G P,DIONYSIOU D D. Radical generation by the interaction of transition metals with common oxidants[J]. Environmental Science & Technology, 2004,38(13):3705.
[15] KUSIC H,PETERNEL I,UKIC S,et al. Modeling of iron activated persulfate oxidation treating reactive azo dye in water matrix[J]. Chemical Engineering Journal, 2011,172(1):109-121.
[16] LIANG C J,BTUELL C J,MARLEY M C. Thermaity activated persulfate oxidation of trichloroethylene (TCE) and 1,1,1 trichloroethane (TCA) in aqueous systems and soil slurries[J]. Soil and Sediment Contamination: An International Journal, 2003,12(2):207-228.
[17] CAO J,ZHANG W X,BROWN D G,et al. Oxidation of lindane with Fe(Ⅱ)-Activated Sodium Persulfate[J]. Environmental Engineering Science, 2008,25(2):221-228.
[18] LIANG C,BMELL C J,MARLEY M C. Persulfate oxidation for in situ remediation of TCE.I. Activated by ferrous ion with and without a persulfate-thiosulfate redox couple[J]. Chemosphere, 2004,55(9):l213-1223.
[19] WALDEMER R H,TRATNYEK P G,JOHNSON R L,et al. Oxidation of chlorinated ethenes by heat-activated persulfate: kinetics and products[J]. Environmental Science & Technology, 2007,41(3):1010-1015.
[20] HOUSE D A. Kinetics and mechanism of oxidations by peroxydisulfate[J]. Chemical Reviews, 1962,62(3):185-203.
[21] HORI H,MURAYAMA M,INOUE N,et al. Efficient mineralization of hydroperfluorocarboxylic acids with persulfate in hot water[J]. Catalysis Today, 2010,151(1/2):131-136.
[22] LAU T K,CHU W,GRAHAM N J D. The aqueous degradation of butylated hydroxyanisole by UV/S20: study of reaction mechanisms via dimerization and mineralization[J]. Environmental Science & Technology, 2007,41(2):613-619.
[23] SALARI D,NIAEI A,ABER S,et al. The photooxidative destruction of C.I. Basic Yellow 2 using UV/S 2082-, process in a rectangular continuous photoreactor[J]. Journal of Hazardous Materials, 2009,166(1):61-66.
[24] HAMDAOUI O,NAFFRECHOUX E,TIFOUTI L,et al. Effects of ultrasound on adsorption-desorption of p-chlorophenol on granular activated carbon[J]. Ultrasonics Sonochemistry, 2003,10(2):109-114.
[25] HAMDAOUI O,NAFFRECHOUX E. Adsorption kinetics of 4-chlorophenol onto granular activated carbon in the presence of high frequency ultrasound[J]. Ultrasonics Sonochemistry, 2009,16(1):15-22.
[26] AND B S S,YANG R T. Ultrasound enhanced adsorption and desorption of phenol on activated carbon and polymeric resin[J]. Industrial & Engineering Chemistry Research, 2001,40(22):4912-4918.
【责任编辑: 胡天慧】
Decolorization Properties of Methyl Orange by Sodium Persulfate Activated with Zero-Valent Iron
MaGuofeng,YeYongqing,ZhangLizhou,DongShizhu,HeChunlin
(Liaoning Province Key Laboratory for Advanced Materials Preparation Technology, Shenyang University, Shenyang 110044, China)
Using the zero-valent iron activated persulfate, sulfate radical oxidant degradation of azo dye methyl orange was produced. The effects of different factors on the degradation efficiency of target pollutant are studied, including the amount of zero valent iron, sodium persulfate concentration, temperature, pH and so on. The experimental results show that: when the dosage of methyl orange solution alone zero valent iron, the removal of methyl orange was only 2.99%; while adding sodium persulfate, the removal rate reached 51.81%, in acidic and neutral conditions will be hydrolyzed to produce sulfuric acid sodium persulfate oxidation solution enables enhanced, so that the methyl orange fade. When pH is 3, temperature is 30 ℃, iron the amount of 11.2 mg/L, 2.0 mol/L concentration of sodium persulfate, the degradation rate of 60 min reached a maximum of about 94%. At the same time also compared with zero-valent iron, sodium persulfate, temperature and pH of different conditions on the degradation efficiency of methyl orange. Ring size, the results of the study show that 30 min before the effects of temperature and the amount of zero-valent iron on the degradation of the maximum magnitude of the effect is: temperature>the amount of iron in >pH. After 30 min of sodium persulfate, the degradation rate is slow, temperature and pH become the main factors that affect the effect of size: the amount of iron concentration>temperature>pH>sodium persulfate.
zero-valent iron; activated; sodium persulfate; methyl orange; degradation efficiency
2016-01-08
中国博士后基金资助项目(2016M601333); 国家自然科学基金资助项目(51171118); 辽宁省自然科学基金资助项目(201602518).
马国峰(1979-),男,辽宁鞍山人,沈阳大学副教授,博士.
2095-5456(2017)03-0173-06
X 703.1
A
