紫杉醇联合洛铂经介入栓塞给药化疗宫颈癌的临床观察Δ
2017-07-18余梦红张丛敏陈益波崇州市妇幼保健院妇科四川崇州611230
刘 静,余梦红,张丛敏,刘 星,钱 莹,陈益波(崇州市妇幼保健院妇科,四川崇州 611230)
紫杉醇联合洛铂经介入栓塞给药化疗宫颈癌的临床观察Δ
刘 静*,余梦红#,张丛敏,刘 星,钱 莹,陈益波(崇州市妇幼保健院妇科,四川崇州 611230)
目的:探讨紫杉醇联合洛铂经介入栓塞给药对宫颈癌患者的化疗疗效和安全性。方法:选取我院2010年5月-2014年3月收治的宫颈癌患者68例,按照治疗方案分为对照组和观察组,各34例。对照组患者给予注射用紫杉醇脂质体175 mg/m2加至5%葡萄糖注射液250 mL,ivgtt+注射用洛铂80 mg/m2加至5%葡萄糖注射液250 mL,ivgtt;观察组患者采用动脉穿刺插管经动脉造影选取子宫动脉和肿瘤血管,以明胶海绵栓塞,同时经穿刺导管注入注射用紫杉醇脂质体175 mg/m2+注射用洛铂80 mg/m2+5%葡萄糖注射液10 mL。两组患者均在每个疗程第1天给药,以21 d为1个疗程,共治疗3个疗程。观察两组患者临床疗效、治疗前后T淋巴细胞亚群(CD4+、CD8+、CD4+/CD8+)水平;记录治疗过程中不良反应发生情况、治疗2年后的局部复发与转移情况,以及生存情况。结果:观察组患者治疗总有效率(85.29%)明显高于对照组(61.76%),差异有统计学意义(P<0.05)。治疗前,两组患者CD4+、CD8+和CD4+/CD8+水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者CD4+和CD4+/CD8+水平均明显升高,CD8+水平明显降低,且观察组患者上述水平改善较对照组明显,差异均有统计学意义(P<0.05)。观察组患者生存时间[(22.58±0.61)个月]明显长于对照组[(17.61±1.32)月],2年生存率(70.59%)明显高于对照组(47.06%),差异均有统计学意义(P<0.05)。两组患者的疾病控制率、总不良反应发生率、局部复发与转移率比较,差异均无统计学意义(P>0.05)。结论:紫杉醇联合洛铂经介入栓塞给药对宫颈癌患者的化疗疗效明确,可改善其T淋巴细胞亚群水平,且安全性较高。
紫杉醇;洛铂;介入栓塞;宫颈癌;T淋巴细胞亚群;安全性
宫颈癌是最常见的妇科恶性肿瘤,全球每年约有50万新发病例,并呈逐年递增和年轻化的趋势,严重威胁女性的生命健康[1]。宫颈癌的治疗应根据临床分期、患者年龄、生育要求、机体情况和医疗技术水平等综合条件考虑并制订个体化的治疗方案,采用以手术和放疗为主、化疗为辅的综合治疗方案[2]。介入栓塞化疗具有局部化疗药物浓度高、毒副作用小、微小转移灶清除率高等优点,是目前动脉化疗的主要方式之一,但其对宫颈癌患者的疗效尚未明确[2-3]。鉴于此,本研究探讨了紫杉醇脂质体联合洛铂经介入栓塞给药对宫颈癌患者的化疗疗效和安全性,现报道如下。
1 资料与方法
1.1 纳入与排除标准
纳入标准:①符合《子宫颈癌诊断》中宫颈癌诊断标准[4];②肿瘤直径≥4 cm;③美国东部肿瘤协作组(ECOG)评分为0~2分[5]。
排除标准:①有既往肿瘤史或放化疗史者;②合并严重感染、心脑血管疾病和糖尿病等其他疾病者;③肝、肾和骨髓功能异常者;④精神异常或精神障碍者。
1.2 研究对象
选取我院2010年5月-2014年3月收治的宫颈癌患者68例,按照治疗方案不同分为对照组和观察组,各34例。两组患者的年龄、宫颈癌国际妇产科联盟(FIGO)分期、肿瘤直径、ECOG评分、肿瘤分化程度和病理类型等一般资料比较,差异均无统计学意义(P>0.05),具有可比性,详见表1。本研究方案经医院医学伦理委员会审核批准,患者均知情同意并签署知情同意书。

表1 两组患者一般资料比较Tab 1 Comparison of general information of patients between 2 groups
1.3 治疗方法
对照组患者给予注射用紫杉醇脂质体(南京绿叶制药有限公司,批准文号:国药准字H20030357,规格:30 mg)175 mg/m2加至5%葡萄糖注射液250 mL,ivgtt(滴注时间约3 h)+注射用洛铂[海南长安国际制药有限公司,批准文号:国药准字H20080359,规格:10 mg(以无水物计)]80 mg/m2加至5%葡萄糖注射液250 mL,ivgtt;观察组患者采用Seldinger技术进行髂内动脉穿刺插管,经动脉造影后选取子宫动脉和肿瘤血管,以吸收性明胶海绵栓塞,同时经穿刺导管注入注射用紫杉醇脂质体175 mg/m2+注射用洛铂80 mg/m2+5%葡萄糖注射液10 mL。两组患者均在每个疗程第1天给药,以21 d为1个疗程,共治疗3个疗程,化疗结束后均行根治性宫颈癌手术。
1.4 疗效评价标准与观察指标
①根据实体瘤疗效评价标准(RECIST)[5]评定两组患者临床疗效。完全缓解(CR):肿瘤完全消失且无新病灶出现,持续时间≥4周;部分缓解(PR):肿瘤最大直径和其最大垂直直径乘积缩小≥50%,持续时间≥4周且无明显加重;稳定(SD):肿瘤最大直径和其最大垂直直径乘积缩小<50%或增大≤25%;进展(PD):肿瘤最大直径和其最大垂直直径乘积增大>25%。治疗总有效=CR+PR;疾病控制=CR+PR+SD。②采用EPICS流式细胞仪(美国Beckman Coulter公司)测定两组患者治疗前后T淋巴细胞亚群(CD4+、CD8+、CD4+/CD8+)水平,结果采用CellQuest软件分析。③记录两组患者治疗过程中不良反应发生情况和治疗2年后的局部复发与转移情况。④记录两组患者生存时间和2年生存率。
1.5 统计学方法
采用SPSS 18.0软件对数据进行统计分析。计量资料以s表示,采用Student-t检验;计数资料以例数或率表示,采用χ2检验;等级资料以例数或率表示,采用方差分析;平均生存时间以Kaplan-Meier法计算,采用Log-Rank检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较
观察组患者治疗总有效率(85.29%)明显高于对照组(61.76%),差异有统计学意义(P<0.05);两组患者疾病控制率比较,差异无统计学意义(P>0.05),详见表2。
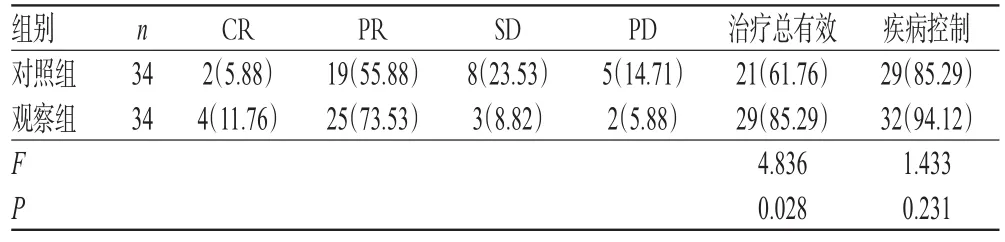
表2 两组患者临床疗效比较[例(%%)]Tab 2 Comparison of clinical efficacies between 2 groups[case(%%)]
2.2 两组患者治疗前后T淋巴细胞亚群水平比较
治疗前,两组患者CD4+、CD8+和CD4+/CD8+水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者CD4+和CD4+/CD8+水平均明显升高,CD8+水平明显降低,且观察组患者上述水平改善较对照组明显,差异均有统计学意义(P<0.05),详见表3。
表3 两组患者治疗前后T淋巴细胞亚群水平比较(s)Tab 3 Comparison of T lymphocyte subset between 2 groups before and after treatment(s)

表3 两组患者治疗前后T淋巴细胞亚群水平比较(s)Tab 3 Comparison of T lymphocyte subset between 2 groups before and after treatment(s)
注:与治疗前比较,*P<0.05Note:vs.before treatment,*P<0.05
组别对照组观察组n tP治疗后0.86±0.16*1.62±0.23*5.879 0.004 34 34 CD4+,%治疗前12.64±3.12 12.52±3.24 0.386 0.727治疗后21.88±4.10*39.36±5.86*5.893 0.003 CD8+,%治疗前31.46±5.11 30.99±5.54 0.792 0.348治疗后25.14±2.83*11.56±1.69*7.526<0.001 CD4+/CD8+治疗前0.34±0.03 0.37±0.06 0.246 0.838
2.3 两组患者不良反应、局部复发与转移情况比较
观察组患者总不良反应发生率(11.76%)与对照组(17.65%)比较,差异无统计学意义(P>0.05);观察组患者局部复发与转移率(14.71%)与对照组(26.47%)比较,差异无统计学意义(P>0.05),详见表4。

表4 两组患者不良反应、局部复发与转移情况比较[例(%%)]Tab 4 Comparison of ADR,local recurrence and metastasis between 2 groups[case(%%)]
2.4 两组患者生存情况比较
观察组患者生存时间[(22.58±0.61)月]明显长于对照组[(17.61±1.32)月],2年生存率(24例,占70.59%)明显高于对照组(16例,占47.06%),差异均有统计学意义(P<0.05)。
3 讨论
宫颈癌是一种常见的妇科生殖系统肿瘤,发病较隐匿,70%以上的患者确诊时已属中晚期[6]。目前,尚缺少中晚期宫颈癌的有效治疗策略,传统放化疗或单纯手术对其疗效并不理想,5年生存率在40%以下[7-8]。因此,如何提高宫颈癌治疗的疗效、缓解患者临床症状、减轻不良反应等,成为宫颈癌治疗中亟待解决的问题。
近年来的研究发现,新辅助化疗对中晚期宫颈癌有较好的疗效,但新辅助化疗策略暂未形成共识,且存有较大争议。本研究采用紫杉醇联合第三代铂类抗肿瘤药物洛铂经动脉化疗介入栓塞的方式给药,结果显示,与静脉滴注给药的对照组相比,观察组患者的治疗总有效率更高,而且观察组患者的不良反应发生率,以及局部复发与转移率与对照组比较并无明显差异。可见,介入栓塞化疗的给药方式对于提高紫杉醇和洛铂的近期临床疗效有积极的促进作用,且使用安全性较高。该给药方式的优势主要体现在以下两个方面:(1)子宫动脉化疗栓塞术能在短时间内缩小肿瘤体积,减少宫旁浸润灶,降低临床分期,提高肿瘤切除率;同时动脉栓塞给药还可降低肿瘤细胞活性,清除弥散卫星转移灶,减少根治性手术后复发转移的风险[9-11]。(2)抗肿瘤药物经动脉直接到达肿瘤部位,滞留时间长,局部药物浓度高,避免了肝肾组织吸收和排泄作用,可使疗效增强数倍。此外,剩余的化疗药物还可经静脉二次到达肿瘤部位,进一步增强化疗效果[12]。本研究结果显示,观察组患者平均生存时间和2年生存率均显著优于对照组,可见该给药方式对提高患者生存率和延长生存时间有明显效果。研究表明,宫颈癌的发生发展与机体免疫功能的水平密切相关[13]。宫颈癌患者免疫水平降低,促使机体清除肿瘤细胞的能力明显下降,导致肿瘤细胞持续增殖。因此,监测机体免疫功能指标的改变可较为及时准确地为肿瘤化疗提供有效的评估手段[2,14]。本研究结果发现,两组患者治疗后的T淋巴细胞亚群水平均明显改善,且观察组患者改善程度明显优于对照组,可见动脉介入栓塞给药对促进T淋巴细胞功能的恢复也具有积极作用。
综上所述,紫杉醇联合洛铂经介入栓塞给药对宫颈癌患者的化疗疗效明确,可改善其T淋巴细胞水平,且安全性较高。但本研究样本量较小,尚待大样本、多中心临床试验对本研究结论进一步验证。
[1] Lim AW,Forbes LJ,Rosenthal AN,et al.Measuring the nature and duration of symptoms of cervical cancer in young women:developing an interview-based approach [J].BMC Womens Health,2013,13(1):357-366.
[2] Chen B,Liu L,Xu H,et al.Effectiveness of immune therapy combined with chemotherapy on the immune function and recurrence rate of cervical cancer[J].Exp Ther Med,2015,9(3):1063-1067.
[3] Downs L.Advances in cervical cancer treatment[J].Gynecol Oncol,2011,121(121):431-433.
[4] 卫生部.子宫颈癌诊断[S].2011-07-01.
[5] Shuster A,Huynh TJ,Rajan DK,et al.Response Evaluation Criteria in Solid Tumors(RECIST)criteria are superior to European Association for Study of the Liver(EASL)criteria at 1 month follow-up for predicting long-term survival in patients treated with transarterial chemoembolization before liver transplantation for hepatocellular cancer[J].J Vasc Interv Radiol,2013,24(6):805-812.
[6] Gutzmer R,Wollenberg A,Ugurel S,et al.Cutaneous side effects of new antitumor drugs:clinical features and management[J].Dtsch Arztebl Int,2012,109(8):133-140.
[7] Lin JF,Berger JL,Krivak TC,et al.Impact of facility volume on therapy and survival for locally-advanced cervical cancer[J].Gynecol Oncol,2014,132(2):416-422.
[8] Eskander RN,Tewari KS.Immunotherapy:an evolving paradigm in the treatment of advanced cervical cancer[J]. Clin Ther,2015,37(1):20-38.
[9] Du TG,Kidd M.Prospective quality of life study of South African women undergoing treatment for advanced-stage cervical cancer[J].Clin Ther,2015,37(10):2324-2331.
[10] Ghezzi F,Cromi A,Ditto A,et al.Laparoscopic versus open radical hysterectomy for stageⅠB2-ⅡB cervical cancer in the setting of neoadjuvant chemotherapy:a multi-institutional cohort study[J].Ann Surg Oncol,2013,20(6):2007-2015.
[11] Heijkoop ST,Franckena M,Thomeer MG,et al.Neoadjuvant chemotherapy followed by radiotherapy and concurrent hyperthermia in patients with advanced-stage cer-vical cancer:a retrospective study[J].Int J Hyperthermia,2012,28(6):554-561.
[12] Lapresa M,Parma G,Portuesi R,et al.Neoadjuvant chemotherapy in cervical cancer:an update[J].Expert Rev Anticancer Ther,2015,15(10):1171-1181.
[13] Tian ZZ,Li S,Wang Y,et al.Investigation of uterine arterial chemoembolization and uterine arterial infusion chemotherapy for advanced cervical cancer before radical radiotherapy:a long-term follow-up study[J].Arch Gynecol Obstet,2014,290(1):155-162.
[14] Li C,Ma C,Zhang W,et al.The immune function differences and high-risk human papillomavirus infection in the progress of cervical cancer[J].Euro J Gynaecol Oncol,2014,35(5):557-561.
Clinical Observation of Paclitaxel Combined with Lobaplatin by Interventional Embolization Chemotherapy for Cervical Cancer
LIU Jing,YU Menghong,ZHANG Congmin,LIU Xing,QIAN Ying,CHEN Yibo(Dept.of Gynaecology,Chongzhou Maternal and Child Health Care Hospital,Sichuan Chongzhou 611230,China)
OBJECTIVE:To investigate chemotherapeutic efficacy and safety of Paclitaxel combined with lobaplatin by interventional embolization for cervical cancer.METHODS:Totally 68 cases of cervical cancer patients selected from our hospital during May 2010-Mar.2014 were divided into control group and observation group according to therapy plan,with 34 cases in each group.Control group was given Paclitaxel liposome for injection 175 mg/m2added into 5%Glucose injection 250 mL,ivgtt+Lobaplatin for injection 80 mg/m2added into 5%Glucose injection 250 mL,ivgtt.Observation group was given Paclitaxel liposome for injection 175 mg/m2+Lobaplatin for injection 80 mg/m2+5%Glucose injection 10 mL via percutaneous catheter after selecting uterine artery and tumor vessel by arterial catheterization arteriography,gelfoam embolization.Both groups were treated in the first day of every treatment course,21 d as a treatment course,for 3 courses.Clinical efficacies were observed in 2 groups as well as the levels of T lymphocyte subsets(CD4+,CD8+,CD4+/CD8+)before and after treatment.The occurrence of ADR during treatment,local recurrence and metastasis after 2 years,and survival situation were recorded.RESULTS:The total response rate of observatio group(85.29%)was significantly higher than that of control group(61.76%),with statistical significance(P<0.05).Before treatment,there was no statistical significance in the levels of CD4+,CD8+or CD4+/CD8+between 2 groups(P>0.05).After treatment,CD4+and CD4+/CD8+of 2 groups were increased significantly,while CD8+was decreased significantly;above indexes of observation group were improved significantly compared to control group,with statistical significance(P<0.05).The survival time of observation group[(22.58±0.61)months]was significantly longer than that of control group[(17.61±1.32)months],and 2-year survival rate(70.59%)was significantly higher than control group(47.06%),with statistical significance(P<0.05).There were no statistical significance in incidence of disease control,incidence of total ADR and incidence of local recurrence and metastasis between 2 groups(P>0.05).CONCLUSIONS:Paclitaxel combined with lobaplatin by interventional embolization show definite chemotherapeutic efficacy for cervical cancer,and can improve the levels of T lymphocyte subset with good safety.
Paclitaxel;Lobaplatin;Interventional embolization;Cervical cancer;T lymphocyte subset;Safety
R737.33
A
1001-0408(2017)17-2374-04
2016-07-25
2016-10-25)
(编辑:陶婷婷)
四川省卫生和计划生育委员会科研课题(No.150049)
*副主任医师。研究方向:妇科肿瘤。电话:028-82202472。E-mail:liujingcz@126.com
#通信作者:副主任医师。研究方向:妇科肿瘤。电话:028-82202472。E-mail:manghongyu@126.com
DOI10.6039/j.issn.1001-0408.2017.17.19
