阜新市2016年ADR监测数据年度分析报告
2017-07-13周晓红沈大鹏吕敏
周晓红+沈大鹏+吕敏

摘 要:目的:掌握我市2016年ADR监测情况,探讨药品不良反应发生的特点及一般规律,为临床安全、合理用药提供参考。方法:对我市药品不良反应监测中心于2016年1~11月收集到的1001份药品不良反应自发报告进行统计分析。结果1001份药品不良反应报告来源于医疗机构占50.45%;报告人职业以药师为主;不良反应发生率女性多于男性且以中年人为主;药品不良反应累及的系统与器官以胃肠系统损害最多(37.177%),其次皮肤及其附件损害(23.799%);药品不良反应发生最多为片剂,严重的药品不良反应发生最多的是注射剂;降血压药品硝苯地平缓释片(Ⅱ)ADR报告数排第一位;药品不良反应的结果,基本痊愈或好转。结论:我市药品不良反应报告来源于医疗机构占比较低,应加强对医疗机构的监测和培训。
关键词:药品不良反应;监测;发生率
中图分类号:F203 文献标识码:A 文章编号:1671-2064(2017)11-0202-03
2016年阜新中心收集、核实、评价、上报ADR报告1001份,每百万人口上报550份。来源于医疗机构占报告总数 50.45%,药品经营企业占报告总数49.55%。严重的和新的ADR病例报告占同期报告总数的15.78%。
1 数据来源
来源于2016年1月1日至2016年11月30日,阜新市药品不良反应监测中心收集、核实、评价并提交至国家药品不良反应监测系统1001例ADR报告。
2 数据处理和统计方法
按照WHO药品不良反应术语集,对药品不良反应名称进行规范和完善,利用Excel软件进行分析统计。
3 药品不良反应发生情况统计
3.1 报告来源及构成(表1)
医疗机构的报告比例较去年同期高3.1个百分点,但还没有达到辽宁省中心考核标准要求(不少于60%)。新的、严重的报告比例较去年同期有所下降。生产企业报告数为零,應加强药品生产企业的培训与日常监测工作的督导。加强药品生产企业第一责任人意识。个人及其他上报的报告中,新的、严重的报告比例较高,应加大对公众宣传、鼓励个人及其他上报。
3.2 报告人情况(表2)
报告人职业以药师为主,397份占同期报告总数的43.56%。严重报告共21例,医生与护士上报14份,占其总数的66.67%。更有价值的报告应来自与患者直接接触的医护人员,所以医护人员是提高报告质量的关健。
3.3 药品不良反应临床情况分析
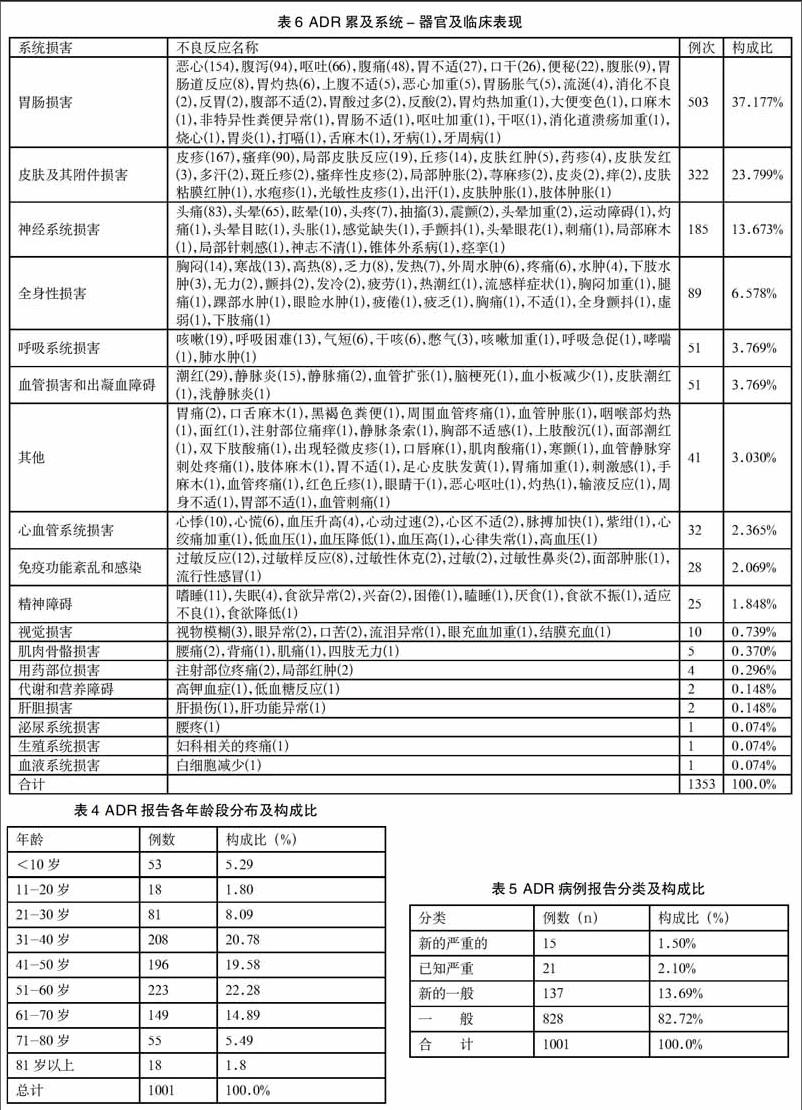
3.3.1 患者基本情况(表3、表4)
药品不良反应发生率女性多于男性,以中年人发生率高,这与我市报告来源于经营企业比例大有关,这个年龄段的人群在药店购买药品自行给药居于多数。
3.3.2 新的、严重的、一般的ADR病例报告分配情况(表5)
新的、严重的报告比例较去年同期有所降低。没有达到世界卫生组织推荐的比例30%。应进一步加强医疗机构监测工作。
3.3.3 ADR累及系统-器官及临床表现(表6)
药品不良反应累及的系统与器官以胃肠系统损害最多达37.177%,其次皮肤及其附件损害达23.799%。
3.4 ADR涉及药品分析
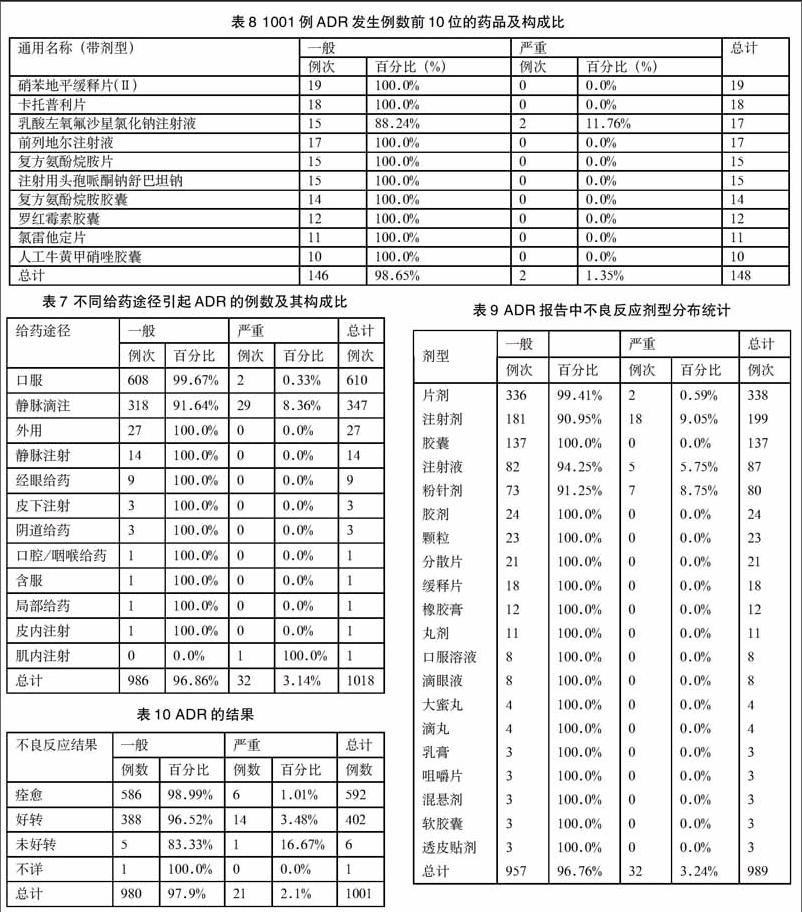
3.4.1 不同给药途径引起ADR的例数及其构成比(表7)
药品不良反应发生以口服最多,其次静脉滴注。口服药占比例多与药品经营企业报告比例大有关,严重报告以静脉滴注最多。
3.4.2 ADR发生例数前10位药药品情况(表8)
降血压药品硝苯地平缓释片(Ⅱ)ADR报告数排第一位,其次是卡托普利片。17年要对硝苯地平缓释片(Ⅱ)、卡托普利片进行重点监测。
3.4.3 不同剂型引起的ADR的例数及其构成比 (表9)
药品不良反应发生最多为片剂,其次为注射剂。严重的药品不良反应发生最多的是注射剂,这是静脉滴注药品不良反应发生率高的原因。
3.5 ADR的结果(表10)
药品不良反应的结果,基本痊全愈或好转,6例未好转,1例不详。
4 讨论
(1)增强生产企业第一责任人意识。阜新辖区内共有三家药品生产企业,全年药品生产企业药品不良反应病例报告数为零,应加强对生产企业监测工作的培训与督导,督导生产企业认真学习贯彻新《办法》,增强生产企业第一责任人意识。
