胆清胶囊的质量标准研究
2017-07-05吴孟岚王定兵龙建丹
苌 玲 吴孟岚 舒 柯* 王定兵 龙建丹 朱 丹
1.贵州省药品检验所,贵州 贵阳 550004;2.黔东南州食品药品检验检测中心,贵州 凯里 556000; 3.贵州圣济堂制药有限公司,贵州 贵阳 550004
胆清胶囊的质量标准研究
苌 玲1吴孟岚2舒 柯1*王定兵3龙建丹3朱 丹3
1.贵州省药品检验所,贵州 贵阳 550004;2.黔东南州食品药品检验检测中心,贵州 凯里 556000; 3.贵州圣济堂制药有限公司,贵州 贵阳 550004
目的:建立胆清胶囊中虎耳草的薄层色谱鉴别及虎耳草中岩白菜素的含量测定方法。方法:采用薄层色谱法对胆清胶囊中虎耳草进行定性鉴别,采用高效液相色谱法测定虎耳草中岩白菜素的含量;色谱柱为Thermo C18(4.6mm×250mm,5μm);流动相以乙腈为流动相A,以0.1%磷酸溶液为流动相B,采用梯度洗脱;流速1mL/min;柱温30℃;检测波长为275nm。结果:薄层色谱鉴别斑点清晰,阴性对照无干扰;岩白菜素在0.05048μg~0.70666μg范围中线性关系良好,r=0.9993,平均回收率为98.01%,RSD为1.39%(n=6)。结论:所建立的方法简便、准确、重复性好,可用于胆清胶囊中虎耳草鉴别和岩白菜素的含量测定。
胆清胶囊;虎耳草;岩白菜素
胆清胶囊是按苗医理论组方的复方制剂,具有清热利湿、舒肝利胆的作用,临床用于肝胆湿热所致的脘胁疼痛、呃逆呕恶、口干口苦、大便秘结,以及胆囊炎、胆石症见上述证候者。胆清胶囊由虎耳草、凤尾草、大黄和牛胆汁四味药材组成[1],方中虎耳草、凤尾草、大黄粉碎成最细粉备用,牛胆汁滤过,与上述最细粉混匀,制成颗粒,干燥,装入胶囊即得。原标准中只有大黄、牛胆汁及凤尾草的薄层色谱鉴别和大黄的含量测定,对组方中成分最多的虎耳草无质量控制标准,为提高该中成药的质量标准,增强用药安全性,特建立虎耳草的薄层色谱鉴别及虎耳草中岩白菜素的含量测定。
1 仪器与材料
1.1 仪器 Waters2695高效液相色谱仪及配套工作站;超声波清洗器(北京医疗设备厂,功率250W,频率33kHz);电子天平(梅特勒XPE205)。
1.2 材料 胆清胶囊(规格为0.3g/粒,批号:20150101、20150301、20150302);阴性样品自制;槲皮素(批号:100081-201408)、岩白菜素(批号: 111532-201203)购自中国食品药品检定研究院。薄层色谱硅胶G(青岛海洋化工有限公司),乙腈为色谱纯、水为超纯水,其他试剂为分析纯。
2 方法与结果
2.1 薄层色谱鉴别 取本品内容物4g,加甲醇20mL,加热回流2h,滤过,滤液加水5mL,蒸去甲醇,残液用石油醚(30~60℃)提取3次,每次5mL,弃去石油醚液,提取后的水溶液加稀盐酸5mL,水浴上加热水解30min,冷却后用乙酸乙酯20mL分2次振摇提取,合并提取液,挥干,残渣加甲醇2mL使溶解,作为供试品溶液;取缺虎耳草的阴性样品同法制成阴性对照溶液;另取槲皮素对照品加甲醇制成1mg/mL的溶液,作为对照品溶液[2]。按照薄层色谱法(《中国药典》2015年版一部附录ⅥB)试验,吸取上述三种溶液各2μL,分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲酸(10∶4∶3)为展开剂,展开,取出,晾干,喷以1%三氯化铝乙醇溶液,在紫外光灯(365nm)下检视。供试品色谱中,在与对照品色谱相应位置上,显相同颜色荧光斑点。结果表明,样品斑点清晰,分离度好,阴性无干扰。见图1。
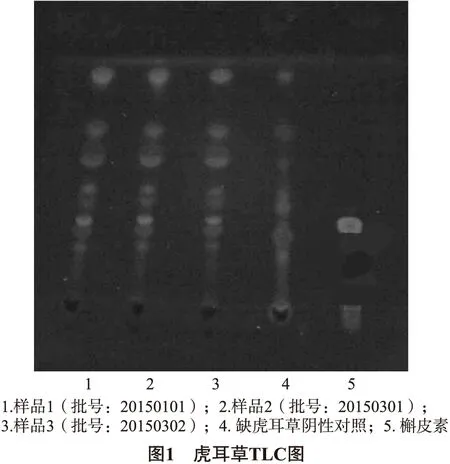
2.2 含量测定
2.2.1 对照品的制备 精密称取岩白菜素对照品,加甲醇制成每1mL含岩白菜素0.04mg的溶液,即为对照品溶液。
2.2.2 供试品的制备 取本品内容物,研细,取1g,精密称定,置具塞锥形瓶中,精密加入50%甲醇25mL,密塞,称定重量,超声处理(功率250W,频率25kHz)1h,放冷,称重,用50%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得供试品溶液。
2.2.3 阴性对照溶液的制备 依照处方工艺,制备缺虎耳草的阴性样品,并按“2.2.2”项下供试品溶液制备方法制备阴性对照溶液。
2.2.4 色谱条件 色谱柱:Thermo-C18(4.6mm×250mm,5μm);流动相:乙腈(A)-0.1%磷酸溶液(B),梯度洗脱(0~20min,9%A;20~22min,9%A→20%A;22~32min,20%A;32~34min,20%A→9%A;34~55min,9%A);检测波长:275nm;流速:1.0mL/min,柱温:30℃;进样量10μL:理论塔板数按岩白菜素计算应不低于5000。结果见图2。2.2.5 线性范围考察 岩白菜素对照品溶液:0.050476mg/mL,进样体积为1、2、4、6、7、10、12、14μL。 按上述色谱条件测定对照品峰面积,以峰面积为纵坐标,岩白菜素的浓度为横坐标绘制标准曲线,得线性回归方程,岩白菜素:y=1569274.1894x+6434.7273,r=0.9993。结果表明岩白菜素在0.05048~0.70666μg范围中线性关系良好。
2.2.6 精密度试验 取上述对照品溶液10μL,按2.2.4项下色谱条件连续进样6次,测定岩白菜素的峰面积。结果岩白菜素峰面积的RSD为0.67%,表明仪器精密度良好。

2.2.7 稳定性试验 取同1份供试品(20150302),按2.2.2项下方法制备,按2.2.4项下色谱条件分别于0、2、4、6、8、10、24h进样,测定岩白菜素峰面积,RSD为0.78%,表明供试品溶液在24h内稳定。2.2.8 重复性试验 取同1份供试品(20150302),按2.2.2项下方法平行制备6份供试品溶液,按2.2.4项下色谱条件测定岩白菜素含量,结果岩白菜素平均含量为0.8999mg/g,RSD为0.51%,表明该方法重复性良好。
2.2.9 加样回收率试验 精密称取已知岩白菜素含量的供试品6份(平均含量为0.8999mg/g),分别精密加入含0.01896mg/mL的岩白菜素对照品溶液25mL,按2.2.2项下方法制备,按2.2.4项下色谱条件测定岩白菜素含量,计算加样回收率,平均加样回收率为98.01%,RSD为1.39%,结果表明该方法回收率较好。结果见表1。
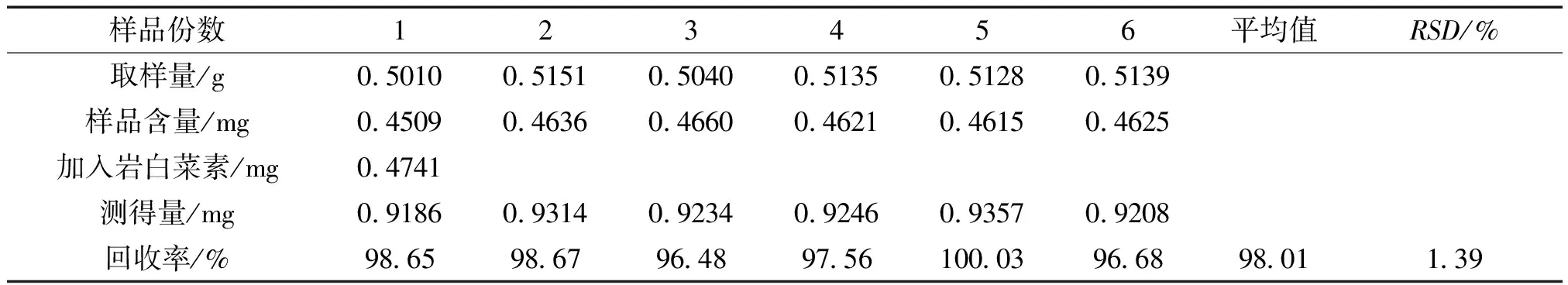
表1 岩白菜素加样回收率试验结果 (n=6)
2.2.9 样品测定 分别精密称取不同批次的供试品粉末1g,按2.2.2项下方法制备,按2.2.4项下色谱条件分别测定峰面积和计算岩白菜素含量,三批样品测定结果见表2。

表2 样品测定 (n=3)
3 讨论
3.1 薄层色谱 试验中分别对温度、湿度、以及薄层板进行了考察,结果表明供试品色谱中,在与对照药材色谱相应的位置上,均显相同颜色的斑点,且斑点清晰,分离度好,阴性无干扰,重现性好。
3.2 供试品的制备 试验中分别对提取方法、提取时间、提取溶剂以及提取溶剂的体积进行了考察,结果表明50%的甲醇25mL超声1h,有效成分提取完全,方法简便。
3.3 检测波长 经查阅资料并对岩白菜素进行光谱扫描后,确定检测波长为275nm。3.4 色谱条件优化 试验中分别比较了不同的流动相系统、柱温及流速,结果以乙腈-0.1%磷酸溶液为流动相,梯度洗脱,柱温30℃,流速1.0mL/min时,色谱峰基线分离,峰型对称,分离较好,保留时间适中。
虎耳草主要化学成分有岩白菜素、槲皮素-3-O-α-L-鼠李糖苷、槲皮素 3-O-β-D-吡喃葡萄糖苷、槲皮素、没食子酸、原儿茶酸、琥珀酸、反甲基丁烯二酸、β-谷甾醇及长链烷烃等[4]。笔者在原标准的基础上经研究,增加了虎耳草的薄层鉴别和含量测定,方法专属性好,灵敏度高,结果稳定可靠,使胆清胶囊的质控标准更趋完善,可有效控制胆清胶囊的质量。
[1]WS-10049(ZD-0049)-2002-2011Z .国家药品标准[S].
[2]贵州省药品监督管理局.贵州省中药材、民族药材质量标准[M]. 贵阳:贵州科技出版社,2003:235.
[3]徐昌艳,张丽艳,李燕. 黔产苗药虎耳草的 HPLC 指纹图谱研究[J].中国实验方剂学杂志,2012,18(5):73-76.
[4]蒲祥,宋良科.虎耳草的研究进展[J].安徽农业科学,2009, 37(31):15224 -15226.
Study on Quality Standard of Danqing Capsule
CHANG Ling1WU Menglan2SHU Ke1*WANG Dingbing3LONG Jiandan3ZHU Dan3
1.Guizhou Provincial Institute for Drug Control, Guiyang 550004,China; 2.Qiandongnan Prefecture Food Drug Inspection Testing Center, Kaili 556000,China; 3.Guizhou Shengjitang Pharmaceutical Co. Ltd.Guiyang 550004,China
Objective To establish a method for the determination of Danqing capsule in the Saxifraga stolonifera by TLC and the content of Bergenin in Saxifraga stolonifera. Methods The TLC method of Danqing capsule in in the Saxifraga stolonifera were identified, the content of Bergenin in Saxifraga stolonifera was determined by HPLC; column chromatography Thermo C18(4.6mm×250mm,5μ), flow phase: with acetonitrile as the mobile phase A, with 0.1% phosphoric acid as mobile phase B, the gradient elution, flow rate of 1ml/min, column temperature 30℃, detection wavelength was 275nm.Results TLC spots were clear, without the interference of negative control; Bergeninum in 0.05048μg~0.70666μg range linear relationship is good,r=0.9993. The average recovery rate was 98.01%,RSD=1.39% (n=6). Conclusion The established method is simple, accurate and with good reproducibility and can be used for the determination of the content of Bergenin in Saxifraga stolonifera in Danqing capsule and the identification of Saxifraga stolonifera.
Danqing Capsule;Saxifragastolonifera; Bergenin
苌玲(1979-),女,本科,主管药师,研究方向为药品复核检验、标准拟定。E-mail:29630048@qq.com
R284.1
A
1007-8517(2017)11-0046-03
2017-04-10 编辑:梁志庆)
