溶胶-凝胶法制备富Li正极材料0.5Li2MnO3·0.5LiMn0.5Ni0.5O2及其特性研究
2017-06-23岳婷青海大学化工学院青海西宁810016
岳婷(青海大学 化工学院,青海 西宁 810016)
溶胶-凝胶法制备富Li正极材料0.5Li2MnO3·0.5LiMn0.5Ni0.5O2及其特性研究
岳婷(青海大学 化工学院,青海 西宁 810016)
在保持电池比容量与电压稳定的条件下,要想提高电池充放电的循环次数,最直接有效的方法就是提高锂离子电池的核心部分-正极材料的的循环充放电次数。我们紧紧抓住提高锂离子电池的正极材料充放电特性的要求,首次尝试了溶胶-凝胶法成功制备了富Li正极材料0.5Li2MnO3·0.5LiMn0.5N i0.5O2。随后,我们借助了XDR(X射线衍射器)、SEM(扫描电子显微镜)、电化学性能测试仪这三种重要仪器对所制备的材料进行研究。结果表明,当我们采用充放电电流密度为20mAh·g-1时,0.5Li2MnO3· 0.5LiMn0.5Ni0.5O2的电化学循环寿命测试结果表明,该材料的容量保持率为86.9%。
锂离子电池;溶胶-凝胶法;0.5Li2MnO3·0.5LiMn0.5N i0.5O2;循环次数
随着青海盐湖提锂工业的快速发展,因地制宜合理有效的扩大锂产品的用途,提高锂产品的可靠性与实用性是促进青海盐湖锂产业的关键,根据我们查阅资料得知,随着经济全球化的发展,石油、煤等不可再生资源日益稀缺,电池储能储能技术的发展被认为是实现可持续性发展的关键,这不仅关系到国家的能源安全,还对生态环境友好起着巨大作用。锂离子电池有着很高的比能量、高功率、高循环寿命等特点,除此之外还有高安全性和环境友好等优点,从而广受关注、成为最理想的储能设备之一,目前其应用领域己从智能手机、笔记本电脑、等便携式移动设备向电动工具、纯电动汽车、甚至宇航卫星等大功率设备转变,在这些关乎国民生活的需求的日常生活劳动中越发举足轻重。因而,发展高比容量、低成本、热稳定性好的正级材料便成为了锂离子电池作为动力电池进程中的关键。经过查阅资料得知,目前锂离子电池负极材料的容量保持率在80%时以上时充放电次数在500次以上,大多数数据显示一般普通电池正极材料的充放电循环次数则一般在200次上下浮动。研究表明多次深度对电池进行充放电时,正负电极材料会对有机电解质溶液有强氧化作用,导致作为正极材料LiCoO2电池的实际可利用的容量仅有理论容量的二分之一左右。目前已经有相关理论表示可以用Mn和Ni来替代LiCoO2中的CO,不但降低了这种材料的成本,还较为明显地提高了材料的安全性和稳定性。富锂层状结构正极材料Li(1+x)k(1-x)02,K可以为,Fe,Co,Ni,Mn, Ti,Cr等多种金属原子,所以组成这种正极材料的物质并不唯一,然而LiCoO2、LiMn2O4(尖晶石)等传统的正极材料在2-4.8V时循环充放电200次后的放电保持率在75%~82%左右,而富锂系列锂离子电池复合材料XLi2MnO3·(1-X)LiMnXNiXO2能够在保持比容量很高的情况下依然有着很好的放电容量保持率。
1 原料的制备
合成原料为青海大学大学实验室提供的分析纯99%的二水醋酸锂(CH3COOLi·2H2O)、分析纯98%的二水醋酸镍((CH3COO)2Ni·2H2O)、分析纯99%的四水醋酸锰((CH3COO)2Mn·4H2O)、分析纯 99.5%柠檬酸(C6H807·H2O).根据0.5Li2MnO3·0.5LiMn0.5Ni0.5O2的化学计量比取一定量的乙酸锉(注意:一定要加入过量的5%的乙酸锉以弥补高温锻烧时的损失)、一定量的乙酸镍、一定量的乙酸锰,与适量的柠檬酸分别加入去离子水中,然后将柠檬酸溶液逐渐滴加到过渡金属盐溶液中不断搅拌,滴加完成后用稀氨水调节混合液的pH值稳定在8~9之间,后将溶液置于水浴中加热5~10分钟蒸发至绿色凝胶状,控制水浴温度在90℃~100℃之间,在真空干燥箱80℃中干燥12h后取出压成圆片,转移至马弗炉中450℃缎烧5h,冷却后,将圆片研磨至细粉状,再次压成圆片,置于马弗炉中900℃锻烧24h,随炉冷却后取出研磨至细粉状,得最终产物0.5Li2MnO3·0.5LiMn0.5Ni0.5O2。
2 结果与分析
2.1 XRD图谱分析
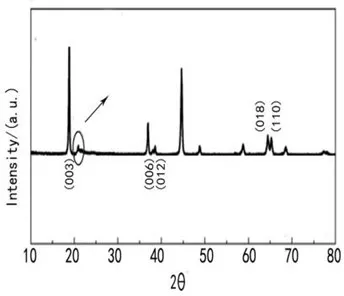
图1 :材料的XRD图谱

图2 :SEM图
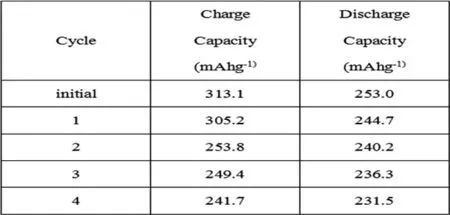
图3 :电池前四周充放电量
层状富锂材料XLi2MnO3·(1-X)LiMn0.5Ni0.5O2包含两种组分LiMnO2与LiNi0.5O2中,LiNi0.5Mn0.5O2具有相同的α-NaFeO2型属于六方晶系R3m空间点阵群,而在另一组LiMnO3中过量的层状结构,Li+在过度金属层中与Mn4+以1:2的比例占据α-NaFeO中Fe3+位,形成LiMn6超结构致其晶格结构,致其晶格对称性较与LiNi0.5Mn0.5O2有所下降,但仍具有由α-NaFeO2衍生而来的层状结构.因此正如图1中所示,(006)/(012)、(018)/(110)两对峰分裂明显,表明具有良好的层状结构.Li+在Li2MnO3组分过渡金属层中形成的LiMn6超结构在XRD表征中表现为2θ=200一25o区域内微弱的超晶格衍射峰强相应增大,这一结构特点在所制备的材料中均得到了体现(图中所圈出来的),且随着Li2MnO3组分的增多,2θ=200一250处微弱的衍射峰峰强相应增大.Li2MnO3有别于LiNi0.5Mn0.5O2的这-结构特点,使得两者相对含量发生变化时,对合成的材料结构产生了影响。
2.2 扫描电子显微镜分析
图2为所制备的材料的SEM图,放大倍数为50000倍.图中可见,材料在形貌上颗粒均匀但呈无规则团聚状,一次粒子粒径较小,均在准微米尺度.很好的反映了材料的六方晶系结构。
2.3 电化学性能测试
材料如图(3)所示xLi2MnO3,·(l-x)LiMn0.5Ni0.5O2的首次充电过程可分为两个阶段,当终止电压在4.5V以下时,Li+的脱嵌伴随Ni2+/4+的氧化还原反应进行,当终止电压在4.5V以上时,则出现一个较长的平台,该平台对应于富锂材料的电化学活化过程.其电池的充放电中涉及的反应,当电压大于4.5V时其充电容量来自于LiMnO3组分的脱锂过程,故当x升高时,4.5V以上的首次充电容量应增大,这与图中实验结果一致.且由图中结果可知充放电压范围为2.0~4.5V。由循坏性能图可知经过多次循环后材料在3.5V以下由于LiMnO3活化后引起的氧化还原反应,其氧化还原电位向低电压方向偏移,由图知的充放电容量为225.3mAh/g,容量保持率86.9%。
3 结语
本文以凝胶溶胶法成功合成了富Li正极材料0.5Li2MnO3· 0.5LiMn0.5Ni0.5O2所用的溶胶一凝胶法具有纯度高、合成时间短、产物粒径小、均一性好等诸多优点,易实现分子水平上的均匀混合,相比固相法等合成方法,较大程度地减少了合成工艺对实验结果的影响,其电池首次充放电量为305.2mAh/g,244.7mAh/g,容量保持率为86.9%
[1]Simultaneous thermogravimetry and differential thermal analysis for comparing burning characteristics between oleaginous and non-oleaginousmicroorganisms[J].Bongmun Kang,Kohsuke Honda,Tsunehiro Aki,TakeshiO masa,HisaoOhtake.2011(1).
[2]Kinetic analysis on LiFePO 4 thin films by CV,GITT,and EIS[J].Kun Tang,Xiqian Yu,Jinpeng Sun,Hong Li,Xuejie Huang. Electrochimica Acta.2011(13).
