骨碎补的研究概况
2017-06-09马洪娜魏升华檀龙颜
马洪娜 魏升华 檀龙颜
贵阳中医学院药学院,贵州 贵阳 550025
骨碎补的研究概况
马洪娜 魏升华 檀龙颜*
贵阳中医学院药学院,贵州 贵阳 550025
骨碎补为临床常用中药,具有疗伤止痛,补肾强骨等功效。骨碎补资源分布是影响其开发利用的关键因素。生药学特性是药材的质量评价及其与混伪品的鉴别的依据。骨碎补炮制工艺的优化能够提高饮片的质量。提取工艺的优化能为药材有效成分的工业化生产提供可靠的技术支持。此外,药物代谢动力学和代谢组学的研究能为药材的临床应用提供良好的参考依据。文章从骨碎补在资源调查、生药学鉴定、炮制工艺、提取工艺、药物代谢动力学和代谢组学等方面的研究进展情况进行概述。
骨碎补;资源;质量;临床应用;研究概况
骨碎补为蕨类植物槲蕨Drynariafortunei(Kunze) J. sm.(槲蕨科Drynariaceae槲蕨属Drynaria植物)的干燥根茎[1]。其味苦温,归肝、肾经,具有疗伤止痛,补肾强骨,消风祛斑的功效[1]。临床用于跌扑闪挫、筋骨折伤、肾虚腰痛、筋骨痿软、耳鸣耳聋、牙齿松动等症,外治斑秃和白癜风[1]。近年来,由于骨碎补良好的药用价值,在资源调查、生药学鉴定、炮制工艺、提取工艺、药代动力学和代谢组学等方面的研究取得了明显的成效。笔者在系统查阅和整理相关文献资料的基础上,对骨碎补涉及以上领域的最新研究结果进行系统的总结,并对该领域存在的问题和前景进行探讨,旨在为骨碎补资源的保护、合理开发和可持续利用提供参考。
1 资源调查
骨碎补原植物喜温暖湿润气候,多附生于树干或林中岩石上。虽然分布较广,但生长环境特殊,且生长缓慢。黄宝优等[2]采用走访和实地调查相结合的方法,对广西骨碎补种质资源分布和生物生态学特性进行了调查研究。发现槲蕨在人为破坏较少的环境下,植株较大,根茎较粗;反之则反,且带孢子的成龄植株也较难采到[2]。近年来,广西骨碎补生境遭到一定程度的破坏,而破坏的生境较难恢复[2]。邹珊珊等[3]查阅了大量文献资料,整理了1400份以上槲蕨及其混淆品标本资料,并到野外实地调查,分析了槲蕨的本草考证、生态环境以及在中国的野生资源分布。结果表明,尽管历代本草对于骨碎补均有记载,但并非为同一种[3]。通过中药材产地适宜性分析地理信息系统(TCMGIS)系统数据库分析显示,槲蕨在中国主要分布于长江流域以南的亚热带季风地区中低海拔的山区[3]。根据文献和标本的结果显示野生槲蕨主要分布于安徽、福建、广东、广西、贵州、湖北、湖南、江西、四川、重庆、云南、浙江等省[3],详见表1。由于对野生资源的盲目采挖,造成野生资源破坏严重,所以亟待建立相应的保护措施。
邹珊珊等[3]到大中型中药材市场实地调查走访多家铺面、零售摊位及药材加工站点,分析了骨碎补的商品产地来源、混淆品种类、产量、销售等情。调查结果显示,骨碎补药材主要来源于安徽、广西、贵州、湖北、湖南、四川、重庆、云南和甘肃,详见表1。混伪品情况调查表明,文献记载混伪品包括槲蕨属8种(中华槲蕨D.sinacaDiels、团叶槲蕨D.boniiChrist、川滇槲蕨D.delavyiChrist、栎叶槲蕨D.quercifolia(L.) J.Sm、石莲姜槲蕨D.propinqua(Wall. ex Mett.) J. Sm. ex Bedd.、小槲蕨D.parishii(Bedd.) Bedd.、毛槲蕨D.mollisBedd.、硬叶槲蕨D.rigidula(Sw.) Bedd.)、骨碎补科4种(圆盖阴石蕨HumatatyermanniiT. Moore、大叶骨碎补DavalliaformosanaHayata、海州骨碎补H.tyermanniiT. Moore、鳞轴小叶膜盖蕨Araiostegiaperdurans(H.Christ) Copel)、水龙骨科3种(崖姜蕨Phymatosoruscuspidatus(D. Don) Pic. Serm.、光亮瘤蕨Phymatosoruscuspidatus(D. Don) Pic. Serm.、光亮密网蕨Phymatodeslucida(Roxb.) Ching),而市场走访调查发现市售混淆品主要有中华槲蕨、石莲姜槲蕨、团叶槲蕨、大叶骨碎补、川滇槲蕨、光叶槲蕨(D.propinqua(Wall. ex Mett.) Bedd.)等6种,详见表1。产量情况调查表明,广西、贵州、云南和湖北4省的产量占据安国、亳州中药材市场上骨碎补货源约90%,但数据包含混伪品的产量,详见表1。从销售情况来看,多数商家认为产于湖北、贵州的为正品,故价格较高[3]。因此,尽管历代本草记载种不同,但应按中国药典规定使用槲蕨。市场销售的骨碎补药材的混伪品较多,应加强区分和市场监管以保证群众利益。从市场供求关系分析表明开展人工育苗和栽培技术研究、建立种植基地方能保障市场供应[3]。

表1 骨碎补分布省份、混伪品种类及产地来源
2 生药学研究
张炎兵等[4]对骨碎补原植物的植株高度、叶型以及营养叶、能育叶和孢子囊群的形态特征做了详细描述,从分类学角度为鉴定其原植物提供了明确的依据。在骨碎补药材性状方面,从形状、长、宽、高、表面颜色及附属物、药材质地和气味等特征方面做了详细的观察和研究。对根茎横切面的鳞片、表皮、维管束和薄壁组织等的结构特性进行了显微观察[4]。利用薄层色谱法对骨碎补粉末特征检验发现,骨碎补供试品色谱中,在与柚皮苷对照品色谱相应的位置上,显示出相同颜色的荧光斑点[4]。此外,Sun等[5]利用分子生物学手段对骨碎补叶绿体全基因组进行了测序,为骨碎补的分子生药学研究奠定了基础。以上研究结果从植物基源、药材性状、粉末特征和薄层色谱鉴别等几个方面为骨碎补药材的鉴定提供了基本的分析依据。
高厚明等[6]测定了10批不同产地骨碎补中柚皮苷、新北美圣草苷和E-4-O-β-D 葡萄糖酰咖啡酸等3种成分含量,建立了骨碎补药材的高效液相色谱(HPLC)指纹图谱,标定8个共有峰,其中5个共有峰的化学成分尚待确定(图 1)。同时,白俊鹏等[7]也利用HPLC方法测定了16批不同产地骨碎补中E-4-O-β-D-吡喃葡萄糖基香豆酸、咖啡酸-4-O-β-D-吡喃葡萄糖苷,5,7,3’,5’-四羟基二氢黄酮-7-O-β-D-吡喃葡萄糖苷和柚皮苷等4种成分的含量,建立了相应的指纹图谱,标定了12个共有峰,确定了6个峰,详见图2。骨碎补HPLC指纹图谱方法特征性及专属性强,可从定性和定量两方面分析和评价骨碎补药材的内在质量,优于常规的单一指标评价方法。

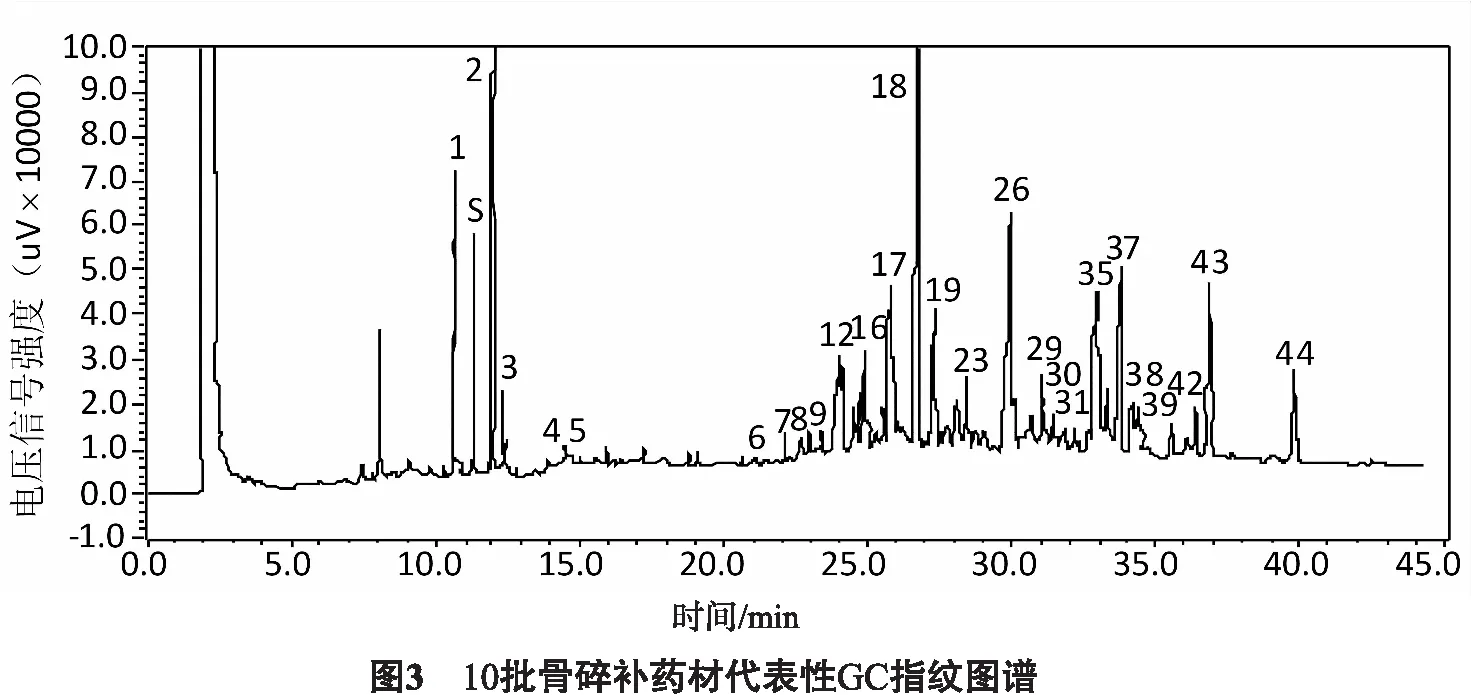
李晓红等[8]利用索式提取法对19批(10批正品、9批伪品)骨碎补药材中的脂溶性成分进行提取,并建立了骨碎补脂溶性成分的气相色谱(GC)指纹图谱。确定了10批骨碎补正品药材的GC指纹图谱中共有峰44个,详见图3,利用主成分分析法(PCA)对指纹图谱进行统计分析表明10批正品结果聚集在一起,而另外供试的9批伪品结果分散在图中不同区域,表明正伪品区分结果良好,且不同基源的药材化学成分差异明显[8]。因此,利用GC指纹图谱鉴定骨碎补中脂溶性成分有助于准确地评价药材的质量。

中药材的微量元素一方面能够补充和调节人体所缺乏的各种微量元素,另一方面能够通过吸收、络合等方式达到治病的效果,因此微量元素的含量也是评价骨碎补质量的一个重要指标。采用电感耦合等离子体原子发射光谱(ICP-AES)法对宁夏、四川、福建等不同产地骨碎补粉剂中微量元素进行测定,结果显示产于宁夏的骨碎补药材中Na、Ca、Zn、Fe的含量高于其他产地,而产于四川的骨碎补药材中K、Mg含量高于其他产地[9]。表明骨碎补的产地可能对其微量元素含量有影响。
国家规定铅(Pb)、镉(Cd)、砷(As)、汞(Hg)、铜(Cu)等元素为中药材重金属残留检测方面的主要指标。王永来等[10]利用原子吸收分光光度法和原子荧光光谱法对10批不同产地的骨碎补药材进行了上述5种重金属元素的残留量分析。结果显示,铜为2.6875~8.5217mg/kg,镉为0.2006~0.2708mg/kg,铅为0.2504~1.0000mg/kg,汞为0.0034~0.0294mg/kg,砷为0.0066~0.0533 mg/kg,均符合药典对重金属标准的规定[10]。该方法的建立有助于中药材中重金属残留量检测方法的标准化,同时为中药材的质量控制提供科学依据。
中药材与其混伪品的鉴定有多种方法,显微鉴定是广泛应用的方法之一。骨碎补入药部位为根茎,而根茎上的鳞片在蕨类植物的分类学上具有重要的意义,所以骨碎补根茎上的鳞片能够为药材的鉴定提供重要的依据。朱迎夏等[11]利用光学显微镜、扫描电子显微镜及石蜡切片方法观察了骨碎补、川滇槲蕨、栎叶槲蕨和崖姜的根状茎鳞片的形态特征。结果显示,骨碎补、栎叶槲蕨和崖姜根状茎的鳞片基在表皮凹陷处着生且分布较均匀,而川滇槲蕨根状茎的鳞片基在表皮凸起处着生且分布较为稀疏[11]。程茂高等[12]利用石蜡切片法观察了骨碎补和普通凤丫蕨根状茎的横切面,同时采用粉末鉴定法对二种药材根状茎上的鳞片进行观察,发现骨碎补根状茎横切面维管束10~20个,鳞片长7~12mm,宽0.8~1.5mm,边缘着生睫毛状锯齿,普通凤丫蕨根状茎横切面维管束2~3个,鳞片,长1~6mm,宽0.3~1.0mm,全缘。性状观察发现,骨碎补药材断面纤维性,红棕色,维管束黄色点状,而普通凤丫蕨药材断面较平坦,灰白色,维管束白色弧形[12]。后含物观察发现骨碎补药材粉末中淀粉粒含量极少,而普通凤丫蕨药材粉末中含有大量淀粉粒[12]。这些结果表明鳞片的着生位置、稀疏程度及形态特性,横切面及维管束特性等均可作为骨碎补及其混伪品显微鉴别的重要参考依据。
以上分析表明,对于骨碎补药材及其与混伪品的鉴定可通过基源鉴定、性状鉴定、显微鉴定、薄层色谱、液相色谱、气相色谱、微量元素含量测定和重金属含量测定等多种方法相结合的方式进行,此外,分子生物学手段能为骨碎补的基源鉴定提供更精确的数据。为骨碎补的质量控制提供充分的依据,并确保广大患者用药安全、稳定和有效。
3 炮制工艺
砂烫法为骨碎补炮制的主要方法,药材经过砂炒后可以提高活性成分柚皮苷等的溶出率[13]。李静等[13]研究了骨碎补的砂烫炮制工艺,首先对加热温度、加热时间、油砂用量等单因素进行优选,再用柚皮苷、黄酮、煎出物含量和膨胀率等指标进行正交设计实验优选。结果表明210℃、加热烫3min、用6倍油砂为砂烫骨碎补的最佳炮制工艺。该工艺炮制出的骨碎补柚皮苷、黄酮、煎出物含量和膨胀率等指标最佳,参数量化,可操作性强,为骨碎补砂烫炮制工艺规范化提供了可靠数据。然而,赵清等[14]在研究骨碎补砂烫制品中柚皮苷含量下降的原因时,发现投药量与柚皮苷含量成负相关,单锅烫制药材投药量过大会造成炮制过火以致成品质量下降,因此在骨碎补烫制过程中投药量不宜过大。
目前临床上骨碎补以砂烫品入药居多,砂烫后质地松脆、鳞片易去除、便于调剂和制剂等[15],但砂烫法也存在诸多缺陷,如不易控制质量、操作费时费工费力、不宜大量炒制。膨化炮制法是将食品膨化技术应用于中药炮制,通过该技术使硬质药材在一定的温度和压力下均匀受热,之后突然减压以破坏药材内部分子间的引力,从而使药材质地疏松[15]。采用正交实验法,以压强和保温时间为因素,并以柚皮苷的含量为指标优选炮制工艺,发现最佳膨化条件为膨化压力2.0kg/cm2,膨化保温时间4min[15]。以水浸出物量和柚皮苷含量为指标考察骨碎补膨化品和砂烫品发现,膨化品中水溶性物浸出量和柚皮苷含量均较高,表明膨化炮制法优于砂烫法[16]。
古人认为骨碎补盐炙走肾,益增补肾之功[17]。耿妍等[18]比较了传统砂烫工艺和改良砂烫工艺(先润盐水后烫品和先烫后润盐水品),发现先润后烫品中柚皮苷含量最高。随后,确定先用盐水闷润再砂烫至鼓起的炮制方法,并对其具体工艺参数进行优选[18]。单因素实验分别考察了盐溶液用量、盐用量、浸泡时间和砂烫温度等因素对评价指标柚皮苷的含量影响,之后选择盐用量、浸泡时间和砂烫温度为考察因素,并以柚皮苷的含量为评价指标进行正交实验。结果显示,每20g药材用30mL盐水(含4g盐),浸泡8h,在190℃下砂烫4min为最佳工艺[18]。蒋晓煌等[19]用食盐代替油砂对骨碎补进行烫制,以柚皮苷、总黄酮、煎出物量、去毛、膨胀率为评价指标,选择加热温度、加热时间、食盐用量为因素水平,采用正交设计法优选盐烫骨碎补的炮制工艺。结果显示,210℃、加热烫制3min、食盐用量为骨碎补量10倍为盐烫骨碎补的最佳炮制工艺[19]。尽管砂烫品和先润盐水后烫品在水分、灰分和醇溶性浸出物等指标方面均符合药典标准,但化学成分上存在明显差异[20]。与砂烫品相比,先润盐水后烫品中1-咖啡酰葡萄糖苷和4-乙酰基-3,5-二甲氧基苯甲酸的含量略微降低,而新北美圣草苷和圣草次苷的含量明显降低,但表没食子儿茶素、北美圣草素-7-O-β-D-吡喃葡萄糖苷、北美圣草素-7-O-[6″-(3‴-羟基-4‴-甲氧基肉桂酰)]-β-D-吡喃葡萄糖苷和柚皮苷的含量则明显升高[20]。因此,骨碎补砂烫品和先润盐水后烫品在临床功效上存在差异可能是由于炮制后化学成分的差异造成的[20],临床上可以根据不同疾病情况选择相应的中药饮片。
微波炮制方法是将骨碎补段置于输出功率为750W的微波炉中,铺叠成1cm厚,中火烘烤2min,取出,冷却后去毛[21]。杨梓懿等[21]研究了微波法和砂烫法对骨碎补中总黄酮和水溶性浸出物含量的影响,与砂烫法相比,微波法炮制的骨碎补中总黄酮和水溶性浸出物的含量均较高,表明微波法优于砂烫法。微波法炮制有利于成分的溶出可能与微波的强穿透力有关[19]。
4 提取工艺
4.1 柚皮苷提取工艺 大孔吸附树脂分离技术是利用大孔吸附树脂的多孔结构和选择性吸附功能从中药提取液中分离精制有效成分的技术。杨蕾等[22]通过静态、动态吸附和解吸相结合的方法,以柚皮苷的吸附率、解吸率为评价指标综合评定树脂型号,并通过考察上柱药材量、上样流速、洗脱乙醇浓度和洗脱溶剂用量等确定纯化工艺条件。结果表明,HPD-100型大孔吸附树脂为最佳型号树脂,药材-大孔吸附树脂为1:1的质量比上样,上样流速为3BV/h,以8倍柱体积水洗,之后以14倍柱体积50%乙醇洗脱为最佳提取工艺条件。方婧等[23]研究了柚皮苷微波协助提取法,并与药典提取方法进行比较。微波提取条件为时间5min,提取温度120℃,提取溶剂50%甲醇,与药典法提取柚皮苷方法相比具有提取率高、简便快速、结果准确等优点。以上结果表明大孔吸附树脂法和微波提取法均为柚皮苷提取的有效方法。
4.2 总黄酮提取工艺 黄艳萍等[24]利用正交实验法,研究了浸泡时间、溶剂量、提取次数和超声时间对骨碎补总黄酮提取率的影响,确定了骨碎补总黄酮超声提取法的最佳条件为加60倍量的水,浸泡4h,超声提取4次,每次20min。超声提取法提取骨碎补总黄酮的量明显高于传统的乙醇回流法,且超声提取法具有操作简单、省时、提取效率高等优点,表明其在中药提取方面有着良好的前景。
张全香等[25]利用静态吸附方法对5种不同树脂纯化骨碎补总黄酮的富集效果进行比较,并对分离纯化总黄酮的工艺进行了优化。结果表明,在室温及pH值4.0条件下,骨碎补总黄酮分离纯化的最佳树脂为HPD-BJQH,50%乙醇溶液为最佳解吸液,10mL/min为最佳流量。岳春华等[26]利用顶空气相色谱法测定了3批骨碎补总黄酮中大孔树脂残留物苯、甲苯、二甲苯、苯乙烯、二乙烯苯及正庚烷的含量,结果表明,3批样品中均未检出以上6种大孔树脂残留物。因此,采用顶空进样气相色谱法测定大孔树脂残留物能够取得良好的效果,而且方法易于操作,分离度高,重现性好,结果准确[26]。
近年来,中药提取工艺采用多种方法进行研究分析,试验结果在一定程度上能反映固定因素水平下的最佳工艺,但某一因素水平发生变化后将无法快速确定对提取结果的影响,提取动力学模型能够很好地解决该问题。张晋等[27]以骨碎补中的总黄酮为测定指标,研究了水煎煮过程中的提取动力学机制,并拟合出提取动力学方程。利用该动力学模型能较好地验证试验结果,且标准偏差均控制在工业可接受范围内。因此,该模型的建立对于水煎煮法提取骨碎补中总黄酮的生产工艺及骨碎补配方颗粒的生产工艺研究具有一定指导意义,随着模型的不断完善将最终达到指导科研与实际工业生产的作用。
5 药物代谢动力学研究
近年来,传统中药的临床应用功效和安全越来越受到关注,药物代谢动力学研究能够为药材的临床应用提供良好的参考。Li等[28]利用超高效液相色谱串联质谱(UPLC-MS/MS)技术对大鼠口服骨碎补提取物后血液中柚皮苷及其代谢物柚苷元的药物代谢动力学进行了研究。结果表明,小鼠口服骨碎补提取物后,血液中柚皮苷和柚苷元的药峰浓度分别是(2.56±0.77)×103ng/mL和(222±45)ng/mL,药峰时间分别为(0.67±0.20)h和(8.0±1.3)h,血药浓度-时间曲线下面积从0h到最后一个可检测浓度分别计算为(3.23±0.54)×103ng/mL·h-1和(1.57±0.37)×103ng/mL·h-1,血药浓度-时间曲线下面积从0 h到∞可计算为 (3.29±0.54)×103ng/mL·h-1和(1.79±0.43)×103ng/mL·h-1,柚皮苷消除半衰期为(4.1±0.8)h,且在8h时还可以看到1个小峰。该方法具有快速、灵敏、专一性强等特性,所获得的柚皮苷及柚苷元的药物代谢动力学参数可为骨碎补的临床应用提供参考。谢雁鸣等[29]通过反相高效液相色谱法测定了大鼠血清和组织中柚皮苷的含量。将18只大鼠分成3个剂量组,按骨碎补总黄酮0.3、0.6、1.2g/kg的剂量灌胃,在用药后30~480min内每隔30分钟取眼底动脉或股动脉血清测定柚皮苷含量。柚皮苷于30min开始吸收,90min达到高峰,灌胃后4h血药浓度明显下降,灌胃后8h仍有一定血药浓度,表明骨碎补柚皮苷吸收较缓,在血中保持时间较长,消失较慢。组织中柚皮苷含量的测定结果显示以胃、肠为最高,但下降迅速;其次肝、肺、肾较高,肌肉、脂肪也有一定分布,脑组织含量甚低。这些结果表明,反相高效液相色谱法具有简便、灵敏、快速,不受样品基质中杂质干扰等特性,适用于大鼠血清和组织中柚皮苷的测定。
群体药代动力学可根据患者个体差异制定个体化给药剂量,将经典的药代动力学基本原理与统计学模型相结合,定量描述患者生理、病理、合并用药等多种个体差异对药物代谢的影响,分析药物代谢动力学特性中存在的变异性,考察患者群体中药物浓度的决定因素[30]。Wang等[31-32]观察了强骨胶囊(骨碎补总黄酮)中柚皮苷在中国女性原发性骨质疏松症患者中群体药代动力学特征。观察的女性患者年龄40~80岁,共98名,居住于北京东直门等5个社区。血液样本在患者口服强骨胶囊(250mg含75mg柚皮苷)后0.5、1、2、3、4、6、8、10、 12和24h收集。利用高效液相色谱串联质谱(HPLC-MS/MS)测定血液样本中的柚皮苷含量,采用非线性混合效应模型软件对群体药代动力学数据进行分析。选取药物清除率(C1 )、中央分布容积(v)、吸收速率常数(ka1)、外周分布容积(vii)和室间清除率(clii)作为参数,并通过基础模型、协变量模型和最终模型进行评估。肾阳虚、肝肾阴虚、年龄、身高、血尿素氮、血清肌酐、丙氨酸转氨酶、天冬氨酸转氨酶、高脂血症等作为协变量。通过正向和逆向模型化建立模型。最终模型通过内部验证、外部验证和可视化预测等进行评估。结果显示最终模型C1、肾阳虚对C1的影响、v、ka1、clii和vii的群体参数分别为37.6μg/L、0.427L、123 L/h、0.12/h、0.3056和1.446,高脂血症和肾阳虚是重要的协变量。结果表明群体药代动力学模型可以有效地表征一剂口服强骨胶囊在中国原发性骨质疏松症患者中的药代动力学特征。
6 代谢组学研究
代谢组学是对生物体内所有代谢物进行定量分析,并寻找代谢物与生理病理变化的相对关系的研究技术,这符合传统中药的完整性和系统性的特征[33]。该技术能为解决中药疗效、中药治疗疾病的分子机制、中药质量控制及新药开发等提供良好的支持。Lu等[33]利用代谢组学技术研究了氢化可的松诱导的大鼠肾阳虚证及骨碎补提取物对该疾病的疗效。采用UPLC/MS技术对大鼠尿液的代谢谱进行检测,并用PCA法对代谢谱差异进行分析。与对照组相比,模型组大鼠的苯丙氨酸和苯乙酰甘氨酸(肠道细菌消化苯丙氨酸的代谢物)表达量上调,苯丙氨酸的上调能够抑制饮食的消化,且在模型组中也发现大鼠食欲下降的情况。模型组大鼠的N2-琥珀酰-L-鸟氨酸(肠道细菌对精氨酸消化的代谢产物)和L-脯氨酸表达量也上调,N2-琥珀酰-L-鸟氨酸和L-脯氨酸均参与精氨酸代谢途径,表明肾阳虚证影响了氨基酸代谢。与对照组相比,模型组大鼠的肌氨酸酐和柠檬酸表达量下调,二者主要参与能量代谢,表明肾阳虚证与能量代谢的机能障碍有关,且在模型组中也发现大鼠肢体温度下降的现象。苯酰胺基醋酸盐是肠道细菌对苯丙氨酸的代谢产物,能够通过干扰羟基化作用来保护肾组织,该化合物的表达量下降可能是肾阳虚证中肾损伤的表现[27]。苯乙酰甘氨酸、N2-琥珀酰-L-鸟氨酸和苯酰胺基醋酸盐均为肠道细菌的代谢产物,所以肾阳虚证能够干扰肠菌群。与模型组相比,骨碎补提取物治疗组中肌氨酸酐和柠檬酸表达量上调,所以骨碎补能够增强能量代谢及线粒体的功能[33]。与模型组相比,治疗组中苯丙氨酸、苯乙酰甘氨酸、N2-琥珀酰-L-鸟氨酸和L-脯氨酸表达量下调,而苯酰胺基醋酸盐表达量上调[33]。以上结果表明肾阳虚证能够干扰氨基酸代谢、能量代谢和肠道菌群的稳态,而骨碎补提取物对由氢化可的松诱导的肾阳虚证有显著的疗效。同时表明代谢组学是研究中药疗效机制的有力工具[33]。Liu等[34]也利用代谢组学技术研究了骨碎补提取物的抗骨质疏松症效应及作用机制,利用UPLC-MS/MS技术获得对照组、模型组和治疗组血浆的代谢谱,并利用PCA法和偏最小二乘判别分析(PLS-DA)法对数据分析。结果表明,与对照组相比,模型组中溶血磷脂胆碱、色氨酸和苯丙氨酸的表达量明显上调,而治疗组中这3类化合物的表达量与对照中相近。因此,骨碎补提取物对骨质疏松症具有明显的疗效,且对骨质疏松症的治疗可能是通过干预抗氧化剂-氧化平衡、色氨酸和苯丙氨酸代谢途径进行。
7 小结
骨碎补作为常用中药,在民间有着广泛的药用经验和历史。对其化学成分和药理作用机制已经有广泛的研究,但在其他方面的研究仍存在诸多不足。如:生药学鉴定方面还缺乏完善的标准;单一炮制和提取工艺不能满足多方面的需要等。笔者认为今后应从以下几方面开展工作:对种质资源进行深入调查,同时探索骨碎补仿野生栽培技术和其他人工繁殖技术,为药材的保护和可持续利用提供保障;完善药材质量标准,为药材的鉴别、分级和商品化规格等提供依据;优化炮制和提取加工技术,指导科研和工业化生产;利用代谢组学和药物代谢动力学等现代技术研究药材的药效和治疗的分子机制,为临床用药安全提供有效的参考。相信随着研究的不断深入,作为常用中药的骨碎补在未来的疾病治疗中将会有更好的应用前景。
[1]国家药典委员会. 中华人民共和国药典(一部)[S]. 北京: 中国医药科技出版社, 2015: 256.
[2] 黄宝优, 黄雪彦, 彭玉德, 等. 广西骨碎补种质资源调查研究[J]. 湖北农业科学, 2014, 53(16): 3832-3834, 3839.
[3] 邹珊珊, 张本刚, 孙红梅, 等. 骨碎补药材的资源调查与分析[J]. 中国农学通报, 2011, 27(6): 374-379.
[4] 张炎兵, 田军明. 骨碎补的生药研究[J]. 中医药导报, 2013, 19(12): 104, 107.
[5] Sun M, Li J, Li D, et al. Complete chloroplast genome sequence of the medical fern Drynaria roosii and its phylogenetic analysis [J]. Mitochondrial DNA Part B: Resources, 2017, 2(1): 7-8.
[6] 高厚明, 熊明玲, 刘凯南, 等. 骨碎补多指标成分指纹图谱控制与药材质量[J]. 中国中医药现代远程教育, 2013, 11(23): 158-159.
[7] 白俊鹏, 尚振苹, 蒋晓文, 等. 骨碎补高效液相指纹图谱研究及主要成分含量测定[J]. 国际药学研究杂志, 2015, 42(3): 398-403.
[8] 李晓红, 姜明燕, 熊志立. 骨碎补药材脂溶性成分的气相色谱指纹图谱[J]. 山西医药杂志, 2013, 42(11): 1211-1212.
[9] 李玲, 樊学敏, 赵燚, 等. 不同产地骨碎补微量元素含量的比较研究[J]. 宁夏医学杂志, 2014, 36(9): 812-814.
[10] 王永来, 熊明玲, 陈红军. 原子吸收分光光度法测定骨碎补药材中的重金属[J]. 中国药业, 2011, 20(13): 19-21.
[11] 朱迎夏, 张本刚, 齐耀东, 等. 中药材骨碎补及其混淆品的显微鉴定方法研究[J]. 中国中药杂志, 2012, 37(8): 1152-1156.
[12] 程茂高, 乔卿梅, 韦小敏, 等. 中药骨碎补与混伪品普通凤丫蕨的鉴别研究[J]. 时珍国医国药, 2016, 27(5): 1132-1133.
[13] 李静, 蒋晓煌, 周孟辉, 等. 正交法优选砂烫骨碎补的炮制工艺[J]. 中国医院药学杂志, 2010, 30(4): 306-308.
[14] 赵清, 郝丽静. 影响手工烫制中药骨碎补质量的因素分析[J]. 内蒙古中医药, 2009, 28(20): 33, 51.
[15] 袁叶飞, 甄汉深, 欧贤红. 正交试验法优选骨碎补膨化炮制工艺的研究[J]. 云南中医中药杂志, 2006, 27(1): 50, 37.
[16] 袁叶飞, 甄汉深, 欧贤红. 骨碎补膨化炮制实验研究[J]. 时珍国医国药, 2006, 17(7): 1230-1231.
[17] 吕侠卿.中药炮制大全[M] .长沙:湖南科学技术出版社, 2004: 193.
[18] 耿妍, 赵启苗, 贾天柱. 正交法优选盐炙骨碎补的最佳炮制工艺[J]. 时珍国医国药, 2007, 18(10): 2501-2502.
[19] 蒋晓煌, 蒋孟良, 李静, 等. 盐烫骨碎补炮制工艺的研究[J]. 中药材, 2012, 35(11): 1751-1754.
[20] 陶益, 蒋妍慧, 李伟东, 等. 骨碎补不同炮制品化学成分的差异研究[J]. 现代医药卫生, 2015, 31(23): 3549-3551.
[21] 杨梓懿, 于定荣, 赵宏冰, 等. 微波炮制对骨碎补中总黄酮及浸出物含量的影响[J]. 中成药, 2005, 27(4): 427-429.
[22] 杨蕾, 柏艳柳, 王永, 等. 大孔树脂纯化骨碎补中柚皮苷的工艺[J]. 中国医院药学杂志, 2011, 31(23): 1950-1952, 1990.
[23] 方婧, 杨洪军, 付梅红, 等. 微波协助提取在中药饮片含量测定中的应用(4)—微波法与药典法测定骨碎补中柚皮苷含量比较[J]. 中国实验方剂学杂志, 2012, 18(6): 75-77.
[24] 黄艳萍, 刘浩, 王金香, 等. 骨碎补总黄酮的超声提取工艺[J]. 医药导报, 2007, 26(7): 793-794.
[25] 张全香, 苑晓威, 赵兴华. 大孔吸附树脂纯化骨碎补总黄酮的研究[J]. 中草药, 2011, 42(4): 708-709.
[26] 岳春华, 李岳, 李顺祥, 等. 顶空气相色谱法测定骨碎补总黄酮中大孔吸附树脂残留物[J]. 中南药学, 2011, 9(2): 95-97.
[27]张晋, 李新存, 葛亮, 等. 水煎煮法提取骨碎补总黄酮的动力学模型适应性研究[J]. 北京中医药大学学报, 2014, 37(2): 121-125.
[28]Li XH, Xiong ZL, Lu S, et al. Pharmacokinetics of naringin and its metabolite naringenin in rats after oral administration of Rhizoma Drynariae extract assayed by UPLC-MS/MS[J]. Chinese Journal of Natural Medicines, 2010, 8(1): 0040-0046.
[29] 谢雁鸣, 邓文龙, 洪诤. 骨碎补中柚皮苷大鼠体内药-时过程研究[J]. 中药新药与临床药理, 2005, 16(5): 350-352.
[30] 张弨, 赵荣生, 翟所迪, 等. 群体药代动力学概述[J]. 中国临床药理学杂志, 2013, 29( 8) : 563.
[31] Wang J, Jiang J, Xie Y, et al. Population Pharmacokinetics of naringin in total flavonoids of Drynaria Fortunei (Kunze) J. Sm. in Chinese women with primary osteoporosis. Journal of Traditional Chinese Medicine, 2012, 18(12): 925-933.
[32] Wang J, Jiang J, Xie Y, et al. Effect of naringenin in Qianggu capsule on population pharmacokinetics in Chinese women with primary osteoporosis. Journal of Traditional Chinese Medicine, 2015, 35(2): 141-153.
[33] Lu XM, Xiong ZL, Li JJ, et al. Metabonomic study on ‘Kidney-Yang Deficiency syndrome’ and intervention effects of Rhizoma Drynariae extracts in rats using ultra performance liquid chromatography coupled with mass spectrometry[J]. Talanta, 2011(83): 700-708.
[34] Liu XY, Zhang SS, Lu XM, et al. Metabonomic study on the anti-osteoporosis effect of Rhizoma Drynariae and its action mechanism using ultra-performance liquid chromatography-tandem mass spectrometry[J]. Journal of Ethnopharmacology, 2012(139): 311-317.
Research Progress of Rhizoma Drynariae
MA Hongna WEI Shenghua TAN Longyan*
School of Pharmaceutical Sciences, Guiyang University of Chinese Medicine, Guiyang 550025,China
Rhizoma drynariae, a commonly used traditional Chinese medicine in clinic, which can promote the healing fracture and relieve pain, replenish the kidney and strengthen the bones. The distribution of resources is the key factor that influences its development and utilization. And the characteristics of pharmacognosy are gist for the quality evaluation of medicinal materials and that for the identification with mixed falsify. Moreover, the optimization of Rhizoma drynariae processing process can improve the quality of slices. Also, the optimization of extraction process could provide reliable technical support for the industrialization of medicinal active ingredients. In addition, pharmacokinetic and metabonomics studies can provide a good reference for the clinical application of medicinal materials. This article summarizes the latest research progress of the rhizoma drynariae in resource investigation, pharmacognosy identification, processing technology, extraction technology, pharmacokinetic and metabonomics.
Rhizoma Drynariae;Resource;Quality;Clinical Application;Research Progress
国家基本药物所需中药材种子种苗繁育(贵州)基地建设(国中医药科技中药便函2014-117号);羊耳菊野生变家种技术研究(贵阳中医学院博士启动基金2015);贵州省贵阳中医学院院士工作站(黔科合院士站2014-4013);国家苗药工程技术研究中心(2014FU125Q09)。
马洪娜(1988-),女,汉族,硕士,助教,研究方向为药用植物栽培学、中药质量鉴定。E-mail: mahongna1988@126.com
檀龙颜(1981-),男,汉族,博士,副教授,研究方向为药用植物栽培学、中药民族药开发。E-mail: lytan1982@126.com
R282
A
1007-8517(2017)09-0059-08
2017-03-08 编辑:梁志庆)
