脉动流下血管支架耦合系统血流动力学实验研究
2017-06-05魏延宾
魏延宾,程 洁*
脉动流下血管支架耦合系统血流动力学实验研究
魏延宾,程 洁*
(东南大学机械工程学院,南京 210096)
为了探究血流动力学性能对再狭窄的影响,本文介绍了一种基于圆柱形内壁模型的血管支架耦合系统血流动力学性能的测试方法,并根据此方法自行设计并搭建一套实验装置,通过此装置对本实验室自制的冠脉支架进行了血流动力学性能测试实验。实验在脉动流下进行,实验结果表明,一个脉动周期内,靠近壁面的粒子运动速度先增大后减小,且速度总体数值很小;在同一时刻随着离壁面距离的增大,速度一直呈递增的趋势;在距离壁面同一位置处,速度随时间先增大后趋于平缓,在周期末尾时急剧下降到零,并伴有回流现象。通过计算壁面剪应力发现,一个周期内,壁面剪应力随时间变化先增大后减小;低于0.4Pa的时间占整个周期的一半,且分布在周期的开端和末端,是容易发生再狭窄的时间区分布。本实验对后续血流动力学性能测量提供了一定的实验基础,并且对后期支架的设计和优化提供了验证的手段。
血管支架;壁面剪应力;脉动流;再狭窄
血管支架是一种近几十年来迅速发展的微创医疗器械,对于由血管堵塞引起的冠心病等疾病,介入疗法以其微创﹑恢复快﹑效果显著等优点,在心血管疾病治疗领域取得了长足的进步,但是支架的引入改变了心血管微环境,术后六个月再狭窄率达到15%至30%[1]。大量研究表明,再狭窄是血管内膜增生导致的[2],而诱发血管内膜增生与血管内局部血流动力学性能密切相关,壁面剪应力(WSS, Wall Shear Stress)的变化可以影响动脉粥样硬化的行程过程[3]。
近年来,随着支架技术的不断推广应用以及应用过程中出现的再狭窄等问题显现,对于支架的研究也越来越多,其中关于支架血流动力学性能的研究也相应增长。Moore等人分析了支架植入对于血流与血管内应力的影响,他们指出支架设计与植入所引起的血流紊乱及血管内应力具有密切联系,因此支架的分析与评价以及优化设计应从流体力学与固体力学两个方面考虑[4]。N.Benard等将血管支架模型在平面上展开,并采用粒子示踪方法 (PTV, Particles Track Velocimetry)研究了流体流过支架网格时的流线分布与速度场,得到了不同的支架区域的剪应力分布情况,探索了0-1.5pa的低壁面剪应力区域,并比较了相同结构在不同流域的应力情况,给出了与再狭窄的关系[5][6]。Glenn等模拟支架植入产生的扰动并将模型放大,对弯曲动脉模型的二次流结构进行研究,在一个脉动周期内的不同时刻分别对弯曲血管从不同角度进行二次流观察,得到复合形态下的涡流对区域分布以及无量纲加速度参数[7];王山山等利用电化学方法对T型动脉分叉模型进行了壁面剪应力的测量,确定了分叉部位的高壁面剪应力和低壁面剪应力分布[8][9]。程洁等对血管支架介入耦合系统进行了血流动力学数值模拟,并研制了脉动流环境下平均WSS测试模块,采用电化学探针方法,实验结果表明,支架植入会明显降低壁面剪应力,产生流动停滞区域[10][11]。中科院物理研究所郑旭等基于3D打印和微流控技术,采用数值模拟和体外实验两种方法,探究了恒流条件下支架植入位置对壁面剪应力分布的影响,并得到支架放入动脉分叉区域后WSS分布,并给出了临界壁面剪应力约为0.4-0.5Pa,低于临界WSS的区域更容易诱发内皮增生,产生再狭窄[12]。
前面的学者对于血流动力学的研究多数是在恒流的条件下进行的,现在国内尚无在脉动流下对血流动力学进行实验研究。目前对于血流动力学性能现代实验研究方法中,对于WSS的测量方法主要就是粒子示踪法和电化学探针法,其中电化学探针法在恒流状态下测试具有一定的准确性,且对设备要求不高,但其测量的是一段极短时间内的平均值,对于脉动状态下的瞬时剪应力的修正方法复杂,误差较大。而粒子示踪方法虽然测试过程复杂﹑数据量庞大,但借助于高速数字摄像机可以准确的测量脉动状态下的瞬时速度分布。故本实验选择粒子示踪方法,自主设计并搭建实验平台,测量速度场分布并计算WSS。
1 材料和方法
本文所采用的实验平台为自主设计的用于测量血管支架血流动力学性能的测试装置。如图1所示,整套装置包括:动力发生装置﹑压力测量模块﹑被测血管支架耦合系统﹑PTV测量模块﹑回路模块。
动力发生装置为蠕动泵(Longer Pump BT100-1F,配YZ1515x泵头);压力测量模块由压力传感器(高华MB300,0-60Kpa)﹑数据采集卡(National Instruments USB-6211)和电脑组成;被测血管支架耦合系统由PDMS模拟血管和36L不锈钢冠脉支架组成;PTV测量模块由光源﹑高速CCD(Ametek Vision Research Phantom V,含软件PCC)和倒置显微镜(Olympus IX71)和电脑组成;回路模块由密闭水箱﹑旋转压力泵和单向阀组成。测量程序基于NI LabVIEW开发,负责测量过程中回路中压力信号的采集与在线处理。测量结果经程序自动导出至Excel (Microsoft 2010, Inc.)。
实验装置的关键模块之一是血管支架耦合系统模块,其中又以模拟血管制作的情况,决定了体外实验模拟真实血管的相似度。蓝蜡的融点在60℃左右,适合用来做流道内模型;PDMS透光性好,便于观察粒子在流道的运动情况。由此,模拟血管的制作过程为:首先用建模软件Pro/E(PTC, Inc.)绘制狭窄血管内芯的实体模型;然后采用3D打印的方法,以蓝蜡为打印材料,制作出用于当作流道内芯的蜡模;将蜡模放入PDMS溶液(溶液与固化剂的配比为11:1)后,放在恒温箱80℃加热2小时;然后水浴融掉蜡模,得到模拟血管。本实验所用的流道内直径2.65mm。

图1 血管支架血流动力学性能PTV测试平台示意图(a)血管支架耦合系统实物图;(b)扩张之前的球囊跟支架;(c)支架在PDMS流道中示意图
本实验所用的血管支架为实验室自主设计制造的一种管形网状冠脉支架。扩张前的冠脉支架参数如表1所示,支架材料为36L不锈钢,由不锈钢微管经激光雕刻而成,其结构为M型连接杆连接在轴向重复的正弦支撑环上,支撑环由周向重复的6个波形单元组成。扩张前支架直径为1.2mm,长度20mm,扩张后的直径达到3mm。图2 (b)为扩张前的支架实物,图2 (c)为支架在PDMS流道中扩张之后的示意图(本文只给出了两个轴向波形单元),图2 (a)为扩张后的血管支架耦合系统实物图。

图2 血管支架耦合系统图

表1 扩张前冠脉支架几何参数
蠕动泵的可以输出的流量范围是0.051~51ml/min,使用的软管内径为2.4mm,外径为4mm。在实验中,设置流量为10ml/min,由压力传感器测得压力变化,由于传感器测出来的信号噪声较大,需对其进行降噪处理:这里采用MATLAB滤波的形式,滤波后的信号如图3所示。这里可以看出,滤波之后的信号经过拟合,已经是明显的脉动分布,且近似于正弦分布。脉动基础压力为13Kpa,峰值和谷值分别为15Kpa﹑11Kpa。与真实的人体冠脉压力环境已经非常接近[13]。
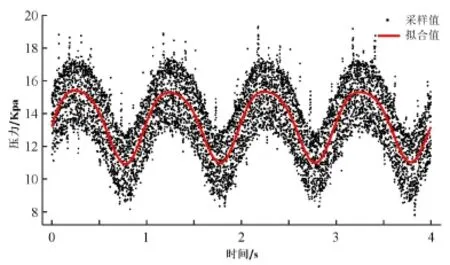
图3 压力传感器信号滤波前与滤波后比较
人体血液的粘度为3.5×10-3Pa·s,密度为1.060×10-3Kg/ m3[14]。全血的透光性差,在目前的条件下,选择PTV方法进行体外实验,采用全血还很难实现。去离子水在粘度和密度方面区别于全血,但透光性好,便于观察,故溶液选择去离子水来模拟血液。同时用15μm的聚苯乙烯粒子来模拟血液细胞[15]。
血管中的血液可认为是不可压缩流体,而血液的雷诺数约为50[10],其流动情况可认为是轴对称层流运动。雷诺数Re定义为:

ρ是血液密度,ν是速度,L是管路直径,μ是血液动力粘度。采用笛卡尔直角坐标系,血管轴线与z轴重合,端面与x y面重合,其运动可以用以下两个方程表示:
连续性方程:
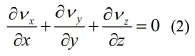
Navier-Stokes方程:
Vx﹑Vy﹑Vz分别是速度 在x﹑y﹑z三个坐标方向上的矢量,ρ是血液密度,p是压力,t是时间,fx﹑fy﹑fz分别为单位质量力在x, y, z方向上的投影,μ是血液动力粘度。
血管壁是具有粘弹性的薄壁管,根据Womersley理论,将其简化为均匀的薄壁圆柱管,即血管壁的厚度h跟血管直径的比值是一个小量。同时假定血管壁是各向同性的胡克弹性体,利用厚度均匀的附加层来代替血管内壁周围的结缔组织,并引进有效壁厚H[16]:

式中,ρ1﹑ r1﹑ h1分别表示附加层的密度﹑半径和厚度, ρw﹑R ﹑h 分别为血管壁的密度﹑半径和厚度。由于H的值很小,而用PDMS制作的血管与真实的人体血管在生物活性上有区别,将其看成无弹性的壁面,故在本实验中忽略血管壁的影响。
冠脉内血流动力学的一项关键指标就是血管壁面剪应力。而壁面剪应力与剪切 速率有关,剪切速率的计算公式[17]为:

式中, u﹑v﹑w 分别为血流速度在x﹑y﹑z三个方向上的分量。由此便可以计算出壁面上各个位置上的剪应力。在本实验中,理论上y和z方向上速度为零,实际操作中可能会出现极小的速度,对此忽略y和z方向上的速度,剪切速率的计算公式可以化为:
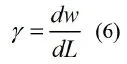
L为到壁面的距离,本实验中流动状况为层流且流体沿着血管流动,根据牛顿内摩擦定律,流体的切应力τ为:
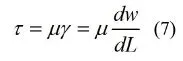
式中,μ动力粘度, y为剪切速率,w为沿轴线方向速度,L为距壁面的距离。
2 实验过程
将实验装置的各个部分按照图1所示,装配完整。蠕动泵的软管接至压力传感器,压力传感器后面接PDMS模拟血管(里面已经含有支架),模拟血管后面是密闭水箱,密闭水箱出来的软管经三叉接头分别接旋转压力泵和单向阀,单向阀的出口接到蠕动泵的软管上面,形成完整回路。取50ml左右的去离子水,在其中添加15μm聚苯乙烯粒子,并摇晃均匀。为了避免管路中有杂质混入到溶液,依次用酒精和去离子水冲洗管路,完毕后将含有聚苯乙烯粒子的溶液注入回路,排干净回路中的空气。
调节蠕动泵的流量输出为10ml/min,接下来是实验的视觉观测模块启动,将荧光显微镜调至明场状态(脉动状态下粒子流速变化快,暗场条件下,荧光粒子被激发的光,难以观察),并打开高速CCD模块,调节PDMS模拟血管在载物台上的位置,使在视野上的图像位置正确,并调节显微镜的光强旋钮,使图像清晰。每张图像的曝光时间为1.7μs,连续两张图像的时间间隔ta是161.29μs,每秒拍摄的张数是6200,拍摄图像的像素是1280×800,拍摄的软件是PCC。蠕动泵运行稳定3分钟后,再开始拍摄图像,以保证管路中的流体做周期性的脉动流动。处理图像的软件是PCC和ImageJ。在PCC软件中的measure模块中设置像素比为1.960784×10-3mm/ pixel,那么出现在视野中的粒子,其距离壁面的距离L可以测得。粒子连续的出现在视野中,将这部分连续的图像在ImageJ中叠加,如图4所示,其运动的轨迹被记录下来,可以得到粒子运动的距离La,这部分图像的张数Z也可以得到,这部分轨迹的运动时间Ta的计算公式为Ta=Z×ta,一般Ta<2ms,时间间隔非常小,可以近似认为粒子在这微小的时间段的平均速度就是粒子的瞬时速度,Va=La/Ta,以此类推,可以得到全场域范围内的粒子瞬时速度分布。每个粒子的同一位置同一时刻,统计5-10组数据取平均值(粒子出现在壁面处的概率小于出现在流道中部的概率,壁面处的粒子统计组数小于流道中部组数),同时也计算出标准差。而每7350张图像,粒子运动会重复一次,故一个周期T=1.185s,每个周期的结束到下个周期的开始的时候会有粒子的回流现象,以视野中的所有粒子开始运动的时刻作为周期的开始,由此可以确定后面的粒子的流过测量位置的时间坐标。

图4 距离壁面不同的距离的时候,粒子叠加后的的运动轨迹
3 实验结果
通过实验发现,粒子到壁面的距离小于100μm的时候,粒子在一个脉动周期的时间内速度很小,而且速度的变化也很小。如图5所示,在一个周期的开端和末端,所有粒子的运动速度都为零;在0.1T的时刻,粒子速度随着距离壁面的的增大而增大;在0.2T 时刻这种现象更加明显,到壁面的距离超过350μm的时候,速度随着距离的增加而趋于平缓;当时间处于0.3T到0.8T的时候,速度的变化曲线非常接近,都是随着距离的变大呈现递增的趋势,并出现最高速度0.054m/s;当处于0.9T时刻的时候,粒子运动方向发生改变,出现反向运动,到壁面距离越大,粒子反向流动的速度越大,但总体回流速度并不大。
如图6所示,速度随着距离增大而增大的现象显得更加明显,粒子在0-0.1T的时间段内,速度开始增加,此段数值较小但斜率较大;在到达0.2T的时候,速度显著增大,L=0.3mm处的速度达到了0.0207m/s,这种增速一直保持到0.3T处,从0.3T时刻到0.8T时刻,粒子的速度处于高位平衡状态,在一定的范围内上下波动,且波动范围较小;而从0.8T时刻到0.9T时刻,粒子的速度急剧下降到零值左右;然后粒子反向流动直至周期结束。
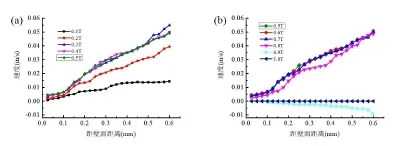
图5 一个周期内不同的时刻的粒子速度随着壁面距离变化
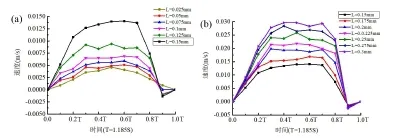
图6 距离壁面不同的位置的粒子速度随着时间的变化
通过对粒子运动轨迹的分析,不但可以获得粒子的速度分布,还可以通过前面的公式来计算WSS。靠近血管壁面的粒子的运动速度除以粒子到壁面的距离,再乘以粘度,即可得到WSS。这里的计算需要引入一个计算系数3.5,去离子水的粘度常温下认为是1×10-3Pa·s,而人体血液的粘度3.5×10-3Pa·s。根据公式 (6) 和公式 (7) 可以计算出一个周期内的壁面剪应力变化。如图7所示,在一个脉动周期内且随着时间WSS先增大后减小,WSS的最大值出现在0.5T时刻,为0.644 Pa ,而在0.1T时刻为0.125 Pa ,在0.9T时刻为0.126 Pa。且0.1T﹑0.2T﹑0.8T﹑0.9T时刻的WSS值低于0.4Pa,根据前面的讨论,WSS低于0.4Pa为低壁面剪应力区域,容易诱发出现再狭窄,而在0.3T﹑0.4T﹑0.5T﹑0.6T﹑0.7T时刻,WSS均高于0.4Pa。一个脉动周期内有一半的时间壁面剪应力处于临界值以下,原因是支架的植入改变了血液流动的微环境,网状的支架在血管壁上会形成流动停滞区域,降低血液的流动速度,从而形成低壁面剪应力区域。
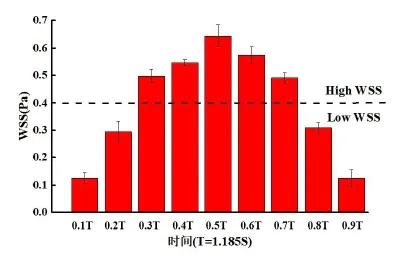
图7 一个周期内WSS的变化
4 结语
本文提出了一种血管支架耦合系统血流动力学分析测试方法,并搭建体外实验测试平台对实验室自制血管支架进行实验。结果表明,支架植入血管后,距离壁面100μm的范围内流速非常低,很容易形成低WSS区域,因此靠近壁面的区域是容易引发再狭窄的区域。在一个血流脉动周期内,0-0.2T和0.8-1T的时间段内,WSS低于0.4Pa,是极易引发内皮增生产生再狭窄的时间区域。下一步的研究方向是探究支架网孔内WSS分布以及入口﹑出口处的WSS分布。
[1] Serruys P W, de Jaegere P, Kiemeneij F, et al.A comparison of balloon-expandable-stent implantation with balloon angioplasty in patients with coronary artery disease[J].New England Journal of Medicine, 1994, 331(8): 489-495.
[2] Carter A J, Laird J R, Farb A, et al.Morphologic characteristics of lesion formation and time course of smooth muscle cell proliferation in a porcine proliferative restenosis model[J].Journal of the American College of Cardiology, 1994, 24(5): 1398-1405.
[3] 戴敬, 吕树铮, 宋现涛, 等.支架再狭窄的机制及防治新进展[J].中华老年心脑血管病杂志, 2014, 16(03): 322-323.
[4] Moore Jr J E, Berry J L.Fluid and solid mechanical implications of vascular stenting[J].Annals of biomedical engineering, 2002, 30(4): 498-508.
[5] Benard N, Coisne D, Donal E, et al.Experimental study of laminar blood flow through an artery treated by a stent implantation: characterisation of intra-stent wall shear stress[J].Journal of biomechanics, 2003, 36(7): 991-998.
[6] Benard N, Coisne D, Perrault R.Experimental study of blood laminar flow through a stented artery [C]//Engineering in Medicine and Biology Society, 2001.Proceedings of the 23rd Annual International Conference of the IEEE.IEEE, 2001, 1: 83-85.
[7] Glenn A L, Bulusu K V, Shu F, et al.Secondary flow structures under stent-induced perturbations for cardiovascular flow in a curved artery model[J].International Journal of Heat and Fluid Flow, 2012, 35: 76-83.
[8] 王山山, 邱玲.用电化学方法测试动脉模型壁面剪应力[J].应用力学学报, 2000, 17(2): 55-61.
[9] 王山山, 邱玲.提高电化学法测试壁面剪应力精度的方法[J].实验力学, 2001, 16(1): 1-6.
[10] 程洁.血管支架介入耦合系统血流动力学数值模拟与实验研究[D].东南大学, 2011.
[11] 程洁, 周啸, 李俐军, 等.冠脉支架的多功能体外力学性能测试装置及实验研究[J].东南大学学报(自然科学版), 2010, 40(2): 341-345.
[12] Wang H, Liu J, Zheng X, et al.Three-dimensional virtual surgery models for percutaneous coronary intervention (PCI) optimization strategies[J].Scientific Reports, 2015, 5: 10945.
[13] Wong K K L, Tu J, Kelso R M, et al.Cardiac flow component analysis [J].Medical Engineering & Physics, 2010, 32(2):174-188.
[14] Foad K, Ghista D N, Boyang S, et al.In vitro measurements of velocity and wall shear stress in a novel sequential anastomotic graft design model under pulsatile flow conditions[J].Medical Engineering & Physics, 2014, 36(10):1233-1245.
[15] Xiang N, Ni Z.High-throughput blood cell focusing and plasma isolation using spiral inertial microfluidic devices[J].Biomedical Microdevices, 2015, 17(6): 1-11.
[16] 柳兆荣.心血管流体力学[M].复旦大学出版社, 1986.
[17] 卡里.血液循环力学[M].科学出版社, 1986.
Hemodynamics Experimental Research of Stent Coupling System of Pulse Flow
Wei Yanbin, Cheng Jie*
(School of Mechanical Engineering, Southeast University, Nanjing 210096, China)
In this report, we presented a novel approach for hemodynamics study of stent coupling system based on cylindrical inner wall model to investigate the ef f ect of hemodynamic performance on restenosis.A set of experimental apparatus has been assembled based on this approach.Coronary artery stent that designed by our lab was used in the hemodynamics experimental research which was done in pulsating flow.The hemodynamics experimental research results showed that the velocities of particles near the wall increase at fi rst then decreases and the overall speed is small.With the increase of distance, velocity has been increased.Velocity increased from the bottom to the peak value, after which became fl at and swooped suddenly to the bottom, with the time passed in a pulsation period.Countercurrent has been captured towards the end of pulsation period.The calculation results have shown that wall shear stress increases with time then decrease.The lasting of wall shear stress which was lower than 0.4Pa accounted for half of the pulsation period and distributed at the beginning and end of the cycle which is prone to restenosis.Consequently, the study not only provided a basis for the subsequent measurement of hemodynamic performance but also supplied artif i ce that provides verif i cation for the design and optimization of stents.
stent; wall shear stress; periodic pulsing fl ow; restenosis
R318.11, TB126 [Document Code] A
10.11967/ 2017150205
R318.11,TB126
A DOI:10.11967/ 2017150205
基金支持:国家自然科学基金资助项目(51275089﹑51575106).
魏延宾(1991-),男,硕士研究生;程洁(联系人),女,博士,副教授,硕士研究生导师,cjgrace@sina.com.
