硝苯地平中空控释微球的处方研究及质量评价Δ
2017-05-16蔚坤妍黄绍秋魏郁梦郑文武西南医科大学附属医院研究生部四川泸州646099西南医科大学药学院药剂学教研室四川泸州646099西南医科大学附属医院心血管内科四川泸州646099
蔚坤妍,黄绍秋,魏郁梦,冯 婷,郑文武,赵 领#(1.西南医科大学附属医院研究生部,四川泸州646099;.西南医科大学药学院药剂学教研室,四川泸州 646099;.西南医科大学附属医院心血管内科,四川泸州 646099)
硝苯地平中空控释微球的处方研究及质量评价Δ
蔚坤妍1*,黄绍秋2,魏郁梦2,冯 婷2,郑文武3,赵 领2#(1.西南医科大学附属医院研究生部,四川泸州646099;2.西南医科大学药学院药剂学教研室,四川泸州 646099;3.西南医科大学附属医院心血管内科,四川泸州 646099)
目的:制备硝苯地平(NF)中空控释微球并评价其质量。方法:采用溶剂扩散挥发法制备微球。以2、12、24 h的累积释放度(Q2h、Q12h、Q24h)的综合评分为指标,设计正交试验筛选处方中载体材料乙基纤维素(EC)、聚乙烯吡咯烷酮(PVP)和主药NF用量;评价最优处方所制微球的外观形态、粒径分布、载药量、漂浮性及累积释放度,并与进口制剂NF控释片(Adalat®)比较体外释放行为。结果:最优处方为NF 3.00 g、PVP 1.60 g、EC 15.65 g。所制NF中空控释微球外观呈球形,粒径主要分布于20~40目,载药量为8.66%;在释放介质中24 h的漂浮率为97.93%;Q2h、Q12h、Q24h分别为20.49%、52.90%、91.00%(RSD<10%,n=3),与进口制剂比较,累积释放度的相似因子(f2)均大于50;体外释药符合零级动力学方程(r=0.999 3),其Ritger-Peppas方程(r=0.980 7)的n为0.478。结论:所制NF中空控释微球与进口制剂具有相似的释药行为,其释药机制为扩散和骨架溶蚀共同作用。
硝苯地平;中空控释微球;处方筛选;制备;正交试验;质量评价
口服缓控释给药系统由于能减少用药频率、血药浓度平稳等优点而得到广泛发展[1]。但是,有时单元口服缓控释药物剂型(如传统的缓释片或胶囊)容易受胃排空的影响而引起较大的个体吸收差异。为了解决这些问题,多单元口服缓控释药物剂型(如微球等)备受研究者关注[2]。微球类的多单元口服缓控释药物剂型不仅能增加难溶药物的溶解度,而且还能增加胃肠道对药物的吸收,同时可以避免单元口服缓控释药物剂型带来的局部药物浓度过高,以及药物突释造成的用药不安全问题[3-4]。中空微球由于在胃内具有良好的漂浮性能,能增加药物在胃内的滞留时间,控制药物释放,已成为国内外释药系统研究的热点之一[5-6]。目前,已报道的中空微球制备方法中大多数使用了毒性较强的二氯甲烷、甲醇等混合溶剂,对环境污染大[2,7-9];而其他的制备方法如冷冻干燥法,不仅成本高,而且工艺复杂[10]。
硝苯地平(Nifedipine,NF)为二氢吡啶类钙通道拮抗药,能抑制血管平滑肌和心肌细胞的钙离子内流,临床上广泛用于高血压、心绞痛等心血管疾病的治疗。但其生物半衰期短(2 h),需频繁给药,血药浓度波动大,易引起反射性心率加快、面部潮红、头痛等不良反应[11]。另外,NF还存在水溶性差、生物利用度低、见光易分解等不足。为了维持NF在体内的平稳释药,减少其不良反应,本研究拟采用课题组的专利技术[12],以乙基纤维素(EC)和聚乙烯吡咯烷酮(PVP)为载体材料,制备NF中空控释微球并评价其质量,以期为临床提供一种缓控释新制剂。
1 材料
1.1 仪器
UV 1700PC紫外分光光度计(上海凤凰光学科仪有限公司);CKX41SF光学显微镜(日本Olympus公司);ZRS-8G智能溶出试验仪(天大天发溶出仪公司)。
1.2 药品与试剂
NF原料药(重庆青阳药业有限公司,批号:H5002-0668,纯度:>98%);NF控释片(商品名:Adalat®,拜耳医药保健有限公司,批号:H20130332,规格:每片30 mg);EC(上海卡乐康技术有限公司,批号:SA14013T01);PVP(美国ISPTechnologies公司,批号:0001920828);其余试剂均为分析纯。
2 方法与结果
2.1 NF中空控释微球的制备
精密称取NF原料药和PVP、EC,溶于适量乙醇和乙醚混合溶剂中,滴加到液体石蜡中,搅拌至有机溶剂挥干,用正己烷洗净,并在40℃真空中干燥1 h,即得NF中空控释微球,避光干燥处保存。由于NF具有光敏感性,整个过程应避光操作。
2.2 载药量的考察
2.2.1 检测波长的确定 精密称取NF原料药及处方配比中的各辅料,分别用无水乙醇制成25µg/m L的NF溶液和空白辅料溶液,分别于200~500 nm波长范围内进行紫外扫描。结果显示,NF在238 nm波长处有最大吸收峰,且辅料在此无干扰。故以238 nm为NF含量测定的检测波长。
2.2.2 方法学考察 按相关方法学要求考察。结果,NF质量浓度(c)与吸光度(A)的回归方程为A=0.065 9c+ 0.062 7(r=0.999 9),线性范围为0.5~10µg/m L;平均回收率为(99.51±0.40)%(RSD<1.0%,n=9);日内RSD<0.97%(n=3),日间RSD<0.95%(n=3)。
2.2.3 载药量的测定 取适量干燥的NF中空控释微球在研钵中研碎,然后精密称取10.0mg,置于50m L量瓶中,用无水乙醇超声溶解定容。从中精密量取1.0m L置于10m L量瓶中,用无水乙醇稀释至刻度,摇匀,用微孔滤膜过滤。取续滤液在238 nm波长处测定A,计算含量和载药量[载药量=(微球中药物质量/微球总质量)× 100%]。
2.3 释放度的考察
2.3.1 检测波长的确定 除将无水乙醇替换成释放介质[含0.25%十二烷基硫酸钠(SDS)的0.1mol/L的盐酸溶液]外,其余方法按“2.2.1”项下操作。结果显示,NF在释放介质中于238 nm波长处有最大吸收峰,且辅料无干扰。故以238 nm为NF中空控释微球释放度的检测波长。
2.3.2 标准曲线的制备 按“2.2.2”项下方法制备含NF 40µg/m L的贮备液,再用释放介质稀释制成质量浓度为2、4、6、8、10µg/m L的系列溶液,在238 nm波长处测定A。以质量浓度(c)对A进行线性回归分析,得回归方程为A=0.058c-0.005 3(r=0.999 7)。结果表明,NF检测质量浓度的线性范围为2~10µg/m L。
2.3.3 释放度的测定 取NF中空控释微球,按2015年版《中国药典》(四部)释放度测定法(第一法),以900m L含0.25%SDS的0.1mol/L的盐酸溶液(NF中空微球)或1%SDS的磷酸盐-枸橼酸盐溶液(pH=6.8)(NF控释片)为释放介质,温度为(37±0.5)℃,转速为120 r/m in,依法操作。分别于0.5、1、2、4、6、8、12、24 h时取样5m L(补加同温等量介质),用0.8µm微孔滤膜过滤,取续滤液在238 nm波长处测定A,计算释放度(Q)。
2.4 漂浮性的考察
[6]方法,采用溶出度测试中的小杯法进行体外漂浮性能测试。取200个NF中空控释微球分散在250m L含0.25%SDS的0.1mol/L的盐酸溶液中,温度为(37±0.5)℃,转速为120 r/min。经2、24 h时,观察漂浮和沉底的微球个数,计算漂浮率[漂浮率=(微球总数量-沉底的微球个数)/微球总数量×100%]。
2.5 形态观察和粒径测定
取NF中空控释微球用适量液体石蜡分散后,用光学显微镜观察其形态和分散性;取干燥后的NF中空控释微球适量,均匀分散在样品台,用导电胶将样品黏在样品座上,置于扫描电镜中观察其形态。采用筛分法,分别以20、40、50、60目筛检测NF中空控释微球的粒径分布,计算各目下的微球质量占比。
2.6 正交试验筛选处方
在单因素试验基础上,确定处方中影响微球质量最显著的EC(A)、PVP(B)、NF(C)的用量为因素,以2、12、24 h的Q的综合评分X(X=│Q2h-20│+│Q12h-45│+│Q24h-90│)[10]为指标,按L9(33)表设计试验,X越小越好。因素与水平见表1,正交试验设计与结果见表2,方差分析结果见表3。
结合表2和表3结果,3个因素影响释放度的大小顺序依次为A>C>B;确定最优处方为A2B3C1,即EC 15.65 g、PVP 1.60 g、NF 3.00 g。按最优处方制备3批NF中空控释微球,测得其平均Q2h、Q12h、Q24h分别为20.49%、52.90%、91.00%(n=3),综合评分X为9.39。
2.7 质量评价
以小试用量的50倍试制3批样品,分别考察其粒径分布、载药量及漂浮性。结果3批样品平均载药量为8.66%,2 h平均漂浮率为98.53%,24 h平均漂浮率为97.93%(n=3)。3批样品的质量评价结果见表4。
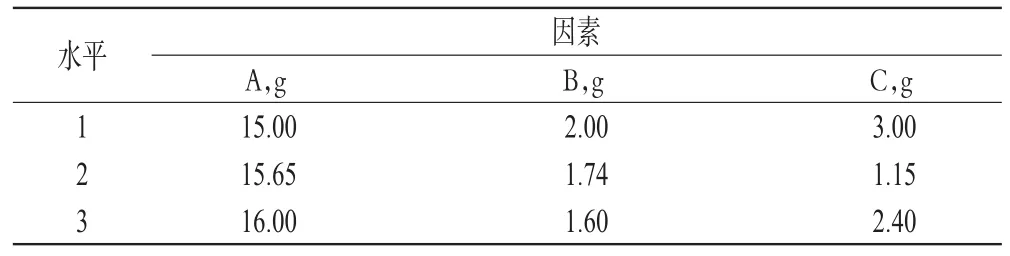
表1 因素与水平(处方量20 g)Tab 1 Factorsand levels(formulation amount20 g)
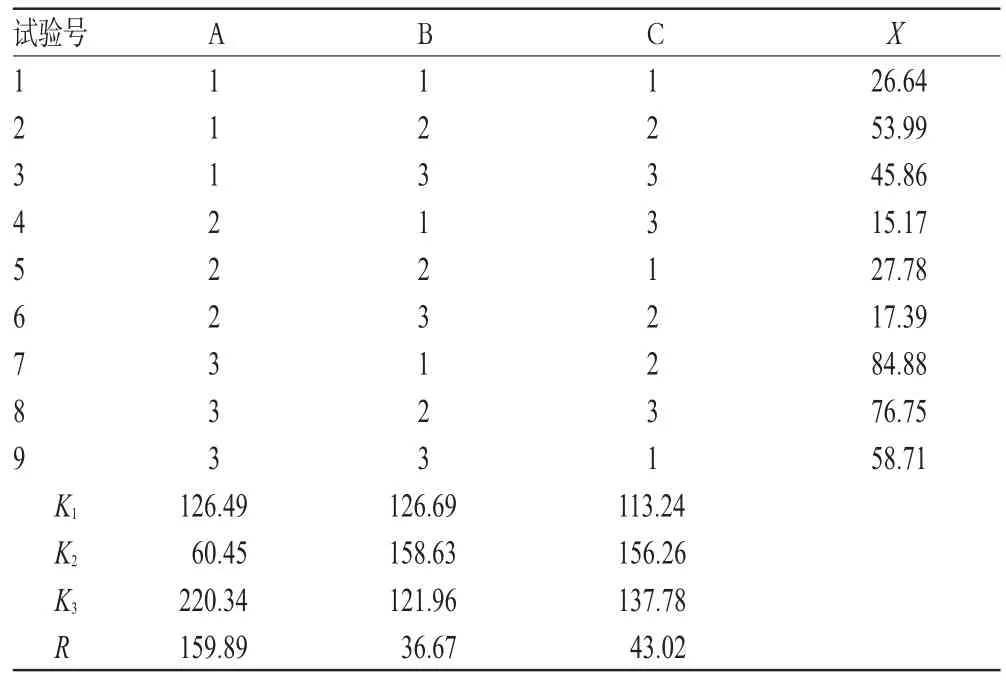
表2 正交试验设计与结果Tab 2 Orthogonal testdesign and results
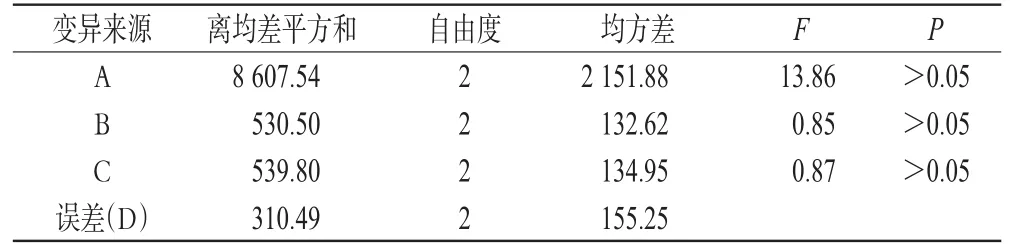
表3 方差分析结果Tab 3 Resultsof varianceanalysis
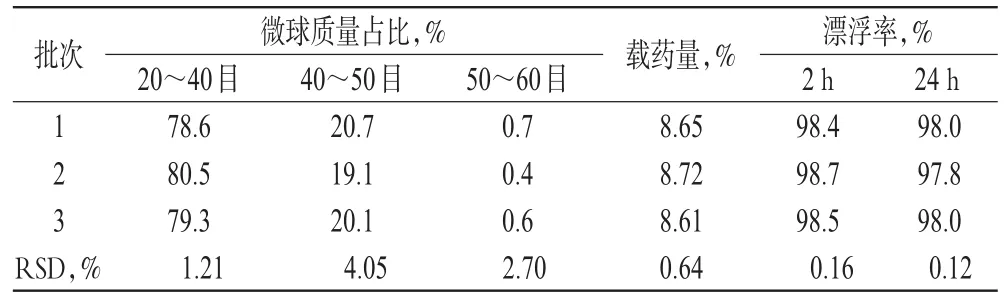
表4 3批样品的质量评价结果Tab 4 Results of quality evaluation of 3 batches of sam p les
2.8 微球的外观及形态
采用优化的处方制备3批样品,观察其外观、形态。结果显示,样品呈圆球形,易分散,粒径均匀,外观光滑,内面有中空腔隙。显微镜图和扫描电镜图见图1。
2.9 体外释放度测定
采用优化的处方制备3批样品,测定其体外累积释放度,比较自制微球与进口制剂NF控释片(Adalat®)的Q,并对二者的体外释放行为进行模型拟合。自制微球与进口制剂Q的测定结果见表5,模型拟合结果见表6。

图1 NF中空控释微球的显微镜图和扫描电镜图Fig 1 M icroscope and scanning electron m icrograph of NFhollow controlled releasem icrospheres
表5 自制微球与进口制剂Q的测定结果(±s,n=6,%%)Tab 5 Determ ination results of Q of self-madem icrospheres and im ported preparations(±s,n=6,%%)
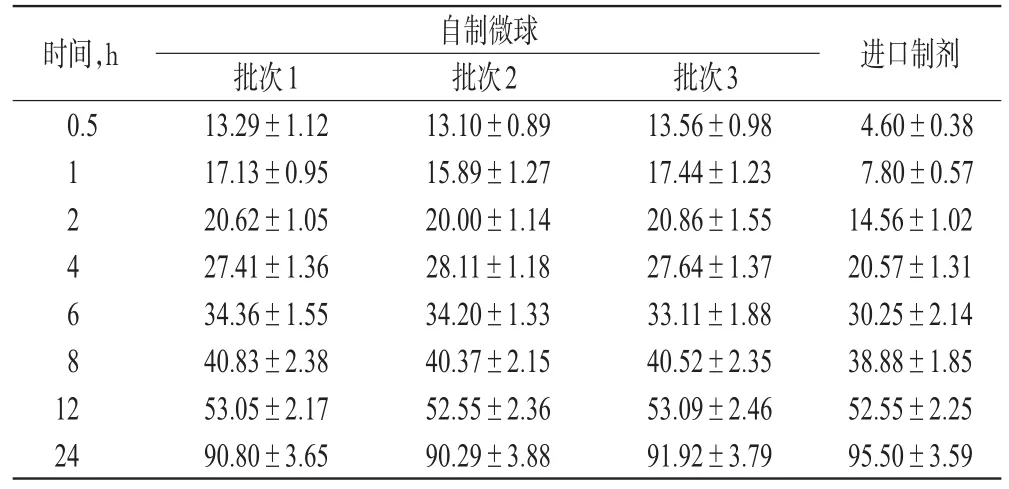
表5 自制微球与进口制剂Q的测定结果(±s,n=6,%%)Tab 5 Determ ination results of Q of self-madem icrospheres and im ported preparations(±s,n=6,%%)
时间,h 0.5 124681 2 24批次1 13.29±1.12 17.13±0.95 20.62±1.05 27.41±1.36 34.36±1.55 40.83±2.38 53.05±2.17 90.80±3.65自制微球批次2 13.10±0.89 15.89±1.27 20.00±1.14 28.11±1.18 34.20±1.33 40.37±2.15 52.55±2.36 90.29±3.88批次3 13.56±0.98 17.44±1.23 20.86±1.55 27.64±1.37 33.11±1.88 40.52±2.35 53.09±2.46 91.92±3.79进口制剂4.60±0.38 7.80±0.57 14.56±1.02 20.57±1.31 30.25±2.14 38.88±1.85 52.55±2.25 95.50±3.59
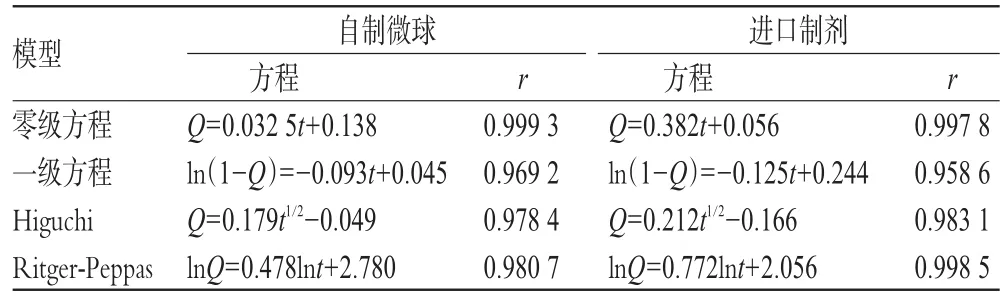
表6 自制微球与进口制剂的体外释放模型拟合结果Tab 6 M odel fitting results of in vitro release of selfmadem icrospheresand im ported preparations
由表5可知,与进口制剂比较,3批自制微球体外释放度的相似因子(f2)分别为60.75、61.51、60.84(均大于50),表明二者体外释药行为基本一致。
3 讨论
NF为结晶型粉末时,水溶性差,导致口服制剂生物利用度不高;而当其呈无定形存在时,其口服生物利用度增加。有研究者将NF与PVP制成固体分散体,能大幅度提高NF的溶解度[13-14],其原因为当NF高度分散在PVP亲水性载体中,一方面PVP能抑制药物结晶,另一方面NF以高能态的无定形存在,从而具有更好的溶解度。因此,本研究结合微球网状骨架缓控释作用与固体分散技术的优点,首次将亲水性聚合物PVP和疏水乳聚合物EC组合,通过正交试验设计优化NF中空控释微球处方,筛选的最优处方(处方量20 g)为NF 15.65 g、PVP 1.60 g、EC 3.00 g。由体外释药结果可知,该中空控释微球能改善难溶性药物NF的Q,与进口制剂Adalat®具有相似的释药行为。
从释药动力学模型拟合可知,NF中空控释微球释药行为符合零级动力学,具有恒定的控释效果。有文献报道,在Ritger-Peppas方程中,ln t前的系数n可用于描述药物的释放机制:当n在0.45~0.89间时,药物释放机制为扩散和骨架溶蚀共同作用;当n<0.45时,为Fick扩散;当n>0.89时,为骨架溶蚀[11]。本研究自制的NF中空控释微球Ritger-Peppas方程中n为0.478,表明其释放机制为药物扩散和骨架溶蚀共同作用。
本研究制备的NF中空缓释微球,体外释药具有零级动力学特征,后续将进一步进行体内药动学研究。
参考文献
[1] 胡雄伟,张倩,宋洪涛.口服缓控释骨架片给药系统的研究进展[J].中国药房,2010,21(17):1619-1622.
[2] Mukund JY,Kantilal BR,Sudhakar RN.Floatingmicrospheres:a review[J].Braz JPharm Sci,2012,48(1):17-30.
[3] Bhosale UV,Devi K,Choudhary S.Multiunit floating drug delivery system of acyclovir:development,characterization and in vitro-in vivo,evaluation of spray-dried hollow microspheres[J].JDDST,2012,22(6):548-554.
[4] Patel HP,Patel JK,PatelMP,etal.Multiple unit particles system of ramipril:an approach to enhance stability [J].JYoung Pharm,2011,3(2):90-96.
[5]Zhang G,Yu L,Wu HB,et al.Formation of ZnMn2O4ball-in-ball hollow microspheres as a high-performance anode for lithium-ion batteries[J].Adv Mater,2012,24(34):4609-4613.
[6] WeiYM,Zhao L.In vitro and in vivo evaluation of ranitidine hydrochloride loaded hollow m icrospheres in rabbits [J].Arch Pharm Res,2008,31(10):1369-1377.
[7] 朱澄云,郑佳妮,周名扬,等.正交试验法优化西咪替丁中空微球的处方工艺及微球体外释药模式研究[J].沈阳药科大学学报,2014,31(9):669-672.
[8] Tekade BW.Design and in-vitro evaluation of ethyl cellulose based floating m icrospheres containing antidiabetic drug[J].Asian JBiomed Pharm Sci,2013,3(23):33-37.
[9] Ghodake JD,Vidhate JS,Shinde DA,etal.Formulation and evaluation of floatingm icrosphere containing anti-diabetic(metformin hydrochloride)drug[J].Int JPharm Res,2010,2(1):378-384.
[10] Dehghan S,Aboofazeli R,Avadi M,et al.Formulation optim ization of nifedipine containing m icrospheres using factorial design[J].Afr J Pharm Pharmaco,2010,4(6):346-354.
[11] Zheng WW,Wei YM,Ye Y,et al.Development and pharmacokinetic evaluation of once-daily sustained-releasedmatrix capsulesof nifedipine using solid dispersion technique[J].Afr J Pharm Pharmaco,2013,7(12):658-665.
[12] 魏郁梦,赵领,索国清,等.胃肠道用药物的中空微球载体的制备方法,中国:ZL200610095105.5[P].2008-10.
[13] 黄好武,罗玉鸿,梁飞华.硝苯地平固体分散体制备工艺的研究[J].今日药学,2011,21(1):20-24.
[14] Wu UY,Ho HO,Chen YC,et al.Thermal analysis and dissolution characteristics of nifedipine solid dispersions [J].JFood Drug Anal,2012,20(1):27-33.
Formulation Study and Quality Evaluation of Nifedipine Hollow Controlled-release M icrospheres
WEI Kunyan1,HUANG Shaoqiu2,WEIYumeng2,FENG Ting2,ZHENG Wenwu3,ZHAO Ling2(1.Dept.of Postgraduate,the Affiliated Hospital,Southwest Medical University,Sichuan Luzhou 646099,China;2.Dept.of Pharmaceutical Sciences,School of Pharmacy,Southwest Medical University,Sichuan Luzhou 646099,China;3.Dept.of Cardiology,the A ffiliated Hospital,SouthwestMedical University,Sichuan Luzhou 646099,China)
OBJECTIVE:To prepare nifedipine(NF)hollow controlled-release microspheres and evaluate the quality.METHODS:Solvent diffusion volatilization method was used to preparem icrospheres,using comprehensive scores of cumulative release in 2,12,24 h(Q2h,Q12h,Q24h)as indexes,orthogonal testwas designed to screen the carriermaterial ethyl cellulose(EC),polyvinyl pyrrolidone(PVP)and main drug NF amounts;appearance,particle size distribution,drug loading,floating and cumulative release of them icrospheres prepared by optimal formulation were evaluated and compared of in vitro release behavior w ith imported preparation of Nifedipine controlled-release tablets(Adalat®).RESULTS:The optimal formulation was as follow as NF 3.00 g,PVP 1.60 g,EC 15.65 g.Prepared NF hollow controlled-releasem icrospheres were spherical in shape w ith particle size distribution of 24-40 mesh and drug loading of 8.66%;24 h floating rate in release medium was 97.93%,Q2h,Q12h,Q24hwere 20.49%,52.90%,91.00%(RSD<10%,n=3).Compared w ith the imported preparation,sim ilarity factor f2values of cumulative release were higher than 50,show ing in vitro drug-release was consistent w ith the zero-order kinetic equation(r=0.999 3);n of Ritger-Peppas equation(r=0.980 7)was 0.478.CONCLUSIONS:Prepare NF hollow controlled-release microspheres show similar drug-release behavior w ith the imported preparation,the drug is released by the combination of diffusion and erosion.
Nifedipine;Hollow controlled release microspheres;Formulation screen;Preparation;Orthogonal test;Quality evaluation
R943
A
1001-0408(2017)13-1820-04
2016-09-05
2016-11-17)
(编辑:邹丽娟)
国家自然科学基金资助项目(No.81341124);四川省科技计划项目(No.2014FZ0105,14ZC0066)
*助教。研究方向:临床药学。电话:0830-3165086。E-mail:weiky2015@sina.com
#通信作者:教授,博士。研究方向:新型药物递送系统和临床药学。电话:0830-3162292。E-mail:zhaoling-998@163.com
DOI10.6039/j.issn.1001-0408.2017.13.26
