元胡止痛片中延胡索乙素血药浓度的UPLC—MS/MS测定及药动学研究
2017-05-11单文静徐新蕊吴健
单文静+徐新蕊+吴健

[摘要] 目的 建立大鼠血浆中延胡索乙素的UPLC-MS/MS测定方法,并探讨大鼠灌胃元胡止痛片后其在大鼠体内的药动学过程。 方法 以流动相乙腈-0.1%甲酸水溶液,梯度洗脱,流速0.35 mL/min;采用电喷雾离子源,正离子检测模式扫描,多反应监测模式检测延胡索乙素血药浓度,并用DAS 3.0软件计算药动学参数。 结果 延胡索乙素在2.93~711 ng/mL线性关系良好,平均回收率均>87.6%,日内、日间RSD均< 15%。大鼠灌胃元胡止痛片后,延胡索乙素AUC0-t为(11 359±3026)ng·min/mL;t1/2为(342±36)min。 结论 UPLC-MS/MS能够快速、灵敏、专属地分析大鼠血浆中延胡索乙素的血药浓度,该方法适用于元胡止痛片在大鼠体内的药代动力学分析。
[关键词] 超高压液相色谱-二级质谱联用法;元胡止痛片;延胡索乙素;药物代谢动力学
[中图分类号] R927 [文献标识码] A [文章编号] 1673-7210(2017)03(a)-0036-04
UPLC-MS/MS determination and pharmacokinetic study of plasma concentration of Tetrahydropalmatine in Yuanhuzhitong Tablets
SHAN Wenjing1 XU Xinrui1 WU Jian2
1.Department of Pharmacy, the Fifth People's Hospital of Dalian City, Liaoning Province, Dalian 116021, China; 2.School of Science, Harbin University of Commerce, Heilongjiang Province, Harbin 150076, China
[Abstract] Objective To establish an UPLC-MS/MS determination method of Tetrahydropalmatine in rat plasma, explore pharmacokinetic process in rat after intragastric administration of Yuanhuzhitong Tablets. Methods The chromatography was eluted with mobile phase consisted of acetonitrile and 0.1% formic acid solution at the flow rate of 0.35 mL/min by gradient elution. Multiple-reaction monitoring scanning mode was employed for quantification with switching electrospray ion source polarity in positive mode. The pharmacokinetic parameters were calculated by using DAS 3.0 software. Results The linear ranges of Tetrahydropalmatine was 2.93-711 ng/mL. RSDs of inta-day and inter-day were all lower than 15%, and the average recovery was more than 87.6%. After intragastric administration of Yuanhuzhitong Tablets, AUC0-t of Tetrahydropalmatine was (11 359±3026) ng·min/mL, t1/2 was (342±36)min. Conclusion UPLC-MS/MS is a rapid, sensitive and specific method for the determination of Tetrahydropalmatine in rat plasma. This method is suitable for pharmacokinetic analysis of Yuanhuzhitong Tablets in rats.
[Key words] UPLC-MS/MS; Yuanhuzhitong Tables; Tetrahydropalmatine; Pharmacokinetics
元胡止痛片是比較典型的处方组成相对简单的中药复方制剂,该方剂是由延胡索(醋制)和白芷两味中药组成,具有理气、活血、止痛之功效,用于治疗气滞血瘀的胃痛、肋痛、头痛和痛经等。由于该方组方简单、疗效确切,被收载于1985年及以后各版《中国药典》。经研究发现,生物碱和香豆素类化合物是延胡索和白芷中的主要活性成分[1-3],且具有广泛的药理活性,如血管舒张、止痛、抗炎、抗焦虑及抗痉挛等[4-9]。其中延胡索乙素是延胡索中的异喹啉类生物碱,是元胡止痛片中的重要活性成分,具有较强的镇痛、镇静、催眠等药理作用,是元胡止痛片中的有效活性成分之一。处方中所用延胡索多经过醋制,因为游离的生物碱较难溶于水,经醋制后生成醋酸盐而易溶于水而发挥疗效[10-12]。
延胡索乙素既是元胡止痛片的物质基础,又是质量控制常用的指标物[13]。已有研究建立了元胡止痛片中延胡索乙素[14]及香豆素类成分[15-20]的质量控制方法,但未见药动学研究报道。本研究首次采用超高效液相色谱-串联质谱法(UPLC-MS/MS),研究元胡止痛片中代表性的延胡索乙素在大鼠体内的药代动力学行为,为该组方更深层次开发利用提供科学依据,为元胡止痛片的临床应用提供参考。
1 仪器、试药与方法
1.1 仪器
UPLC-MS/MS分析系统(由Agilent 1290高效液相色谱仪和Agilent 6460质谱检测器组成);LG16-B型高速离心机(北京雷勃尔离心机有限公司);Bandelin Sonorex RK 1208BH超声波清洗器(德国);HWS 24型电热恒温水浴锅(上海一恒科学仪器有限公司);Milipore超纯水机(美国Mililpore公司);METTLER Toledo AB265-S电子天平(瑞士)。
1.2 药品
甲醇、乙腈购于美国ACS恩科化学,乙酸、乙酸铵购于Sigma公司,均为色谱纯。水为超纯水,其余试剂均为分析纯。元胡止痛片购于哈尔滨人民同泰药房,生产厂家为河南宛西制药有限公司,生产批号:160102。延胡索乙素、柚皮苷购于中国食品药品检定研究院。
1.3 实验动物
清洁级雄性SD大鼠,体重(270±30)g,月龄为4个月,哈尔滨医科大学实验动物中心,许可证号:SCXK(黑)2013-001。
1.4 方法
1.4.1 标准溶液的配制 精密称取对照品延胡索乙素适量,用甲醇溶解并定容,得延胡索乙素(1.31 mg/L)的对照品储备液。
1.4.2 标准曲线血浆样品及质控样品的制备 精密吸取“1.4.1”项中延胡索乙素标准品溶液10 μL,加入空白血浆90 μL,涡旋30 s,配制成延胡索乙素2.93~659 ng/mL标准曲线血浆样品。延胡索乙素质控样品为4.35、47.9、527 ng/mL。
1.4.3 色谱条件 采用Waters ACQULTY UPLC C18(2.1 mm×100 mm,1.7 μm)色譜柱进行分析,以水(含0.1%甲酸溶液)为流动相A,乙腈为B,进行梯度洗脱。0~2 min,流动相A(%)为95→80;2~3 min,流动相A(%)为80→70;3~4 min,流动相A(%)为70→50;4~5 min,流速为0.35 mL/min进样量为1 μL,柱温为30℃。
1.4.4 质谱条件 电喷雾离子源(ESI源),检测方式:正离子检测,扫描方式:多反应离子监测(MRM),对照品的选择检测离子质荷比为延胡索乙素:356.2→192.1干燥气(N2)流速11.0 L/min,Nebulizer 0.10335 MPa,干燥气温度300℃,检测器电压4000 V。
1.4.5 血浆样品处理方法 取大鼠血浆50 μL,加入200 μL内标柚皮苷溶液(20.0 ng/mL)涡旋1 min,于4℃、15 000 r/min离心10 min,取上清液置离心管中,氮吹仪下氮气吹干,残留物用50 μL甲醇-水(50︰50)溶解,于4℃、15 000 r/min离心10 min,取上清液1 μL进样。
1.4.6 药动学 实验大鼠6只,自由饮水,给药前禁食12 h,灌胃给药,给予元胡止痛片3.0 g/kg。分别于给药后0.083、0.25、0.5、1、1.5、2、4、6、8、12、24 h眼底静脉丛毛细管取血0.1 mL/只,肝素钠抗凝,4500 r/min离心10 min,分离上层血浆,-40℃保存备用。
1.4.7 数据分析 血药浓度-时间数据采用DAS 3.0药动学软件按非房室模型处理,计算药动学参数,所得数据以x±s表示。
2 结果
2.1 方法学考察
2.1.1 专属性考察 取大鼠空白血浆、空白血浆+内标溶液、空白血浆+对照品、血浆样品,按血样处理方法处理,进样,结果见图1~4,血浆的内源性物质不干扰各成分和内标的测定,表明液质行为及专属性良好。
2.1.2 标准曲线和线性范围 取大鼠空白血浆,每份90 μL,加入延胡索乙素对照品系列溶液10 μL,制得被分析物的血药浓度为延胡索乙素2.93、8.79、26.3、79.1、237、711 ng/mL;分别精密吸取各标准曲线血浆样品50 μL,按“1.4.5”项的方法处理,在“1.4.3”项条件下进样测定,记录色谱图。采用加权(1/X2)最小二乘法,以待测成分峰面积与内标峰面积的比值(Y)对样品质量浓度(X)进行曲线拟合回归,得工作方程,定量限以S/N≥10计,线性方程Y=0.0416X+0.361,R2为0.9959,线性范围为2.93~711 ng/mL,延胡索乙素在相应的范围内线性良好。
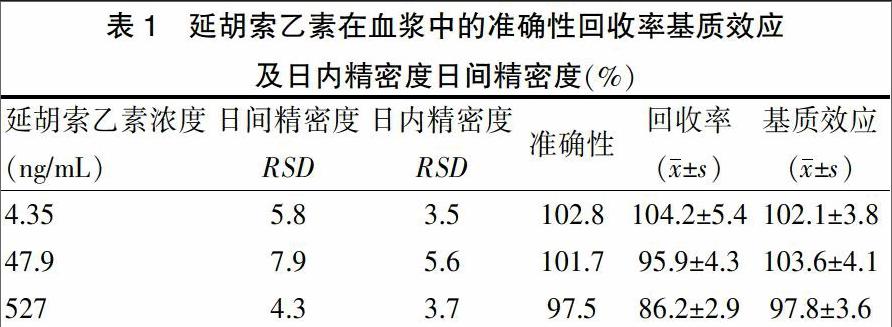
2.1.3 准确度和精密度 配制低、中、高3个质量浓度的对照品血浆样品,按“1.4.5”项下方法处理,每个质量浓度取6份样本,1 d内分别测定6份样品,并各取1份样品连续测定3 d,计算日内、日间精密度见表1。
2.1.4 回收率与基质效应 分别制备低、中、高浓度的含药QC样品,按“1.4.5”项下方法操作,进样分析,记录峰面积,每一浓度平行测定6份,记录待测物和内标的峰面积比值为A;另取空白血浆,按“1.4.5”项下方法操作处理后,加入对应的低、中、高浓度的系列对照品溶液进样分析,记录待测物和内标的峰面积比值为B,每一浓度平行测定6份;A/B×100%即得提取回收率。另用流动相将标准系列溶液配制成与上述理论浓度相同的低、中、高浓度溶液直接进样分析,每一浓度平行测定6份,记录待测物和内标的峰面积比值为C,基质效应的计算方法为B/C×100%。延胡索乙素低、中、高浓度的回收率和基质效应见表1。结果表明所建方法能够满足生物样品的测定要求。
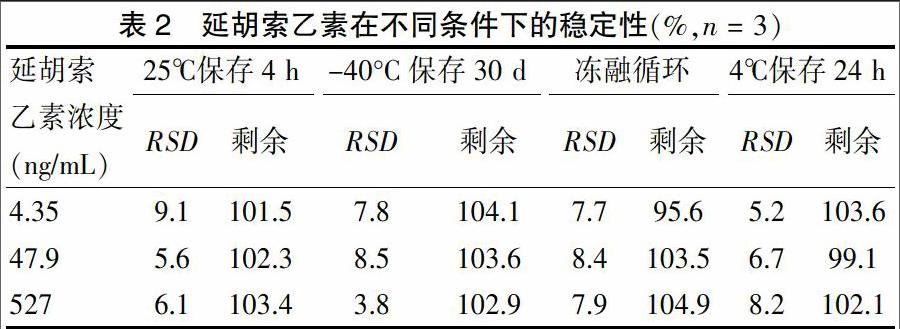
2.1.5 样本稳定性考察 考察各成分低、中、高3个质量浓度的质控样品室温放置、自动进样器内、-40℃长期冷冻、冷冻-解冻3个循环等不同存储条件下的稳定性。结果表明,血浆样品室温放置4 h、血浆样品处理后在自动进样器内放置24 h、血浆样品冷冻-解冻循环3次、血浆样品长期冷冻于-40℃冰箱内30 d,各成分的RSD均< 15%。见表2。
2.2 药动学试验
取健康SD大鼠6只,实验前12 h禁食不禁水。按3.0 g/kg(按照元胡止痛片使用说明书每人每次用量为1.5 g,药动学研究采用其给药量20倍灌胃给药,即每人每次30 g,参照人体-大鼠给药量折算方法,得大鼠给药量为3.0 g/kg)灌胃元胡止痛片,分别于给药后5、10、15、20、30、45、60、90、120、150、180、240、360、480、720、1440 min经大鼠眼球后静脉丛采血约0.1 mL,置肝素化试管中,4500 r/min离心10 min,分取上清,血浆置于-40℃冰箱中保存待测。样品按“1.4.5”项下方法处理,取上清进行UPLC-MS/MS测定。延胡索乙素在大鼠体内的血药浓度数据采用DAS 3.0软件进行计算,t1/2为(342±36)min,达峰浓度(Cmax)为(49.3±1.25)ng/mL,达峰时间(Tmax)为180 min和药-时曲线下面积(AUC0-t)为(10 246±2735)ng·min/mL,平均驻留时间(MRT0-t)为(482±38)min。见图5。
3 讨论
中药药代动力学是借助于药代动力学的基本理论研究中草药活性成分、组分、中药单方和复方体内吸收、分布、代谢和排泄的动态变化规律及其体内时量-时效关系。中药药代动力学虽起步较晚,但新理论、新方法的涌现以及HPLC、LC-MS和LC-NMR等检测手段的出现,为认识中药体内过程中所产生的药物信息提供了有力技术支撑。中药药代动力学为研究中药各化学成分的体内代谢过程和各组分间在体内的相互作用提供了新途径,但由于中药复方中的化学成分相对复杂且微量,如何从整体上阐明中药的药效物质基础是目前所面临的问题之一。延胡素作为君药,是元胡止痛片中的重要组成部分,其化學成分是发挥药理作用的物质基础。本文通过分析这种有效成分在体内的药代动力学过程,为阐明元胡止痛片的药理作用提供参考。本文采用UPLC-MS/MS及内标法对延胡索乙素进行定量测定,保证了血药浓度结果的准确性。UPLC-MS/MS检测一个样品所需时间短,且所需的血浆样本量少,非常适合药代动力学等研究中的大批量样品研究。
在样品处理过程中,分别考察了甲醇沉淀蛋白法、乙腈沉淀蛋白法、乙酸乙酯萃取法,对各自所得回收率进行分析,结果显示,甲醇沉淀蛋白法提取回收率最高且处理方法较为简单。根据UPLC-MS/MS的分析结果,发现元胡止痛片灌胃给药后,延胡索乙素能迅速吸收入血发挥作用。
[参考文献]
[1] 曹庆忱,刘威,李功妍,等.HPLC法测定元胡止痛片中欧前胡素的含量[J].辽宁中医杂志,2010,37(12):2427-2429.
[2] 王景刚,邹宇,李可强.HPLC法测定元胡止痛片中欧前胡素的含量[J].辽宁中医杂志,2010,37(5):897-899.
[3] 朱海琳,孟兆青,丁岗,等.HPLC指纹图谱技术评价不同厂家元胡止痛片质量[J].世界科学技术,2015,17(7):1460-1466.
[4] 刘严宏,刘延平,耿雅杰,等.LC-MS/MS法同时测定犬血浆中延胡索乙素和欧前胡素及其在元胡止痛片药动学研究中的应用[J].中草药,2016,47(15):2668-2675.
[5] 孙绍鑫,韩立炜,黄银峰.不同厂家元胡止痛片中延胡索乙素含有量比较[J].中成药,2012,34(1):180-182.
[6] 刘源,马双成.反相高效液相色谱法测定元胡止痛片中延胡索乙素含量[J].中国药业,2010,19(15):27-29.
[7] 刘琳琳,李正国,刘丽芳,等.分光光度法测定元胡止痛片中延胡索总生物碱的含量[J].中国医药科学,2012,2(3):141-143.
[8] 王云龙,陈晓辉,许世伟,等.高效液相色谱法同时测定元胡止痛片中欧前胡素、延胡索乙素与异欧前胡素的含量[J].中国医药导报,2010,7(1):58-60.
[9] 龚红全,曾承辉,毋福海,等.毛细管电泳法同时测定元胡止痛片中欧前胡素和异欧前胡素的含量[J].中国药房,2010,21(15):1389-1391.
[10] 肖炳燚,聂平,蒋秋桃,等.元胡止痛片UPLC特征图谱的研究[J].中南药学,2014,12(4):294-296.
[11] 俞晓艳,原永芳.元胡止痛片联合布洛芬和维生素B1治疗带状疱疹后遗神经痛的疗效观察[J].现代药物与临床,2015,30(10):1251-1253.
[12] 李方帅.元胡止痛片联合芬太尼在骨科老年患者术后镇痛中的应用[J].亚太传统医药,2016,12(3):125-127.
[13] 高俐.元胡止痛片联合膈下逐瘀汤对气滞血瘀型原发性痛经的疗效及血清性激素的影响[J].中国药物与临床,2016,16(2):249-251.
[14] 邱鹏程,张笑恺,王四旺.元胡止痛方的研究进展[J].时珍国医国药,2015,26(12):2993-2996.
[15] 俞峭拔,何淑霞,应晓剑,等.双歧杆菌四联活菌联合元胡止痛片治疗腹泻型肠易激综合征效果观察[J].中国乡村医药,2016,23(17):36-38.
[16] 张波,易清,虞泽,等.元胡止痛片快速显微、化学反应和荧光鉴别法[J].中国医院药学杂志,2013,33(5):412-414.
[17] 刘瑞新,王青晓.元胡止痛片的质量控制研究[J].中国药品标准,2010,11(5):343-346.
[18] 陈岳涛,曹蔚,谢艳华,等.元胡止痛片及其主要成分对大鼠实验性痛经的影响[J].陕西中医,2013,34(1):111-114.
[19] 谭镭,詹雁,阮佳,等.胃内漂浮缓释制剂在复方左金和元胡止痛片中的应用研究[J].世界中医药,2013,8(5):557-561.
[20] 张笑恺,曹蔚,王四旺.元胡止痛片有效成分作用机制和药代动力学研究进展[J].亚太传统医药,2010,6(4):107-109.
