高效液相色谱法测定芩香清解口服液中黄芩苷的含量
2017-05-11黄娟萍庄满贤黄大森萧雪莹王显著
黄娟萍,庄满贤,黄大森,陈 元,萧雪莹,王 霆,王显著
(广州一品红制药有限公司研发中心,广东 广州510765)
高效液相色谱法测定芩香清解口服液中黄芩苷的含量
黄娟萍*,庄满贤,黄大森,陈 元,萧雪莹,王 霆,王显著#
(广州一品红制药有限公司研发中心,广东 广州510765)
目的:建立高效液相色谱法测定芩香清解口服液中黄芩苷含量的方法,以建立芩香清解口服液的质量控制标准。方法:色谱柱为Agilent SB-C18柱(250 mm×4.6 mm,5 μm),流动相为甲醇-水-磷酸(V∶V∶V=47 ∶53 ∶0.2),检测波长为280 nm,流速为1.0 ml/min,进样量为10 μl,柱温为30 ℃。结果:黄芩苷质量浓度在2.409~77.080 μg/ml范围内线性关系良好,平均加样回收率100.0%,RSD为1.7%。结论:本研究方法操作简便、准确度高、重复性好,可用于芩香清解口服液的质量控制。
芩香清解口服液; 质量标准; 高效液相色谱法
芩香清解口服液由黄芩、广藿香、蝉蜕、石膏、葛根、大黄、芍药等12味中药制成,具有疏散风热、清泻里热、解毒利咽的功效,主要用于小儿上呼吸道感染表里俱热证,症见发热、鼻塞、流涕、咳嗽、咽红肿痛、便秘、口渴烦躁、舌红苔黄、脉洪数等者。临床研究表明,其在治疗小儿急性上呼吸道感染表里俱热证是有效及安全的[1]。 芩香清解口服液的处方药材较多,成分复杂,因此建立完善的制剂质量标准对产品质量控制意义较大。为保障本品的质量可控性,本研究对芩香清解口服液中黄芩苷的含量进行测定。
1 材料
1.1 仪器
安捷伦1260型高效液相色谱仪(美国Agilent公司),DAD检测器,Chem Station Edition数据处理系统;Sartorius CPA225D型十万分之一天平(德国赛多利斯公司);Masrer-QUT型纯水机(上海和泰仪器有限公司)。
1.2 药品与试剂
芩香清解口服液[太阳石(唐山)药业有限公司,批号:20150501、20150502、20150503;广州一品红制药有限公司,批号:20150801、20150802、20150803]。黄芩苷对照品(批号:110715-201318)购买于中国食品药品检定研究院;甲醇为色谱纯,水为实验室自制超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 供试品溶液:精密吸取本品5 ml,置于100 ml容量瓶中,加70%乙醇稀释至刻度,摇匀。精密吸取1.0 ml,置于10 ml容量瓶中,加70%乙醇稀释至刻度,摇匀,用0.45 μm微孔滤膜滤过,即得。
2.1.2 对照品溶液:取黄芩苷对照品适量,精密称定,加70%乙醇制成每1 ml含18 μg的溶液,即得。
2.1.3 阴性对照溶液:按处方比例分别称取除黄芩外的其余药味,按处方制备方法制备缺黄芩阴性样品,再按照“2.1.1”项下方法制备阴性对照溶液。
2.2 色谱条件
填充剂为十八烷基硅烷键合硅胶,色谱柱为Agilent SB-C18柱(250 mm×4.6 mm,5 μm);流动相为甲醇-水-磷酸(V∶V∶V=47 ∶53 ∶0.2);检测波长为280 nm;流速为1.0 ml/min;进样量为10 μl;柱温为30 ℃。
2.3 系统适应性试验
分别取对照品溶液、供试品溶液和阴性对照溶液,按照“2.2”项下色谱条件进样测定,理论板数按黄芩苷峰面积计算≥2 500。黄芩苷与相邻峰之间分离度>1.5,表明阴性对照测定无干扰,见图1。
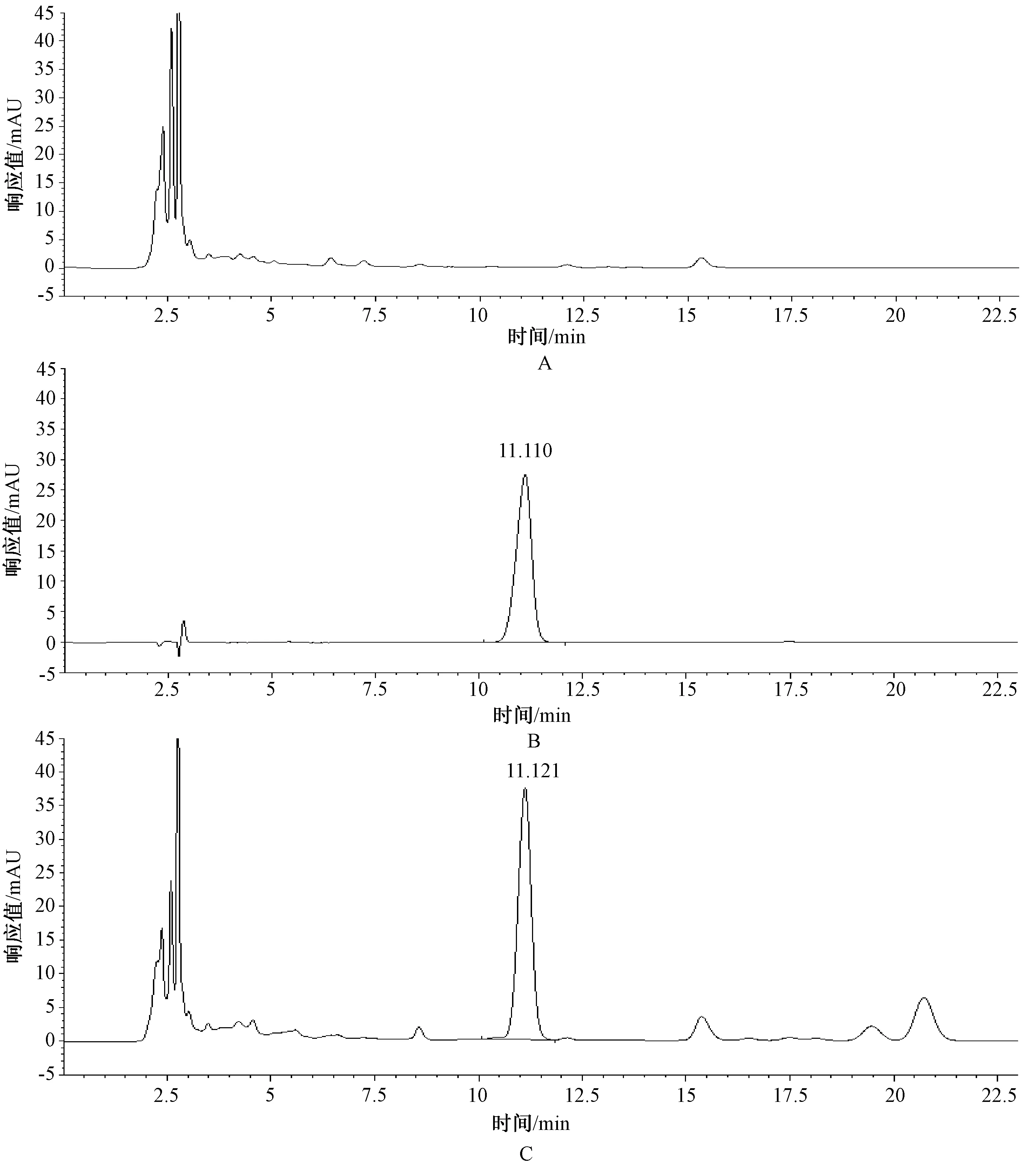
A.阴性对照溶液;B.对照品溶液;C.供试品溶液A. negative control solution; B. control solution; C. test solution图1 高效液相色谱图Fig 1 HPLC
2.4 精密度试验
取“2.1.2”项下对照品溶液,按照“2.2”项下色谱条件连续进样6次,计算黄芩苷峰面积的RSD=0.4%。结果表明,仪器精密度良好。
2.5 线性关系考察
按“2.1.2”项下方法分别配制质量浓度为2.409、4.818、9.636、19.270、38.540、57.810、77.080 μg/ml的溶液,按照“2.2”项下色谱条件分别进样10 μl,记录色谱图。以对照品溶液浓度为横坐标(X),峰面积为纵坐标(Y),进行线性回归,得线性回归方程Y=37.244 56X+3.629 44,r=0.999 97,结果表明黄芩苷质量浓度在2.409~77.080 μg/ml范围内线性关系良好。
2.6 重复性试验
取同一批样品(批号:20150501),按“2.1.1”项下方法制备供试品溶液6份,按照“2.2”项下色谱条件进样测定,计算黄芩苷含量的平均值(n=6)为4.6 mg/ml,RSD为0.8%。结果表明,本方法重复性良好。
2.7 稳定性试验
取“2.1.1”项下供试品溶液(批号:20150501)适量,分别于室温(25 ℃)下放置0、3、7、13、22、48 h时按照“2.2”项下色谱条件进样测定,计算黄芩苷含量RSD=1.3%(n=6)。结果表明,供试品溶液在室温下48 h内稳定性良好。
2.8 中间精密度试验
由2位不同分析员,在不同时间分别取同一批样品(批号:20150501),按“2.1.1”项下方法制备供试品溶液6份,并使用不同的仪器进行分析,记录色谱图并计算黄芩苷含量RSD=1.0%(n=12)。结果表明,本方法中间精密度良好。
2.9 加样回收率试验
取已知含量的供试品(批号:20150501)9份,每份2.5 ml,分别加入低、中、高3个质量浓度(分别为0.240 62 mg/ml)的黄芩苷对照品40、50、60 ml,每个质量浓度3份,按照“2.2”项下色谱条件进样测定,结果见表1。
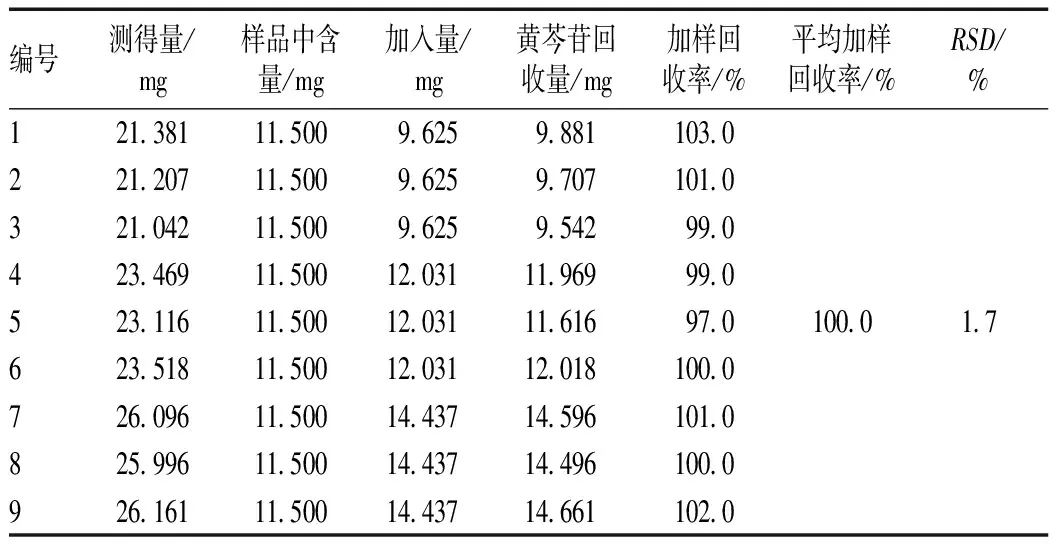
表1 黄芩苷加样回收率试验结果
2.10 黄芩苷的含量测定
取6批芩香清解口服液样品(批号:20150501、2150502、20150503、20150801、2150802、20150803),按“2.1.1”项下方法制备供试品溶液各2份,按照“2.2”项下色谱条件进样测定,采用外标法计算芩香清解口服液中黄芩苷的含量,见表2。

表2 黄芩苷的含量测定结果
3 讨论
3.1 测定成分的选择
黄芩以根入药,味苦、性寒,有清热燥湿、泻火解毒、止血、安胎等功效,现多与其他药物组合成中药复方制剂,治疗感冒、发热和流感病毒感染等疾病[2-3]。黄芩含多种黄酮类化合物,主要为黄芩苷、黄芩素、汉黄芩苷、汉黄芩素等[4-6],而黄芩苷为黄芩的主要有效成分,常被选择为制剂的质量控制指标[7-10]。黄芩为本方中君药,故选择其主要成分黄芩苷作为指标成分进行测定。
3.2 波长及流动相的选择
在200~400 nm对样品进行波长扫描,黄芩苷在280 nm处有最大吸收,扫描结果与相关研究[8-12]结果一致,故选择280 nm作为检测波长。本研究曾考察过多种溶液作为流动相,包括不同比例的甲醇-水、乙腈-水、甲醇-磷酸溶液,发现甲醇-水-磷酸(V∶V∶V=47 ∶53 ∶0.2)作为流动相时,黄芩苷的分离度及峰性状是最好的,故选择此流动相[13-16]。
3.3 耐用性试验
本研究考察了色谱条件中的流速、柱温、波长、流动相比例、色谱柱等发生微小变化时,黄芩苷含量测定结果受影响的程度。结果表明,流速分别为0.95、1.00、1.05 ml/min时,黄芩苷含量RSD=1.1%(n=6);柱温分别为20、30、40 ℃时,黄芩苷含量RSD=0.0%(n=6);波长分别为270、280、290 nm时,黄芩苷含量RSD=0.0%(n=6);流动相分别为甲醇-水-磷酸(V∶V∶V=45 ∶55 ∶0.2)、甲醇-水-磷酸(V∶V∶V=47 ∶53 ∶0.2)、甲醇-水-磷酸(V∶V∶V=49 ∶51 ∶0.2)时,黄芩苷含量RSD=1.1%(n=6);色谱柱分别为Thermo ODS HYPERSIC色谱柱(250 mm×4.6 mm,5 μm)、Agilent SB-C18柱(250 mm×4.6 mm,5 μm)、依利特Hypersil ODS2柱(250 mm×4.6 mm,5 μm)时,黄芩苷含量RSD=0.0%(n=6),因此本方法耐用性较好,适用范围广。
[1]李井锋,马融,胡思源,等.芩香清解口服液治疗小儿急性上呼吸道感染表里俱热证的多中心临床研究[J].中华中医药杂志,2015,30(10):3794-3796.
[2]国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:301-302.
[3]Ding Y,Dou J,Teng Z,et al.Antiviral axtivity og baicalin against influenza A(H1N1/H3N2) virus in cell culture and in mice and its inhibition of neuraminidase[J].Arch Virol,2014,159(12):3269-3278.
[4]王孟华,曲玮,梁敬钰.黄芩的研究进展[J].海峡药学,2013,25(9):6-13.
[5]刘金欣,孟繁蕴,张胜海,等.UPLC同时测定黄芩中黄芩苷、黄芩素、汉黄芩苷、汉黄芩素、千层纸素A[J].中草药,2014,45(10):1477-1480.
[6]郑勇凤,王佳婧,傅超美,等.黄芩的化学成分与药理作用研究进展[J].中成药,2016,38(1):141-148.
[7]安静,董占军,孙源.HPLC测定茵桅黄口服液中的黄芩苷[J].华西药学杂志,2015,30(2):236-237.
[8]宋宗华,王鹏,陈晓辉,等.中药黄芩和一清颗粒中黄芩苷HPLC定量分析方法学验证参数限度考察[J].药物分析杂志,2010,30(6):1140-1144.
[9]王葳,刘冬丽,李维熙,等.蒲地蓝消炎片中黄芩苷的含量测定[J].中国民族民间医药,2016,25(3):17-18.
[10] 陈旭,田明.柴胡桂姜颗粒中黄芩苷含量测定方法研究[J].中国执业药师,2016,13(11):27-30.
[11] 林超,史敏,王永和.HPLC测定和胃化滞丸中黄芩苷的含量[J].中国执业药师,2016,13(8):32-34.
[12] 何玲玲,韦国兵,胡奇军.高效液相色谱法测定银黄口服液中黄芩苷含量及不确定度分析[J].中国现代医学杂志,2015,25(34):15-18.
[13] 翟媛媛,师永清.HPLC法同时测定清心明目上清片中栀子苷、连翘苷、黄芩苷和盐酸小檗碱的含量[J].西北民族大学学报:自然科学版,2016,36(1):13-17.
[14] 李昂,阚红玉,张囡.HPLC法同时测定疏表灵颗粒中绿原酸、橙皮苷、黄芩苷的含量[J].中国药房,2016,27(27):3872-3874.
[15] 孙艳涛.HPLC双波长法同时测定消石利胆胶囊中芍药苷、橙皮苷、黄芩苷和大黄酚的含量[J].中国药师,2016,19(4):801-803.
[16] 邵礼梅,王云龙,李延雪.高效液相色谱法测定蒲地蓝消炎片中黄芩苷与黄芩素含量[J].中国药业,2012,21(4):37-38.
Content Determination of Baicalin in Qinxiangqingjie Oral Liquid by HPLC
HUANG Juanping, ZHUANG Manxian, HUANG Dasen,CHEN Yuan, XIAO Xueying, WANG Ting, WANG Xianzhu
(Research and Development Center, Guangzhou Yipinhong Pharmaceutical Co., Ltd., Guangdong Guangzhou 510760, China)
OBJECTIVE:To establish the method for content determination of baicalin in Qinxiangqingjie oral liquid by HPLC, so as to establish the quality control specification of Qinxiangqingjie oral liquid. METHODS:The chromatographic column was Agilent SB-C18(250 mm×4.6 mm,5 μm), the mobile phase was methanol - water - phosphoric acid(V∶V∶V=47 ∶53 ∶0.2), with detective wave length of 280 nm, flow rate of 1.0 ml/min, sample size of 10 μl and column temperature of 30 ℃. RESULTS:Baicalin in 2.409 μg/ml-77.080 μg/ml had good linear relationship, the average recovery rate was 100.0%,RSDwas 1.7%. CONCLUSIONS:The method is simple, high accuracy and good repeatability, which could be used for quality control of Qinxiangqingjie oral liquid.
Qinxiangqingjie oral liquid; quality standards; HPLC
R927.2
A
1672-2124(2017)04-0526-04
2016-11-17)
*工程师,硕士。研究方向:新药研发。E-mail:390447099@qq.com
#通信作者:高级工程师,硕士。研究方向:新药研发。E-mail:wxz971509@163.com
DOI 10.14009/j.issn.1672-2124.2017.04.037
