重组人血管内皮抑制素联合替吉奥胶囊治疗中晚期原发性肝癌的临床观察Δ
2017-04-28史克志许新华三峡大学第一临床医学院宜昌市中心人民医院肿瘤科湖北宜昌443002三峡大学肿瘤防治中心湖北宜昌443002
苏 进,史克志,刘 洋,钱 莹,许新华(.三峡大学第一临床医学院/宜昌市中心人民医院肿瘤科,湖北宜昌 443002;2.三峡大学肿瘤防治中心,湖北宜昌 443002)
·药物与临床·
重组人血管内皮抑制素联合替吉奥胶囊治疗中晚期原发性肝癌的临床观察Δ
苏 进1*,史克志1,刘 洋1,钱 莹1,许新华2#(1.三峡大学第一临床医学院/宜昌市中心人民医院肿瘤科,湖北宜昌 443002;2.三峡大学肿瘤防治中心,湖北宜昌 443002)
目的:观察重组人血管内皮抑制素联合替吉奥胶囊治疗中晚期原发性肝癌的疗效和安全性。方法:将2012年2月-2014年12月三峡大学第一临床医学院收治的94例中晚期原发性肝癌患者按随机数字表法分为联合组(48例)和对照组(46例),对照组患者每天早晚餐后30 min内口服替吉奥胶囊40~60 mg,bid;联合组患者在对照组基础上给予重组人血管内皮抑制素注射液150 mg加入0.9%氯化钠注射液210 mL中,采用便携式微量泵持续泵注120 h。治疗14 d后间隔7 d为1个周期,两组患者均治疗2个周期后评价近期客观疗效、临床受益反应(CBR)及不良反应,并比较病情进展时间和平均生存期。结果:联合组患者客观有效率为14.6%,疾病控制率为66.7%,疾病进展时间为(5.5±1.3)个月,平均生存期为(10.7±3.8)个月;对照组患者客观有效率为8.7%。疾病控制率为45.6%,疾病进展时间为(4.8±1.2)个月,平均生存期为(8.9±3.3)个月,组间比较差异均有统计学意义(P<0.05)。联合组患者总CBR率(79.2%)显著高于对照组(52.2%),差异有统计学意义(P<0.05)。两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。结论:重组人血管内皮抑制素联合替吉奥治疗中晚期原发性肝癌可获得较好的疗效和耐受性,且不会增加不良反应发生率。
替吉奥胶囊;重组人血管内皮抑制素;原发性肝癌
原发性肝癌是我国死亡风险最高的消化道恶性肿瘤;大多数患者就诊时已达中晚期,临床治疗以经肝动脉介入栓塞化疗(TACE)、消融(射频、微波和无水乙醇)、全身化疗等保守治疗为主。受多方面原因限制,原发性肝癌缺乏系统化疗的标准方案。近年来,奥沙利铂、卡培他滨和替吉奥等高效低毒的新型细胞毒性药物陆续上市和广泛应用,有力地推动了肝癌系统性化疗的相关研究[1]。重组人血管内皮抑制素作为我国自主创新研发的新型人血管内皮抑制素,联合长春瑞滨+顺铂(NP)方案治疗非小细胞肺癌取得了显著疗效[2]。原发性肝癌是富血管恶性肿瘤,丰富的血管在临床上是一个潜在的治疗靶点,吴梨华等[3]曾报道TACE联合血管内皮抑素治疗中晚期原发性肝癌近期疗效优于单用TACE治疗,但关于新型化疗药物联合重组人血管内皮抑制素治疗原发性肝癌的安全性尚有待评价。因此,本研究观察了替吉奥胶囊联合重组人血管内皮抑制素治疗原发性肝癌的疗效和安全性,现报道如下。
1 资料与方法
1.1 纳入与排除标准
纳入标准:(1)符合《中国常见恶性肿瘤诊治规范》[4]诊断标准者;(2)所有患者均为首次确诊,有可评价的病灶;(3)无手术及介入治疗的禁忌证,愿意接受全身化疗。排除标准:(1)有明显器质性病变者;(2)对本研究药物有禁忌证者;(3)精神障碍者。
1.2 研究对象
选取2012年2月-2014年12月三峡大学第一临床医学院收治的原发性肝癌患者94例,按随机数字表法分为对照组(46例)和联合组(48例)。其中,对照组患者男性30例,女性16例;年龄55~75岁,平均年龄(60.4± 5.14)岁;Ⅱ期34例,Ⅲ期12例;Child分级[4]A级17例,Child B级23例,Child C级6例。联合组患者男性32例,女性16例;年龄55~75岁,平均年龄(61.4±4.84)岁;Ⅱ期34例,Ⅲ期14例;Child分级,A级17例,Child B级24例,Child C级7例。两组患者一般资料比较,差异均无统计学意义(P>0.05),具有可比性。本研究方案经医院医学伦理委员会批准,患者知情同意并签署知情同意书。
1.3 治疗方法
对照组患者每天早晚餐后30 min内口服替吉奥胶囊(山东新时代药业有限公司,批准文号:国药准字H20080802,规格:20 mg)40~60 mg,bid;联合组患者在对照组基础上给予重组人血管内皮抑制素注射液(山东先声麦得津生物制药有限公司,批准文号:国药准字S20050088,规格:15 mg)150 mg加入0.9%氯化钠注射液210 mL中,采用便携式微量泵以2 mL/h持续泵注120 h。治疗14 d后间隔7 d为1个周期,两组患者均治疗2个周期后进行疗效评定。
1.4 观察指标
(1)观察两组患者临床疗效。按世界卫生组织(WHO)实体瘤评价标准[5]将近期客观疗效——完全缓解(CR),即所有目标病灶消失;部分缓解(PR),即基线病灶长径总和缩小>30%;稳定(SD),即基线病灶长径总和增加>20%或出现新病灶;进展(PD):基线病灶长径总和有缩小但未达PR或有增加但未达PD。客观有效率(ORR)=(CR例数+PR例数)/总例数×100%,疾病控制率(DCR)=(CR例数+PR例数+SD例数)/总例数× 100%。在治疗前和第2周期疗程结束后复查肝脏增强电子计算机断层扫描(CT)或磁共振(MRI),评价肝内病灶改变情况。(2)临床受益反应(CBR)评价标准[6]:每周评估止痛药用量、疼痛评分、卡氏(KPS)评分及体质量变化。当KPS评分提高≥20分、体质量增加≥7%、止痛药物用量减少≥50%中任意一项指标阳性并持续4周,则判定CBR获益。(3)观察两组患者疾病进展时间、平均生存时间及不良反应发生情况。所有病例随诊至2015年9月。
1.5 统计学方法
采用SPSS 17.0软件对数据进行统计学分析。计量资料以±s表示,组间比较采用配对t检验;计数资料以例数或率表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者近期客观疗效比较
联合组患者ORR为14.6%、DCR为66.7%,显著高于对照组的8.7%和45.6%,差异均有统计学意义(P<0.05),详见表1。
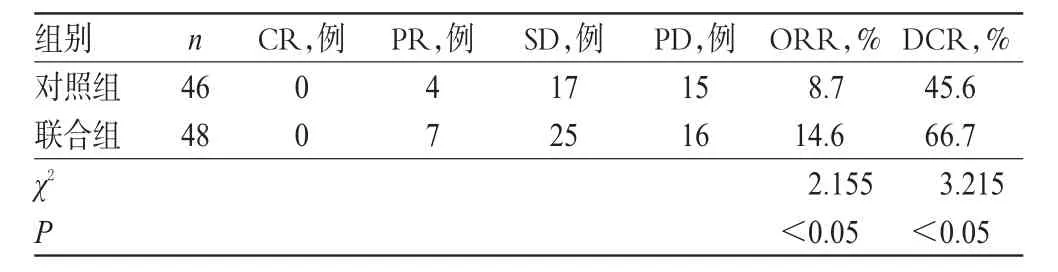
表1 两组患者近期客观疗效比较Tab 1 Comparison of short-term objective therapeutic efficacy between 2 groups
2.2 两组患者CBR比较
联合组患者总CBR率为79.2%,显著高于对照组的52.2%,差异有统计学意义(P<0.05),详见表2。
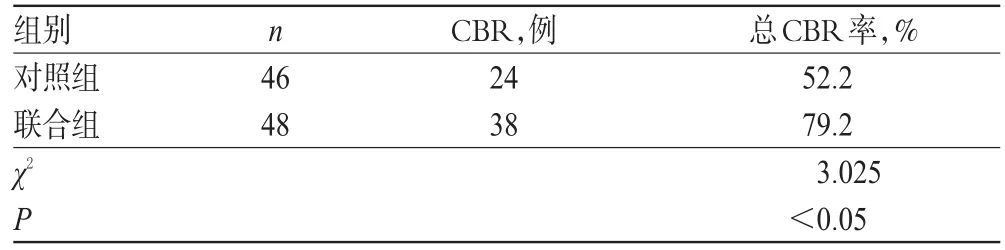
表2 两组患者CBR比较Tab 2 Comparison of clinical benefit response between 2 groups
2.3 两组患者疾病进展时间和平均生存时间比较
随访采取来院复查或电话询问方式,随访至患者死亡或2015年9月。共5例患者失访,其中联合组2例,对照组3例,失访率为5.3%(5/94),失访者按死亡计。结果显示,联合组患者疾病进展时间和平均生存时间显著长于对照组,差异有统计学意义(P<0.05),详见表3。
表3 两组患者疾病进展时间和平均生存时间比较(x± s,月)Tab 3 Comparison of disease progression time and average survival period between 2 groups(±s,month)
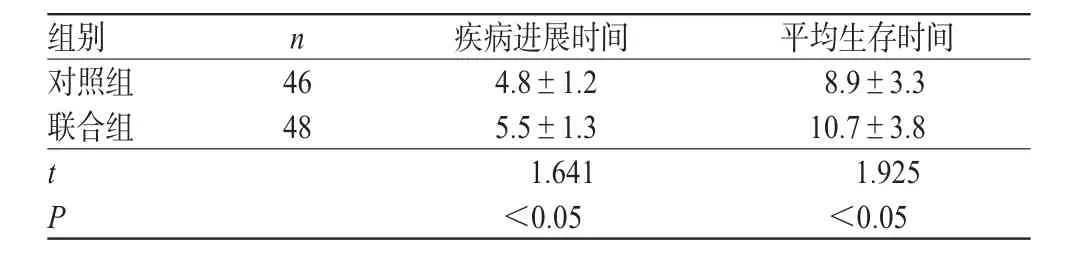
表3 两组患者疾病进展时间和平均生存时间比较(x± s,月)Tab 3 Comparison of disease progression time and average survival period between 2 groups(±s,month)
组别对照组联合组n 4 6 4 8 t P疾病进展时间4.8 ± 1.2 5.5 ± 1.3 1.6 4 1<0.0 5平均生存时间8.9 ± 3.3 1 0.7 ± 3.8 1.9 2 5<0.0 5
2.4 不良反应
两组患者不良反应包括骨髓抑制、食欲减退、肝功能损害及手足综合征等与化疗相关的毒副反应,多以Ⅰ~Ⅱ级为主,经对症处理后患者基本可耐受。其中,联合组患者骨髓抑制发生率为31.25%,消化系统反应(恶心、呕吐、食欲下降等)发生率为18.75%,其他发生率为6.25%。对照组骨髓抑制发生率为34.78%,消化系统反应发生率为15.22%,其他发生率为4.35%。两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。
3 讨论
原发性肝癌是严重危害人类生命健康的重大疾病之一,大部分原发性肝癌患者诊断时仅能选择保守治疗。大多数肝癌细胞对化学药物的敏感性较差,至今临床尚无统一成熟的标准化疗方案。虽然分子靶向药物如索拉非尼已获批用于晚期原发性肝癌,但存在客观有效率低、价格昂贵、不良反应较多等缺点。
近年来,奥沙利铂和替吉奥在内的新型细胞毒性药物陆续问世和广泛应用,有力地推动肝癌化疗治疗的研究。2010年的研究首次证明了全身化疗特别是含奥沙利铂的方案能够为晚期肝癌患者带来较好的DCR和生存获益[6]。因此,FOLFOX 4方案(奥沙利铂+亚叶酸钙+氟尿嘧啶)作为晚期原发性肝癌治疗的推荐方案被原卫生部颁发的《原发性肝癌诊疗规范(2011年版)》所收录[7]。
替吉奥胶囊是新一代氟尿嘧啶类口服复合制剂,其活性成分包括替加氟(FT)、吉美嘧啶(CDHP)及奥替拉西(Oxo)3种生物调节剂。其中FT为5-氟尿嘧啶(5-FU)的前体药物,能在活体内转化为5-FU,干扰和阻断DNA、RNA及蛋白质合成;CDHP通过抑制在二氢嘧啶脱氢酶(DPD)作用下从FT转化而来的5-FU的分解代谢,有助于长时间维持机体特别是瘤体组织中5-FU的有效浓度,达到甚至超越5-FU持续静滴的疗效;Oxo具有阻断5-FU磷酸化的能力,其在胃肠组织中具有非常高的浓度分布,可降低5-FU在胃肠道中产生的毒性和不良反应。由于原发性肝癌细胞内一般高表达DPD,而替吉奥具有明显抑制DPD活性的作用,所以替吉奥相比其他氟尿嘧啶类药物,更具有治疗优势[8]。
肿瘤血管靶向药物重组人血管内皮抑制素的研发应用给恶性肿瘤治疗带来了新的曙光,其能够特异性抑制肿瘤新生血管形成,阻断肿瘤细胞的营养供应,加速其细胞凋亡过程,目前已被非小细胞肺癌临床实践指南(中国版)推荐为一线治疗药。根据Gompertzian定律[9],肿瘤主体经化学治疗减负荷后,体内残存的肿瘤细胞进入快速再增殖周期,通过邻近的肿瘤血管获得氧气和养料,进而分泌肿瘤血管生成因子,引起血管内皮细胞增殖、在瘤内形成新血管,供养其继续生长。因此,抗血管生成药物与化疗药物具有协同抗肿瘤作用,并在多项临床研究中已得到证实[10-11]。原发性肝癌丰富的肿瘤血管是临床上潜在的治疗靶点。本研究结果也显示,联合组患者ORR、DCR和CBR均显著高于对照组,疾病进展时间和平均生存时间均长于对照组,提示替吉奥胶囊与重组人血管内皮抑制素联用具有较好的协同作用。
重组人血管内皮抑制素的半衰期为8~12 h,传统的给药方式为每日静滴3~4 h,连续2周。这种间断性短程用药导致药物浓度波动较大,无法维持稳态的浓度,同时患者依从性较差[12-13]。本研究采用便携式静脉泵连续泵注的给药方式,较静脉滴注给药减少了护理人员配制药物的工作量;患者随身携带重组人血管内皮抑制素泵,可自由活动,免受每日静滴长时间卧床对日常生活造成的不便,大大提高了患者的依从性和舒适度。
综上所述,重组人血管内皮抑制素联合替吉奥治疗中晚期原发性肝癌可获得较好的疗效和耐受性,且不会增加不良反应发生率。但本研究随访时间较短,有待延长随访时间,进一步观察患者的远期生存率。
[1] 龚新雷,秦叔逵.系统化疗治疗原发性肝细胞癌的现状和研究进展[J].中国新药杂志,2014,23(17):1994-2015.
[2] 马红莲,惠周光,赵路军,等.不可切除Ⅲ期NSCLC持续静脉泵注恩度联合同期放化疗前瞻性多中心Ⅱ期临床试验初步结果[J].中华放射肿瘤学杂志,2016,25(2):114-118.
[3] 吴梨华,吴建兵,余志宏,等.重组人血管内皮抑素联合经皮肝动脉化学栓塞术治疗中晚期原发性肝癌[J].实用医学杂志,2011,27(14):2539-2541.
[4] 中国抗癌协会.新编常见恶性肿瘤诊治规范[M].北京:中国协和医科大学出版社,1999:20-85.
[5] 刘秋华,林榕波.实体瘤疗效评价标准(RECIST)指南1.1版[C]//全国临床肿瘤大会暨2009年CSCO学术年会. 2009.
[6] Qin SK,Bai Y,Sun Y,et al.PhaseⅢstudy of oxaliplatin plus 5-fluorouracil/leucovorin(FOLFOX4)versus doxorubicin as palliative systemic chemotherapy in advanced HCC in Asian patients[J].J Clin Oncol,2010,28(15 Suppl):4008.
[7] 卫生部.原发性肝癌诊疗规范:2011年版[J].临床肿瘤学杂志,2011,16(10):929-946.
[8] Burris HA,Moore M J,Andersen J,et al.Improvements in survival and clinical benefit with gemcitabine as firsttime therapy for patients with advanced pancreas cancer:a randomized trial[J].J Clin Oncol,1997,15(6):2403-2413.
[9] Parkin DM,Bray F,Ferlay J,Pisani P.Global cancer sta-tistics,2002[J].CA Cancer J Clin,2005,55(2):74-108. [10] Kim SJ,Han SW,Oh DY,et al.Combination chemotherapy with S-1 and platinum in advanced hepatocellular carcinoma[J].Anticancer Res,2010,30(12):5245-5250.
[11] 周琦超,包勇,余忠华,等.不可手术切除Ⅲ期非小细胞肺癌恩度联合同期放化疗多中心Ⅰ+Ⅱ期临床试验[J].
中华放射肿瘤学杂志,2012,21(6):500-503.
[12] 汪露,江涛.重组人血管内皮抑制素联合化疗治疗晚期非小细胞肺癌的临床观察[J].中国药房,2014,25(46):4361-4364.
[13] 吕畅,王红芳,阎雪莹.以血管内皮生长因子及其受体为靶点的抗肿瘤药的研究进展[J].中国药房,2016,27(13):1851-1853.
Clinical Observation of S-1 Capsules Combined with Recombinant Human Endostatin in the Treatment of Middle and Advanced Primary Liver Carcinoma
SU Jin1,SHI Kezhi1,LIU Yang1,QIAN Ying1,XU Xinhua2(1.Dept.of Oncology,the First College of Clinical Medical Science,China Three Gorges University/Yichang Central People’s Hospital,Hubei Yichang 443002,China;2.Cancer Center,China Three Gorges University,Hubei Yichang 443002,China)
OBJECTIVE:To observe therapeutic efficacy and safety of S-1 capsules combined with recombinant human endostatin in the treatment of middle and advanced primary liver carcinoma.METHODS:Totally 94 patients with middle and advanced primary liver carcinoma in the First College of Clinical Medical Science of China Three Gorges university during Feb.2012-Dec. 2014 were divided into combination group(48 cases)and control group(46 cases)according to random number table.Both groups were given S-1 capsules 40-60 mg orally within 30 min after breakfast and supper.Combination group additionally received Recombinant human endostatin injection 150 mg added into 0.9%Sodium chloride injection 210 mL with portable micro pump for continuous pump of 120 h.A course involved 14 d treatment and 7 d interval.Short-term objective therapeutic efficacy,clinical benefit response(CBR)and ADR were evaluated after 2 courses.Disease progression time and average survival period were compared between 2 groups.RESULTS:Objective response rate,disease control rate,disease progression time and average survival period of combination group were 14.6%,66.7%,(5.5±1.3)months,(10.7±3.8)months;those of control group were 8.7%,45.6%,(4.8±1.2)months,(8.9±3.3)months,with statistical significance between 2 groups(P<0.05).CBR rate of combination group(79.2%)was significantly higher than control group(52.2%),with statistical significance(P<0.05).There was no statistical significance in the incidence of ADR between 2 groups(P>0.05).CONCLUSIONS:S-1 combined with recombinant human endostatin show good therapeutic efficacy and tolerance for patients with middle and advanced primary liver carcinoma,and do not increase the incidence of ADR.
S-1 capsules;Recombinant human endostatin;Primary liver carcinoma
R614
A
1001-0408(2017)11-1496-04
2016-05-23
2016-09-09)
(编辑:黄 欢)
中华国际医学交流基金会项目(No.CIMF-FH001-312)
*主治医师,硕士。研究方向:实体恶性肿瘤的综合治疗。电话:0717-6486997。E-mail:sujin15253@126.com
#通信作者:主任医师,教授,硕士生导师。研究方向:实体恶性肿瘤的综合治疗。电话:0717-6485551。E-mail:xuxinhua@medmail. com.cn
DOI10.6039/j.issn.1001-0408.2017.11.16
