酵母菌生物模板法制备TiO2
2017-04-19孙文会段二红
孙文会, 岳 琳, 段二红, 罗 晓, 廉 静, 杨 勤
(1. 河北科技大学 环境科学与工程学院, 河北 石家庄 050018;2. 河北科技大学 河北省污染防治生物技术实验室, 河北 石家庄 050018)
酵母菌生物模板法制备TiO2
孙文会1,2, 岳 琳1,2, 段二红1,2, 罗 晓1,2, 廉 静1,2, 杨 勤1,2
(1. 河北科技大学 环境科学与工程学院, 河北 石家庄 050018;2. 河北科技大学 河北省污染防治生物技术实验室, 河北 石家庄 050018)
以酵母菌为生物模板,利用水热合成法制备TiO2。在模板剂添加量为5.0%、水热合成温度为140℃、水热合成时间为4.5 h、煅烧温度为350℃、煅烧时间为3.0 h的制备条件下,所制备的TiO2与未添加酵母菌模板的TiO2相比,光催化降解酸性大红3R的性能提高23.3%。通过X射线衍射、扫描电子显微镜、透射电子显微镜等对催化剂的微观结构和形貌进行分析,制备的TiO2为锐钛矿型,颗粒粒径为19~20 nm。
TiO2制备; 酵母菌; 生物模板; 光催化; 水热合成
二氧化钛(TiO2)是一种非常重要的半导体材料,具有化学性质稳定、 耐化学和光化学腐蚀以及无毒等特性,在可见光催化、污水处理及空气净化等方面有着很大的潜在应用价值[1-5]。不同的应用对TiO2的晶型、表面结构的形貌及尺寸有不同的要求,这对TiO2的合成提出了巨大的挑战[2]。常用的合成方法包括溶胶-凝胶法、化学沉积法、固相法、液相沉积法,水热合成法等[6-8],然而,在合成过程中TiO2易出现团聚现象,降低了比表面积、空穴和电荷的分离速率,从而降低了样品的光催化活性。
模板法制备TiO2可以解决这些问题。模板法的原理是使金属半导体微粒吸附在模板的表面,再通过高温焙烧、溶剂溶解等方式去除模板[1]。常用的模板法有非生物模板法和生物模板法[9]。生物模板法具有形貌多样化(筛状、网状、球形、筒形等)、尺寸纳米级、自组装、生物模板形貌重复性高、制备产物结构性能可预期等特点,以及廉价、丰富、可再生、容易得到、环境友好等优点[10]。在本研究中,利用酵母菌为生物模板制备了空心微球TiO2并对其结构进行了表征,探索了反应机理和光催化活性。
1 实验
1.1 试剂和仪器
试剂:钛酸丁酯(Ti(OC4H9)4)(天津市永大化学试剂有限公司),无水乙醇(CH3CH2OH)(天津市永大化学试剂有限公司),氢氟酸(HF)(天津市大茂化学试剂厂),葡萄糖(C6H12O6.H2O)(天津市百世化工有限公司),以上药品均为分析纯;酵母浸粉(北京奥博星生物技术有限公司),实验室所用水均为去离子水。
仪器:101-OAB型 X射线衍射仪(XRD,日本东京司乐仪器有限公司,Cu 靶,Kα射线λ=1.541 84,V=60 kV,I=300 mA,2θ=0.5°~140°);S4800扫描电子显微镜(SEM,日本东京司乐仪器有限公司);JEM-2100透射电子显微镜(TEM,日本东京司乐仪器有限公司);GEL-LAB500 光化学反应器(北京中教金源科技有限公司);UV2600紫外/可见光分光光度计(上海天美科学仪器有限公司)。
1.2 生物模板法制备TiO2
取酵母浸粉并在葡萄糖溶液中培养1 h,然后将Ti(OC4H9)4(控制酵母菌和Ti质量比为1∶5,1∶10,1∶15,1∶20,1∶25)、CH3CH2OH和HF加入到酵母溶液中,持续搅拌1 h,之后将混合溶液放入高压釜内水热合成一定时间,用乙醇、蒸馏水交替洗涤3次,直至上清液pH为3~4,45℃烘干8 h,用马弗炉煅烧。
1.3 光催化降解实验
光催化反应在光化学反应器(GEL-LAB500)中进行,光源为氙灯。每次实验取0.1 g TiO2样品、30 mL酸性大红3R(100 mg/L)于石英玻璃管中。光反应前先进行暗反应30 min,使溶液达到吸附和解吸平衡;每隔15 min 取样一次,每次取2 mL离心分离过滤,将过滤后的溶液在紫外/可见光分光光度计下测定酸性大红的吸光度,绘制时间-酸性大红3R去除率曲线,用以表征催化剂的活性。
2 结果与讨论
2.1 合成条件的优化
2.1.1 模板剂添加量
采用不同酵母菌添加量制备TiO2,降解酸性大红3R的效果见图1。当加入酵母模板后,催化剂的光催化性能明显提高,酵母菌添加量为5.0%时,TiO2的光催化性能最好,与未添加酵母菌的TiO2相比催化效率提高了23.3%。酵母菌剂添加量为20.0%、10.0%和6.7%时,催化剂的光催化性能也有明显提高,但相比于5.0%的样品,光催化活性有所降低。酵母菌添加量较大时,TiO2不能较均匀地被吸附在酵母球表面;而当酵母菌为4.0%时,由于被吸附在酵母小球间隙的TiO2层较厚,比表面积减小,从而降低了光催化活性。因此,酵母菌添加量为5.0%所制得的TiO2具有较好的光催化活性。与Zhang Qian[11]、Chen Xiaoyu[12]、Tang Guogang[13]等课题组对颗粒状TiO2与多孔TiO2降解目标污染的去除率比较见表1,结果表明,本实验的去除率相对较高,效果明显。另外多孔结构在一定程度上可以提高催化剂的光催化性能,这可能是由于其多孔结构增加了催化剂的比表面积,其大孔结构为电荷的转移提供了通道。
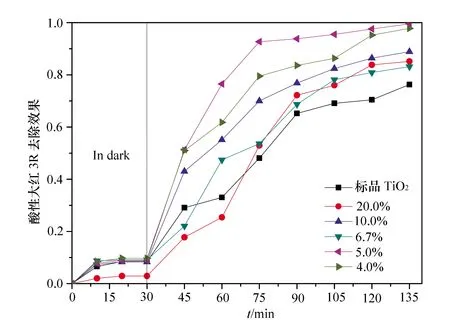
图1 模板剂添加量对TiO2光催化性能的影响

表1 颗粒状与多孔结构TiO2对目标污染物去除率的比较
2.1.2 水热合成温度
不同水热合成温度制备的TiO2对酸性大红3R的降解效果见图2。可以看出:水热合成温度为140 ℃时TiO2的降解效果最好,当温度从120 ℃升高到140 ℃时,光催化性能逐渐升高;温度较低时结晶度起主要作用,随着温度的升高,催化剂的结晶度越好,越有利于晶型的形成;但当温度继续升高时,催化性能反而降低,主要是由于温度过高不利于水解反应向成核方向进行,使体系中晶核数量相对较少,而且温度的升高还会导致能稳定存在的临界晶核尺寸增大,颗粒间及颗粒中的孔隙逐渐变小,从而使比表面积随温度升高而逐渐减小[14]。因此,实验中将采用140 ℃作为水热合成温度。

图2 水热和合成温度催TiO2光催化性能的影响
2.1.3 水热合成时间
不同水热合成时间制备的TiO2对酸性大红3R的降解效果见图3。可以看出:在140 ℃水热合成4.5 h时,TiO2的光催化活性最好,随着水热时间的增加,晶粒的结晶度越来越好,所以催化性能越来越好;但当到达一定的合成时间后结晶度不起主导作用,而比表面积开始起主导作用,随着合成时间的增加,晶粒的尺寸逐渐增加,晶粒颗粒间及颗粒中的孔隙逐渐变小,导致比表面积减小,光催化性能也随之降低[15]。因此,实验中控制水热合成时间为4.5 h。
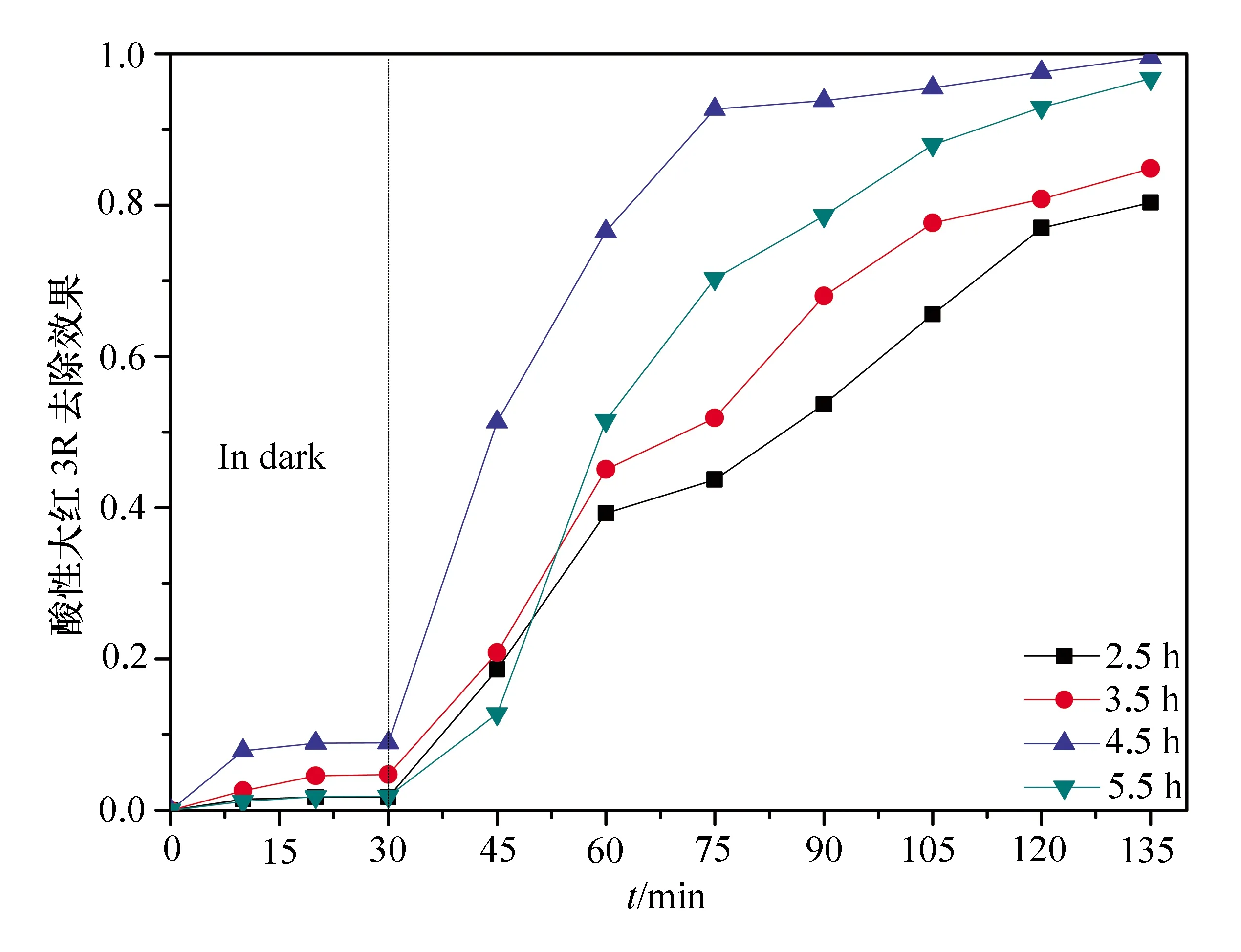
图3 水热合成时间对TiO2光催化性能的影响
2.1.4 煅烧温度
煅烧温度影响TiO2的晶型结构和比表面积,不同煅烧温度制备的TiO2对酸性大红3R的降解效果见图4。可以看出:煅烧温度为350 ℃时有较好的光催化活性,去除率可达98.2%;当温度低于350℃时,不能将酵母菌完全去除,而且低温不能使TiO2较好地结晶形成锐钛矿相[16];但随着煅烧温度持续升高,比表面积成为催化剂催化活性的主导因素[17],煅烧温度逐渐升高,TiO2的颗粒直径逐渐增大,使颗粒间的孔道减小,以至于比表面积减小;当温度过高时,空心结构发生坍塌,会减小比表面积,从而降低TiO2的光催化活性[9],温度过高,TiO2由锐钛矿逐渐向金红石相转变,影响催化剂的光催化活性[18]。
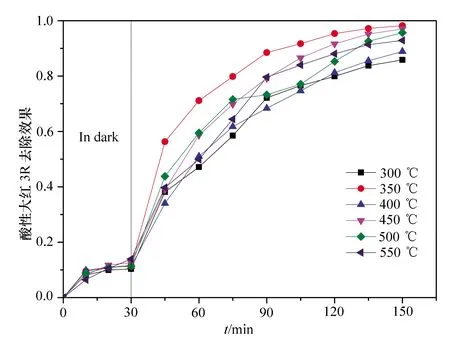
图4 煅烧温度对TiO2光催化性能的影响
2.1.5 煅烧时间
不同煅烧时间制备的TiO2对酸性大红3R的降解效果见图5。从图5可以看出:煅烧时间为3.0 h时酸性大红3R去除效率最高,TiO2光催化活性最好,TiO2的结晶度和比表面积对催化剂的光催化活性都有重要影响[19];当煅烧时间较短时,结晶度起主要作用,随着煅烧时间的增加,催化剂的结晶度越好,光催化活性逐渐升高;但当超过3.0 h时,比表面起主要作用,随着煅烧时间的增加,颗粒尺寸逐渐增加,颗粒间的空隙减小降低了比表面积,从而降低了催化剂的催化活性[20]。
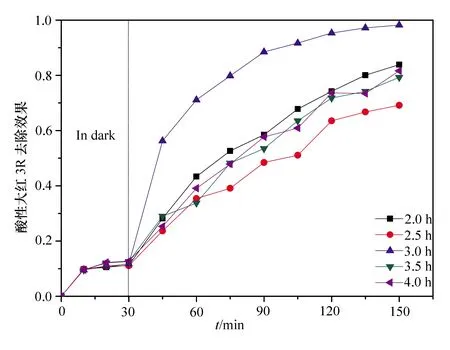
图5 煅烧时间对TiO2光催化性能的影响
2.2 表征
2.2.1 X射线衍射XRD图谱分析
实验制备的TiO2的XRD谱图见图6。由图可知:标品锐钛矿型TiO2的XRD谱图在25.2°、37.7°、48.0°、53.8°处出现锐钛矿的特征峰;以酵母菌为生物模板所制备的TiO2在25.3°、37.8°、48.0°、53.9°出现锐钛矿的特征峰,未出现金红石和板钛矿相的峰,说明通过煅烧去除模板的过程中并未改变TiO2的晶型。根据谢乐公式:
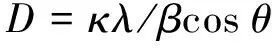
(1)
其中:D为颗粒直径;κ是晶粒的形状因子,一般取0.9;λ是X射线的波长,λ=1.5418;β是衍射角的半峰宽度;θ是半衍射角度。计算得TiO2的颗粒直径为19.3 nm。
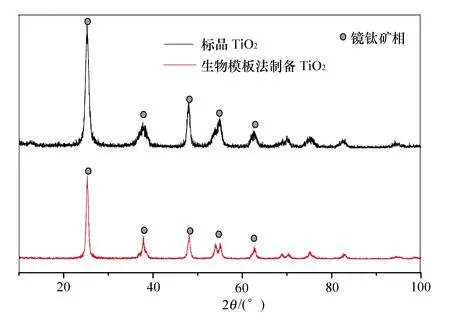
图6 添加生物模板与未添加生物模板TiO2 的XRD谱图
2.2.2 扫描电镜(SEM)分析
图7为所制备的分层多孔结构TiO2的扫描电镜图,图中a和b图为未添加生物模板所制备的TiO2,a图是在低倍率下观察到的TiO2,可以看出催化剂团聚现象严重,成块明显;b图是在高倍率下观察到的TiO2,可以看出所制备的催化剂呈颗粒状分布。图7中c和d图为添加生物模板所制备的TiO2样品,c图是与a图在相同倍率下观察的,可以看出其表面较为蓬松且有多孔结构;d图是与b图在相同倍率下观察到的TiO2微观形态,可以看出所制备的样品有多孔结构,大孔孔径约为3~4 μm,壁厚2~3μm,TiO2纳米粒排布比较蓬松;添加酵母菌生物模板后,可以得到多孔结构的TiO2,增加了其比表面积,为电荷转移提供了孔道,增大其光催化氧化反应效率,从而增加其光催化活性[21]。

图7 TiO2的扫描电镜图
2.2.3 透射电镜(TEM)分析
TiO2的透射电镜图见图8,其中a图为高倍率图,b为TiO2晶格衍射图。从a图可以看出,TiO2的粒径大概为20 nm左右,与XRD测试结果相吻合。从b图中可以看出,TiO2有明显的晶格条纹,晶格尺寸约为0.35 nm,是典型的锐钛矿相TiO2,与XRD测试结果相一致。

图8 TiO2透射电镜图
2.2.4 合成机理
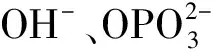
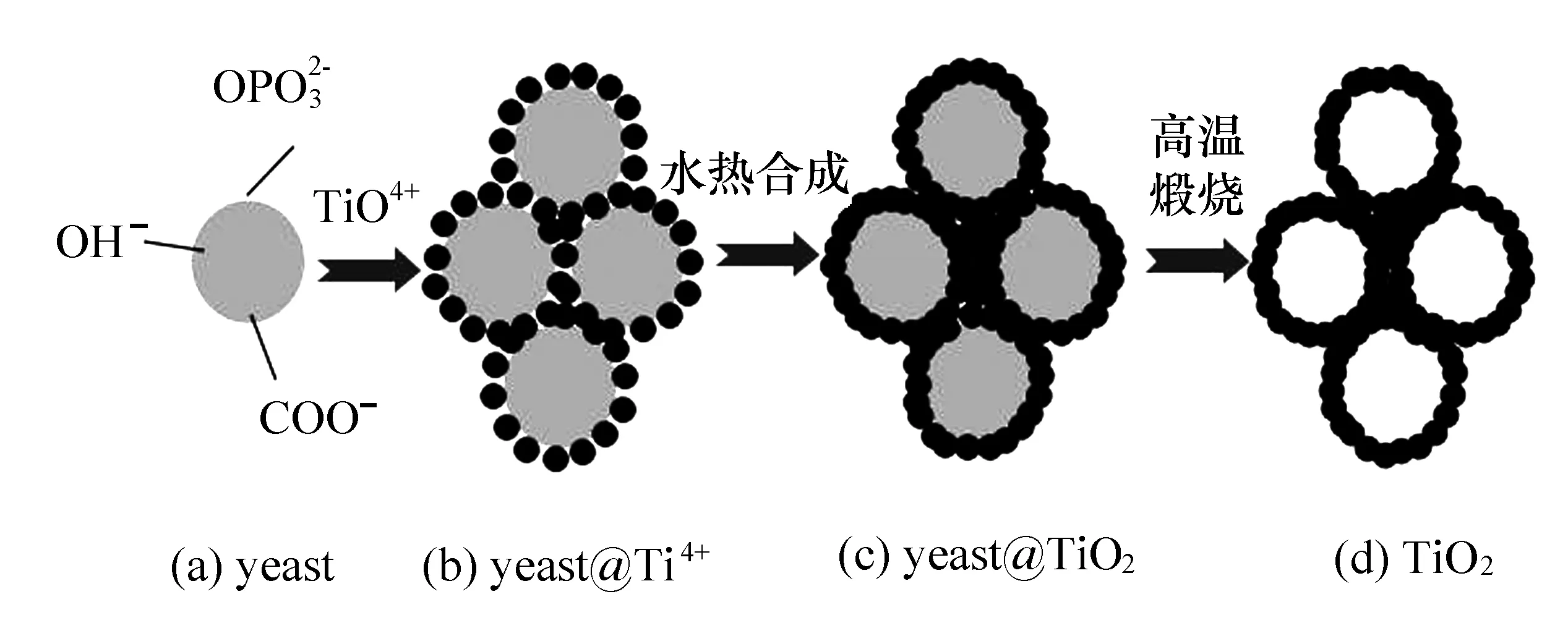
图9 多孔TiO2的合成途径
3 结论
(1) 以酵母菌为生物模板、水热法合成TiO2,高温煅烧去除模板得到分层多孔结构。
(2) 合成过程中酵母菌添加量、水热合成温度、水热合成时间、煅烧温度和时间都会影响分层多孔结构形成和水解反应向成核方向的进行,从而影响TiO2的光催化性能。
(3) 通过降解酸性大红3R优化其合成条件,当模板剂添加量为5.0%、水热合成温度为140 ℃、水热合成时间为4.5 h、煅烧温度为350 ℃、煅烧时间为3.0 h时,其光催化性能比同条件下未添加生物模板的TiO2提高23.3%。
(4) 通过XRD、SEM、TEM等表征手段对催化剂的微观结构和形貌进行分析,制备的TiO2为锐钛矿型,大孔孔径约为3~4 μm,壁厚2~3 μm,颗粒粒径为19~20 nm。
References)
[1] 嵇天浩,杨芳,周娇艳,等.可见光响应的BiVO4/TiO2纳米复合光催化剂[J].光谱学与光谱分析,2010,30(7):1944-1947.
[2] 潘峰,张旺,张荻.模板法制备TiO2研究进展[J].材料导报A(综述篇),2015,29(1):22-30.
[3] Mohamed M M, Al-Sharif M S.Visible light assisted reduction of 4-nitrophenol to 4-aminophenol on Ag/TiO2photocatalysts synthesized by hybrid templates[J].Applied Catalysis B:Environmental,2013(142/143):432-441.
[4] 邹晓梅,陈启胜,柯小雪,等.PW11Cu/TiO2膜光催化剂的制备及可见光催化性能[J].无机化学学报,2015,30(10):2037-2047.
[5] 白波,王鹏鹏,王翠芳,等.酵母菌生物模板法组装Ti-W-Si三元复合空心微球及其光催化性能[J].现代化工,2009,29(6):37-41.
[6] 龚良玉,曹永军,李群国,等.纳米CeO2的生物模板法制备[J].化学研究.2009,20(04):31-33.
[7] Li Y N , SU J , LV X Y ,et al. Yeast bio-template synthesis of porous anatase TiO2and potential application as an anode for sodium-ion batteries[J].Electrochimica Acta,2015(182):596-603.
[8] Jaiswal R, Patel N, Alpaid,et al .Efficient Co-B-codoped TiO2photocatalyst for degradation of organic water pollutant under visible light[J].Applied Catalysis B:Environmental,2016(183):242-253.
[9] Yue L. Biotemplate synthesis of mesoporous iron phosphomolybdate supported on silica with enhanced photocatalytic property[J].Materials Letters,2015(157):225-227.
[10] 卜珃,庄惠生.生物模板法制备铜掺杂TiO2空心球光催化性能及其性质研究[D].上海:东华大学,2011.
[11] Zhang Q,Li W,Liu S X.Controlled fabrication of nanosized TiO2 hollow sphere particles via acid catalytic hydrolysis/hydrothermal treatment[J].Powder Technology,2011(212):145-150.
[12] Chen X Y, Kuo D H, Lu D F, et al. Synthesis and Photocalalytic activity of mesoporous TiO2nanoparticle using biological renewable resource of un-modified lignin as a template[J]. Microporous and mesoporous Materials,2016(223):145-151.
[13] Tang G G,Liu S S,Tang H,et al.Template-assisted hydrothermal synthesis and photocatalytic activity of novel TiO2 hollow nanostructure[J].SciVerse Science Direct,2013(39):4969-4974.
[14] 冉凡勇,曹文斌,李艳红,等.水热合成法制备锐钛矿TiO2粉体的研究[J].无机材料学报,2006,21(3):552-557.
[15] 刘素芹,戴高鹏,梁英,等.原位碳、氮共掺杂二氧化钛空心球的制备与可见光光催化性能[J].物理化学学报,2013,29(3):585-589.
[16] Wu Q, Li W,Wang D P,et al. Preparation and characterization of N-dopped visible-light-responsive mesoporous TiO2hollow spheres[J].Applied Surface Science,2014(299):35-40.
[17] 孙振宇,牛笛,刘祎飞,等.水热合成法制备纳米TiO2催化剂及其催化性能的研究[J].广州化工,2013,41(3):62-65.
[18] Lin L, Wang H Y, Luo H M, et al. Enhanced photocatalysis using side-glowing optical fiber coated with Fe-doped TiO2nanocomposite thin films[J].Journal of Photochemistry and Photobiology A:Chemistry,2015(307/308):88-98.
[19] 林正迎,谢磊,俞卫平.模拟阳光下Ag/I-TiO2光催化预处理山核桃加工废水[J].环境工程学报,2014,8(4):1549-1553.
[20] 熊晶晶,李可心,黄黎明,等.介孔电气石/TiO2复合材料的制备及其模拟太阳光光催化性能[J].复合材料学报,2014,31(6):1481-1489.
[21] 刘天成,黄家卫,王天丽,等.光催化剂磷钨酸钾的制备及结构表征[J].环境工程学报,2016,10(1):127-130.
[22] Cabib E, Roh D H, Schmidt M, et al. The yeast cell wall andseptum as paradigms of cell growth and morphogenesis[J]. J Biol Chem,2001(276):19679.
[23] Nevoigt E. Progress in metabolic engineering of Saccharomyces cerevisiae[J].Microbiol Mol Biol Rev,2008(72):379.
[24] He W, Cui J, Yue Y, et al. High-performance TiO2frombaker’s yeast[J]. J Colloid Interface Sci,2011(354):109.
[25] Chang Y C, Lee C Y, Chiu H T. Porous inorganic materials from living porogens: channel-like TiO2from yeast-assisted sol-gel process[J]. ACS Appl Mater Interfaces,2014(6):31.
[26] Bao S J, Lei C, Xu M W, et al. Environment-friendly biomimetic synthesis of TiO2nanomaterials for photocatalytic application[J].Nanotechnology,2012(23):205601.
Preparation of TiO2by using yeast bio-template method
Sun Wenhui1,2, Yue Lin1,2, Duan Erhong1,2, Luo Xiao1,2, Lian Jing1,2, Yang Qin1,2
(1. School of Environmental Science and Engineering, Hebei University of Science and Technology, Shijiazhuang 050018, China; 2. Pollution Prevention and Biotechnology Laboratory of Hebei Province, Hebei University of Science and Technology, Shijiazhuang 050018, China;)
By using yeast as biological template, TiO2is prepared by hydrothermal synthesis. Under the conditions that the template dosage is 5.0%, the hydrothermal synthesis temperature is 140℃, the hydrothermal synthesis time is 4.5 h, the calcination temperature is 350℃ and the calcination time is 3.0 h, the performance of photocatalytic degradation of acid red 3R is increased by 23.3% when the prepared TiO2is compared with that of TiO2without yeast template. Through the analysis of the microstructure and morphology of the catalyst by X-ray diffraction, scanning electric microscopy, transmission electron microscopy, etc., the prepared TiO2is the anatase type and the particle size is 19-20 nm.
TiO2preparation; yeast; bio-template; photocatalysis; hydrothermal synthesis
10.16791/j.cnki.sjg.2017.03.018
2016-09-27
河北省自然科学基金青年基金项目(B2014208096);河北省高等学校科学技术研究计划项目(QN2015017)
孙文会(1992—),女,河北沧州,硕士研究生,研究方向为水污染控制工程
E-mail:270123138@qq.com
岳琳(1980—),女,河北石家庄,博士,副教授,研究方向为水污染控制工程.
E-mail:yuelintj@126.com
TB34
B
1002-4956(2017)3-0068-05
