1HNMR导向的天然药物化学研究性实验教学探索
2017-04-19丁唯嘉祝钧杰宋高鹏杨卓鸿李春远
丁唯嘉, 祝钧杰, 陈 敏, 宋高鹏, 杨卓鸿, 李春远
(1. 华南农业大学 材料与能源学院, 广东 广州 510642;2. 华南农业大学 公共基础课实验教学中心, 广东 广州 510006)
1HNMR导向的天然药物化学研究性实验教学探索
丁唯嘉1, 祝钧杰1, 陈 敏2, 宋高鹏1, 杨卓鸿1, 李春远1
(1. 华南农业大学 材料与能源学院, 广东 广州 510642;2. 华南农业大学 公共基础课实验教学中心, 广东 广州 510006)
以微生物为对象设计了研究性实验,以核磁共振氢谱(1HNMR)为导向优选代谢产物产量高且有特色化学位移的菌株,用反相十八烷基硅烷键合硅胶(ODS)减压柱层析和制备高效液相色谱分别进行提取物分段和单体纯化,成功跟踪分离到一个环四肽化合物,鉴定了结构。综合运用了超声波辅助提取、核磁共振测试、减压柱层析,制备高效液相分离等操作,并通过结构式查阅网络数据库和用核磁共振鉴定结构的方法,有助于学生全面认识天然药物化学的发展趋势和科研流程、增加学习兴趣、提升操作技能和创新能力。实验的整个流程可推广到微生物代谢产物分离纯化的其他研究性实验当中。
微生物; 天然药物化学;研究性实验; 核磁共振氢谱
天然产物具有多样性的化学结构和生理活性,因此在新药开发方面具有无可替代的重要地位[1]。但相同结构的天然活性物质的重复发现正变得日益严重,例如近年来,从土壤链霉菌中被重复发现的抗生素高达95%,同时耐药病原菌正不断出现并迅速蔓延[2-3]。在此形势下,以液相色谱-质谱联用,核磁共振等为导向开展研究的新思路正越来越广泛被应用在天然产物分离纯化的科研流程中以提高效率,有选择性地获取更多新颖药物模板分子[4-6]。然而目前国内中药学、药学、制药工程、应用化学等药学或化学类专业本科生开设的天然药物化学课程,其配套的天然产物成分提取分离实验往往以验证性为主[7],而少数综合性或研究性实验均缺乏导向分离的创新性内容,这在客观上制约了学生对当前天然产物研究新技术的了解和掌握,不利于学生学习兴趣的激发和创新思维及创新能力的培养。为此,紧跟天然药物化学科研发展趋势,针对相关专业的高年级学生,优选实验内容,开设以核磁共振氢谱(1HNMR)为导向的研究性实验,以充分发挥大型仪器实验平台的作用,促进学生对天然药物化学更加全面深刻的认识。
1 1HNMR指导下优选实验对象
天然产物研究对象包括动物、植物、微生物、矿物等[8],其中以微生物为对象进行1HNMR筛选确立为本实验的研究对象相对更为合适,其原因在于微生物种类丰富,具有采集不破坏环境、可人工发酵等优点[9]。微生物在土壤、水、动植物体表和体内等均有广泛分布。然而,从对比研究的角度考虑,不宜选择来源不同的菌株供学生筛选,可采用同一植物的内生微生物为对象,使学生通过1HNMR对比了解同种植物不同内生菌株之间化学成分的差异。因此,在任课教师科研项目研究成果的基础上,我们提供了4株分离自海洋半红树植物苦槛蓝的内生真菌供学生进行对比筛选。
1.1 菌株培养和发酵产物1HNMR测试
核磁共振(NMR)是天然产物结构鉴定、药物筛选等研究最可靠的工具之一[10],其中1HNMR具有高灵敏度,分子量500以下的毫克级样品在数分钟内即可完成测试,因此本实验的待筛菌株无需大量培养。每株菌各接种至5块PDA培养基平板,室温静置培养72 h,将培养好的同种菌株合并,用无水乙醇浸泡超声辅助提取20 min,高速离心后减压浓缩上清液,真空干燥得待测样品。用0.5 mL氘代试剂溶解,小心加入核磁管中、加塞;将核磁管插入转子,用量规使处于合适高度后,放入核磁共振仪,经进样、匀场、锁场、采样等操作命令后即可获得4株待筛菌株代谢产物化学成分的1HNMR谱(见图1,图中δ为化学位移)。
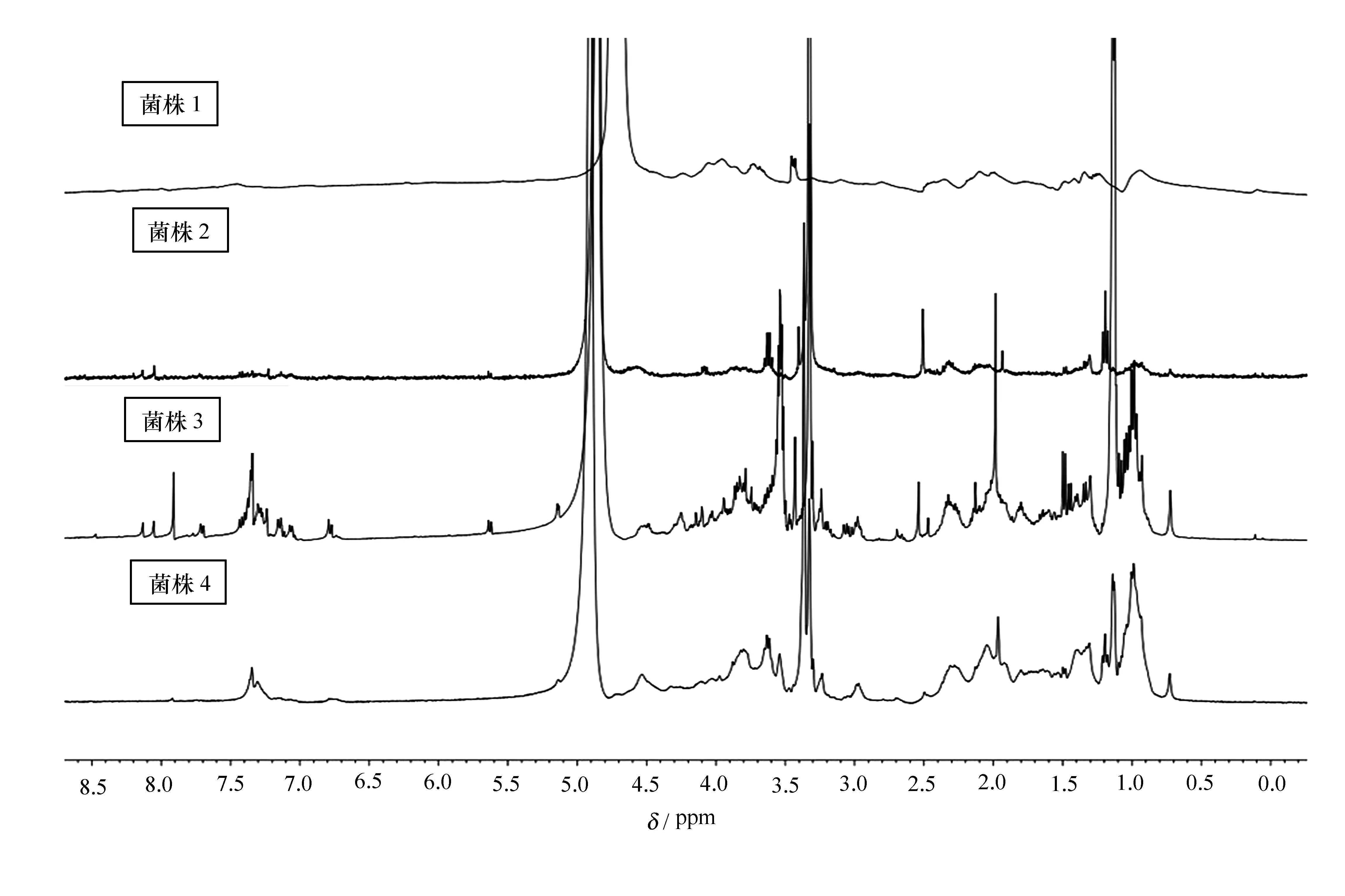
图1 4株待筛菌株代谢产物化学成分的1H NMR谱
1.2 根据1HNMR谱分析代谢物产量和特色化学位移峰确定研究对象
1HNMR谱中,化学位移值可用来判断样品可能的结构单元,信号峰的强度高低可直观地反映样品摩尔浓度的大小[11],因此可引导学生从这2个方面入手对图1测试结果进行分析。菌株1和菌株2峰的信号偏低,表明相同培养条件下其代谢产物产量低,不适合开展后续研究;菌株3和菌株4代谢产物产量均较高,其中菌株3信号更为丰富,并且在化学位移8.0 ppm左右多出多个小峰,通常该数值附近的化学位移是酰胺中活泼H的信号[12],表明菌株3可能含有高浓度的多肽类化合物。多肽类化合物通常结构新颖,活性较强,属于热点化合物[13]。因此实验进一步选取菌株3为研究对象(Phoma属,分离自植物苦槛蓝叶片,保藏在华南农业大学材料与能源学院,编号Phomasp. L28[14]),以其所产生的具有8.0 ppm左右化学位移值的代谢产物为目标化合物,开展分离纯化实验。
2 1HNMR指导下所筛菌株目标化合物的分离纯化
2.1 采用反相ODS填料与减压柱层析结合进行提取物不同极性部位分段
反相填料ODS特别适合分离中等以上极性化合物,具有粒度小、分离效果好等优点。本实验拟分离的目标化合物在δ=8.0 ppm附近有多个活泼氢,表明极性中等或偏大,用ODS进行分离成为首选。然而ODS常压柱层析装柱耗时长且流动相流速缓慢,因此我们将具有装置简单、装柱方便、可将固定相抽干、分离操作时间短、分离效果好等优点的减压柱层析[15]与反相ODS填料结合使用,这样不仅能大大缩短装柱时间,而且能显著增加流动相流速、提高分离效率。装柱完成后,将菌株放大培养3倍所得的提取物用少量甲醇溶解,湿法上样,以水和甲醇按比例混合(体积比为90∶10,80∶20,70∶30,0∶50,30∶70,20∶80,0∶100)作为溶剂进行减压梯度洗脱,分别得到5个不同极性分段部位,减压浓缩,所得样品真空干燥,分别测试1HNMR,结果见图2。查找8.0 ppm附近的化学位移信号,可以很明显看到主要集中在水与甲醇的体积比为80∶20分段部位,有待从该部位进一步纯化目标化合物。
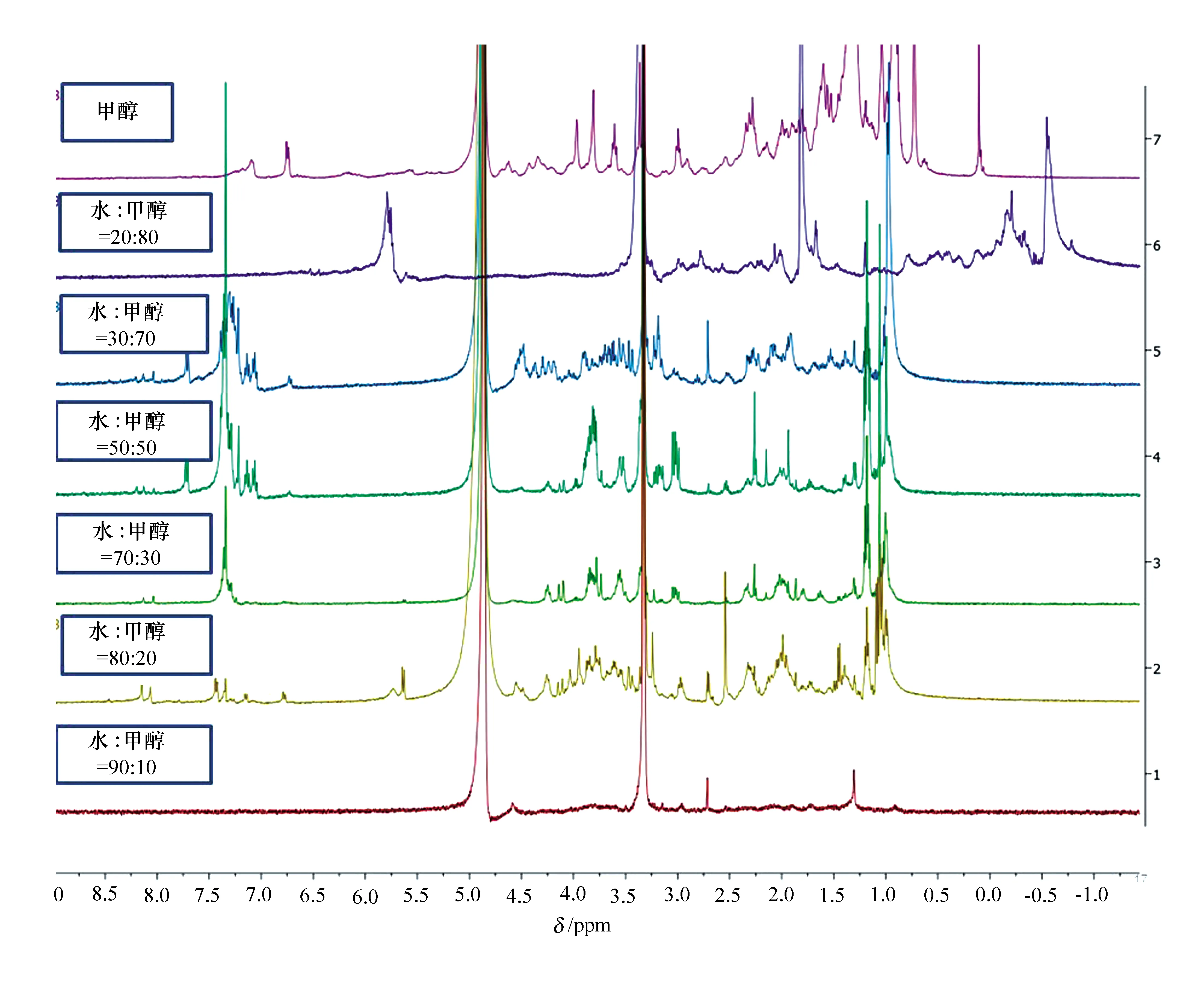
图2 菌株3(Phoma sp. L28)代谢产物5种不同极性分段部位化学成分的1HNMR谱
2. 2 采用制备高效液相色谱仪进行目标化合物的最终纯化
制备高效液相色谱仪的高压输液系统使其分离速度较传统分离方法大大加快,所配备的专业色谱柱不破坏样品、分离效能高、可反复使用,紫外等检测器灵敏度高同时连接电脑等输出设备,实现了不同结构物质的可视化分离[16]。基于上述种种优点,近年来,制备高效液相色谱仪的使用已在天然药物化学的科研中得到了普及。然而,目前国内多数院校的天然药物化学教学中却缺乏运用该设备进行天然产物分离纯化的学生实验,十分有必要在研究性实验中合理使用该设备,使学生熟悉相关的操作流程。
本实验采用制备高效液相色谱仪对水与甲醇体积比为80∶20分段部位中的目标单体化合物进行纯化。根据所得样品量选用的色谱柱为ODS半制备柱(Synergi Hydro 250 mm×10mm),参考之前的减压ODS柱的分离情况,设定30 min时间,以水与甲醇的体积比90∶10~75∶25进行梯度洗脱,以220 nm为检测波长,流速为1.5 mL/min,结果在18 min左右收集到一个峰形对称的纯净化合物,减压干燥后,测其1HNMR谱和13CNMR,分别见图3和图4。
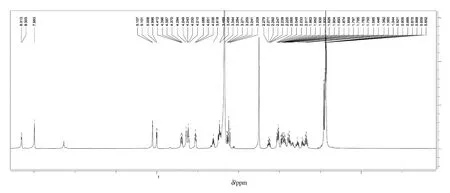
图3 实验所得目标化合物的1HNMR谱
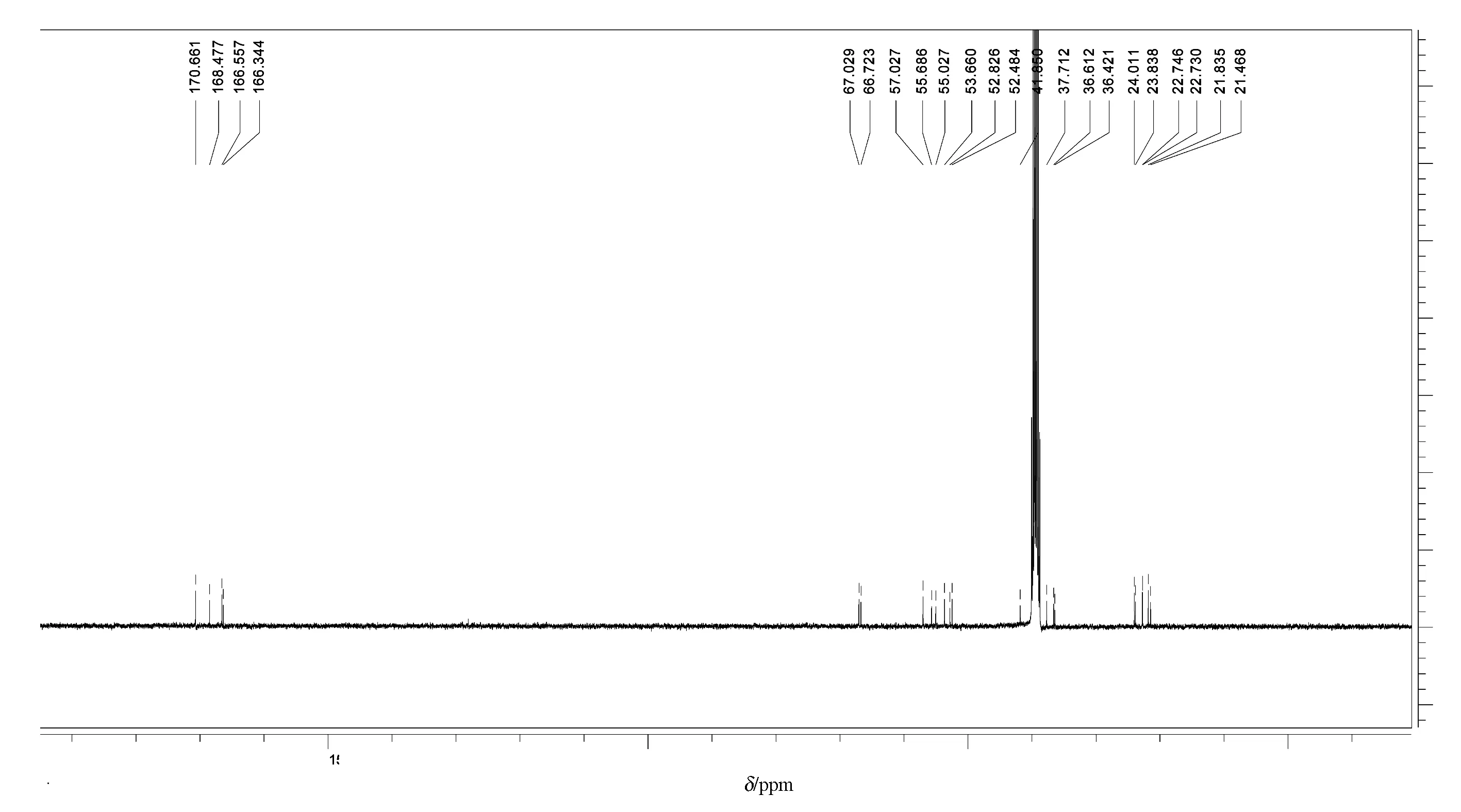
图4 实验所得目标化合物的13CNMR谱
3 引导学生采用类比组合法分析核磁共振结果进行结构鉴定
运用核磁共振谱解析复杂化合物的结构可根据所鉴定化合物的特点把它拆解成不同的结构片段,引导学生在熟悉各片段的核磁数据特点的基础上再进行类比和总体结构的组合,是最近报道的一种行之有效的教学方法[17]。本实验所得的多肽类化合物由不同氨基酸组成,因此教师先指导学生查阅文献,熟悉常见氨基酸和二肽类的化学位移数值,然后引导学生从峰的裂分情况、积分高度,质子数、化学位移数值与官能团(基团) 关系等处入手与文献氨基酸数据进行对比。学生通过认真观察分析,相互讨论得出如下结果:该化合物是由2个相同构型的4-羟基亮氨酸和2个不同构型的脯氨酸组成的环四肽。在此基础上学生将4种氨基酸片段组合自主画出可能的结构式,教师指导学生使用Scifinder数据库进行结构式检索出文献,对照波谱数据[18]基本一致,鉴定化合物为环(L-亮氨酰-反-4-羟基-L-脯氨酰-D-亮氨酰-反-4-羟基- L-脯氨酰)四肽。此步骤激发了学生的学习兴趣,使学生较好地掌握了核磁共振谱表征与推导天然产物结构的方法。
4 结语
传统的天然产物成分研究经常分离到一些无价值的化合物,此过程浪费了大量溶剂,耗资耗时。因此如何选择性地快速从天然产物中发现新颖的活性化合物,是天然产物学家一直迫切想要解决的问题。近年来,核磁共振仪、色谱质谱联用仪等大型仪器及化合物波谱数据库的普及为此问题的解决提供了思路,一些基于这些仪器和数据库指导下的天然产物分离纯化研究取得了丰硕成果。与此大背景不相符的是,当前国内高校极少开设相关的天然产物提取分离实验。针对上述情况,我们依托自身科研项目,设计了以微生物为对象的研究性实验,在1HNMR指导下优选代谢产物产量高且有特色化学位移的菌株,使用反相ODS减压柱层析和高效制备液相分别进行提取物分段和单体化合物纯化,成功跟踪到一个环四肽化合物并运用核磁共振鉴定了结构。该化合物为首次从Phoma属真菌中分离到,体现了实验的创新性。实验综合运用了超声波辅助提取、核磁共振测试、减压柱层析、制备高效液相等操作,并通过结构式查阅网络文献数据库和运用NMR解析天然产物结构的方法,有助于学生全面深刻认识天然药物化学的发展趋势和科研流程,增加学习兴趣,提升操作技能和创新能力。实验的整个流程可以方便地推广应用到其他微生物代谢产物分离纯化的研究性实验当中。
References)
[1] Newman D J, Cragg G M. Natural products as sources of new drugs over the 30 years from 1981 to 2010[J]. Journal of natural products, 2012,75(3):311-335.
[2] Burgess J G, Jordan E M, Bregu M, et al. Microbial antagonism: a neglected avenue of natural products research[J]. Journal of Biotechnology, 1999,70(1/2/3):27-32.
[3] ChangC M, Chern J, Chen M Y, et al. Avenaciolides: potential MurA-targeted inhibitors against peptidoglycan biosynthesis in methicillin-resistantStaphylococcusaureus(MRSA) [J]. Journal of the American Chemical Society, 2015,137(1):267-275.
[4] Wolfender J L, Marti G, Queiroz E F. Advances in techniques for profiling crude extracts and for the rapid identification of natural products: dereplication, quality control and metabolomics[J]. Current Organic Chemistry, 2010,14(16):1808-1832.
[5] Feng Q, James B M, David C L, et al. 2D NMR barcoding and differential analysis of complex mixtures for chemical identification[J]. Analytical Chemistry, 2014,86(8):3964-3972.
[6] Grkovic T, Pouwer R H, Vial M L, et al. NMR fingerprints of the drug-like natural-product space identify Iotrochotazine A: a chemical probe to study Parkinson’s disease[J]. Angewandte Chemie International Edition, 2014,53(24):6184-6188.
[7] 康文艺,王金梅,关爱民,等.自主设计法在天然药物化学实验教学中的应用[J]. 药学教育,2011,27(3):55-57.
[8] 吴立军. 天然药物化学[M].5版.北京:人民卫生出版社, 2010.
[9] 李春远,丁唯嘉,王秀芳,等. 一则海洋微生物天然药物化学综合实验的教学设计[J]. 实验技术与管理,2014,31(5):187-190.
[10] 王聪,王远红, 王乂,等. 核磁共振波谱仪引入仪器分析实验教学的探索[J]. 实验技术与管理,2016,33(7):160-162.
[11] 苏克曼,潘铁兰,张玉兰. 波谱解析法[M]. 上海: 华东理工大学出版社, 2002:149-174.
[12] 李春远,黄松,佘志刚,等. 两株红树林内生真菌共培养正丁醇萃取部位化学成分研究[J]. 中山大学学报(自然科学版),2014,53(2):77-81.
[13] 许文彦,赵思蒙,曾广智,等. 一些重要天然活性环肽化学和生物活性研究进展[J]. 药学学报, 2012 ,47(3):271-279.
[14] 丁唯嘉,张穗强,龚兵,等. 半红树植物苦槛蓝内生真菌的分离及抗植物病原菌活性研究[J]. 广东农业科学,2014,41(3):74-78.
[15] Pelletier S W, Chokshi H P, Desai H K. Separation of Diterpenoid Alkaloid Mixtures Using Vacuum Liquid Chromatography[J]. Journal of natural products, 1986,49(5):892-900.
[16] 叶献曾,张新祥. 仪器分析教程[M].2版.北京:北京大学出版社, 2007:348-370.
[17] Gonzalez E, Dolino D, Schwartzenburg D, et al. Dipeptide structural analysis using two-dimensional NMR for the undergraduate advanced laboratory[J]. Journal of Chemical Education, 2015, 92(3):557-560.
[18] Li C, Wang J, Luo C, et al. A new cyclopeptide with antifungal activity from the co-culture broth of two marine mangrove fungi[J]. Natural product research, 2014, 28(9):616-621.
Exploration of research experimental teaching of natural pharmaceutical chemistry based on1HNMR
Ding Weijia1, Zhu Junjie1, Chen Min2, Song Gaopeng1, Yang Zhuohong1, Li Chunyuan1
(1. College of Materials and Energy, South China Agricultural University, Guangzhou 510642,China; 2. Center of Experimental Teaching for Basic Courses, South China Agricultural University, Guangzhou 510006, China)
By taking micro-organisms as an object, a research-oriented experiment is designed. Guided by1H nuclear magnetic resonance spectroscopy (1HNMR), the optimal production of metabolites is high with the decompression column chromatography of bacterial strain for reversed phase eighteen alkyl silane bonded silica gel (ODS) of unique chemical shifts. The high performance liquid chromatography is prepared to carry out the object segmentation and monomer purification of extracts respectively. A cyclotetrapeptide is successfully traced and isolated, and its structure is identified. By comprehensive application of the ultrasonic assisted extraction of nuclear magnetic resonance and vacuum column chromatography, the operations such as high performance liquid phase separation are prepared. By the method for checking network database with the structure type and identifying the structure by nuclear magnetic resonance, it is helpful for the students to fully understand the development trend and research process of natural medicinal chemistry, stir up their interest in learning, and improve their operational skills and innovative ability. The whole experimental process can be expended to other research-oriented experiments for the isolation and purification of the metabolites of microorganisms.
microorganism; natural medicinal chemistry; research-oriented experiment;1HNMR
10.16791/j.cnki.sjg.2017.03.013
2016-10-09
国家自然科学基金项目(21102049);广东省自然科学基金项目(2015A030313405);广东省科技计划公益研究与能力建设专项基金项目(2016A020222019);教育部留学回国人员科研启动基金项目([2015]311);广东省高等学校教学质量与教学改革工程项目(GDJG20142098);广东省高等教育学会实验室管理专业委员会基金项目(GDJ2014069);华南农业大学教育教学改革与研究项目(JG16060,JG10109);广东省大学生科技创新训练计划资助项目(201610564225)
丁唯嘉(1979—),女,河南周口,博士,讲师,主要从事应用化学研究
E-mail:dwjzsu@scau.edu.cn
李春远(1978—),男,河南扶沟,博士,副教授,主要从事天然产物化学研究.
E-mail:chunyuan-li@163.com
G642.0;R914
A
1002-4956(2017)3-0047-05
