基于高效液相色谱法的牛黄解毒制剂中胆红素含量测定
2017-04-14罗亚玲齐景梁
罗亚玲, 周 娟, 齐景梁
(四川省食品药品检验检测院, 四川 成都 610097)
基于高效液相色谱法的牛黄解毒制剂中胆红素含量测定
罗亚玲, 周 娟, 齐景梁
(四川省食品药品检验检测院, 四川 成都 610097)
利用高效液相色谱法建立牛黄解毒制剂中胆红素的含量测定方法,色谱柱为Agilent Zorbax SB-C18色谱柱,流动相为乙腈—1%冰醋酸(95∶5),检测波长为450 nm.结果显示,胆红素进样量在0.8321~208.032 ng范围内具有良好的线性关系,r=0.9995,牛黄解毒片平均回收率为105.6%,RSD为1.42%,牛黄解毒丸平均回收率为96.2%,RSD为1.83%.结果表明,方法准确、简便,可作为牛黄解毒片及牛黄解毒丸等制剂中胆红素含量的测定方法.
牛黄解毒制剂;胆红素;液相色谱法
0 引 言
牛黄解毒片和牛黄解毒丸的处方主要由人工牛黄、雄黄和黄芩等8味药材组成[1],具有清热解毒之功效,临床上常用于火热内盛、咽喉肿痛、牙龈肿痛、口舌生疮及目赤肿痛等症.人工牛黄为方中主药,系我国药学工作者根据天然牛黄的成分研制而成,具体由胆红素、胆酸、胆固醇等配制而成.胆红素是人工牛黄中的主要成分,有解热、降压、抗病毒等作用,也是评价人工牛黄品质优劣的依据[2-5],故考察牛黄解毒制剂中胆红素的含量具有现实意义.
1 材料与仪器
1.1 材 料
实验所用材料包括:胆红素对照品(批号,100077-200805,含量测定用,含量以98.5%计,使用前无需干燥处理),由中国生物制品检定所提供;牛黄解毒片(批号,B82015),由天津同仁堂集团股份有限公司生产;牛黄解毒丸(水蜜丸)(批号,1120668),由北京同仁堂科技发展股份有限公司制药厂生产;乙腈为色谱纯,水为超纯水,其余试剂均为分析纯.
1.2 仪 器
实验所用主要仪器为Waters 2695-2489-2998型液相色谱仪(美国沃特世公司).
2 方法与结果
2.1 色谱条件
实验色谱条件为:色谱柱,Agilent Zorbax SB-C18色谱柱(4.6 mm×250 mm,5 μm);流动相为乙腈—1%冰醋酸溶液(95∶5);柱温35 ℃;流速0.7 mL·min-1;检测波长450 nm.
2.2 溶液制备
2.2.1 对照品溶液的制备.
取胆红素对照品适量,精密称定,加三氯甲烷制成每1 mL含4.16 μg的溶液,制得对照品溶液.
2.2.2 供试品溶液的制备.
精密称取牛黄解毒片细粉适量(相当于大片4片或小片6片(糖衣片除糖衣,或水蜜丸细粉2 g)),置50 mL棕色量瓶中,精密加入二氯甲烷—甲醇(1∶1)混合溶剂25 mL(水蜜丸加10 mL),称重,冰水浴超声20 min,取出,补重,滤过,取续滤液,制得供试品溶液.
2.3 测定法
分别吸取对照品溶液与供试品溶液各5 μL,注入液相色谱仪,测定.
2.4 专属性考察
分别取阴性样品(缺胆红素)供试溶液、胆红素对照品溶液、牛黄解毒片供试品溶液,按上述色谱条件进行实验.结果显示,阴性样品对胆红素的测定无干扰,结果如图1、2所示.
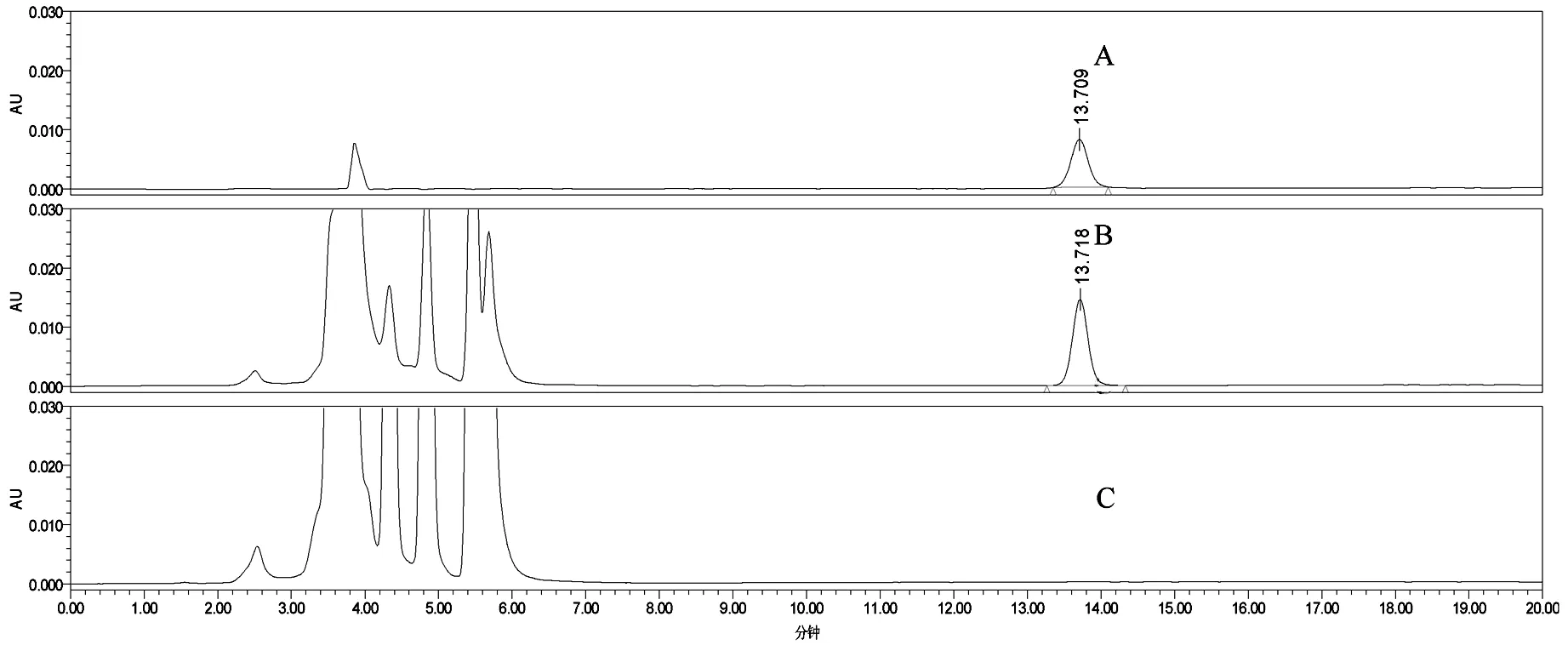
A.胆红素对照品、牛黄解毒片样品;B.和阴性样品;C.色谱图
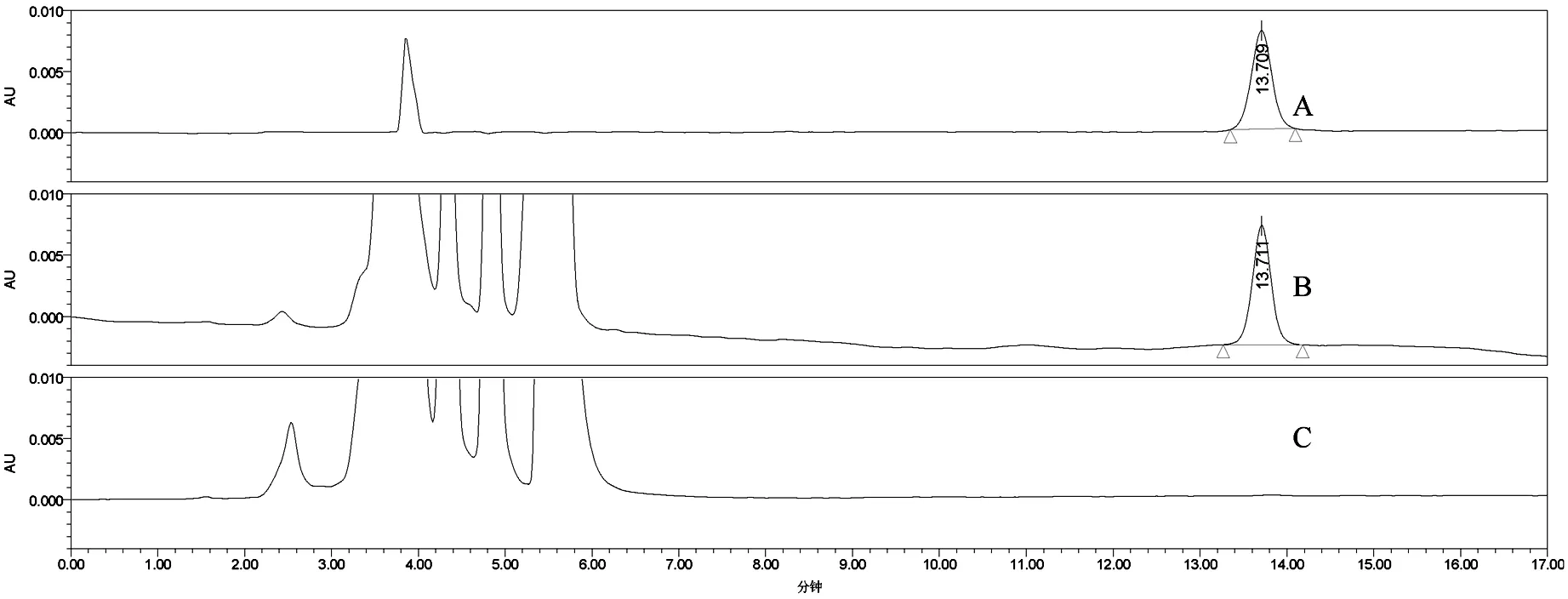
A.胆红素对照品;B.牛黄解毒丸样品和阴性样品;C.色谱图
2.5 线性范围考察
精密称取胆红素对照品(含量98.5%)10.56 mg,置于100 mL棕色量瓶中,加三氯甲烷溶解并稀释至刻度,摇匀,作为S1;精密吸取S1 1mL,加三氯甲烷稀释至25 mL量瓶中,摇匀,作为S2;精密吸取S2 1 mL,加三氯甲烷稀释至10 mL量瓶中,摇匀,作为S3.分别精密吸取S3 2 μL、5 μL、10 μL及S2 5 μL、10 μL及S1 2 μL,注入液相色谱仪,记录色谱图,测定其峰面积,并以峰面积(A)为纵座标,胆红素进样量(ng)为横座标,进行回归,得回归方程,
A=8 158.06C-11 324.30,r=0.9995
结果表明,胆红素在进样量为0.8321~208.032 ng时,与峰面积线性关系良好.
2.6 精密度
精密量取胆红素对照品溶液(浓度10.9532 μg·mL-1)5 μL,连续进样6次,其RSD为0.52%.表明仪器的精密度良好.
2.7 重复性
取牛黄解毒片细粉适量(相当于大片4片或小片6片(糖衣片除糖衣,或水蜜丸细粉2 g)),精密称定,各6份,照“2.2.2”项下方法制备溶液并测定含量,测得牛黄解毒片胆红素平均含量为67.24 μg·g-1(RSD=0.91%),牛黄解毒丸胆红素平均含量为32.24 μg·g-1(RSD=1.73%).结果表明,方法的重复性良好.
2.8 加样回收率
分别取已知含量的牛黄解毒片细粉(含量为67.24 μg·g-1)1.0 g,牛黄解毒丸细粉(含量为32.24 μg/g)1.0 g,各6份,精密称定,置于50 mL棕色量瓶中,精密加入胆红素对照品溶液(C=3.5051 μg·mL-1)25 mL(片剂)或10 mL(丸剂),称定质量,按照拟定方法制备供试品溶液,按上述色谱条件测定,记录色谱图,计算回收率,结果见表1、表2.
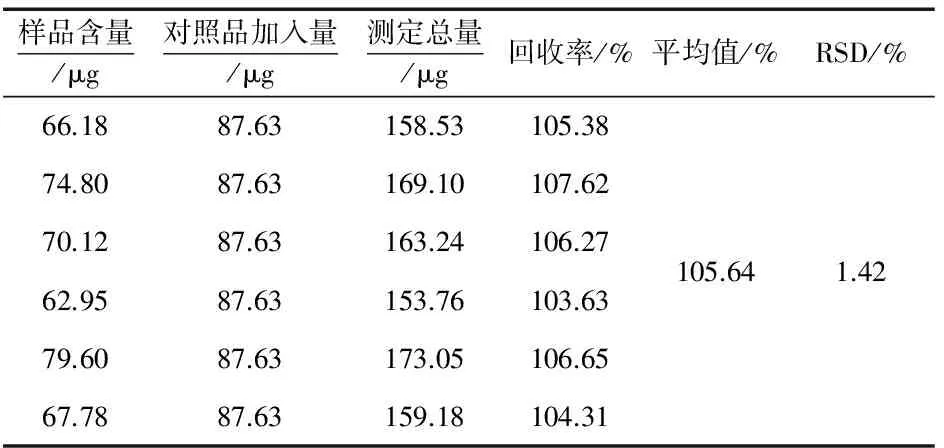
表1 牛黄解毒片中胆红素的加样回收实验结果(n=6)

表2 牛黄解毒丸中胆红素的加样回收实验结果(n=6)
2.9 检测限考察
精密量取胆红素对照品溶液(C=0.09266 μg·mL-1)5 μL,按“2.1”项下色谱条件测定,结果显示,S/N≈3.确定本品检测限为0.46 ng,折算成样品中的检测限即为:牛黄解毒片0.4 μg·片-1或大片0.6 μg·片-1,牛黄解毒丸1.15 μg·g-1(水蜜丸/水丸)或大蜜丸0.46 μg·g-1.
2.10 样品测定
依据建立的胆红素含量测定方法,对2批次牛黄解毒丸(水蜜丸)和246批次的牛黄解毒片进行了考察.2批次水蜜丸中,胆红毒含量分别为46.91 μg·g-1和48.42 μg·g-1;246批次牛黄解毒片剂样品中,胆红素含量从0.00 μg·片-1~50.82 μg·片-1(220批次小片),9.80 μg·片-1~55.602 μg·片-1(26批次大片),含量差异很大.结果见图3、图4.
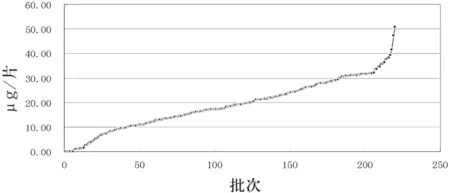
图3 牛黄解毒片(小片)胆红素含量结果
3 讨 论
由于胆红素不溶于水,可溶于苯、三氯甲烷及二硫化碳等有机溶剂中,但这些溶剂毒性均较大.对此,本研究考察了毒性较低的二氯甲烷、二氯甲烷—甲醇(8∶2)、二氯甲烷—甲醇(1∶1)3种提取溶剂,并同三氯甲烷作了比较.结果表明,二氯甲烷同三氯甲烷提取效果一致,二氯甲烷—甲醇(8∶2)同二氯甲烷—甲醇(1∶1)提取效果一致,且所提取的胆红素含量高于二氯甲烷与三氯甲烷,原因可能是加了甲醇后,溶剂对样品的渗透性较好,因而提取率更高.考虑到二氯甲烷的挥发性较强,最终选择了甲醇比例更高的溶剂,即二氯甲烷—甲醇(1∶1)为提取溶剂.
胆红素对光和热不稳定,因此本实验全程避光,并采用冰浴超声的方法进行提取.在制备工艺中,人工牛黄一般在压片或制丸之前加入,根据牛黄解毒片处方分析,胆红素理论含量分别为32 μg·片-1(大片)、21 μg·片-1(小片)、27 μg·g-1(水蜜丸).测定结果显示,246批样品胆红素含量相互之间差异较大,原因可能是由于原标准中无胆红素的含量测定项目,缺乏对厂家投料的监控.因此,本品标准的完善具有紧迫性和重要性.
本研究采用高效液相色谱法测定牛黄解毒片/水蜜丸中胆红素的含量,结果准确,重复性好,获得了理想的检测效果,可以作为牛黄解毒制剂的人工牛黄的质量评价鉴定方法,为其质量控制提供依据.本研究建议在牛黄解毒剂原标准中增加胆红素的含量测定,具体为:牛黄解素片中胆红素大片含量不得少于30 μg·片-1,小片胆红素含量不得少于20 μg·片-1;牛黄解毒丸(水蜜丸)中含胆红素含量不得少于25 μg·片-1.
[1]国家药典委员会.中华人民共和国药典[S].北京:中国医药科技出版社,2015.
[2]吴红霞,付锦江.高效液相色谱法测定西黄片中人工牛黄的胆红素含量测定[J].当代医学,2009,15(4):124-125.
[3]杨云沛,黄志东,李海生.人工牛黄及天然牛黄中胆红素的HPLC测定方法研究[J].天津药学,1995,7(2):15-16.
[4]罗珍妹,陈晓玲.高效液相色谱法测定人工牛黄中胆红素的含量[J].海峡药学,2010,22(6):48-50.
[5]王宜祥,傅剑飞.HPLC法测定小儿速效感冒灵中胆红素含量[J].现代应用药学,1996,13(6):59-61.
Determination of Bilirubin Content in Bezoar Detoxication Preparation by HPLC
LUOYaling,ZHOUJuan,QIJingliang
(Sichuan Institute for Food and Drug Control, Chengdu 610097, China)
The paper is going to establish a method for the determination of bilirubin in bezoar detoxicatio preparation.Liquid chromatography is used.The chromatography column is C18column;mobile phase is acetonitrile-1% acetic acid(95∶5);the detection wavelength is 450 nm.The results show that the amount of bilirubin in the sample has a high linearity among the range of 0.8321~208.032 ng,r=0.9995;the average recovery rate of the bezoar detoxicatio tablets is 105.6%,RSD=1.42%;the average recovery rate of bezoar detoxicatio pills is 96.2%,RSD=1.83%.The results demonstrate that this method is accurate and simple,and can be used as the method to determine the bilirubin content in bezoar detoxicatio tablets and pills.
bezoar detoxication preparation;bilirubin;liquid chromatography
1004-5422(2017)01-0021-04
1004-5422(2017)01-0018-03
2016-11-21.
罗亚玲(1978 — ), 女, 中药师, 从事中成药制剂有效成分检测与分析.
R927.2;O657.7+2
A
