碳水化合物种类和水平对大黄鱼生长性能、血清生化指标、肝脏糖代谢相关酶活性及肝糖原含量的影响
2017-04-11马红娜王猛强周歧存
马红娜 王猛强 陆 游 袁 野 孙 蓬 周歧存
(宁波大学海洋学院鱼类营养研究室,宁波315211)
碳水化合物种类和水平对大黄鱼生长性能、血清生化指标、肝脏糖代谢相关酶活性及肝糖原含量的影响
马红娜 王猛强 陆 游 袁 野 孙 蓬 周歧存*
(宁波大学海洋学院鱼类营养研究室,宁波315211)
本试验旨在研究碳水化合物种类和水平对大黄鱼生长性能、全鱼和肌肉常规成分、血清生化指标、肝脏糖代谢相关酶活性及肝糖原含量的影响。采用2×3双因素试验设计,选取葡萄糖和小麦淀粉2种碳水化合物,分别设0、15%、30% 3个碳水化合物水平,共配制5种等氮等脂试验饲料。每种饲料饲喂3个重复,每个重复放养初始体重为(8.53±0.07) g的大黄鱼50尾,养殖试验持续8周。结果表明:饲料碳水化合物种类和水平及其交互作用对大黄鱼的终末体重、增重率(WGR)、特定生长率(SGR)、饲料系数(FCR)有显著影响(P<0.05)。饲料葡萄糖水平由0增加到30%时,大黄鱼的终末体重、WGR和SGR显著降低(P<0.05);饲料小麦淀粉水平由0增加到15%时,大黄鱼的终末体重、WGR和SGR显著升高(P<0.05),饲料小麦淀粉水平由15%增加到30%时,大黄鱼的终末体重、WGR和SGR显著降低(P<0.05)。FCR随饲料葡萄糖水平的升高显著升高(P<0.05);FCR在饲料小麦淀粉水平由0增加到15%时显著降低(P<0.05),由15%增加到30%时显著升高(P<0.05)。15%或30%水平下,小麦淀粉组大黄鱼的终末体重、WGR和SGR均显著高于葡萄糖组(P<0.05),饲料系数显著低于葡萄糖组(P<0.05)。饲料碳水化合物种类和水平的交互作用对大黄鱼血清总蛋白(TP)、总胆固醇(TC)、甘油三酯(TG)、葡萄糖含量有显著影响(P<0.05)。血清葡萄糖含量随饲料葡萄糖的水平升高先降低后升高,各组间差异显著(P<0.05);血清葡萄糖含量随饲料小麦淀粉水平的升高逐渐降低,且30%小麦淀粉组显著低于0小麦淀粉组(P<0.05)。饲料碳水化合物种类和水平的交互作用对大黄鱼肝脏葡萄糖激酶(GK)、6-磷酸果糖激酶(PFK)、葡萄糖-6-磷酸酶(G6Pase)活性及肝糖原含量有显著影响(P<0.05)。肝糖原含量随饲料葡萄糖的水平升高持续升高,而随饲料小麦淀粉水平的升高先升高后降低,且15%和30%水平下葡萄糖组均显著高于小麦淀粉组(P<0.05)。由此得出,与葡萄糖相比,摄食含小麦淀粉饲料的大黄鱼能够通过调节糖代谢相关酶活性及肝糖原含量来维持血糖浓度的相对恒定,且饲料中添加15%小麦淀粉时能促进大黄鱼生长。
大黄鱼;碳水化合物;生长性能;糖代谢相关酶;肝糖原
碳水化合物是鱼类饲料中重要的能源物质,且比蛋白质和脂肪廉价[1],饲料中添加适量的碳水化合物不仅能促进鱼类生长,还能节省饲料成本、减轻氮排泄对养殖水体的污染[2]。但饲料中碳水化合物水平过高却会抑制鱼类的生长、降低饲料利用率、减弱鱼体抗病力、提高死亡率[3-4]。鱼类对碳水化合物的利用能力与葡萄糖耐受能力密切相关[1]。刘泓宇等[5]的研究表明,杂食性的吉富罗非鱼(Oreochromisniloticus)葡萄糖耐受能力最强,肉食性的卵形鲳鲹次之,肉食性的军曹鱼葡萄糖耐受能力最低。这说明肉食性鱼类对葡萄糖的利用能力较杂食性鱼类低,且鱼类对葡萄糖的利用存在着种类差异性[6-9]。鱼类对碳水化合物的利用状况也会因碳水化合物复杂程度而存在差异,研究表明石斑鱼(Epinephelusmalabaricus)[10]、草鱼(Ctenopharyngodonidella)[11]、金头鲷(Sparusaurata)[12]等对小分子糖利用较好,胭脂鱼(Myxocyprinusasiaticus)幼鱼[13]、吉富罗非鱼[14]、大菱鲆(Scophthalmusmaximus)[15]等对大分子糖利用较好,但这些研究均是在相同碳水化合物水平间的比较。研究表明,饲料碳水化合物水平可以调节鱼类肝脏糖酵解和糖异生关键酶的活性,从而调节鱼体血液中葡萄糖的含量[16],目前在翘嘴红鲌(ErythroculterilishaeformisBleeker)[4]、大菱鲆[17]、舌齿鲈(Dicentrarchuslabrax)[18]、瓦氏黄颡鱼(Pelteobagrusfulvidraco)[19]、金头鲷[12]和欧洲鳗鲡(Anguillaanguilla)[20]等鱼类中均有研究,通过这些酶活性的变化来探究鱼类糖代谢机制,从而解释鱼类对碳水化合物利用能力出现较大差异的原因。
大黄鱼(PseudosciaenacroceaRichardson)是我国传统“海洋四大经济鱼类”之一[21],为暖温性近海中下层集群洄游性鱼类,是肉食性鱼类中营养价值较高的养殖鱼类,因肉质鲜美而颇受消费者欢迎。目前对大黄鱼的蛋白质、脂肪及氨基酸需求量,替代蛋白质源,饲料原料消化率,营养成分及其风味均有研究[21-25],而有关大黄鱼碳水化合物利用的研究[26-28]较少。鉴于此,本试验选取葡萄糖和小麦淀粉2种碳水化合物,设计0、15%、30% 3个碳水化合物水平,研究碳水化合物种类和水平对大黄鱼生长性能、肝脏糖代谢相关酶活性的影响,从而为大黄鱼资源节约型配合饲料的研制提供基础数据和理论参考。
1 材料与方法
1.1 试验设计与饲料配制
以秘鲁鱼粉、豆粕、小麦蛋白粉为蛋白质源,鱼油、豆油、卵磷脂为脂肪源,并分别以0、15%、30% 3个水平的小麦淀粉或葡萄糖为糖源,配制5种等氮等脂饲料,试验饲料组成及营养水平见表1。将所有固态原料粉碎后过80目筛,按表1比例混合均匀(维生素和矿物质等微量组分采用逐级扩大法混合),再加入鱼油、豆油和卵磷脂以及水混合均匀,用双螺杆挤条机[F(Ⅱ)-26,华南理工大学,广州]加工制成粒径分别为2和4 mm的硬颗粒饲料,在烘箱中90 ℃熟化30 min,自然风干,密封保存于-20 ℃冰箱。
1.2 饲养管理
试验用大黄鱼鱼苗购自象山港湾水产苗种有限公司,养殖试验在浙江省象山县西沪港港湾鱼排上进行。正式试验前所有鱼苗先在鱼排上暂养2周,之后,挑选体质健壮、初始体重为(8.53±0.07) g的大黄鱼750尾,随机分配于15个网箱(1.5 m×1.5 m×2.0 m)中,每个网箱放养50尾鱼。将15个网箱随机分为5组,每组3个网箱(重复)。试验期间每天05:00和17:00各投喂1次,投饲率为体重的4%~6%。试验期间海水温度为26.5~31.5 ℃,盐度为19‰~25‰,溶解氧浓度不低于7.0 mg/L。养殖试验持续8周。
1.3 样品采集与指标测定
养殖试验结束后将鱼捞出,并用丁香酚(1∶10 000)麻醉,然后记录每个网箱的大黄鱼尾数并称量总重,用于计算增重率(WGR)、特定生长率(SGR)、成活率(SR)和饲料系数(FCR);每个网箱随机取3尾鱼,装于密封袋中,用于检测全鱼常规成分;每个网箱另随机取3尾鱼称重、量体长,取其肝脏、内脏并称重,用于计算肥满度(CF)、肝体比(HSI)、脏体比(VSI);每个网箱再随机取8尾鱼,从尾部静脉抽取血样(血样不混合),注入1.5 mL离心管中,4 ℃冰箱静置过夜后,3 000 r/min离心5 min,取上清液,每个网箱(重复)的血清进行混样后再分装至PCR管,置于-80 ℃冰箱备用;将上述取过血的大黄鱼解剖取肝脏,将肝脏放置于2 mL离心管中(每个网箱的肝脏混样,取完立即放入液氮中),用于检测肝脏葡萄糖激酶(GK)、6-磷酸果糖激酶(PFK)、丙酮酸激酶(PK)、葡萄糖-6-磷酸酶(G6Pase)、果糖-1,6-二磷酸酶(FBPase)、磷酸烯醇式丙酮酸羧激酶(PEPCK)活性及肝糖原含量;将上述取过肝脏的大黄鱼的背部肌肉剥离,取30 g左右,装于密封袋中,用于测定肌肉常规成分。

表1 试验饲料组成及营养水平(风干基础)
1)矿物质预混料和维生素预混料均参照Mai等[29]配制。Mineral premix and vitamin premix were prepared according to Mai et al[29].
2)营养水平为实测值。Nutrient levels were measured values.
参照AOAC(1995)[30]的方法测定饲料及大黄鱼全鱼和肌肉水分、粗蛋白质、粗脂肪和粗灰分含量。水分含量采用105 ℃恒温干燥法测定,粗蛋白质含量采用Leco FP-528全自动蛋白质分析仪测定,粗脂肪含量采用索氏抽提法测定,粗灰分含量采用550 ℃马弗炉灼烧法测定。部分血清生化指标使用日立7600-110型全自动生化分析仪测定;肝脏代谢酶活性及血清胰岛素和胰高血糖素含量均采用上海乔杜生物科技公司生产的酶联免疫吸附试验(ELISA)试剂盒进行测定。肝糖原含量采用南京建成生物工程研究所生产的肝糖原试剂盒检测。
1.4 计算公式
增重率(%)=100×(终末总重-
初始总重)/初始总重;
特定生长率(%/d)=100×(ln终末总重-
ln初始总重)/试验天数;
成活率(%)=100×终末尾数/初始尾数;
饲料系数=(投饲总量×饲料干物质含量)/
(终末总重-初始总重);
肝体比(%)=100×肝脏重/体重;
脏体比(%)=100×内脏重/体重;
肥满度(g/cm3)=100×体重/体长3。
1.5 统计分析
试验数据采用SPSS 19.0统计软件进行分析,先进行双因素方差分析(two-way ANOVA),以检验碳水化合物种类和水平及其交互作用对各指标平均值影响的显著性。若碳水化合物水平对指标平均值有显著影响,则进行Tukey’s多重比较;若碳水化合物种类对指标平均值有显著影响,则进行独立样本t检验。各指标数据采用平均值±标准差(mean±SD)表示,P<0.05表示差异显著。
2 结 果
2.1 碳水化合物种类和水平对大黄鱼生长性能和形态学指标的影响
由表2可知,饲料碳水化合物种类和水平及其交互作用对大黄鱼的终末体重、增重率、特定生长率、饲料系数有显著影响(P<0.05),但对成活率、肥满度、肝体比、脏体比无显著影响(P>0.05)。
大黄鱼的终末体重、增重率和特定生长率随饲料葡萄糖水平的升高显著降低(P<0.05);而当饲料中小麦淀粉水平由0增加到15%时,大黄鱼的终末体重、增重率和特定生长率显著升高(P<0.05),而随饲料小麦淀粉水平由15%的进一步增加到30%,大黄鱼的终末体重、增重率和特定生长率显著降低(P<0.05)。饲料系数随饲料葡萄糖水平的升高显著升高(P<0.05);而饲料系数随饲料小麦淀粉水平的升高先升高后降低,且15%小麦淀粉组的饲料系数显著低于0和30%小麦淀粉组(P<0.05)。在15%或30%水平下,小麦淀粉组大黄鱼的终末体重、增重率和特定生长率均显著高于葡萄糖组(P<0.05),饲料系数则显著低于葡萄糖组(P<0.05)。

表2 碳水化合物种类和水平对大黄鱼生长性能和形态学指标的影响
同行数据肩标不同小写字母表示同种碳水化合物不同水平组间差异显著(P<0.05);同列数据肩标不同大写字母表示同一水平不同种类碳水化合物组间差异显著(P<0.05)。P:碳水化合物种类;C:碳水化合物水平。下表同。
In the same row, values with different small letter superscripts indicated significant difference among different carbohydrate level groups following the same carbohydrate type (P<0.05); in the same column, values with different capital letter superscripts indicated significant difference among different carbohydrate groups following the same carbohydrate level (P<0.05). P: carbohydrate type; C: carbohydrate level. The same as below.
2.2 碳水化合物种类和水平对大黄鱼全鱼和肌肉常规成分的影响
由表3可知,饲料碳水化合物种类和水平的交互作用对大黄鱼全鱼和肌肉的水分、粗脂肪含量有显著影响(P<0.05),但对全鱼和肌肉的粗蛋白质、粗灰分含量无显著影响(P>0.05)。全鱼和肌肉的粗脂肪含量随饲料小麦淀粉水平的升高而升高,30%小麦淀粉组显著高于0和15%小麦淀粉组(P<0.05);肌肉粗脂肪含量随饲料葡萄糖的水平的升高先升高后降低,15%葡萄糖组显著高于0和30%葡萄糖组(P<0.05)。在15%水平下,葡萄糖组肌肉粗脂肪含量显著高于小麦淀粉组(P<0.05);在30%水平下,葡萄糖组肌肉粗脂肪含量显著低于小麦淀粉组(P<0.05)。
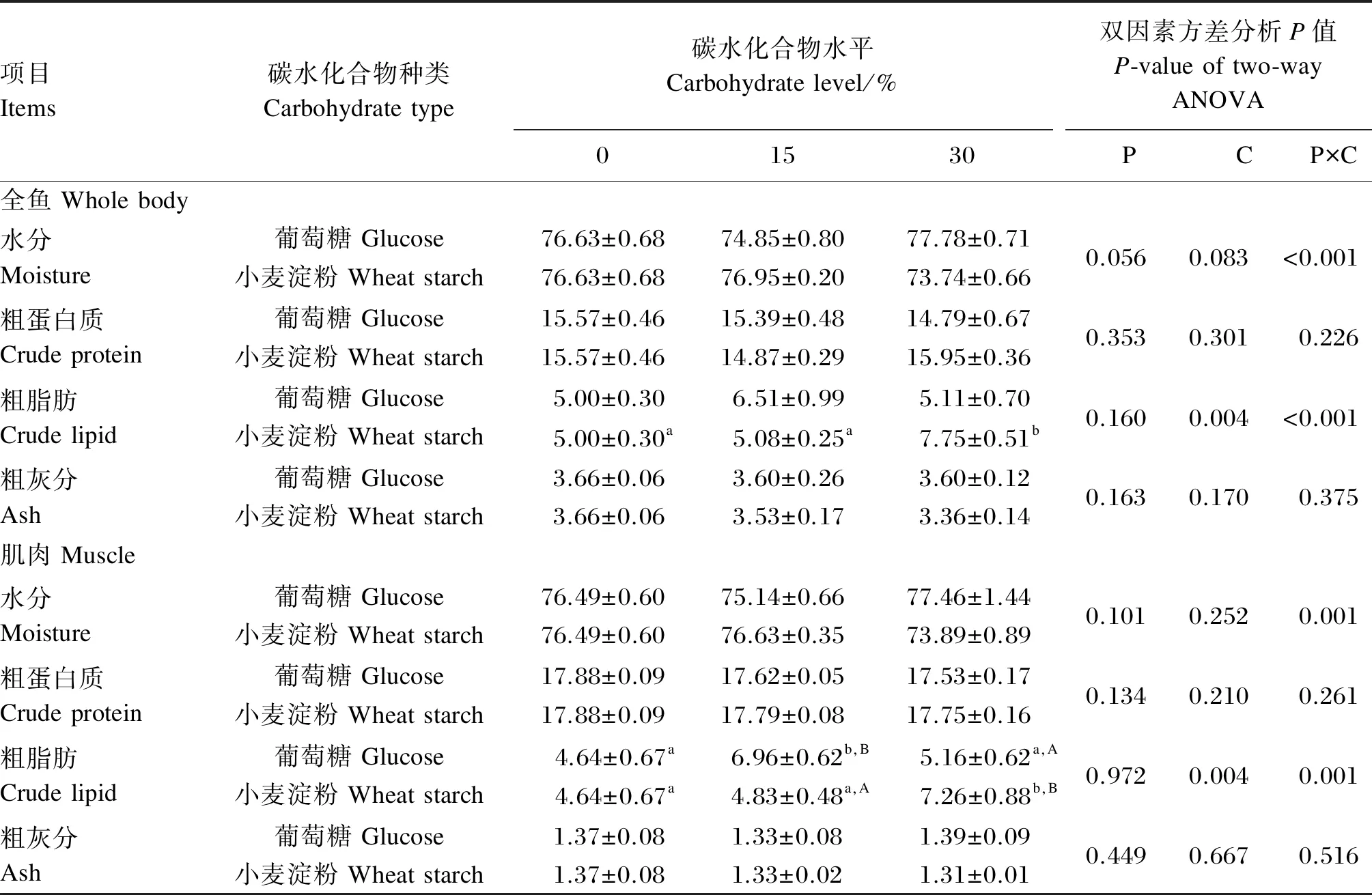
表3 碳水化合物不同种类和水平对大黄鱼全鱼和肌肉常规成分的影响
2.3 碳水化合物种类和水平对大黄鱼血清生化指标的影响
由表4可知,饲料碳水化合物种类和水平的交互作用对大黄鱼血清总蛋白、总胆固醇、甘油三酯、葡萄糖含量有显著影响(P<0.05),但对胰岛素、胰高血糖素含量无显著影响(P>0.05)。血清总胆固醇含量随饲料葡萄糖水平的升高先升高后降低,30%葡萄糖组显著低于0和15%葡萄糖组(P<0.05),且15%葡萄糖组显著高于15%小麦淀粉组(P<0.05),30%葡萄糖组显著低于30%小麦淀粉组(P<0.05)。血清甘油三酯含量随饲料葡萄糖水平的升高先升高后降低,30%葡萄糖组显著低于15%葡萄糖组(P<0.05);血清甘油三酯含量随饲料小麦淀粉水平的升高先降低后升高,30%小麦淀粉组显著高于0、15%小麦淀粉组(P<0.05)。血清葡萄糖含量随饲料葡萄糖的水平升高先降低后升高,各组间差异显著(P<0.05);血清葡萄糖含量随饲料小麦淀粉水平的升高逐渐降低,且30%小麦淀粉组显著低于0小麦淀粉组(P<0.05)。

表4 碳水化合物种类和水平对大黄鱼血清生化指标的影响
2.4 碳水化合物种类和水平对大黄鱼肝脏糖代谢相关酶活性及肝糖原含量的影响
由表5可知,饲料碳水化合物种类和水平的交互作用对大黄鱼肝脏葡萄糖激酶、6-磷酸果糖激酶、葡萄糖-6-磷酸酶活性及肝糖原含量有显著影响(P<0.05),但对丙酮酸激酶、果糖-1,6-二磷酸酶、磷酸烯醇式丙酮酸羧激酶活性无显著影响(P>0.05)。肝脏葡萄糖激酶活性随饲料葡萄糖水平的升高而升高,随小麦淀粉水平的升高先升高后降低,且15%葡萄糖组显著低于15%小麦淀粉组(P<0.05)。肝脏6-磷酸果糖激酶活性随饲料葡萄糖水平的升高先升高后降低,随小麦淀粉水平的升高而升高,且30%葡萄糖组显著低于30%小麦淀粉组(P<0.05)。肝脏丙酮酸激酶活性随饲料小麦淀粉水平的升高先降低后升高,且15%小麦淀粉显著低于0和30%小麦淀粉组(P<0.05)。肝脏葡萄糖-6-磷酸酶活性随饲料葡萄糖水平的升高先稍有降低而后显著升高(P<0.05),随小麦淀粉水平的升高先显著升高(P<0.05)后保持平稳。肝糖原含量随饲料葡萄糖水平的升高显著升高(P<0.05),而当饲料小麦淀粉水平由0增加到15%时,大黄鱼肝糖原含量显著升高(P<0.05),当饲料小麦淀粉水平由15%增加到30%时,大黄鱼肝糖原含量显著降低(P<0.05),且15%、30%葡萄糖组分别显著高于15%、30%小麦淀粉组(P<0.05)。
3 讨 论
3.1 碳水化合物种类和水平对大黄鱼生长性能和形态学指标的影响
碳水化合物对于鱼类的成活和生长并非必需的,鱼类摄食不含碳水化合物的饲料也能正常生长[31]。在本试验中,含15%小麦淀粉饲料更有利于大黄鱼生长,表明适宜的饲料碳水化合物水平能促进鱼类生长[2]。本研究结果表明大黄鱼对小麦淀粉的利用能力要高于葡萄糖,这一结果与李弋等[28]的研究结果相同。然而,一些研究结果表明鱼类对葡萄糖的利用能力好于淀粉等多糖[11-12,32]。在青鱼的研究中发现分别用20%和40%的葡萄糖和小麦淀粉进行16周的投喂后增重率各组之间无显著差异[33];在石斑鱼的研究中也发现同样的结果,即石斑鱼对小麦淀粉和葡萄糖的利用效果无显著差异[10]。本试验结果与以上研究者的研究结果不相同,这可能是由于不同鱼类对碳水化合物的利用能力不同所致[34]。肝脏是机体的重要代谢器官,鱼类吸收的碳水化合物很大一部分转化为脂肪积累在肝脏中[35],因此鱼类摄食含高水平碳水化合物的饲料后肝体比会上升[33,36],但本试验中发现碳水化合物水平对肝体比无显著影响,这与王猛强等[26-27]的研究结果一致。究其原因,可能是大黄鱼利用碳水化合物合成脂肪并在肝脏中沉积的能力较低。本试验中,同一水平下,葡萄糖组大黄鱼的饲料系数显著高于小麦淀粉组,表明小麦淀粉组大黄鱼的饲料转化率较高,即大黄鱼对小麦淀粉的利用效果更好。

表5 碳水化合物种类和水平对大黄鱼肝脏糖代谢相关酶活性及肝糖原含量的影响
3.2 碳水化合物种类和水平对大黄鱼全鱼和肌肉常规成分的影响
有研究表明,饲料碳水化合物水平对鱼类粗脂肪含量的影响显著,而对鱼类水分、粗蛋白质、粗灰分含量的影响均不显著[37-38],本试验结果与之相似。本试验结果发现,大黄鱼全鱼和肌肉粗脂肪含量与小麦淀粉水平呈正相关,这与在鲤鱼[39]、尼罗罗非鱼(OreochromisniloticusL.)[40]、南方鲇[41]、军曹鱼(RachycentroncanadumL.)[42]、翘嘴红鲌[43]中的研究结果相似,说明饲料碳水化合物水平的升高加快碳水化合物转化为脂肪,从而使得鱼体粗脂肪含量升高。另一些研究发现,随饲料碳水化合物水平的升高,非洲鲇(Clariasgariepinus)[37]、星斑川碟(Platichthysstellatus)[38]、黄鳍鲷(Sparuslatus)[44]鱼体粗脂肪含量降低,与本试验结果不一致,这可能是由于鱼体脂肪摄入量减少且不同鱼类将碳水化合物转化为脂肪的能力不同所致。脂肪是动物储存的主要能量物质,有研究表明,淀粉类多糖比单糖更易于鱼类吸收储存[32],本试验也发现,较于葡萄糖,大黄鱼更善于将饲料中的小麦淀粉转化为脂肪储存在体内,从而促进其生长。
3.3 碳水化合物种类和水平对大黄鱼血清生化指标的影响
在正常生理状态下动物一般能使自身各项生理指标保持动态稳定,因此血液组分的变化在一定程度上能够反映动物的健康情况[45]。血清胆固醇和甘油三酯含量变化在一定程度上能够反映肝脏代谢功能[46]。在哺乳动物中发现,当肝细胞受损时,血清胆固醇含量降低[47],且研究表明鱼类胆固醇代谢几乎与哺乳动物一样[43]。本试验发现,30%葡萄糖组血清总胆固醇含量显著低于15%葡萄糖组、30%小麦淀粉组,这与在翘嘴红鲌[43]中的研究结果一致,表明高葡萄糖水平导致大黄鱼肝脏生理机能发生了变化;30%葡萄糖组血清葡萄糖含量显著高于0、15%葡萄糖组,表明大黄鱼对葡萄糖的利用能力有限,高水平的葡萄糖会导致大黄鱼持续高血糖浓度,对生长不利;而小麦淀粉水平对血清总胆固醇含量无显著影响,且血清葡萄糖含量随小麦淀粉水平的升高而降低,在翘嘴红鲌[43]的研究中也发现血清葡萄糖含量并没有随着α-淀粉水平的升高而上升,反而在高α-淀粉水平有下降的趋势,与本研究结果相似。这一方面可能是因为经过8周的饲养,大黄鱼对小麦淀粉出现了代谢适应,能够有效利用小麦淀粉,从而在摄食高水平小麦淀粉饲料时表现良好的生长状况;另一方面可能是因为对于淀粉等大分子糖类,大黄鱼消化吸收速率较慢,鱼体内的糖代谢相关酶的活化与葡萄糖的吸收速率达到同步,从而缓解了高水平葡萄糖对鱼体造成的不利影响;此外,这也可能是由于当鱼体摄入含中等水平的小麦淀粉饲料时,鱼体仅表现为血清葡萄糖和肝糖原含量的增高,但是当摄入高水平的小麦淀粉饲料时,鱼体相对增高了血清葡萄糖和肝糖原含量,同时也增高了体内脂肪的合成和累积率,从而使鱼体的血清葡萄糖和肝糖原含量保持在一定的阈值内[41],因此出现本试验的结果,但具体原因仍需进一步探究。胰岛素是唯一能降低血液葡萄糖含量的激素。本试验发现,碳水化合物种类和水平对大黄鱼血清胰岛素含量无显著影响,表明鱼类胰岛素的分泌与饲料碳水化合物种类和水平无关[7],对血液葡萄糖含量的调节主要依赖肝脏糖代谢相关酶活性及肝糖原含量。
3.4 碳水化合物种类和水平对大黄鱼肝脏糖代谢相关酶活性及肝糖原含量的影响

4 结 论
饲料添加15%小麦淀粉时,大黄鱼能够通过调节糖代谢相关酶活性及肝糖原含量来维持血糖浓度的平衡,并能促进大黄鱼生长;饲料添加30%小麦淀粉时,大黄鱼能够通过调节糖代谢相关酶活性及肝糖原含量来维持血糖的平衡,但对生长有一定的抑制作用。而随饲料葡萄糖水平的升高,大黄鱼通过调节肝脏葡萄糖激酶、6-磷酸果糖激酶活性及肝糖原含量仍不能维持血糖浓度的相对恒定,且大黄鱼生长严重受抑。
[1] 毛义波,刘泓宇,谭北平,等.饲料碳水化合物水平及饥饿处理对斜带石斑鱼生长及葡萄糖耐受能力的影响[J].水产学报,2014,38(4):550-559.
[2] 吴凡,文华,蒋明,等.饲料碳水化合物水平对奥尼罗非鱼幼鱼生长、体成分和血清生化指标的影响[J].华南农业大学学报,2011,32(4):91-95.
[3] LI X F,LIU W B,LU K L,et al.Dietary carbohydrate/lipid ratios affect stress,oxidative status and non-specific immune responses of fingerling blunt snout bream,Megalobramaamblycephala[J].Fish & Shellfish Immunology,2012,33(2):316-323.
[4] 戈贤平,刘波,谢骏,等.饲料中不同碳水化合物水平对翘嘴红鲌生长及血液指标和糖代谢酶的影响[J].南京农业大学学报,2007,30(3):88-93.
[5] 刘泓宇,毛义波,谭北平,等.饲料糖水平对不同食性鱼类生长及葡萄糖耐受能力的影响[J].水产学报,2015,39(12):1852-1862.
[6] FURUICHI M,YONE Y.Change of blood sugar and plasma insulin levels of fishes in glucose tolerance test[J].Nippon Suisan Gakkaishi,1981,47(6):761-764.
[7] CAPILLA E,MÉDALE F,NAVARRO I,et al.Muscle insulin binding and plasma levels in relation to liver glucokinase activity,glucose metabolism and dietary carbohydrates in rainbow trout[J].Regulatory Peptides,2003,110(2):123-132.
[8] PERES H,GONÇALVES P,OLIVA-TELES A.Glucose tolerance in gilthead seabream (Sparusaurata) and European seabass (Dicentrarchuslabrax)[J].Aquaculture,1999,179(1/2/3/4):415-423.
[9] LEGATE N J,BONEN A,MOON T W.Glucose tolerance and peripheral glucose utilization in rainbow trout (Oncorhynchusmykiss),American eel (Anguillarostrata),and black bullhead catfish (Ameiurusmelas)[J].General and Comparative Endocrinology,2001,122(1):48-59.
[10] SHIAU S Y,LIN Y H.Carbohydrate utilization and its protein-sparing effect in diets for grouper (Epinephelusmalabaricus)[J].Animal Science,2001,73(2):299-304.
[11] TIAN L X,LIU Y J,HUNG S S O.Utilization of glucose and cornstarch by juvenile grass carp[J].North American Journal of Aquaculture,2004,66(2):141-145.
[12] ENES P,PANSERAT S,KAUSHIK S,et al.Growth performance and metabolic utilization of diets with native and waxy maize starch by gilthead sea bream (Sparusaurata) juveniles[J].Aquaculture,2008,274(1):101-108.
[13] 张颂.胭脂鱼幼鱼饲料中适宜碳脂比、糖源和脂肪源的研究[D].硕士学位论文.武汉:华中农业大学,2014.
[14] 吴彬,彭淇,陈斌,等.日粮中不同糖源对吉富罗非鱼(Oreochromisniloticus)稚鱼养殖效果与机理研究[J].海洋与湖沼,2013,44(4):1050-1055.
[15] 苗淑彦,苗惠君,聂琴,等.饲料中不同种类的碳水化合物对大菱鲆生长性能和代谢反应的影响[J].水产学报,2013,37(6):910-919.
[16] ENES P,PANSERAT S,KAUSHIK S,et al.Nutritional regulation of hepatic glucose metabolism in fish[J].Fish Physiology and Biochemistry,2009,35(3):519-539.
[17] 聂琴,苗惠君,苗淑彦,等.不同糖源及糖水平对大菱鲆糖代谢酶活性的影响[J].水生生物学报,2013,37(3):425-433.
[18] ENES P,PANSERAT S,KAUSHIK S,et al.Effect of normal and waxy maize starch on growth,food utilization and hepatic glucose metabolism in European sea bass (Dicentrarchuslabrax) juveniles[J].Comparative Biochemistry and Physiology Part A:Molecular & Integrative Physiology,2006,143(1):89-96.
[19] 张世亮.饲料中糖结构、糖水平及糖脂比对瓦氏黄颡鱼幼鱼生长及糖代谢的影响[D].硕士学位论文.青岛:中国海洋大学,2011.
[21] 张帆.大黄鱼(PseudosciaenacroceaR.)脂类营养生理和饲料替代蛋白源的研究[D].硕士学位论文.青岛:中国海洋大学,2012.
[22] 林淑琴.不同生长阶段大黄鱼的蛋白质和蛋/能比营养研究[D].硕士学位论文.青岛:中国海洋大学,2013.
[23] 何志刚.大黄鱼(PseudosciaenacroceaR.)和鲈鱼(Lateolabraxjaponicus)苏氨酸和苯丙氨酸营养生理研究[D].硕士学位论文.青岛:中国海洋大学,2008.
[24] 申屠基康.大黄鱼对21种饲料原料表观消化率及色氨酸营养需要研究[D].硕士学位论文.青岛:中国海洋大学,2010.
[25] 周飘苹,金敏,吴文俊,等.不同养殖模式、投喂不同饵料及不同品系大黄鱼营养成分比较[J].动物营养学报,2014,26(4):969-980.
[26] 王猛强,周飘苹,黄文文,等.不同蛋白质水平下葡萄糖添加水平对大黄鱼生长性能、糖酵解和糖异生关键酶活性的影响[J].动物营养学报,2015,27(8):2431-2442.
[27] 王猛强,黄文文,周飘苹,等.不同蛋白质和小麦淀粉水平对大黄鱼生长性能、糖酵解和糖异生关键酶活性的影响[J].水产学报,2015,39(11):1690-1701.
[28] 李弋,周飘苹,邱红,等.饲料中糖源对大黄鱼生长性能及消化酶、糖代谢关键酶活性的影响[J].动物营养学报,2015,27(11):3438-3447.
[29] MAI K S,WAN J L,AI Q H,et al.Dietary methionine requirement of large yellow croaker,PseudosciaenacroceaR[J].Aquaculture,2006,253(1/2/3/4):564-572.
[30] AOAC.Official methods of analysis of the Association of Official Analytical Chemists[S].16th ed.Arlington,VA:Association of Official Analytical Chemists,1995.
[31] NRC.Nutrient requirements of fish and shrimp[S].Washington,D.C.:National Academies Press,2011.
[32] 林小植,罗毅平,谢小军.饲料碳水化合物水平对南方鲇幼鱼餐后糖酵解酶活性及血糖浓度的影响[J].水生生物学报,2006,30(3):304-310.
[33] 蔡春芳,陈立侨,叶元土,等.日粮糖种类和水平对青鱼生长性能和生理指标的影响[J].动物营养学报,2009,21(2):212-218.
[34] 蔡春芳,陈立侨.鱼类对糖的利用评述[J].水生生物学报,2006,30(5):608-613.
[35] 田丽霞.草鱼糖代谢研究[D].博士学位论文.广州:中山大学,2002:10-44.
[36] DENG D F,REFSTIE S,HUNG S S O.Glycemic and glycosuric responses in white sturgeon (Acipensertransmontanus) after oral administration of simple and complex carbohydrates[J].Aquaculture,2001,199(1/2):107-117.
[37] ALI M Z,JAUNCEY K.Optimal dietary carbohydrate to lipid ratio in African catfishClariasgariepinus(Burchell 1822)[J].Aquaculture International,2004,12(2):169-180.
[38] LEE S M,LEE J H.Effect of dietary glucose,dextrin and starch on growth and body composition of juvenile starry flounderPlatichthysstellatus[J].Fisheries Science,2004,70(1):53-58.
[39] KESHAVANATH P,MANJAPPA K,GANGADHARA B.Evaluation of carbohydrate rich diets through common carp culture in manured tanks[J].Aquaculture Nutrition,2002,8(3):169-174.
[40] GAYE-SIESSEGGER J,FOCKEN U,BECKER K.Effect of dietary protein/carbohydrate ratio on activities of hepatic enzymes involved in the amino acid metabolism of Nile tilapia,Oreochromisniloticus(L.)[J].Fish Physiology and Biochemistry,2006,32(4):275-282.
[41] 罗毅平.肉食性鱼类南方鲇对饲料碳水化合物营养胁迫的生理生态学反应[D].博士学位论文.重庆:西南大学,2007.
[42] REN M C,AI Q H,MAI K S,et al.Effect of dietary carbohydrate level on growth performance,body composition,apparent digestibility coefficient and digestive enzyme activities of juvenile cobia,RachycentroncanadumL.[J].Aquaculture Research,2011,42(10):1467-1475.
[43] 王广宇.日粮碳水化合物水平对翘嘴红鲌生长、血液指标及GK、G6Pase、HSC70基因表达的影响[D].硕士学位论文.南京:南京农业大学,2009.
[44] HU Y H,LIU Y J,TIAN L X,et al.Optimal dietary carbohydrate to lipid ratio for juvenile yellowfin seabream (Sparuslatus)[J].Aquaculture Nutrition,2007,13(4):291-297.
[45] DJANGMAH J S.The effects of feeding and starvation on copper in the blood and hepatopancreas,and on blood proteins ofCrangonvulgaris(Fabricius)[J].Comparative Biochemistry and Physiology,1970,32(4):709-731.
[46] 程汉良,夏德全,吴婷婷.鱼类脂类代谢调控与脂肪肝[J].动物营养学报,2006,18(4):294-298.
[47] 阎红卫,张欣.血清总胆固醇在肝病中的应用[J].世界核心医学期刊文摘:胃肠病学分册,2006,2(2):1-3.
[48] LIN J H,SHIAU S Y.Hepatic enzyme adaptation to different dietary carbohydrates in juvenile tilapiaOreochromisniloticus×O.aureus[J].Fish Physiology and Biochemistry,1995,14(2):165-170.
[49] SHIAU S Y,LIANG H S.Carbohydrate utilization and digestibility by tilapia,Oreochromisniloticus×O.aureus,are affected by chromic oxide inclusion in the diet[J].The Journal of Nutrition,1995,125(4):976-982.
[50] ENES P,PANSERAT S,KAUSHIK S,et al.Rapid metabolic adaptation in European sea bass (Dicentrarchuslabrax) juveniles fed different carbohydrate sources after heat shock stress[J].Comparative Biochemistry and Physiology Part A:Molecular & Integrative Physiology,2006,145(1):73-81.
[51] TAN Q,XIE S,ZHU X,et al.Effect of dietary carbohydrate sources on growth performance and utilization for gibel carp (Carassiusauratusgibelio) and Chinese longsnout catfish (LeiocassislongirostrisGünther)[J].Aquaculture Nutrition,2006,12(1):61-70.
[52] PANSERAT S,MÉDALE F,BRQUE J,et al.Lack of significant long-term effect of dietary carbohydrates on hepatic glucose-6-phosphatase expression in rainbow trout (Oncorhynchusmykiss)[J].The Journal of Nutritional Biochemistry,2000,11(1):22-29.
[53] 李爱杰.水产动物营养与饲料学[M].北京:中国农业出版社,1996:26-36.
[54] HEMRE G I,MOMMSEN T P,KROGDAHL Å.Carbohydrates in fish nutrition:effects on growth,glucose metabolism and hepatic enzymes[J].Aquaculture Nutrition,2002,8(3):175-194.
*Corresponding author, professor, E-mail: zhouqicun@nbu.edu.cn
(责任编辑 菅景颖)
Effects of Carbohydrate Type and Level on Growth Performance, Serum Biochemical Indices, Hepatic Glycometabolism-Related Enzyme Activities and Hepatic Glycogen Content of Large Yellow Croaker (LarimichthyscroceaRichardson)
MA Hongna WANG Mengqiang LU You YUAN Ye SUN Peng ZHOU Qicun*
(LaboratoryofFishNutrition,SchoolofMarineSciences,NingboUniversity,Ningbo315211,China)
An 8-week feeding trial was conducted to evaluate the effects of carbohydrate type and level on growth performance, whole body and muscle conventional components, serum biochemical indices, hepatic glycometabolism-related enzyme activities and hepatic glycogen content of large yellow croaker (LarimichthyscroceaRichardson). Using a 2×3 two-factor experiment design, five isonitrogenous and isolipidic experimental diets were formulated to contain three carbohydrate levels (0, 15% and 30%), and glucose and wheat starch were used as carbohydrate sources, respectively. Each diet was randomly assigned to 3 replicates and each replicate had 50 large yellow croakers with the initial body weight of (8.53±0.07) g. The results showed that the final body weight, weight gain rate (WGR), specific growth rate (SGR) and feed conversion ratio (FCR) were significantly affected by dietary carbohydrate type and level and their interaction (P<0.05). The final body weight, WGR and SGR significantly decreased with dietary glucose level increasing from 0 to 30% (P<0.05); however, the final weight, WGR and SGR significantly increased with dietary wheat starch level increasing from 0 to 15% and then significantly decreased with dietary wheat starch level increasing from 15% to 30% (P<0.05). FCR significantly increased with of dietary glucose level increasing (P<0.05), but it significantly decreased with dietary wheat starch level increasing from 0 to 15% (P<0.05) and significantly increased with dietary wheat starch level increasing from 15% to 30% (P<0.05). Total protein (TP), total cholesterol (TC), triglyceride (TG) and glucose contents in serum were significantly affected by the interaction of dietary carbohydrate type and level (P<0.05). Glucose content in serum was firstly decreased and then increased with dietary glucose level increasing, and the difference was significant among groups (P<0.05). With dietary wheat starch level increasing, glucose content in serum had a decrease trend, and it in 30% wheat starch group was significantly lower than that in 0 wheat starch group (P<0.05). Hepatic glucokinase (GK), phosphofructokinase (PFK) and glucose-6-phosphatase (G6Pase) activities and hepatic glycogen content were significantly affected by the interaction of dietary carbohydrate type and level (P<0.05). Hepatic glycogen content had a continuously increase with dietary glucose level increasing, but it increased at first and then decreased with dietary wheat starch increasing. Fish fed the diets with wheat starch had significantly higher hepatic glycogen content than those fed the diets with glucose under the 15% or 30% level (P<0.05). These results demonstrate that compared with glucose, diet with wheat starch can make large yellow croaker has the ability to maintain a relatively constant concentration of blood glucose by adjusting hepatic glycometabolism-related enzyme activities and hepatic glycogen content, and the growth performance of large yellow croaker can be improved when the diet with 15% wheat starch.[ChineseJournalofAnimalNutrition, 2017, 29(3):824-835]
large yellow croaker (LarmichthyscroceaRichardson); carbohydrate; growth performance; glycometabolism-related enzymes; hepatic glycogen
10.3969/j.issn.1006-267x.2017.03.012
2016-09-08
国家自然科学基金项目(31272670);宁波市农业科技攻关重大项目(2012C10025);国家科技部星火重大计划项目(2014GA701001);浙江省重中之重一级学科(水产)开放基金
马红娜(1994—),女,山西临汾人,硕士研究生,从事水生动物营养与饲料研究。E-mail: 121848841@qq.com
*通信作者:周歧存,教授,博士生导师,E-mail: zhouqicun@nbu.edu.cn
S963
A
1006-267X(2017)03-0824-12
