硫化铋精矿还原造锍熔炼一步炼铋
2017-04-06唐朝波叶龙刚陈永明唐谟堂杨声海
唐朝波,刘 永,叶龙刚, 2,陈永明,唐谟堂,杨声海
硫化铋精矿还原造锍熔炼一步炼铋
唐朝波1,刘 永1,叶龙刚1, 2,陈永明1,唐谟堂1,杨声海1
(1. 中南大学冶金与环境学院,长沙 410083;2. 湖南工业大学冶金工程学院,株洲 412007)
为解决我国当前火法炼铋厂普遍存在低浓度二氧化硫烟气污染、铋回收率低、试剂消耗大等问题,提出一种硫化铋精矿清洁冶金的工艺即硫化铋精矿还原造锍一步熔炼。采用单因素条件实验法考察添加剂用量、熔炼渣型、熔炼温度、反应时间等因素对金属铋直收率和渣含铋的影响,得出最佳熔炼工艺条件为:添加剂碳酸钠用量为精矿用量的20%(质量分数)、(FeO)/(SiO2)=1.0、(CaO)/(SiO2)=0.9、熔炼温度为1300 ℃、熔炼时间为2 h。在此最优条件下,金属铋直收率为85.86 %,渣含铋0.11%,固硫率达98.32%。同时,铅、钼、银在粗铋中的直收率分别达81.34%、80.95%、79.11%,说明新工艺的熔炼过程中对有价金属富集较好。
硫化铋精矿;还原造锍;清洁冶金;一步熔炼
铋是一种应用广泛的“绿色金属”,广泛用于冶金添加剂、低熔点合金、化工、光电材料、医药、国防等领域。全球铋资源储量约33万t,其中中国铋矿储量占世界总储备量的75%。金属铋的现代生产方法可分为湿法冶炼和火法冶炼两大类[1]。湿法工艺方面,主要过程包括铋矿浸出和含铋液提取铋两段。对于铋的氧化矿一般采取酸性浸出,硫化铋矿则多采用三氯化铁浸出、氯气选择性浸出、矿浆电解等工艺,含铋浸出液提取铋则主要采用铁粉置换、水解沉铋、隔膜电解等工艺[2],其共同缺点是设备容易腐蚀、生产成本高、电流效率低、废水量大、溶液中杂质难处理等缺点。新氯化水解法[3]、邱定蕃等[4]提出的矿浆电解法、张杜超[5]提出的碱性加压浸出工艺,各有优势,但目前仍处于试验阶段,尚未工业化。
目前,铋的主要工业生产方法以火法冶炼为主,适用于高品位的铋精矿和含铋物料。针对原料成分和性质的不同釆用不同的熔炼工艺,主要有熔析熔炼、沉淀熔炼、还原熔炼和混合熔炼[6]。熔析熔炼只能得到含铋的硫化物而不能直接得到金属铋,且熔析渣含铋高,须从渣中再回收铋金属,进一步处理十分困难;沉淀熔炼,又称置换熔炼,目前,我国湖南柿竹园有色金属有限责任公司采用此工艺生产金属铋,该工艺流程短、操作容易[7];但不宜处理低品位硫化矿和氧化矿的混合矿,且需消耗大量的铁屑和添加剂碳酸钠,具有一定局限性。还原熔炼只能处理铋的氧化矿(对于多为硫化物的铋矿,需先进行焙烧处理),因此,对于一般的铋精矿不可避免地存在低浓度二氧化硫烟气的问题[8−10]。混合熔炼是氧化铋矿的还原和硫化铋矿的置换在同一个反应炉进行的一种熔炼方法,此熔炼对原料的适应性强,但其反应也会产生大量难以处理的低浓度二氧化硫,且熔炼条件较难控制。因此针对以上问题,有学者研究开发了多种火法炼铋新工艺,唐谟堂、张传福等将低温碱性熔炼方法用于处理铅、锑、铋的硫化精矿[11−15],该工艺具有熔炼温度低、清洁无污染、金属回收率高等优点,但由于生产成本高、碱耗大、熔盐渣难处理等不足,仍处于实验阶段。
还原造锍熔炼是将硫化精矿与造锍剂、还原剂、添加剂混合后在1000~1300 ℃下进行熔炼一步产出粗金属、锍及炉渣,该工艺具有流程简单、试剂消耗少、成本低、清洁无污染等优点。因此,在文献[1]的基础上,本文作者提出用富含铁氧化物的磁铁矿作为造锍剂的硫化铋精矿还原造锍熔炼工艺,硫以FeS的形式固定在铁锍中(铁锍送至炼铜厂回收铜或外售制酸厂回收硫),从而消除了我国火法炼铋行业中存在的低浓度SO2烟气污染问题,同时将精矿中含量较高的有价金属(Mo、Pb)富集于合金,起到综合回收利用的效果。
1 实验
1.1 实验原料及试剂
本文作者所采用的实验原料为湖南有色集团柿竹园有色金属材料股份有限公司提供的铋精矿,其化学成分和XRD谱如表1和图1所示。

表1 铋精矿的化学成分
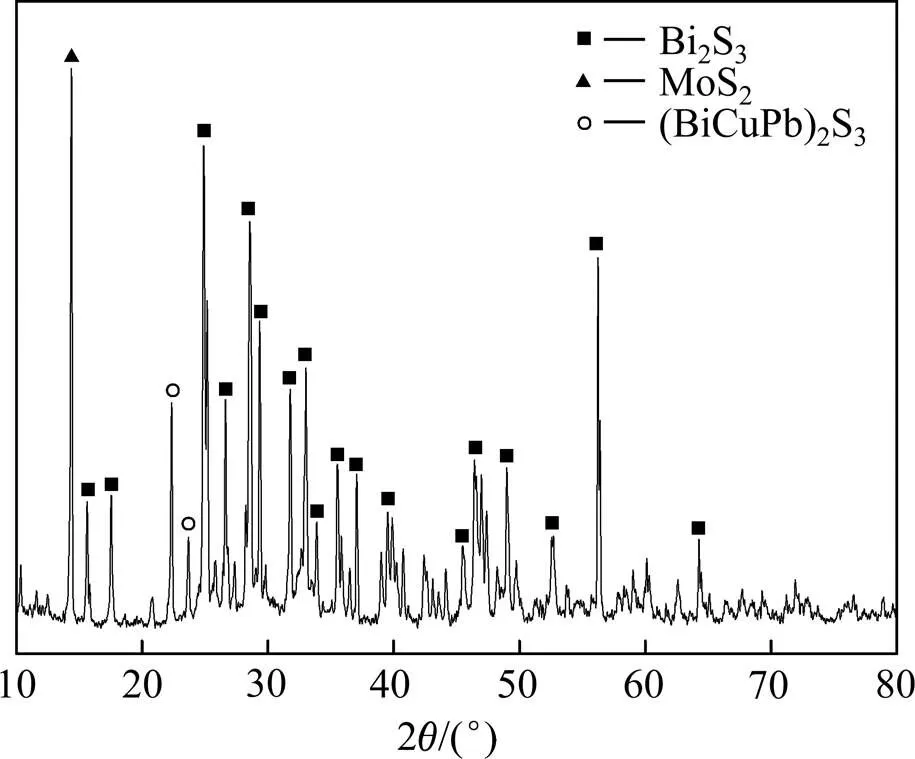
图1 铋精矿的XRD谱
实验所用辅助原料包括磁铁矿、焦粉、添加剂(分析纯碳酸钠)以及分析纯CaO。其中,磁铁矿和焦粉的成分分别如表2和3所示。
1.2 实验方法
本实验中采用单因素条件实验探究高温熔炼中硫化铋精矿还原造锍熔炼工艺的可行性以及其主要工艺条件(包括熔剂用量,熔渣组成,磁铁矿用量,反应温度及反应时间)对该工艺的影响,得出最佳熔炼条件并进行综合条件实验。每次实验称取100 g硫化铋精矿,根据原料及辅助原料中的硫全部与FeO反应生成FeS,并加上以脉石中SiO2含量计算出相应(FeO)/(SiO2)所确定的FeO量,计算磁铁矿的理论加入量,配入相应量的焦粉、添加剂以及CaO后,研磨混匀,装入石墨坩埚(直径()为75 mm;高度()为135 mm),然后放入箱式马弗炉(长沙远东电炉厂提供的1台6 kW三相碳硅棒箱式马弗炉)中。在一定条件下熔炼一定时间后,保温一段时间,然后取出石墨坩埚,放置于室温下急冷,接着将粗铋、铁锍及炉渣分离,并分别取样称取质量、分析。实验原则流程图如图2所示。
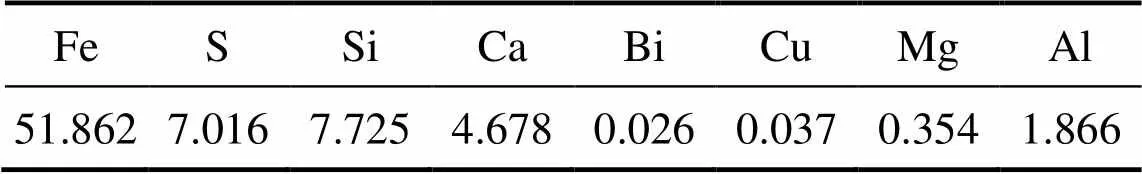
表2 磁铁矿的化学成分

表3 焦粉的化学成分
FeT: Total Fe amount.
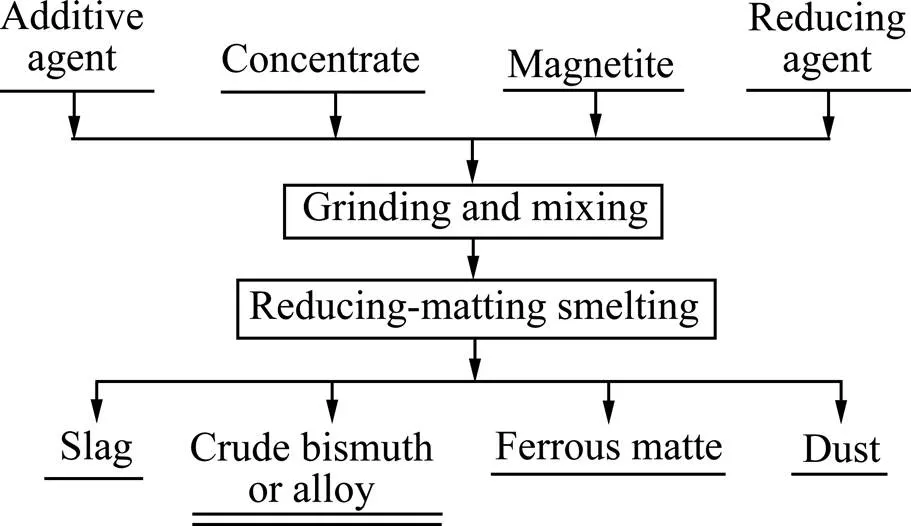
图2 硫化铋精矿还原造锍熔炼原则流程图
2 热力学分析
硫化铋的还原造锍熔炼是在1000~1300 ℃温度时,高价态的造锍剂四氧化三铁被过剩还原剂还原成低价FeO,硫化铋精矿在FeO与还原气氛共存的情况下发生还原造锍反应一步产出粗铋、铁锍及炉渣。主要反应如下:
Fe3O4+C=3FeO+CO(g) (1)
Fe3O4+CO(g)=3FeO+CO2(g) (2)
Bi2S3+3FeO+3C=2Bi+3FeS+3CO(g) (3)
Bi2S3+3FeO+3CO(g)=2Bi+3FeS+3CO2(g) (4)
精矿及辅助原料中的脉石成分与小部分氧化亚铁反应,生成黏度较大、熔点较高的FeO-SiO2-CaO三元渣。由于精矿及磁铁矿中硅含量较高(原料中硅主要以SiO2形式存在,熔炼时渣的黏度随着SiO2含量的增加而上升,使得熔渣流动性变差,不利于主金属的沉淀分离),单纯的调节铁硅比和钙硅比无法达到合适的熔点和黏度,因此需添加少量熔剂Na2CO3。碳酸钠一部分造渣,另一部分会与硫化铋发生还原造锍反应,生成Na2S,可降低炉渣及铁锍的熔点和黏度,其反应式为
Na2CO3+Al2O3+2SiO2=2NaAlSiO4+CO2(g) (5)
2Bi2S3+6Na2CO3+3C=4Bi+6Na2S+9CO2(g) (6)
2Bi2S3+6Na2O+3C=4Bi+6Na2S+3CO2(g) (7)
在高于1000 ℃的温度下主要考虑间接还原反应,即反应(4)的热力学平衡,通过查阅热力学数据手册计算结果如图3所示。从图3可看出,在标准状态下,Bi2S3的还原造锍反应较易发生,可以在较低温度和弱还原性气氛下进行,即使当熔体中Bi2S3浓度低至 1×10−4时,所需平衡的CO含量也不超过24%(质量分数),故控制合适的气氛可以避免FeO的还原。因此,硫化铋精矿的还原造锍熔炼反应在热力学上是可行的,且可以控制金属铁的生成。
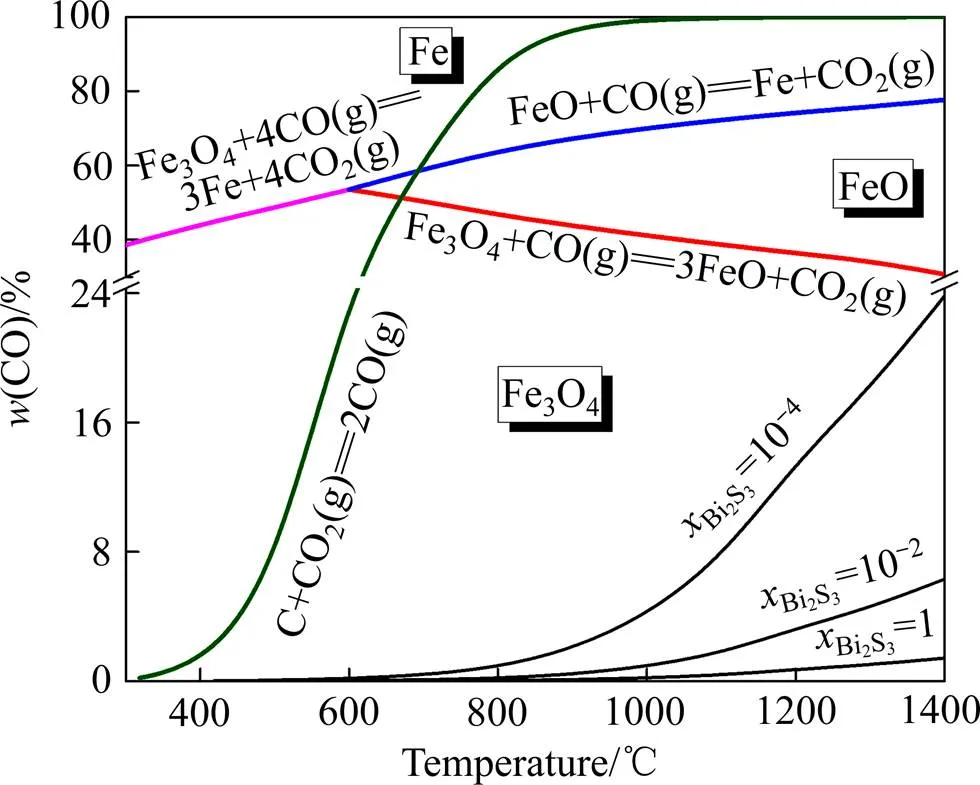
图3 Bi2S3的还原平衡图
3 结果及讨论
3.1 添加剂用量的影响
按铋精矿、磁铁矿、焦粉、CaO的质量比为100:113:10:9配制炉料((FeO)/(SiO2)=1.2,(CaO)/(SiO2)=0.7),在1300 ℃下熔炼1.5 h,改变添加剂碳酸钠的加入量,考察它们对金属铋直收率及渣含铋的影响,实验结果如图4所示。
由图4可知,碳酸钠在20%以内随着其用量的增加,粗铋的直收率先明显上升,在Na2CO3加入量为精矿含量的20%时达到最高值87.82%,超过20%后稍有降低;与铋的直收率相对应,渣含铋则随着苏打用量增加先降低后上升,当Na2CO3加入量达20%时有最低值0.03%,随后上升至较高值0.11%。其主要原因是:添加剂Na2CO3能降低渣的熔点、黏度、增加渣的流动性,同时,还能降低铁锍相的密度和熔点,使粗铋、铁锍、渣三相更好地沉降分离。但当添加剂超过一定量后,会有更多的Na2S生成,与Bi2S3结合成复杂化合物[16],增加还原难度,导致直收率降低,渣含铋升高。另外,纯碱价格昂贵,且熔剂对炉子腐蚀性较强,因此,添加剂Na2CO3最佳加入量为精矿用量的20%。
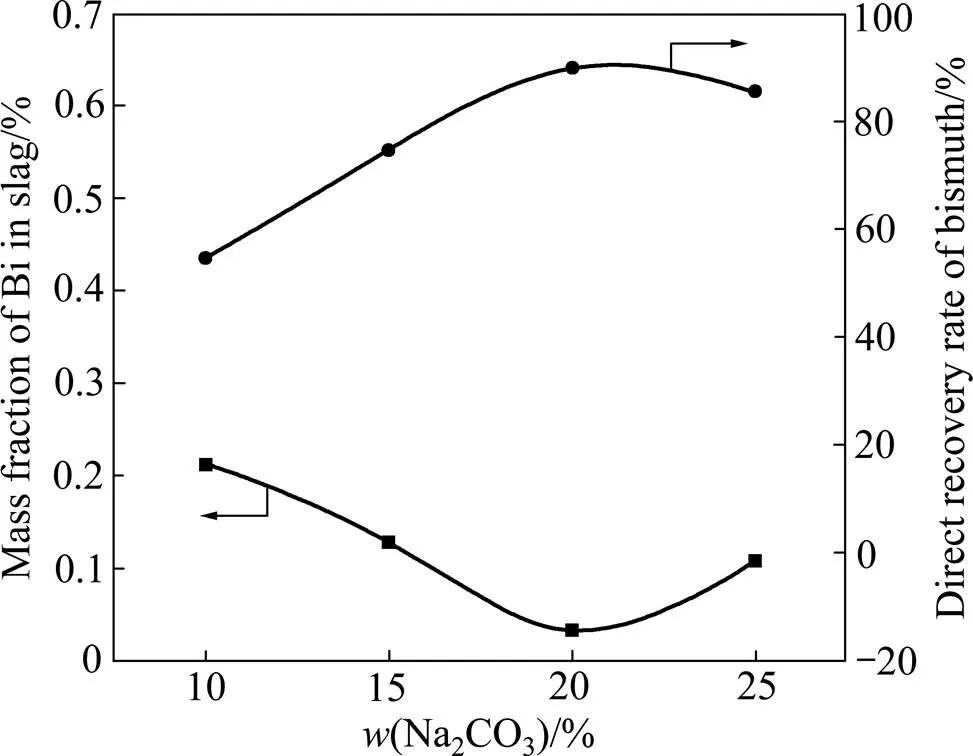
图4 碳酸钠加入量对金属铋直收率和渣含铋的影响
3.2 温度的影响
按铋精矿、磁铁矿、焦粉、苏打、CaO的质量比为100:113:10:20:9配制炉料((FeO)/(SiO2)=1.2,(CaO)/(SiO2)= 0.7),在不同温度下熔炼1.5 h,实验结果如图5所示。
由图5可看出,当温度从1100 ℃提高到1250 ℃时,铋的直收率明显上升,从11.45%升至86.62%,继续升高温度,铋的直收率上升得比较缓慢;而随着温度的提高,渣含铋先急剧下降,从1100 ℃时的2.02%降到1250 ℃时的0.05%,随后随着温度的继续提高变化不大。这是由于升高温度有利于降低黏度,促进流动性,增加金属直收率。但温度过高,硫化铋和铋的挥发都增大,降低金属直收率。综上所述,再考虑到能耗与成本等实际问题,取最佳熔炼温度为1250 ℃。
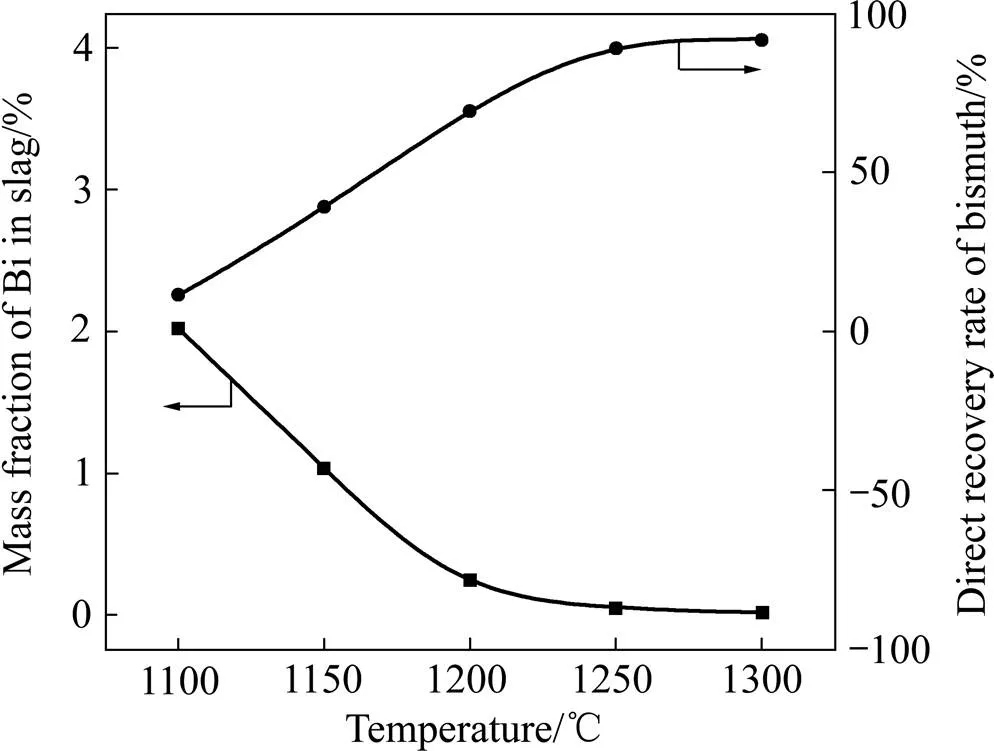
图5 熔炼温度对金属直收率和渣含铋的影响
3.3 FeO与SiO2质量比的影响
按铋精矿、焦粉、苏打的质量比为100:10:20配制炉料,定(CaO)/(SiO2)=0.7,改变磁铁矿和CaO的加入量,分别使(FeO)/(SiO2)=0.6,0.8,1.0,1.2,1.4。在1250 ℃下熔炼1.5 h,验结果如图6所示。

图6 m(FeO)/m(SiO2)对金属直收率和渣含铋的影响
由图6可知,当钙硅比为0.9时,随着铁硅比从0.6~1.4的变化,金属铋的直收率先升高,在铁硅比为1.0时有最高值88.78%;当铁硅比大于1.0后,金属铋的直收率开始降低。而随铁硅比从0.6增加到0.8时,渣中含铋明显降低,从0.32%降至0.03%;当铁硅比从0.8增加到1.2时,渣含铋有一定的波动,但变化不大;当铁硅比从1.2增加到1.4时,渣含铋明显升高,达到较高值0.19%。
结合不同铁硅比时金属铋的直收率及渣中含铋的变化情况,可知当铁硅比较低时,随着氧化铁的增加,使酸性的硅氧阴离子团分解,降低熔渣黏度,增加渣的流动性,使得金属直收率和渣含铋均有较明显的改观;当氧化铁达到一定量后,能置换出和硅氧团结合生成硅酸盐的金属氧化物,使铋的氧化物参与交互反应,增加金属直收率,但也可能增加金属以氧化物的形式入渣或进入烟尘的几率,使得渣含铋有一定的波动;当进一步增加铁的含量时,有可能生成Fe3O4,促使增加渣黏度的泡沫渣产生,也可能生成铁酸盐,增大渣的密度,不利分层。因此,综上得知铁硅比的最优值为1.0。
3.4 CaO与SiO2质量比的影响
按铋精矿、磁铁矿、焦粉、苏打的质量比为100:108:10:20配制炉料,定(FeO)/(SiO2)=1.0,改变CaO的加入量,分别使(CaO)/(SiO2)为0.5、0.7、0.9、1.1、1.3。在1250℃下熔炼1.5 h,实验结果如图7所示。
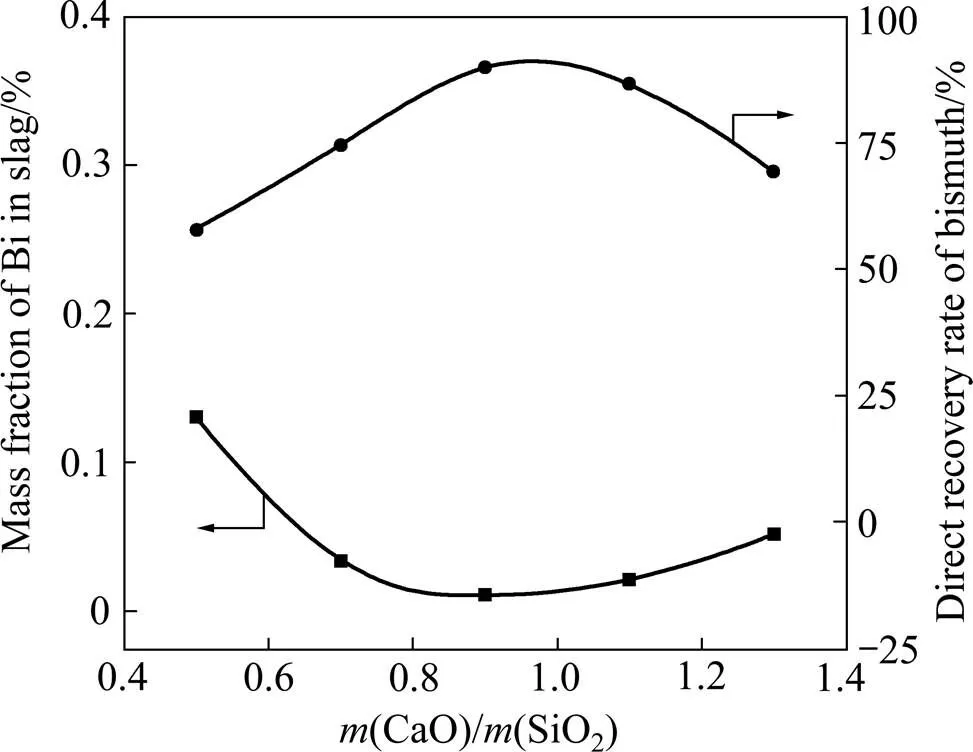
图7 m(CaO)/m(SiO2)对金属直收率和渣含铋的影响
由图7可知,当铁硅比为1.0时,随着钙硅比的增加,金属铋的直收率先明显升高,在钙硅比为0.9时有较高值86.93%;当钙硅比大于0.9后,铋的直收率开始降低。钙硅比为0.5时,渣含铋有较高值0.13%。而随着钙硅比增加,渣中含铋先明显降低,在钙硅比为0.9时达到较低值0.01%,随后缓慢上升至0.05%。
结合不同钙硅比时金属铋的直收率及渣中含铋的变化情况:当钙硅比较低时,FeO含量较高,渣密度较大,溶解金属的能力较大,使得金属铋在渣中的损失较大,加入一定的CaO可破坏熔渣中的硅氧阴离子,降低渣的黏度,促进流动性;当进一步加入适量的CaO,可降低渣的密度、熔点及黏度,有利于金属直收率的提高和降低铋在渣中的溶解;但若加入的CaO过多,则它可能与其他金属氧化物结合生成高熔点化合物,升高渣的熔点和黏度。由此可知,钙硅比的最优值为0.9。
3.5 反应时间的影响
按铋精矿、磁铁矿、焦粉、苏打、CaO的质量比为100:108:10:20:14.6配制炉料((FeO)/(SiO2)=1.0,(CaO)/(SiO2)=0.9),改变熔炼反应的时间,考察其对金属铋的直收率及渣含铋的影响,实验结果如图8所示。
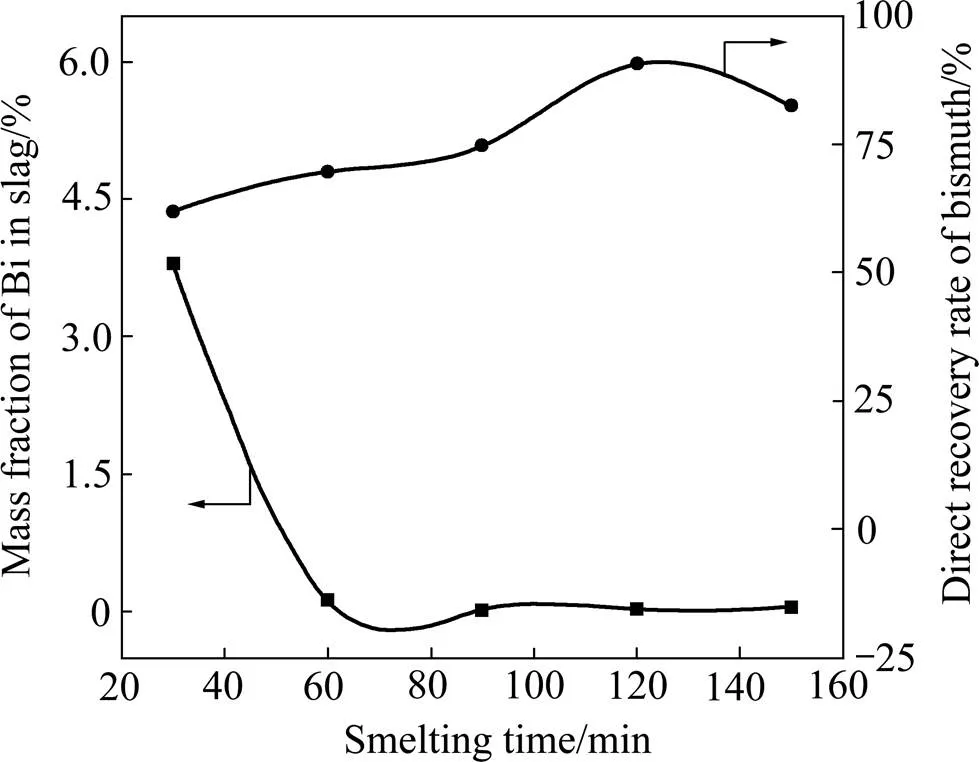
图8 熔炼时间对金属直收率和渣含铋的影响
由图8可知,当反应时间由30 min上升到60 min时,金属直收率变化不大,仅有略微的上升,而渣含铋却明显降低,由很高值3.79%降到0.13%;随着熔炼时间由60 min上升到90 min,铋的直收率缓慢增加,而渣含铋先略微降低,在熔炼时间为75 min时达到一个较小值,随后略微升高至0.02%;当反应时间由90 min上升至150 min时,金属铋的直收率先有较明显的升高,在熔炼时间为120 min时达到最高值87.62%,随后铋的直收率开始缓慢下降。
结合不同反应时间时金属铋的直收率及渣中含铋的变化情况可知,熔炼时间很短时,造锍反应未进行完全或金属氧化物的还原还不够充分,如图中反应时间为30 min时,金属直收率低(61.92%),且渣含铋非常高;随着熔炼时间的延长,有利于还原造锍反应的发生、金属液滴的聚集分相及金属与炉渣的分离,但也可能增加易挥发的金属氧化物入渣或入烟尘的几率,如图中反应时间在60~150 min变化时,金属铋的直收率先升高后下降,而渣中铋含量下降到一定程度后变化不大。综上所述可知,选择熔炼时间在120 min附近较适宜。
3.6 最佳条件综合实验
根据单因素条件实验结果,称取铋精矿200 g,进行最优条件综合实验。主要元素的物料平衡列于表4。
试验共产出金属粗铋47.5 g,由表4可知,熔炼过程中主金属和硫的平衡情况良好:精矿与磁铁矿中的铋大部分进入粗铋,铋的直收率为85.86 %;硫几乎全部固定在铁锍中,不产生SO2烟气污染;另外,铅、钼及银等有价金属的富集效果好,有待精炼中提取。

表4 主要元素的物料平衡情况
冶炼产物分层情况如图9(a)所示,将炉渣和铁锍研磨到0.074 mm以下,分别取样进行XRD分析,其结果如图9(b)和(c)所示。
由图9(a)中的A、B及C可知,反应后的产物渣、铁锍、粗金属分层明显,还原造锍熔炼效果较好。图9(b)表明炉渣的物相成分比较复杂,主要为Ca、Si、Al、F相互结合组成的化合物及SiO2、FeO,这可能是由于精矿及磁铁矿的成分复杂(其中主要原因为硅含量偏高)使得渣量大,成分复杂。另外,渣中有NaAlSiO4生成,说明部分碳酸钠参与了造渣,与热力学分析吻合。由图9(c)可知,大部分硫以FeS的形式固定在铁锍中,经计算FeO的固硫率为98.32%,小部分硫仍以CuS2的形式或以NaCu2S2的形式固定在铁锍中,以便后续铁锍的应用中回收铜和硫。
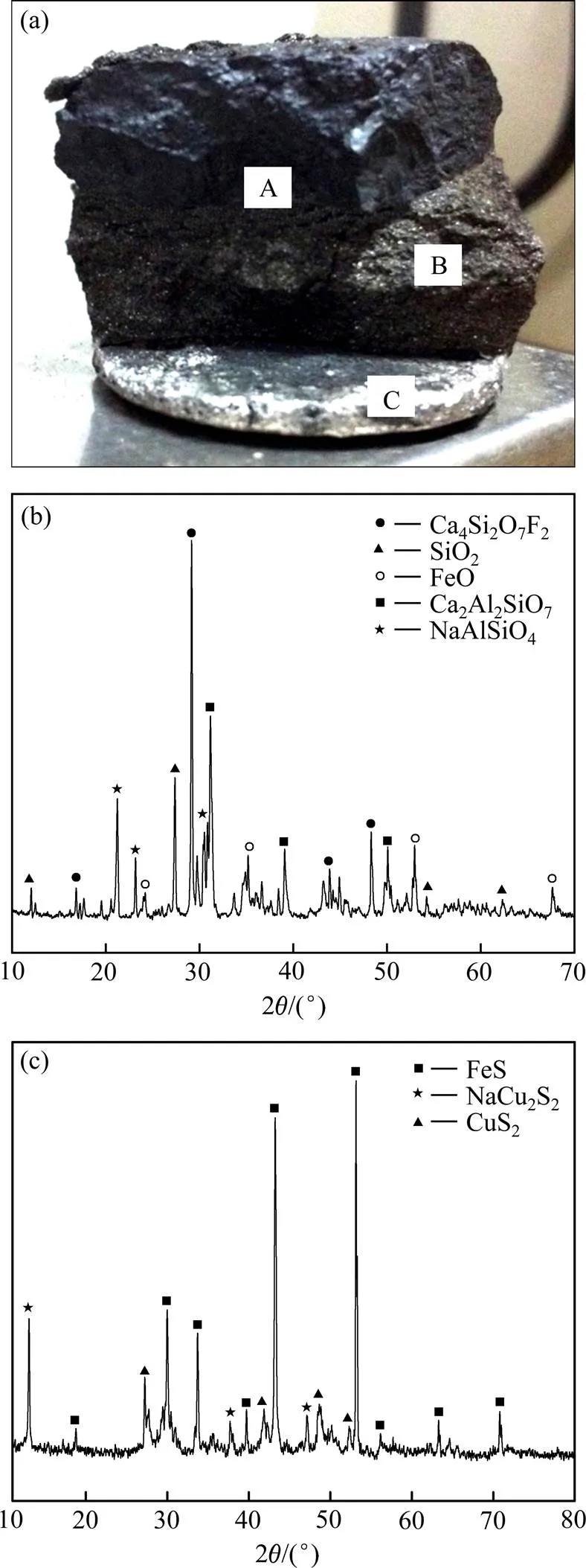
图9 冶炼产物分层照片以及炉渣和铁锍XRD谱
4 结论
1) Bi2S3的还原平衡结果表明,1000~1300 ℃温度下,在有固硫剂及还原气氛下,硫化铋精矿还原造锍熔炼一步产出粗金属、锍及炉渣的反应在热力学上是可行的。
2) 最佳的工艺条件:添加剂碳酸钠用量为20%(质量分数),熔炼温度1300 ℃,(FeO)/(SiO2)= 1.0,(CaO)/(SiO2)=0.9及熔炼时间2 h,此时,铋、铅、钼及银的直收率分别为85.86 %、81.34%、80.95%及79.11%,固硫率达98.32%,基本消除了含硫气体对环境的污染。
3) 粗铋中含铅7%~9%(质量分数),含钼1%~2%(质量分数),含铁5%~7%(质量分数),需进一步火法精炼处理以回收Pb、Mo并除去Fe。
[1] 陈永明, 黄 潮, 唐谟堂, 姚维义, 唐朝波, 皮关华. 硫化锑精矿还原造锍熔炼一步炼锑[J]. 中国有色金属学报, 2006, 15(8): 1311−1316. CHEN Yong-ming. HUANG Chao, TANG Mo-tang, YAO Wei-yi, TANG Chao-bo, PI Guan-hua. Production of antimony by directly reducing-matting smelting of stibnite concentrate[J]. The Chinese Journal of Nonferrous Metals, 2006, 15(8): 1311−1316.
[2] 李 俊. 铋精矿富氧熔池熔炼的工艺及基础研究[D]. 长沙: 中南大学, 2013. LI Jun. Research on the fundamental and process of smelting bismuth concentrate with oxygen in bath[D]. Changsha: Central South University, 2013.
[3] LONG Yang-yang, LI Jian-zhi, TIMMER D H, JONES R E, GONZALEZ M A. Modeling and optimization of the molten salt cleaning process[J]. Journal of Cleaner Production, 2014, 68: 243−251.
[4] 邱定蕃. 清洁高效的提取冶金−矿浆电解[J]. 中国工程科学, 1999(1): 67−72. QIU Ding-fan. Clean and efficient extraction of metallurgy−pulp electrolysis[J]. Chinese Engineering Science, 1999(1): 67−72.
[5] 张杜超. 碱性加压氧化分离硫化铋精矿中钨钼与铋的研究[D]. 长沙: 中南大学, 2012. ZHONG Du-chao. Tungsten and molybdenum separation from bismuth by alkaline pressure oxidation of bismuth sulfide concentrate[D]. Changsha: Central South University, 2012.
[6] CHEN Lin, HAO Zhan-dong, YANG Tian-zu, XIAO Hui, LIU Wei-feng, ZHANG Du-chao, BIN Shu, BIN Wan-da. An efficient technology for smelting low grade bismuth-lead concentrate: Oxygen-rich side blow process[J]. JOM, 2015, 67(9): 1997−2004.
[7] 周晓源, 张自军. 湖南柿竹园铋冶炼改扩建工艺设计[J]. 有色金属, 2007, 59(3): 75−79. ZHOU Xiao-yuan, ZHANG Zi-jun. Process design for reconstruction and expansion of Hunan Shi-zhu-yuan bismuth smelter[J]. Nonferrous Metals, 2007, 59(3): 75−79.
[8] 杨继生, 杨德香. 硫化铋精矿处理新工艺研究[J]. 有色金属(冶炼部分), 2014(11): 9−11. YANG Ji-sheng, YANG De-xiang. New processing to treat bismuth sulfide concentrate[J]. Nonferrous Metals (Metallurgy Section), 2014(11): 9−11.
[9] YE Long-gang, TANG Chao-bo, CHEN Yong-ming, YANG Sheng-hai, YANG Jian-guang, ZHANG Wen-hai. One-step extraction of antimony from low-grade stibnite in Sodium Carbonate–Sodium Chloride binary molten salt[J]. Journal of Cleaner Production, 2015, 93: 134−139.
[10] CHAI Li-yuan, WU Jian-xun, WU Yan-jing, TANG Chao-bo, YANG Wei-chun. Environmental risk assessment on slag and iron-rich matte produced from reducing-matting smelting of lead-bearing wastes and iron-rich wastes[J]. Transactions of Nonferrous Metals Society of China, 2015, 25(10): 3429−3435.
[11] HU Yu-jie, TANG Chao-bo, TANG Mo-tang, CHEN Yong-ming. Reductive smelting of spent lead–acid battery colloid sludge in a molten Na2CO3salt[J]. International Journal of Minerals, Metallurgy, and Materials, 2015, 22(8): 798−803.
[12] 胡宇杰, 唐朝波, 唐谟堂, 陈永明. 再生铅低温碱性固硫熔炼的实验研究[J]. 工程科学学报, 2015, 37(5): 588−594. HU Yu-jie, TANG Chao-bo, TANG Mo-tang, CHEN Yong-ming. Extraction of lead from secondary lead through a low- temperature alkaline and sulfur-fixing smelting process[J]. Journal of Science and Engineering, 2015, 37(5): 588−594.
[13] XIA Ji-yong, TANG Mo-tang, CHEN Cui, JIN Sheng-ming, CHEN Yong-ming. Preparation of-Bi2O3from bismuth powders through low-temperature oxidation[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(9): 2289−2294.
[14] 唐谟堂, 唐朝波, 陈永明, 杨建广, 杨声海, 何 静, 欧 召. 一种很有前途的低碳清洁冶金方法——重金属低温熔盐冶金[J]. 中国有色冶金, 2010, 20(4): 49−53. TANG Mo-tang, TANG Chao-bo, CHEN Yong-ming, YANG Jian-guang, HE Jing, OU Zhao. A promising low carbon clean metallurgical method——Low-temperature molten salt metallurgy of heavy metal[J]. Nonferrous Metallurgical of China, 2010, 20(4): 49−53.
[15] 刘小文, 杨建广, 李 静, 陈永明, 孙亚辉, 唐谟堂. Bi2S3-ZnO-Na2CO3体系热力学分析及应用[J]. 中国有金属学报, 2012, 22(1): 310−314. LIU Xiao-wen, YANG Jian-guang, LI Jing, CHEN Yong-ming, SUN Ya-hui, TANG Mo-tang. Thermodynamic analysis of Bi2S3-ZnO-Na2CO3and its application[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(1): 310−314.
[16] BUBA A D A, AJALA E O, SAMSON D O. Deposition and characterization of Bi2S3for photoelectrochemical solar cell application[J]. Asian Journal of Science and Technology, 2015, 6(2): 1146−1151.
Production of bismuth by directly reducing-matting smelting from bismuth sulfide concentrate
TANG Chao-bo1, LIU Yong1, YE Long-gang1, 2, CHEN Yong-ming1, TANG Mo-tang1, YANG Sheng-hai1
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;2. School of Metallurgy Engineering, Hunan University of Technology, Zhuzhou 412007, China)
In order to solve the shortcomings of bismuth extraction in current bismuth smelters, such as environment pollution of sulfur dioxide, low direct recovery ratio of bismuth and large dosage of additive agent consumption, a direct process of reducing-matting smelting to treat bismuth sulfide concentrate, was proposed. The effects of parameters, including the dosage of additive agent, slag type, smelting temperature and time, on the direct recovery rate of bismuth and the content of bismuth in slag were investigated by single-factor experiments. After that, optimum conditions are obtained as follows: the mass fraction of soda to bismuth concentrate is 20%,(FeO)/(SiO2)=1.0,(CaO)/(SiO2)= 0.9, smelting temperature is 1300 ℃, and reaction time is 120 min, and the direct recovery rate of bismuth can reach up to 85.86%, the content of bismuth in slag is 0.11%, and the sulfur capture capacity is 98.32%. At the meantime, the direct recovery rates of lead, molybdenum and silver are 81.34%, 80.95% and 79.11%, respectively. The proposed process of new technology has good effect for enrichment of valuable metals.
bismuth sulfide concentrate; reducing-matting smelting; clean metallurgy; direct smelting
(编辑 李艳红)
2016-02-24; Accepted date:2016-06-24
TANG Chao-bo; Tel: +86-731-88830470; E-mail: tangchaobo9043@163.com
1004-0609(2017)-02-0363-08
TF817
A
2016-02-24;
2016-06-24
唐朝波,副教授,博士;电话:0731-88830470;E-mail: tangchaobo9043@163.com
