贵金属-非贵金属室温除甲醛催化剂性能研究
2017-03-29杜世睿
王 杰,戴 霖,杜世睿
(厦门宇净环保科技有限公司,福建 厦门 361005)
贵金属-非贵金属室温除甲醛催化剂性能研究
王 杰,戴 霖,杜世睿
(厦门宇净环保科技有限公司,福建 厦门 361005)
以水热法制备CeO2载体,以醇热还原法将贵金属-非贵金属纳米合金颗粒负载于CeO2载体上,获得贵金属-非贵金属纳米合金催化剂。该催化剂在室温下即可将甲醛彻底分解成H2O和CO2,除醛效率可以达到99%,且具有良好的稳定性。
室温除甲醛;贵金属;非贵金属;催化剂
1 引言
甲醛的主要危害表现为对皮肤粘膜的刺激作用,甲醛在室内达到一定浓度时,人就有不适感。大于0.1mg/m3的甲醛浓度可引起眼红、眼痒、咽喉不适或疼痛、声音嘶哑、喷嚏、胸闷、气喘、皮炎等。此外,甲醛还能与空气中的离子性氯化物反应生成二氯甲基醚,而后者是一种致癌物质。家具和室内装饰材料释放的甲醛,会造成严重的室内空气污染,危害人体健康。因此,如何有效去除甲醛以改善室内空气质量已成为人们关注的焦点[1]。
目前,用于消除甲醛的主要技术是采用活性炭作为吸附剂,此种方法较为简单,但净化周期长,且活性炭需要定期更换。较为理想的甲醛消除方法是催化氧化技术,该法是在催化剂的催化作用下,利用空气将甲醛催化氧化为对人类完全无害的H2O和CO2。催化氧化消除甲醛技术的关键在于成本低且低温(最好是室温)高效稳定的催化剂的研发。能在室温条件下较为有效消除甲醛的催化剂多为贵金属催化剂,如纳米立方体CeO2负载的Pd(1wt%)催化剂能在室温和空速为10,000h-1条件下有效脱除甲醛(浓度:600ppm)[2]。与常规浸渍法相比,沉积-沉淀法制备且经甲醛溶液预还原的Pt/TiO2催化剂具有良好的甲醛脱除性能,即使Pt的负载量低至0.4%和在室温条件下,连续测定100h内,仍能稳定有效的脱除甲醛,但该催化剂仅适用于脱除低浓度的甲醛(50ppb)[3]。0.1%Pt/TiO2催化剂在水蒸汽(湿度30%)存在条件下,在室温下可完全脱除污染浓度为22ppm的甲醛,但在干燥条件下,完全脱除同样量甲醛的Pt的负载量要高达1%[4]。低成本(低贵金属用量)、室温高效且持久有效的甲醛消除催化剂仍是当前研发的热点和难点。
本文以水热法制备CeO2载体,以醇热还原法将贵金属-非贵金属纳米合金颗粒负载于CeO2载体上,获得贵金属-非贵金属纳米合金催化剂,以其获得一种成本低、性能高的室温除甲醛催化剂,为实用性室内甲醛净化催化剂的研究提供参考。
2 实验部分
2.1 实验主要仪器与试剂
电热套(ZNHW-II,上海玛尼仪器设备有限公司);马弗炉(SX2-2.5-12N,浙江赛德仪器设备有限公司);氢气还原炉(HB-In30·60,咸阳蓝光热工科技有限公司)气相色谱仪(GC-2060,北京金洋万达科技有限公司);NiCl2·6H2O(AR,上海国药集团);CoCl2·6H2O(AR,上海国药集团);H2PtCl6·6H2O(AR,上海思域化工);Fe S O4·4 H2O(A R,上海国药集团);Ce(NO3)3·6H2O(AR,上海国药集团)。
2.2 催化剂的性能评价
催化剂甲醛去除率测试,在固定床流动相反应器中进行,称取0.100g催化剂装于石英管反应器(直径0.8 cm,长度45cm)中,通过控温仪来控制反应温度,反应温度设定25℃。气态甲醛由压缩空气吹扫置于恒温器的多聚甲醛产生,气体总流量50mL/min,湿度50%±10%,压强101.325kPa。采用气相色谱分析方法检测反应气体中的甲醛的浓度,通过分析反应前后甲醛的浓度计算出甲醛去除率。评价流程示意图见图1。
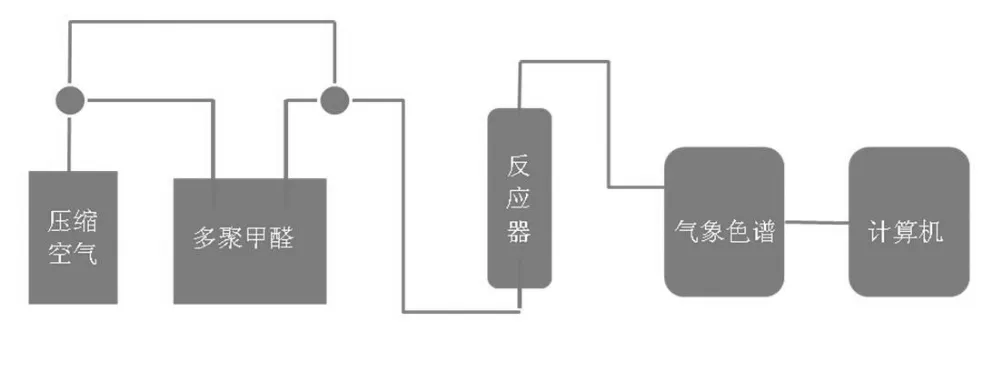
图1 催化剂评价装置示意图
2.3 样品制备
2.3.1 CeO2载体制备
将6g的Ce(NO3)3·6H2O溶于40mL去离子水中后加入水热反应釜并搅拌,逐滴加入10%NaOH将溶液,pH调至12,超声30min后,将水热反应釜于100oC恒温18h,降至室温,过滤、洗涤,干燥后在马弗炉中400oC焙烧4h制得CeO2载体。
2.3.2 催化剂制备
称取1g所制备的CeO2载体置于250mL的圆底烧瓶中,加入100mL丙三醇,超声60min后,加入0.16gFeSO4·4H2O和2.08mLRuCl3溶液(1mg/mL)并通入N2进行保护,1h后用1mol/L的NaOH调节混合液pH值至13,然后于150oC恒温4h,降至室温后,用HCl调节混合液pH值至1.5,室温搅拌12h后,洗涤、过滤、干燥,最后于N2气氛中400oC焙烧4 h制得Ru0.1Fe4.0/CeO2催化剂。
将步骤2.3.2中的RuCl3溶液换做2.64mL、1mg/mL的H2PtCl6·6H2O溶液,其余条件相同,制得Pt0.1Fe4.0/CeO2催化剂。
将步骤2.3.2中的RuCl3溶液换做2.56mL、1mg/mL的RhCl3·3H2O溶液,其余条件相同,制得Rh0.1Fe4.0/CeO2催化剂。
将步骤2.3.2中的RuCl3溶液换做1.68mL、1mg/mL的PdCl2溶液,其余条件相同,制得Pd0.1Fe4.0/CeO2催化剂。
将步骤2.3.2中的FeSO4·4H2O换做0.1624g的NiCl2·6H2O,将RuCl3溶液换做2.64mL、1mg/mL的H2PtCl6·6H2O溶液,其余条件相同,制得Pt0.1Ni4.0/CeO2催化剂。
将步骤2.3.2中的FeSO4·4H2O换做0.1624g的CoCl2·6H2O,将RuCl3溶液换做2.64mL、1mg/mL的H2PtCl6·6H2O溶液,其余条件相同,制得Pt0.1Co4.0/CeO2催化剂。
将步骤2.3.2中的FeSO4·4H2O换做0.1044g的CuCl2·2H2O,将RuCl3溶液换做2.64mL、1mg/mL的H2PtCl6·6H2O溶液,其余条件相同,制得Pt0.1Cu4.0/CeO2催化剂。
2.3.3 催化剂还原
将2.3.2中制备的催化剂置于还原炉中,350oC下用氢气预还原1h,升温速率为10℃/min,还原结束后自然冷却。
3 结果与讨论
3.1 不同贵金属纳米合金催化剂的甲醛催化脱除性能
表1展示了以CeO2为载体,Fe参杂不同贵金属合金催化剂的除醛性能,可以看出,Ru、Pt、Rh、Pd四种贵金属催化剂均表现出非常高的除醛效果,且二氧化碳选择性均可以达到100%,证明反应无有害副产物产生。其中贵金属Pt催化剂除醛效果相对最好。

表1 不同贵金属纳米合金催化剂的甲醛催化脱除性能*
3.2 不同非贵金属掺杂纳米合金催化剂的甲醛催化脱除性能
表2展示了以CeO2为载体、贵金属Pt为主要活性成分,Ni、Co、Cu掺杂后的催化剂的甲醛脱除性能,可看出不同非贵金属掺杂后的催化剂均具有较高的除醛效果,二氧化碳选择性均可以达到100%。

表2 不同非贵金属掺杂纳米合金催化剂的甲醛催化脱除性能*
3.3 催化剂稳定性能测试
通过催化剂长时间、高浓度的催化作用,以验证其催化效果的稳定性,图2展示了Pt0.1Co4.0/CeO2催化剂在连续测试120h后除醛效率仍可维持在98%以上,说明该催化剂具有很高的稳定性。

图2 Pt0.1Co4.0/CeO2催化剂甲醛催化脱除性能稳定性测试
4 结论
以水热法制备CeO2载体,以醇热还原法将贵金属-非贵金属纳米合金颗粒负载于CeO2载体上,获得贵金属-非贵金属纳米合金催化剂,该方法制备催化剂中贵金属含量低至0.1%,室温可将甲醛彻底分解成无毒的H2O和CO2,且性能稳定,连续高浓度下作用120h后仍能维持原有的除醛效率,因此具有非常好的应用前景。
[1] 陈莹,贺军辉,田华,等.涂覆在堇青石上的负载贵金属催化剂催化氧化甲醛的性能研究[J].化学通报,2015,78(3)231-235.
[2] Hongyi Tan,Jin Wang,Shuzhen Yu,and Kebin Zhou*,Support Morphology-Dependent Catalytic Activity of Pd/CeO2for Formaldehyde Oxidation. Environmental Science&Technology,2015, 49(14),8675-8682.
[3] HuayaoChen, ZebaoRu, HongbingJia. Titania-supported Pt catalyst reduced with HCHO for HCHO oxidation under mild conditions.Chinese Journal of Catalysis,2015,36(2),188-196.
[4] DongWookKwon,PhilWonSeo, GeoJongKim,SungChangHong. Characteristics of the HCHO oxidation reaction over Pt/TiO2catalystsat room temperature: The effect of relative humidity on catalyticactivity.Applied Catalysis B: Environmental,2015,163,436-443.
Formaldehyde Catalysts Removal of Noble Metal-Non-Noble Metal at Room Temperature
WANG Jie, DAI Lin, DU Shi-rui
(Xiamen Yujing Environmental Technology Co., Ltd, Fujian Xiamen 361005, China)
By taking the hydrothermal method to prepare CeO2carrier and by taking alcohol-thermal reduction method to load noble metal-non-noble metal nano alloy particles on CeO2carrier, in order to obtain the nano alloy catalyst of noble metal-non-noble metal. The result shows that the catalyst can completely decompose formaldehyde into H2O and CO2at room temperature. It is worth to mention that the efficiency of formaldehyde removal can reach 99% and has a favorable stability.
formaldehyde removal at room temperature; noble metal; non-noble metal; catalyst
X512
A
1006-5377(2017)03-0047-03
