Hi5-SF悬浮细胞系的建立及鉴定
2017-03-23王家敏马桂兰乔自林马忠仁冯玉萍
马 伟,王家敏,马桂兰,马 祺,马 花,乔自林,马忠仁,冯玉萍
(1.西北民族大学 甘肃省动物细胞工程技术研究中心,兰州 730030;2.兰州百灵生物技术有限公司,兰州 730010;3.西北民族大学 生物工程与技术国家民委重点实验室,兰州 730030)
Hi5-SF悬浮细胞系的建立及鉴定
马 伟1,王家敏1,马桂兰2,马 祺2,马 花1,乔自林1,马忠仁3,冯玉萍3
(1.西北民族大学 甘肃省动物细胞工程技术研究中心,兰州 730030;2.兰州百灵生物技术有限公司,兰州 730010;3.西北民族大学 生物工程与技术国家民委重点实验室,兰州 730030)
从中国典型培养物保藏中心(CCTCC)引进High Five细胞并对其进行驯化,获得无血清悬浮驯化株(Hi5-SF)。依据《中华人民共和国药典(2010年版三部)》对其进行细胞生物学特性研究、微生物污染、病毒外源因子及细胞致瘤性检测。结果发现,Hi5-SF细胞复苏活力76.3%,生长曲线呈“S”型,最大增殖密度可达3.50×106mL-1,群体倍增时间为26.2 h;细菌、真菌及支原体检查均为阴性;血细胞吸附试验、致细胞病变试验和特异性病毒荧光抗体结合物检查结果均为阴性;致瘤性检查结果也为阴性。说明该细胞株符合兽用疫苗生产用细胞质量要求,可以在疫苗研究与生产中应用。
High five细胞;悬浮培养;质量评价
粉纹夜蛾(Trichoplusiani)卵巢细胞株BTI-TN-5B1-4是20世纪90年代Robert R和李国勋等从粉纹夜蛾卵巢细胞系BTI-TN-5B1克隆得到的新型宿主细胞,Invitrogen公司注册商标为High Five细胞[1-2]。西北民族大学甘肃省动物细胞工程技术研究中心的High Five细胞引自中国典型培养物保藏中心(CCTCC),为淋巴母细胞样形态,半贴壁生长,培养液为Grace’s Insect Medium(含φ=10%的FBS)。High Five细胞对多种病毒敏感并能支持外源基因高效表达,尤其具有较高的多角体病毒增殖能力和重组蛋白表达水平,是当前应用昆虫杆状病毒表达载体系统(Baculovirus expression vector system,BEVS)生产病毒样颗粒(Virus-like particles,VLPs)疫苗的主要细胞系[3-5]。该细胞可在HyQ SFX-Insect、EX-CELLTM405和Express FiveTMSFM等培养基中无血清悬浮培养,然而上述进口培养基价格昂贵,实际生产中并不适用。贴壁生长的High Five细胞需要进行较长时间的悬浮适应培养才能够在上述商品化无血清培养基正常生长,即使已经适应在某种培养基中悬浮生长,当更换培养基时,细胞仍需要3~5代的适应培养方可正常生长[3]。High Five细胞的高密度无血清悬浮培养在疫苗研究和生产上具有重要意义。本研究利用兰州百灵生物技术有限公司开发的BFLM502 SFM培养基对引进的High Five细胞(CCTCC株)进行无血清悬浮驯化,获得可无血清悬浮生长的Hi5-SF细胞株,并对其进行细胞生物学特性研究和质量检测,以评价该悬浮细胞株用于动物疫苗研究和生产的可能性。
1 材料与方法
1.1 材 料
High Five细胞(CCTCC);新生牛血清(NBS,兰州民海)、胰蛋白酶液(Gibco)及无血清培养基(SFLM502 SFM,兰州百灵);无菌检查与支原体检查培养基(北京三药科技)、Heochst33258(Sigma);脑心肌炎病毒VR-739株、牛腺病毒3型WBR-1株、牛腺病毒5型、牛细小病毒Haden株、牛副流感病毒3型SB株和呼肠孤病毒Abney株(ATCC)以及牛病毒性腹泻病毒Oregon C24V株(中国兽医药品监察所);脑心肌炎病毒、牛腺病毒3型、牛腺病毒5型、牛细小病毒、牛副流感病毒3型、呼肠孤病毒和牛病毒性腹泻病毒荧光抗体结合物(VMRD);Vero细胞、MRC-5细胞、ST细胞、牛肾原代细胞和Hela细胞均为甘肃省动物细胞工程技术研究中心保存;SPF级BALB/c Nude 裸鼠(北京维通利华)等。
3111型CO2培养箱(Thermo)、CKX41型倒置相差显微镜、IX71型荧光倒置差相显微镜(Olympus)、ZHWY-2102C型恒温培养振荡器(上海智城),等。
1.2 方 法
1.2.1 High Five细胞悬浮驯化 选取状态良好的High Five贴壁细胞,在细胞培养瓶中扩增培养,培养液为BFLM502(含φ=10%的NBS)。待细胞铺满单层后用吸管轻轻吹打,收集细胞悬液离心,用新鲜培养液悬浮以50×104mL-1接种到三角摇瓶中,27 ℃、60 r/min悬浮培养,至细胞密度达100×104mL-1以上时离心并收集细胞,按1∶2传代并提高转速至80 r/min,同法至转速提高为120 r/min,稳定传3代后冻存,并命名为Hi5-S。
1.2.2 High Five悬浮细胞无血清驯化 将悬浮驯化后的Hi5-S细胞,采用逐步降血清法进行无血清培养驯化。血清由φ=10%逐步降至φ=5%、φ=3%、φ=1.5%和φ=0%。无血清稳定培养5代后建库冻存,并命名为Hi5-SF[6],冻存液为BFLM502(φ=70%)+NBS(φ=20%)+DMSO(φ=10%)。
1.2.3 Hi5-SF细胞鉴定 复苏及活力检查:采用常规方法于27 ℃水浴复苏细胞,在10 mL BFLM502培养基中悬浮细胞后1 000 r/min离心10 min,换新鲜BFLM502培养基悬浮培养,同时抽样,台盼蓝染色检测复苏活力[7]。细胞培养过程中不定时进行显微观察并采集图像。
生长特性:取状态良好的Hi5-SF细胞,台盼蓝染色计数,以活细胞密度50×104mL-1接种细胞于三角瓶中,培养体积40 mL,平行3组。27 ℃、120 r/min悬浮培养,每24 h取样1 mL 计数,直至活细胞密度降低,绘制细胞生长曲线并求出细胞最大增殖密度和倍增时间[8]。
微生物污染检查和病毒检查:按照《中华人民共和国药典(2010年版三部)》进行[9]。
致瘤性检查:按照《中华人民共和国药典(2010年版三部)》进行检查。阳性对照组为5×106mL-1的Hela细胞悬液,阴性对照组为5×107mL-1的MRC-5细胞悬液,待检组为5×107mL-1的Hi5-SF细胞悬液,注射剂量为每只0.2 mL,每组10 只裸鼠。每3~4 d观察测量肿瘤大小并称体质量[9]。试验在甘肃中医学院实验动物中心进行。
2 结果与分析
2.1 复苏及活力检查
含血清培养的Hi5-S细胞冻存前活力为88.5%,平均复苏活力为80.5%;无血清驯化的Hi5-SF细胞冻存前活力为87.8%,平均复苏活力76.3%。与冻存前活力相比复苏活力均有所下降,表明冻存过程对细胞有一定损伤,细胞复苏后72~96 h可1∶4传代扩增培养。
2.2 形态学观察及生长特性
2.2.1 形态学观察 High Five细胞(CCTCC株)未悬浮驯化前,细胞半贴壁生长,贴附的细胞多呈不规则多角形,为淋巴母细胞样;经无血清悬浮驯化后的悬浮细胞株Hi5-SF细胞为圆球状,大小均一,边缘光滑、明亮(图1)。
2.2.2 生长特性 Hi5-SF悬浮细胞以50×104mL-1活细胞密度接种时生长潜伏期较短,接种第2~3 d为明显的指数生长期,第4 天进入稳定期,之后细胞活力下降,活细胞密度开始降低。生长曲线为较典型的“S”型(图2),最大增殖密度为3.50×106mL-1,群体倍增时间为26.2 h。
2.3 微生物污染检查
Hi5-SF细胞经过培养和显微观察未发现细菌和真菌污染。支原体DNA染色法结果显示,阳性对照细胞的细胞核呈蓝色荧光,核外出现蓝色荧光颗粒和丝状点(图3-a);阴性对照只有细胞核呈蓝色荧光,核外无蓝色荧光颗粒(图3-b);待检细胞的细胞核发出蓝色荧光,核周围无蓝色荧光颗粒(图3-c),结果与阴性对照相同,说明待检细胞没有发生支原体污染。
2.4 病毒外源因子检查
细胞培养观察和血细胞吸附试验结果显示,细胞形态正常且无吸附血细胞现象。细胞裂解液接种到Vero、MRC-5和牛肾原代细胞上培养观察和血凝试验结果显示,3种细胞均形态正常,血凝试验和致细胞病变试验结果均为阴性。

a.High Five细胞的φ=10% NBS培养,72 h High Five cell culture with NBS(φ=10%),72 h;b.Hi5-SF细胞无血清培养,24 h Hi5-SF cell serum-free culture,24 h
图1 High Five细胞和Hi5-SF细胞形态
Fig.1 Morphology of High Five cell and Hi5-SF cell
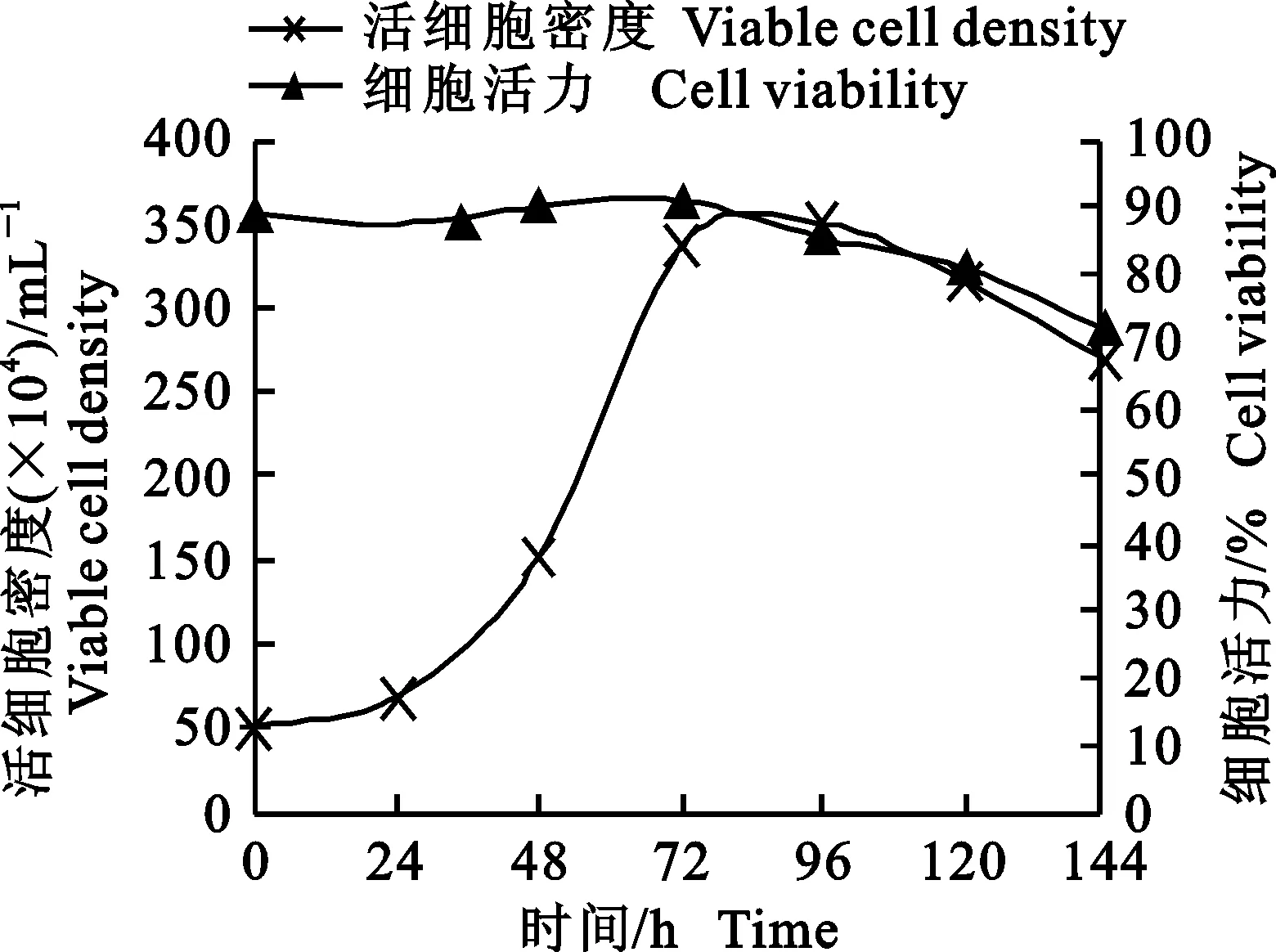
图2 Hi5-SF细胞生长曲线Fig.2 Growth curve of Hi5-SF cell
特异性病毒荧光抗体结合物检查试验中,阳性对照结果(图4-A)显示,牛肾原代细胞上接种牛腺病毒3型(BAV-3)和牛腺病毒5型(BAV-5),其细胞核呈现出较强的黄绿色荧光,细胞质也着色较淡且呈弥散装(图4-a,4-b);接种牛腹泻病毒(BVDV)后细胞质呈黄绿色荧光(图4-c);接种牛细小病毒(BPV)后细胞核呈强黄绿色荧光,细胞质几乎不着色(图4-f);接种牛副流感病毒3型(PI-3)的细胞体呈黄绿色荧光,胞体中有着色较轻的球形斑(图4-g);接种呼肠孤病毒(REO)后细胞质呈强黄绿色荧光,胞质胞浆呈弥漫性淡黄绿色荧光(图4-h)。在ST细胞上接种猪细小病毒(PPV)后细胞核呈明亮的黄绿色荧光(图4-k)。阴性对照中(图4-B),牛肾原代细胞和ST细胞均未呈现荧光。试验组(图4-C)结果显示,Hi5-SF细胞冻融裂解后的上清液接种到牛肾原代细胞和ST细胞中均未呈现荧光,与阴性对照一致,表明细胞未受外源病毒污染。

a.阳性对照 Positive control; b.阴性对照 Negative control;c.Hi5-SF细胞待检样 The sample of Hi5-SF cell
2.5 致瘤性检查
致瘤性试验结果显示(图5),注射后第1周阳性对照组和阴性对照组均出现大小不一的肿瘤,第2周开始均减小并消失,待检组裸鼠第2周肿瘤减小,但未消失。阳性对照组2周后开始成瘤且肿瘤逐渐增大,成瘤率100%(10/10)(图5-A);阴性对照组2周后肿瘤全部消失,成瘤率0%(0/10)(图5-B);待检组2周后肿瘤增大,第40 天时全部消失,解剖未见转移瘤形成,表明Hi5-SF悬浮细胞不致瘤。

A.阳性对照 Positive control; B.阴性对照 Negative control; C.试验组 Sample group
a.BAV-3; b.BAV-5; c.BVDV; d.BAV-3; e.BAV-3; f.BPV g.PI-3; h.REO; i.BPV; j.BPV; k.:PPV; l.PPV; m.PPV
图4 特异性病毒荧光抗体结合物检查
Fig.4 Virus-specific fluorescent antibody conjugate test

A.阳性对照 Positive control; B.阴性对照 Negative control;C.试验组 Sample group
3 讨论与结论
细胞作为疫苗生产的基质,其质量直接影响疫苗的质量和安全性,1株细胞用于生产前必须进行全面的生物学鉴定和质量评价[10]。鉴别的方法包括观察法(如显微观察)、生物化学法(如同工酶试验)、免疫学检测法(如组织相容性抗原)、细胞遗传学检测(如染色体核型)、分子生物学检测法(如DNA指纹图谱)等,评价内容包括细胞种属鉴别、生长特征、微生物污染、内源和外源病毒因子检查等,用于人用疫苗生产的细胞株还要进行活细胞的成瘤性、细胞碎片和细胞DNA的致癌性检查,有时还需进行均一性及传代稳定性检查。
High Five细胞为半贴壁生长细胞,较容易驯化成悬浮细胞。驯化好的Hi5-SF细胞在26~28 ℃、120 r/min悬浮培养,细胞可稳定生长。刚适应无血清培养的细胞形态大小不均,细胞个体增大,并且容易结团,传代稳定后细胞缩小且大小均一,表面圆滑,结团现象也消失。无血清悬浮培养的细胞由于缺少血清保护,以及摇晃过程中剪切力对细胞的损伤,细胞活力不是很稳定,一般情况细胞活力在85% 以上都是可接受的。增加冻存液中血清的含量能够降低冻存过程对细胞的损伤。无血清培养的Hi5-SF细胞增殖速度快,50×104mL-1接种72 h平均可达到3.0×106mL-1左右。
本研究获得的Hi5-SF悬浮细胞来源历史清楚,生长状态良好,生长曲线呈典型的“S”型,最大增殖密度为3.50×106mL-1,指数生长期倍增时间为26.2 h。细胞没有被细菌、真菌和支原体等微生物污染。通过内源和外源病毒因子检查排除致细胞病变和致红细胞吸附病毒的污染可能。通过特异性荧光抗体结合物排除驯化前传代培养过程中使用牛血清和胰蛋白酶可能造成的病毒污染,致瘤性检查试验排除细胞的致瘤性,表明用该细胞株进行兽用疫苗研究是安全的。
Reference:
[1] 李国勋.粉纹夜蛾(Trichoplusiani)卵巢细胞系克隆株Tn5B1-4特性的研究[J].东北农学院学报,1993,24(4):328-332.
LI G X.Characterization of clonal strain Tn5B1-4 fromTrichoplusianiovary cell line Tn5B1[J].JournalofNortheastAgriculturalCollege,1993,24(4):328-332(in Chinese with English abstract).
[2] GRANADOS R R,LI G X,DERKSEN A C G,etal.A new insect cell line fromTrichoplusiani(BTI-Tn-5B1-4) susceptible toTrichoplusianisingle enveloped nuclear polyhedrosis virus[J].JournalofInvertebratePathology,1994,64(3):260-266.
[3] RHIEL M,MITHCHELL-LOGEAN C M,MURHAMMER D W.Comparison ofTrichoplusianiBTI-Tn-5B1-4 (high five) andSpodopterafrugiperdaSf-9 insect cell line metabolism in suspension cultures[J].BiotechnologyandBioengineering,1997,55(6):909-920.
[4] SUGIURA T,AMANN E.Properties of two insect cell lines useful for the baculovirus expression system in serum-free culture[J].BiotechnologyandBioengineering,1996,51(4):494-499.
[5] BOGLI N C,RIES C,ADAMS T,etal.Large-scale,insect-cell-based vaccine development[J].BioProcessInternationalAwards,2012,10(S5):40-49.
[6] 戴 琥,赵 佼,谭文松,等.无血清培养昆虫细胞 (BTI-Tn-5B1-4) 的适应过程[J].生物工程学报,2000,16(2):232-234.
DAI H,ZHAO J,TAN W S,etal.Adaptation of insect cells(BTI-Tn-5B1-4) to serum-free culture[J].ChineseJournalofBiotechnology,2000,16(2):232-234(in Chinese with English abstract).
[7] 乔自林,冯若飞,李明生,等.欧拉羊胎儿皮肤细胞的培养、保存与鉴定[J].西北农业学报,2012,21(12):7-10.
QIAO Z L,FENG R F,LI M SH,etal.Culturing,preservation and identification of Oula sheep embryo skin cells[J].ActaAgriculturaeBoreali-occidentalisSinica,2012,21(12):7-10(in Chinese with English abstract).
[8] 王家敏,平 玲,沈武玲,等.MDCK细胞库的建立及其生物学特性研究[J].山西农业科学,2013,40(12):1231-1234,1261.
WANG J M,PING L,SHEN W L,etal.Study on the establishment and biological characteristics of MDCK cells bank[J].JournalofShanxiAgriculturalSciences,2013,40(12):1231-1234,1261(in Chinese with English abstract).
[9] 国家药典委员会.中华人民共和国药典(2010年版三部)[M].北京:中国医药科技出版社,2010.
PHARMACOPOEIA COMMISSION OF PEOPLE’S REPUBLIC OF CHINA.Pharmacopoeia of the People's Republic of China(2010 Edition Volume Ⅲ)[M].Beijing:China Medical Science Press,2010 (in Chinese).
[10] 吴雪伶,冯建平,樊金萍,等.流感疫苗生产用新型细胞基质MDCK细胞的质量控制研究[J].中华微生物学和免疫学杂志,2013,33(12):943-949.
WU X L,FENG J P,FAN J P,etal.Study on quality control of MDCK cells used for the production of influenza vaccine[J].ChineseJournalofMicrobiologyandImmunology,2013,33(12):943-949(in Chinese with English abstract).
(责任编辑:顾玉兰 Responsible editor:GU Yulan)
Establishment and Identification of Hi5-SF Suspension Cell Line
MA Wei1,WANG Jiamin1,MA Guilan2,MA Qi2,MA Hua1,QIAO Zilin1,MA Zhongren3and FENG Yuping3
(1.Gansu Engineering Research Center for Animal Cell,Northwest University for Nationalities,Lanzhou 730030,China; 2.Lanzhou Bailing Bio-Tech CO.,LTD.,Lanzhou 730010,China;3.Key Laboratory of Bioengineering and Biotechnology of the State Ethnic Affairs Commission,Northwest University for Nationalities,Lanzhou 730030,China)
High Five cells were introduced from CCTCC and domestecated,,and we obtained semi-adherent cells to suspension growth cell line (Hi5-SF).Subsequently,the biological characteristics,microbial contamination,viral exogenous factors and tumorigenicity of Hi5-SF cell line were detected according to the Pharmacopoeia of People’s Republic of China (3rd Edition,2010).The results showed that the recovery vitality of Hi5-SF cells was 76.3%,the growth curve was S-shape,and maximum concentration was 3.50×106cells·mL-1with the population doubling time(PDT) of 26.2 h.The cells were free of bacteria,fungi and mycoplasmas;hemadsorption test,cytopathic test,specific virus fluorescent antibody binding test and tumorigenicity test were all negative.The resultus indicated that the Hi5-SF cell line meets the quality requirements of veterinary vaccine production.
High five cell; Suspension culture; Quality evaluation
MA Wei,male,master student.Research area:cell culture,the research and development of veterinary biological products.E-mail:670267497@qq.com
FENG Yuping,female,Ph.D,professor.Research area:development and utilization of biotechnology materials.E-mail:119236672@qq.com
日期:2016-12-29
网络出版地址:http://www.cnki.net/kcms/detail/61.1220.S.20161229.1005.006.html
2016-01-11
2016-03-27
教育部“长江学者和创新团队发展计划” (IRT13091);甘肃省科技计划(144FKCA082);西北民族大学中央高校基本科研业务费专项资金(31920150029,zyp2015006)。
马 伟,男,硕士研究生,从事细胞培养、兽用生物制品的开发研究。E-mail:670267497@qq.com
冯玉萍,女,博士,教授,主要从事生物技术材料的开发利用研究。E-mail:119236672 @qq.com
S85
A
1004-1389(2017)02-0173-06
Received 2016-01-11 Returned 2016-03-27
Foundation item The Pogram for Changjiang Scholars and Innovative Team of Ministry of Education(No.IRT13091); Science and Technology Project of Gansu Province (No.144FKCA082); the Project Fundamental Research Funds for the Central Universities of Northwest University For Nationalities (No.31920150029,No.zyp2015006).
