定量思想在复习过程中的渗透
2017-03-21江波
江波
中图分类号:G633.8 文献标识码:B 文章编号:1672-1578(2016)12-0293-01
化学是一门以实验为基础的学科,物质间发生化学变化是化学的核心。在化学变化过程中,若参加反应的物质之间量发生改变,会导致生成物的质量甚至生成物的种类和性质也发生改变,同时该反应产生的反应热也随之改变。而高考的考试说明也明确了对将化学问题抽象成数学问题,利用数学工具通过计算(结合化学知识)解决问题的能力的考查。历年高考化学试题的定量(或半定量)计算都给予了应有的重视,涉及的题目占整个题数的一半以上。因此,在指导学生复习物质的性质及物质间的化学反应时,引导学生建立化学中的定量思想,把握一个化学反应中反应物之间量的关系,正确分析和判断该反应进行的程度和实质,对培养学生的思维能力、分析问题和解决问题的能力大有帮助。
1.把握"少量"、"适量"、"足量"、"过量"、"一定量"等词语的含义,正确理解反应物间量的关系对反应进行程度的影响
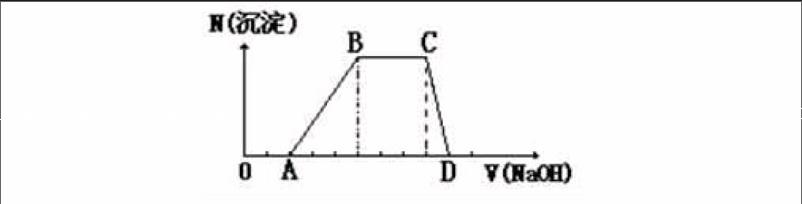
例1 将2molNaHCO3和一定量的Na2O2固体混合,在加热条件下使其充分反应,经测定无Na2O2剩余,设最后所得固体的物质的量为xmol,则( )
A.1
解析:"一定量"的Na2O2可理解为Na2O2极少量,少量(①不足以与NaHCO3分解的CO2完全反应;②恰好与NaHCO3分解的CO2完全反应;③能使CO2反应完全,但不足以使H2O反应完全),足量(恰好与CO2、H2O反应完全)等情况,因此所得固体可能是①Na2CO3,②Na2CO3和NaOH的混合物。解答此题可用极值法,若无Na2O2固体时,2mol NaHCO3受热分解生成1mol Na2CO3;若Na2O2恰好与NaHCO3分解生成的CO2和H2O完全反应,则又可生成1mol Na2CO3和2molNaOH,即固体最多可以为4mol,即1 答案C。 2.正确把握反应物的浓度、反应物间量的关系对生成物种类和性质的影响 例2 将一定量的锌与100mL18.5mol/L浓H2SO4充分反应后,锌完全溶解,同时生成气体A33.6L(标准状况),将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol/L,则下列叙述中错误的是( ) A.气体A为SO2和H2的混合物 B.反应中共消耗锌97.5g C.反应中共转移电子3mol D.气体A中SO2和H2的体积比为4﹕1 解析: 此题考察金属与硫酸反应时,硫酸的浓度对反应的类型和反应产物的影响。开始时浓H2SO4与Zn发生反应Zn+2H2SO4(浓)=ZnSO4+SO2↑+2H2O,随着反应的进行,H2SO4的浓度变稀,当反应进行到一定程度时,又发生Zn+2H2SO4(稀) =ZnSO4+H2↑,故A中含有SO2和H2两种成分。 n(Zn)=n(SO2)+n(H2)= 3.6L/22.4L·mol-=1.5mol ,n(e_)=2n(Zn)=3mol 2n(SO2)+n(H2)+0.5n(H+)=n(H2SO4)=1.85mol ∴n(SO2)=0.3mol n(H2)=1.2mol 即V(SO2)﹕V(H2)=1﹕4 答案C。 例3 (1)在10mL1.0mol/L的純碱溶液中,不断搅拌并逐滴加入12mL0.5mol/L的盐酸,完全反应后在标准状况下生成CO2的体积为_____mL。 (2)在12ml0.5mol/L的盐酸中,不断搅拌并逐滴加入10mL1.0mol/L的纯碱溶液,完全反应后在标准状况生成CO2的体积为_____mL。 解析:此题属Na2CO3与HCl反应时,反应过程及生成物受到Na2CO3和HCl的相对量的不同的影响。 (1)当向Na2CO3溶液滴入HCl时,①当n(HCl)/n(Na2CO3)≤1时,发生反应为 Na2CO3+HCl=NaHCO3+NaCl,n(CO2)=0;②当1 (2)当向HCl溶液滴入Na2CO3时,①当n(HCl)/n(Na2CO3)≥2时,发生反应:Na2CO3 + 2HCl=2NaCl+H2O+CO2↑,n(CO2)=n(Na2CO3);②当n(HCl)/n(Na2CO3) <2时,NaHCO3过量,n(CO2)=0.5n(HCl) 答案:(1)0;(2)67.2。 3.正确理解题目所给的图象(或表格)中所列点、面、曲线数据的意义 借助图形,图式和线路中的点、线、面之间的关联来分析化学反应原理和化学反应中各物质的量的关系,化抽象为直观。 例4 某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是______,且各离子的物质的量之比为________;肯定不含的阳离子是________,若溶液中也不含有Na+,则C(SO42-)﹕C(H+)=______。 解析:根据图象分析加NaOH产生沉淀并且沉淀最后完全溶解的离子只可能是Al3+离子,不含Mg2+、Fe3+离子,在0→A段加NaOH无现象,B→C段沉淀的量没有发生变化,引起这种变化的只可能是H+、NH4+两种离子,而这些离子与NaOH反应的先后顺序为H+、Al3+、NH4+,然后是生成的Al(OH)3再与NaOH反应,即C→D段,因此含有的阳离子为H+、Al3+、NH4+,根据电荷守恒,必定含有SO42-离子,在条件中发生的反应有: ①H++OH-=H2O(OA段) ②Al3++3OH-=Al(OH)3↓(AB段) ③NH4++OH-=NH3·H2O,(BC段) ④Al(OH)3+OH=AlO2-+2H2O(CD段) 由①②③消耗的NaOH知H+、Al3+、NH4+三种离子的物质的量之比为2﹕1﹕3,若溶液中也不含有Na+,由电荷守恒知溶液中阴阳离子存在2c(SO42-)=c(H+)+c(NH4+)+3c(Al3+)关系,令H+、Al3+、NH4+ 三种离子的浓度分别为2mol/L、1mol/L、3mol/L,此时SO42-的浓度为4mol/L,由此C(SO42-)﹕C(H+)=2﹕1。 答案:H+、Al3+、NH4-+,2﹕1﹕3,Mg、Fe2+,2﹕1 体会并熟练掌握化学变化中的守恒规律的应用,通过质量守恒、得失电子守恒、离子所带电荷守恒等规律找出各物质之间量的关系,从而使化学计算更简捷快速。如例2中的
