布洛芬甲硝唑酯的合成路线设计及工艺优化
2017-03-20杨俊杰
潘 岩,陈 重,刘 琰,陈 琼,杨俊杰
(信阳农林学院生物与制药工程学院,河南信阳464000)
甲硝唑(Metronidazole,化学名:2-甲基-5-硝基咪唑-1-乙醇,1)为硝基咪唑类化合物,临床上用于治疗厌氧菌感染性疾病[1]。布洛芬(Ibuprofen,化学名:α-甲基-4-(2-甲基丙基)苯乙酸,2)是一种经典的非甾体抗炎药,表现出解热、镇痛、消炎作用,在临床上广泛应用[2]。二者配合,联合用药,临床上用于治疗由厌氧菌感染引起的各种疼痛,如厌氧菌感染引起的牙痛。布洛芬、甲硝唑联合给药具有很好的抗菌、消炎效果,但不可避免的是布洛芬和甲硝唑都会产生胃肠道反应,引起患者不适[3]。本文根据前药和挛药设计原理,设计新化合物布洛芬甲硝唑酯(4)。该化合物为布洛芬和甲硝唑缩合所得的酯类药物,首先它一种生物体前药,经代谢释放出具有活性的布洛芬和甲硝唑,不但减小了胃肠道反应,而且延长了药物作用时间;其次,它也是一种挛药,在体内代谢产生的布洛芬和甲硝唑,可发挥协同作用,增强药效。
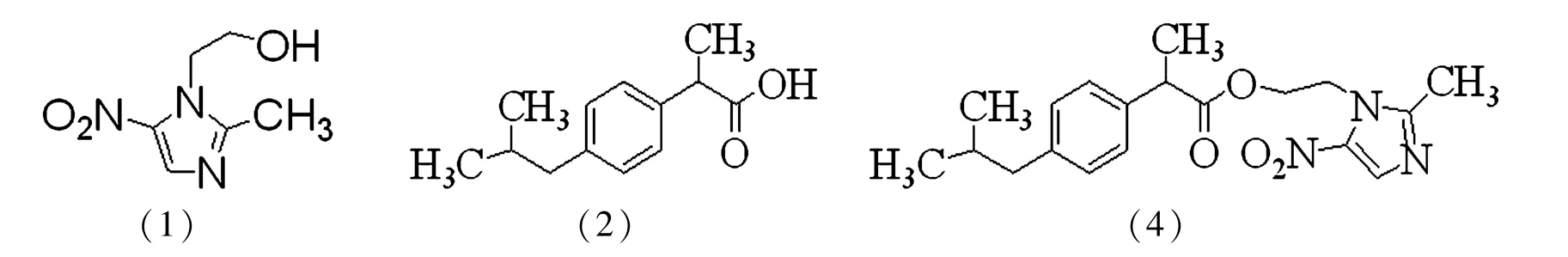
1 布洛芬甲硝唑酯(4)的合成方法
笔者设计了两条合成路线,并选择了一条经济、绿色、易行的合成路线对布洛芬甲硝唑酯进行制备。布洛芬甲硝唑酯相对分子质量为359,结构式为:
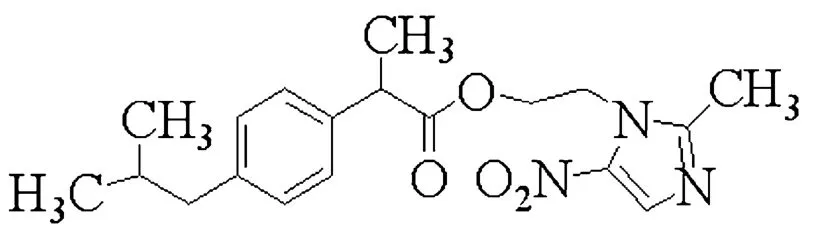
路线一
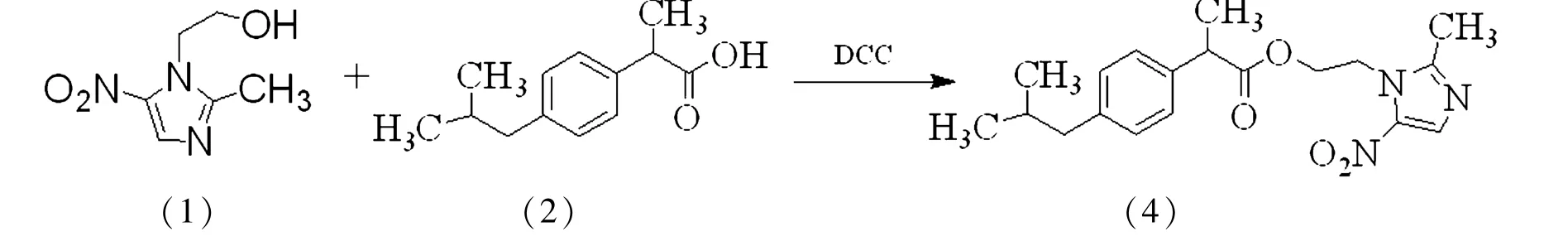
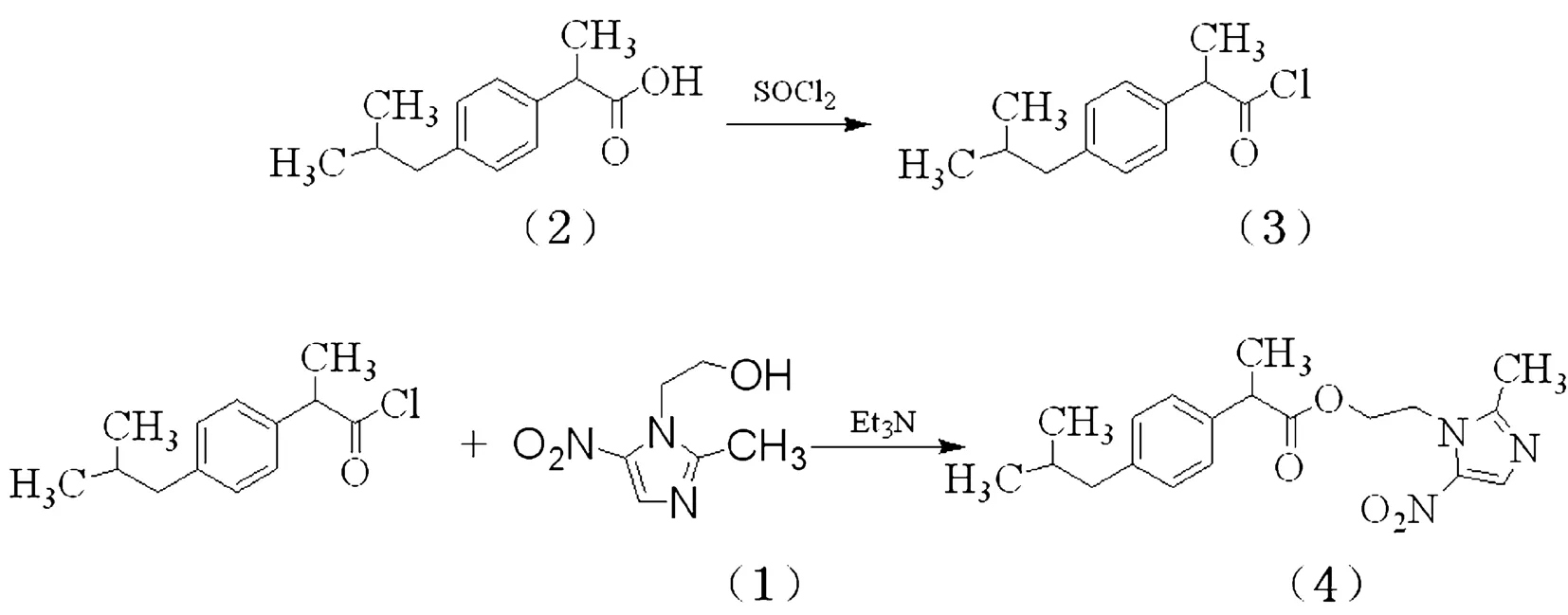
路线二
路线一,二环己基碳亚胺(DCC)脱水法:原料1和原料2在DCC催化下,一步合成布洛芬甲硝唑酯。总产率为52.0%。
路线二,氯化、酰化法:原料2和氯化亚砜(SOCl2)发生氯化反应,得到中间体3(α-甲基-4-(2- 甲基丙基)苯酰氯),中间体3在有机碱三乙胺存在下,与原料1反应生成目标产物4。总产率为72.9%。
比较而知:路线一,原料DCC昂贵,不易得;路线二,所需原料廉价易得,操作简单,产率较高。故选择路线二对布洛芬甲硝唑酯(4)进行制备,并考察了反应中物料配比、反应温度、有机碱种类对反应的影响。
2 实验部分
2.1 实验仪器和试剂
仪器:高效液相色谱:安捷伦液相色谱仪1200;液质联用色谱:Agilent1100-LC-MSD-Trap-SL;
试剂:氯化亚砜(山东茂发化工有限公司);二氯甲烷(AR);三乙胺(济南鑫博化工有限公司);二环己基碳亚胺(广州洛品化工有限公司)。
2.2 实验步骤
2.2.1 α-甲基-4-(2-甲基丙基)苯乙酰氯(3)的合成 在装置有温度计、球形冷凝管、加料漏斗的500ml三颈瓶中,加入 20.6g(0.1mol)布洛芬和 200ml二氯甲烷,搅拌溶解,室温下缓慢滴加 12.0g (0.12mol)氯化亚砜,30min滴毕,水浴升温至二氯甲烷回流,继续反应2h。TLC监测,反应全后,40℃减压旋蒸去溶剂,得淡黄色油状残余物(3)22.0g。
2.2.2 布洛芬甲硝唑酯的(4)的合成 将13.7g(0.08mol)甲硝唑溶于20ml无水二氯甲烷中备用。在装置有低温温度计、球形冷凝管、加料漏斗的500ml三颈瓶中加入上步所得油状残余物(3)、200ml无水二氯甲烷,搅拌溶解。低温冷却至-10℃,缓慢滴加甲硝唑的二氯甲烷溶液,控制滴加温度-10~ -5℃,40min滴毕,继续-10 ~ -5℃低温反应1h。TLC监测,反应完全后,加入100ml水,搅拌10min。继续加入稀盐酸(0.1mol/L),调节 pH≈7,静置分层,弃水相,得有机相。 水洗有机相(50ml×3),静置分离,得二氯甲烷层,无水硫酸镁干燥,过滤去除干燥剂后,旋蒸去溶剂,得淡黄色固体25.9g,加入甲醇:水(1:1)混合溶剂100ml进行重结晶,得白色固体(4)22.8g,m.p.180.5 ~181.3℃;LC/MC[M +1] +m/Z(%):360;HPLC 99.6%。
3 结果与讨论
3.1 中间体(3)的合成
用布洛芬(2)和过量的氯化亚砜反应,考察了物料比对反应的影响。其结果见表1。
由表1 可知,n(2):n(SO2Cl) =1:1.2 时,产率最高。
3.2 布洛芬甲硝唑酯(4)的合成
目标产物(4)的合成中,主要考察了反应温度和碱的种类对反应的影响。其结果见表2。
由表2可知,将反应温度降低至-15~ -10℃,产率未见增大,且延长了反应时间;将反应温度升至-5℃以上,副产物增加,故最佳反应温度为-10~ -5℃。

表1 二氯亚砜用量的影响
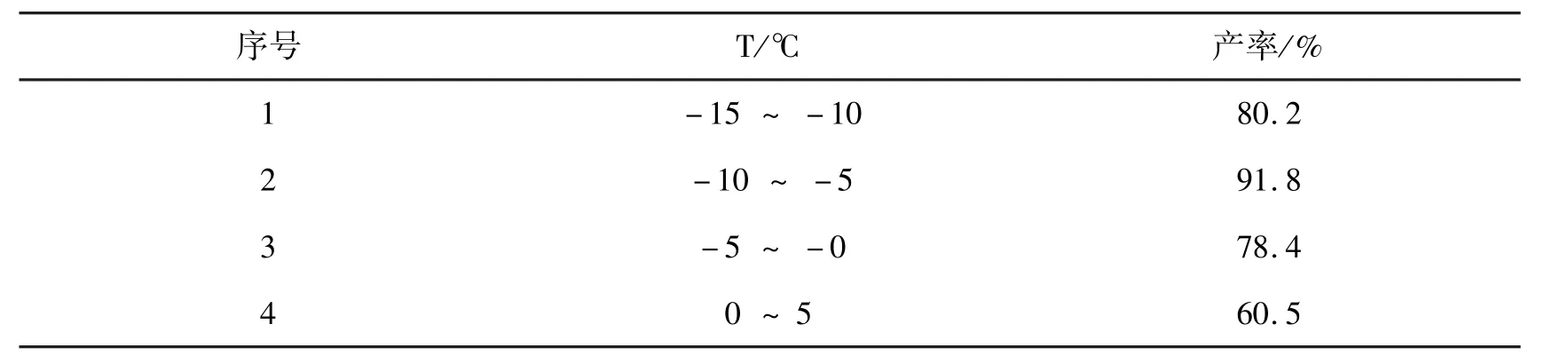
表2 温度的影响
碱的种类对反应的影响,其结果如表3:
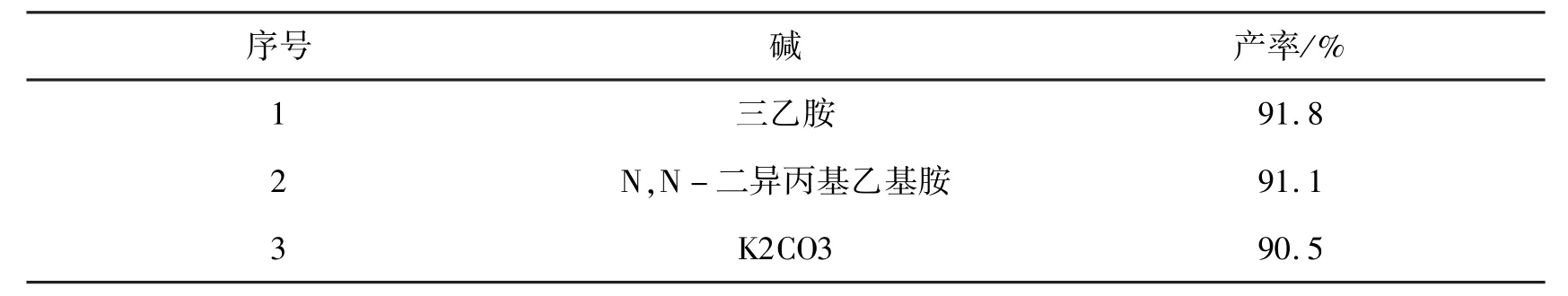
表3 碱的影响
由表3可知,不同的碱作为缚酸剂对产率影响不大,故选择收率较高、廉价易得的三乙胺为缚酸剂。
4 结束语
布洛芬甲硝唑酯具有很好的市场前景,以甲硝唑、布洛芬为起始原料经过氯化、酰化、重结晶得到了目标化合物。通过考察氯化亚砜用量、反应温度、碱的种类对反应收率的影响,确定了最佳反应条件:氯化亚砜与布洛芬摩尔比为1.2:1;布洛芬甲硝唑酯(4)合成的反应温度-5~-10℃;三乙胺作为碱。反应的总收率可达72.9%,目标化合物的纯度达到了99.6%。
[1] 陈新谦,金有豫,汤 光.新编药物学[M].16 版.北京:人民卫生出版社,2007:110 -111.
[2] 张 娇.布洛芬的临床研究进展[J].中国药业,2010,19(5):63.
[3] 路长飞,田月洁,谢彦军,等.布洛芬口服制剂致不良反应/事件监测数据分析[J].2013,32(10):618 -620.
