瓣环组织运动位移评价扩张型心肌病左室纵向收缩功能
2017-03-18李春梅李文华
王 珊,李春梅△,孔 洪,李文华
1.四川省医学科学院·四川省人民医院 心血管超声及心功能科(成都 610072);2. 四川省医学科学院·四川省人民医院 心内科(成都 610072)
瓣环组织运动位移评价扩张型心肌病左室纵向收缩功能
王 珊1,李春梅1△,孔 洪2,李文华1
1.四川省医学科学院·四川省人民医院 心血管超声及心功能科(成都 610072);2. 四川省医学科学院·四川省人民医院 心内科(成都 610072)
目的 探讨二尖瓣环、主动脉瓣环组织运动位移评价扩张型心肌病患者左室纵向收缩功能的临床应用价值。方法 选取2013年07月至2014年12月在四川省人民医院心内科入院治疗的扩张型心肌病患者共38例,正常对照组46例,均实施常规经胸超声心动图检查,采集并储存左室心尖四腔、三腔、二腔心切面3个完整心动周期实时灰阶超声图像。采用Q-Lab图像工作站测量二尖瓣环后室间隔、侧壁及二者瓣环连线中点最大位移,二尖瓣环前室间隔、后壁及二者瓣环连线中点最大位移,二尖瓣环前壁、下壁及二者瓣环连线中点最大位移,主动脉瓣环无冠瓣、右冠瓣及二者瓣环连线中点最大位移,应用双平面Simpson’s法计算左室射血分数(left ventricular ejection fraction,LVEF),分析扩张型心肌病患者和正常对照组二尖瓣环、主动脉瓣环位移变化,及其与左室LVEF值之间的关系。结果 1)扩张型心肌病组较正常对照组二尖瓣环后室间隔、侧壁及二者瓣环连线中点最大位移,二尖瓣环前室间隔、后壁及二者瓣环连线中点最大位移,二尖瓣环前壁、下壁及二者瓣环连线中点最大位移,主动脉瓣环无冠瓣、右冠瓣及二者瓣环连线中点最大位移及左室LVEF值均明显降低,差异有统计学意义(P<0.01)。2)正常对照组中,二尖瓣环所有位点位移、主动脉瓣环右冠瓣位移及右冠瓣和无冠瓣连线中点位移与左室LVEF值呈明显正相关(P<0.01);主动脉瓣环无冠瓣位移与左室LVEF值呈正相关(P<0.05)。扩张型心肌病组中,大多数二尖瓣环位移和主动脉瓣环位移与左室LVEF值呈正相关(P<0.05),仅二尖瓣环后壁、前室间隔、主动脉瓣无冠瓣位移与左室LVEF值无相关性(P>0.05)。结论 二尖瓣环、主动脉瓣环组织运动位移能够快速、客观反映扩张型心肌病患者左室心肌纵向收缩功能,可成为超声评价左室纵向收缩功能的一种新方法。
扩张型心肌病;位移;瓣环;左室收缩功能
随着心血管超声诊断技术不断进步,超声心动图评价心肌功能变化的敏感性和可靠性明显提高,提供了更加丰富的反映心肌收缩功能的力学信息。近年来,瓣环组织运动位移自动追踪技术是基于二维斑点瓣环运动追踪显像,无角度依赖性,充分考虑到左室心腔大小、径向运动对心肌有效做功产生的影响,能够快速、客观、较准确地反映左室心肌纵向收缩功能[1]。扩张型心肌病(dilated cardiomyopathy,DCM)是最常见的原发心肌疾病之一,主要表现为左室或双侧心室扩大,心肌收缩及舒张功能障碍,心脏排血量降低,出现心力衰竭、心律失常等,严重可导致患者猝死。本研究主要采用瓣环组织运动位移技术观察DCM患者二尖瓣环位移(mitrial annular displacement,MAD)和主动脉瓣环位移(aortic annular displacement,AAD)的变化特征,为超声评价左室心肌纵向收缩功能提供更加简单、可行的方法。
1 资料与方法
1.1 临床资料
选取2013年07月至2014年12月在四川省人民医院心内科入院治疗DCM患者共38例,设为DCM 组,其中,男32例,女6例,年龄40~65(52.78±7.57)岁,所有患者均经检查,排除严重的肝肾疾病、糖尿病、瓣膜性心脏病、缺血性心肌病、冠心病、心包疾病等。正常对照组:选择健康志愿者46例,其中,男37例,女 9例,年龄44~60(50.25±4.22)岁。所有入选对象均经询问病史、心电图、超声心动图、实验室检查无明显异常,排除冠心病、高血压、瓣膜性心脏病、心律失常、糖尿病性心脏病等心血管疾病。
1.2 仪器与方法
1.2.1 仪器 采用Philips iE Elite 彩色超声诊断仪,探头型号X5-1,探头频率1.3~3.8 MHz。Q-Lab 9.1超声图像分析工作站。
1.2.2 图像采集 超声心动图检查室温度适宜,安静,受检者左侧卧位,平静呼吸,同步记录心电图。常规超声心动图检查,测量经胸骨旁左室长轴切面舒张末期左室内径(left ventricular end-diastolic diameter,LVEDd)、舒张末期左室后壁厚度(left ventricular posterior wall end-diastolic thickness,LVPWd)、舒张末期室间隔厚度(interventricular septal end-diastolic thickness,IVSd)、左室长轴切面收缩末期左室内径(left ventricular end-systolic diameter,LVEDs)、收缩末期左室后壁厚度(left ventricular posterior wall end-systolic thickness,LVPWs)、收缩末期室间隔厚度(interventricular septal end-systolic thickness,IVSs);采用双平面Simpson’s法测量左室射血分数(left ventricular ejection fraction,LVEF)。让受检者尽量屏气,采集左室心尖二腔、三腔、二腔心切面二维超声心动图,获取3个连续心动周期并保存。
1.2.3 图像分析 将经胸二维超声心动图左室心尖四腔、三腔、二腔心切面图像导入Q-Lab 9.1图像分析工作站,选择心脏运动定量分析模式。左室心尖四腔心切面二尖瓣环后室间隔和侧壁放置两点、左室心尖三腔心切面二尖瓣环前间隔和后壁放置两点、左室心尖二腔心切面二尖瓣环前壁和下壁放置两点、左室心尖三腔心切面主动脉瓣环无冠瓣和右冠瓣放置两点,以上图像第3个取样分析点均放置在左室心尖心内膜面,分析软件自动跟踪MAD及AAD,以上数据均测量3个心动周期,取均值。
1.2.4 重复性检验 由另1名超声心动图诊断医师从受检组中随机选取20例,按照上述方法再次测量MAD、AAD参数,记录数据并分析。
1.3 统计学方法
2 结果
2.1 DCM组与正常对照组常规超声心动图参数比较
DCM组较正常对照组,LVEDd、LVEDs均明显增大,LVEF值明显降低,差异有统计学意义(P<0.01)(表1)。
2.2 DCM组与正常对照组MAD、AAD参数比较
DCM组较正常对照组二尖瓣环后室间隔、侧壁及二者连线中点最大位移(4 chamber-middle,4C-mid),二尖瓣环前室间隔、后壁及二者瓣环连线中点最大位移(3 chamber-middle,3C-mid),二尖瓣环前壁、下壁及二者瓣环连线中点最大位移(2 chamber-middle,2C-mid),主动脉瓣环无冠瓣、右冠瓣及二者瓣环连线中点最大位移(aortic annular-middle,AV-mid)均明显降低,差异有统计学意义(P<0.01)(图1、表2)。
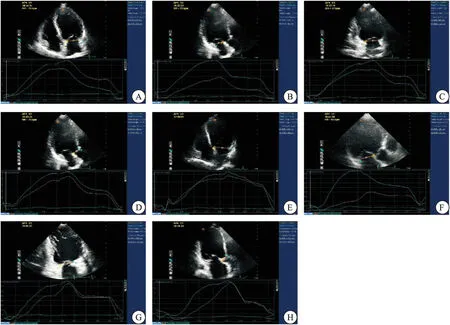
图1 正常组与DCM组MAD、AAD运动曲线比较
表2 DCM组与正常对照组MAD、AAD参数比较
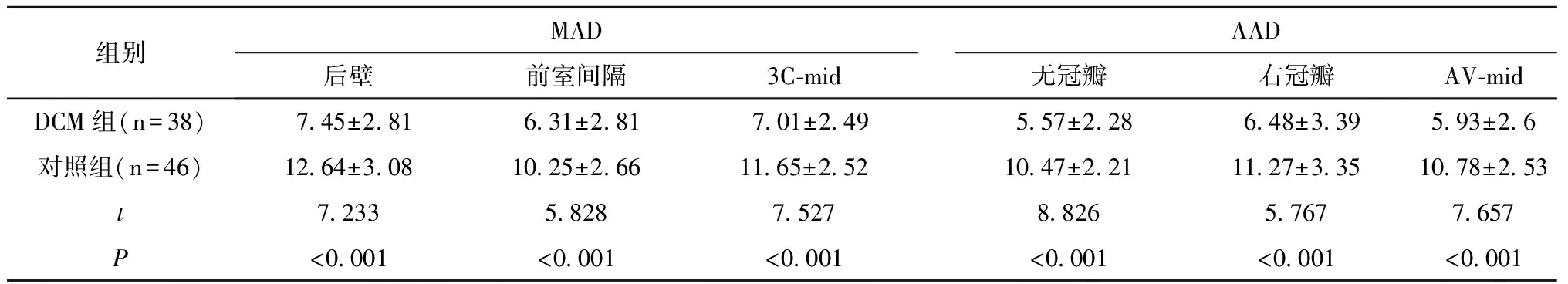
组别MADAAD后壁前室间隔3C⁃mid无冠瓣右冠瓣AV⁃midDCM组(n=38)7 45±2 816 31±2 817 01±2 495 57±2 286 48±3 395 93±2 6对照组(n=46)12 64±3 0810 25±2 6611 65±2 5210 47±2 2111 27±3 3510 78±2 53t7 2335 8287 5278 8265 7677 657P<0 001<0 001<0 001<0 001<0 001<0 001
2.3 两组LVEF与MAD、AAD相关性比较
正常对照组中,LVEF与MAD、AAD右冠瓣环及相应连线中点位移呈正相关(P<0.01);正常对照组LVEF与主动脉瓣环无冠瓣位移呈正相关(P<0.05)。DCM组中,LVEF与二尖瓣环侧壁、后室间隔及4C-mid呈正相关(P<0.05);LVEF与二尖瓣环前壁、下壁及2C-mid呈正相关(P<0.05);LVEF与二尖瓣环3C-mid呈正相关(P<0.05);LVEF与主动脉瓣右冠瓣、AV-mid呈正相关(P<0.05);LVEF与二尖瓣环后壁、前室间隔、主动脉瓣环无冠瓣位移无相关性(P>0.05)。
2.4 重复性检验
由另1名超声心动图诊断医师从受检人员中随机选取20例,再次测量MAD、AAD,检测结果行Pearson相关性分析,相关系数为:r=0.842(P<0.05),说明测量可重复性较好。
3 讨论
心脏是基于复杂的心肌纤维排列和运动的泵器官,因此,需要尽可能的建立一种简单并充分考虑心肌运动状态的评价方法,不仅用于疾病诊断,而且能够成为治疗疾病及估计预后的重要指标。长期以来,LVEF值是反映左室整体收缩功能最常用的指标,但是采用二维超声心动图测量LVEF需要手动跟踪左室舒张期和收缩期心内膜,对二维图像质量要求高,操作相对繁琐,受操作者主观经验影响等干扰因素较多,重复性较差。瓣环组织运动位移技术较小依赖于二维超声图像质量,无角度依赖,容易跟踪二尖瓣环、主动脉瓣环及其运动轨迹,这些均优于二维超声Simpson’s法的LVEF值测量,是评价左室收缩功能的有力补充[2]。
本研究发现,DCM组较正常对照组左室瓣环MAD、AAD均明显降低,差异有统计学意义(P<0.01)。左室心肌是一个复杂的螺旋带结构,包括径向、纵向、环向和扭转等多重综合运动,瓣环纵向运动是心肌收缩舒张最基本的运动,不仅反映左室纵向运动,而且部分反映左室环向运动,是心脏整体运动功能重要的组成部分[3]。左室射血是心肌纵向和环向的形变过程,中层环形心肌是左室心肌收缩的驱动纤维,并主要引起心肌增厚,而纵形心肌纤维主要引起心室缩短。Black 等[4]研究认为,MAD、纵向应变和应变率可以有效反映左室径向功能,并与LVEF密切联系。Nishikage等[5]研究发现,高血压患者LVEF值正常,但MAD、AAD已经表现出降低趋势,说明MAD、AAD可以更早、更敏感地反映左室纵向心肌纤维运动产生的收缩功能,左室心肌纵向缩短占有效射血功能的70%左右,对早期诊断心脏功能受损有重要的应用价值。Zahid等[6]研究发现,冠心病早期,LVEF没有明显降低,但MAD与纵向应变已经降低,说明MAD可以独立预测心肌运动状态,是临床评价左室纵向收缩功能的有力补充。Decloedt 等[7]研究认为,早期心肌收缩功能受损,传统超声诊断指标仍表现正常,但心肌纵向缩短已经发生减低,说明纵向运动能够敏感反映微小心肌功能损伤,根本原因可能是心内膜下纵向心肌纤维具有易损性,而环向心肌纤维不易受到不利因素影响,反而可以补偿纵向心肌纤维功能障碍产生的不良后果,最终维持左室心肌有效的收缩和舒张运动功能。
本研究发现,正常对照组LVEF值与MAD、AAD大多数节段呈正相关(P<0.01);正常对照组LVEF值与主动脉瓣环无冠瓣位移呈正相关(P<0.05)。左室二尖瓣环高度、形态、大小以及瓣叶的启闭与主动脉瓣环的高度、形态、大小以及瓣叶启闭密切联系,两者互相依赖、互相影响,引起瓣叶有效的启闭和心室有效的做功[6]。De等[8]研究认为,主动脉瓣置换术后,可以降低二尖瓣返流程度,与纵向应变相关性非常好,同时,二尖瓣环位移与LVEF高度相关(P<0.001),与年龄和体表面积相关性较差(P=0.043)。二尖瓣环、主动脉瓣环是心脏纤维骨架重要的组成部分,参与左室基底到心尖方向的纵向运动,纵向心肌纤维收缩二尖瓣环、主动脉瓣环向心尖方向移动,使左室长轴纵向缩短,保证心肌的有效射血[9]。DCM组LVEF值与大多数瓣环位点的MAD、AAD呈正相关(P<0.05),LVEF仅与二尖瓣环后壁、前室间隔、主动脉瓣环无冠瓣位移无相关性(P>0.05),这可能与DCM患者心室内运动传导减慢、心肌间质纤维化及细胞间或细胞内钙离子通道障碍有关,也可能与该临床研究样本量偏少有关。
本研究是小样本临床研究,未能获得MAD、AAD的有效参考值,而且左室心肌运动与两者之间的关系也不是非常清楚,只能简单地反映各瓣环位点左室纵向的收缩功能,不能反映各个节段心肌的力学状态。瓣环组织运动位移与瓣环速度、心肌运动及心腔内血流动力学之间的关系等尚需进一步的深入探讨。
[1] Thapa P, Xing Y Y, Li Y H. Mitral annulus displacement measured by two-dimensional speckle tracking imaging to assess the left ventricular longitudinal systolic function in coronary heart disease[J]. J Clin Ultrasound, 2014, 42(9): 544-549.
[2] Suzuki K, Akashi Y J, Mizukoshi K,etal. Relationship between left ventricular ejection fraction and mitral annular displacement derived by speckle tracking echocardiography in patients with different heart diseases[J]. J Cardiol, 2012, 60(1): 55-60.
[3] Buss S J, Mereles D, Emami M,etal. Rapid assessment of longitudinal systolic left ventricular function using speckle tracking of the mitral annulus[J]. Clin Res Cardiol, 2012, 101(4): 273-280.
[4] Black D E, Bryant J, Peebles C,etal. Tissue motion annular displacement of the mitral valve using two-dimensional speckle tracking echocardiography predicts the left ventricular ejection fraction in normal children[J]. Cardiol Young, 2014, 24(4): 640-648.
[5] Nishikage T, Nakai H, Lang R M,etal. Subclinical left ventricular longitudinal systolic dysfunction in hypertension with no evidence of heart failure[J]. Circ J, 2008, 72(2): 189-194.
[6] Zahid W, Johnson J, Westholm C,etal. Mitral annular displacement by Doppler tissue imaging may identify coronary occlusion and predict mortality in patients with non-ST-elevation myocardial infarction[J]. J Am Soc Echocardiogr, 2013, 26(8): 875-884.
[7] Decloedt A, Verheyen T, Sys S,etal. Quantification of left ventricular longitudinal strain, strain rate, velocity, and displacement in healthy horses by 2-dimensional speckle tracking[J]. J Vet Intern Med, 2011, 25(2): 330-338.
[8] de Knegt M C, Biering-Sorensen T, Sogaard P,etal. Concordance and reproducibility between M-mode, tissue Doppler imaging, and two-dimensional strain imaging in the assessment of mitral annular displacement and velocity in patients with various heart conditions[J]. Eur Heart J Cardiovasc Imaging, 2014, 15(1): 62-69.
[9] Liu L, Tuo S, Zhang J,etal. Reduction of left ventricular longitudinal global and segmental systolic functions in patients with hypertrophic cardiomyopathy: Study of two-dimensional tissue motion annular displacement[J]. Exp Ther Med, 2014, 7(6): 1457-1464.
Evaluation of Left Ventricular Longitudinal Systolic Function by Mitral and Aortic Annular Displacements in Patients with Dilated Cardiomyopathy
WangShan1,LiChunmei1△,KongHong2,LiWenhua1.
1.InstituteofUltrasoundMedicine,SichuanAcademyofMedialSciences&SichuanProvincialPeople’sHospital,Chengdu610072,China; 2.CardiologyDepartment,SichuanAcademyofMedialSciences&SichuanProvincialPeople’sHospital,Chengdu610072,China
Objective To investigate the clinical application value of mitral annular displacement (MAD) and aortic annular displacement (AAD) in the evaluation of left ventricular longitudinal systolic function in patients with dilated cardiomyopathy (DCM). Methods A total of 38 DCM patients treated in Sichuan Provincial People’s Hospital from July of 2013 to December of 2014 were selected and divided into the DCM group, and the other 46 age-matched healthy subjects were selected and divided into the control group. The routine echocardiography was performed to collect the real-time grayscale ultrasound images of three continuous cardiac cycles from the left ventricular apical four-chamber, three-chamber and two-chamber views. The image workstation Q-lab 9.1 was used to measure the maximum displacements respectively at the mitral posterior interventricular septum, lateral wall and midpoint of the line from the posterior interventricular septum to the lateral wall, the mitral anterior and inferior walls and the midpoint of the line from the anterior wall to the inferior wall, and the aortic noncoronary cusp, right coronary cusp, and midpoint of the line from the noncoronary cusp to the right coronary cusp. The two-plane Simpson’s method was adopted to calculate the left ventricular ejection fraction (LVEF). The changes of MAD and AAD were analyzed and compared between the DCM patients and the healthy subjects, and the correlations were explored among the parameters of MAD, AAD and LVEF. Results Firstly, Compared with those in the control group, the levels of MAD, AAD and LVEF in the DCM group decreased significantly (P<0.01). Secondly, the levels of left ventricular LVEF in the control group were positively correlated with the levels of MAD (P<0.01) and those of AAD at the right coronary cusp and midpoint of the line from the noncoronary cusp to the right coronary cusp (P<0.01), and at the aortic noncoronary cusp (P<0.05), while those in the DCM group were positively correlated with all the levels of MAD and AAD (P<0.05) except those of MAD at the posterior wall and anterior interventricular septum (P>0.05) and those of AAD at the noncoronary cusp (P>0.05). Conclusion MAD and AAD can indicate the left ventricular systolic function of DCM patients quickly and objectively, so it can be a new method to evaluate the left ventricular systolic function.
Dilated Cardiomyopathy; Displacement; Annulus; Left ventricular systolic function
http://www.cnki.net/kcms/detail/51.1705.R.20170220.1144.014.html
10.3969/j.issn.1674-2257.2017.01.014
R445.1
A
△通信作者:李春梅,E-mail:licmxxg@163.com
