鲑鱼降钙素温度敏感型原位凝胶的制备与评价*
2017-03-15王小宁常体伟张存劳
王小宁,常体伟,屈 勇,张存劳
(西安医学院 药学院,陕西 西安 710021)
降钙素(calcitonin,CT)是一种32肽的激素,它是由甲状腺内的滤泡旁细胞(C细胞)以及其它脊椎动物的腮腺分泌的,其具有强力的抑制骨吸收的作用,能直接抑制破骨细胞的活性,刺激成骨细胞的形成,加快钙在骨骼中的沉积,因此在治疗骨质疏松症方面显示了良好的疗效[1]。目前临床常用的为鲑鱼降钙素(Salmon Calcitonin,sCT),活性比人降钙素强数十倍[2]。作为大分子多肽类药物,降钙素在胃肠道易被降解,因此给药方式受限,目前上市的降钙素剂型有注射剂和鼻喷剂两种。但注射剂和鼻喷剂给药后,药物达峰快,半衰期短,维持作用时间短,患者顺应性差。由于降钙素不能口服以及注射后药物半衰期短的不足,研究其缓控释剂型就显得尤为重要。
温敏凝胶在室温下是溶液状态,可通过皮下注射给药,由于环境条件的改变而发生相转变形成半固态的凝胶。载药凝胶长时间与作用部位发生紧密接触,缓慢地、持续地释放药物,可避免首过效应,减少给药次数,延长药物生物半衰期,提高药物的生物利用度,因此作为蛋白多肽类药物的缓控释给药系统具有一定应用前景[3-4]。作者的目的在于制备一种以壳聚糖(chitosan)和葡萄糖磷酸二钠(disodium Glucose phosphate,GP)为基质材料的鲑鱼降钙素温度敏感型原位凝胶,并对该凝胶的处方筛选、体外释放以及生物相容性进行研究,为开发降钙素的缓释给药制剂奠定基础。
1 实验部分
1.1 试剂与仪器
鲑鱼降钙素原料药(sCT):质量分数>98%,上海肽仕生物科技有限公司;壳聚糖:相对分子质量507 kD,济南海得贝海洋生物工程有限公司;葡萄糖磷酸二钠(GP):西格玛奥德里奇公司;鲑鱼降钙素ELISA试剂盒:A03727,上海纪宁实业有限公司;GS-E90003胎鼠成纤维细胞:实验用细胞代数为第4代,西安医学院药理教研室;Dulbecco’s modified Eagle 高糖培养基(DMEM)、胰酶:质量分数0.25%,脉晨科技有限公司;特级胎牛血清(FBS):美国Gibco公司;罗丹明B(SRB):Sigma-Aldrich公司;MTT:Sigma-Aldrich公司;Tris:生工生物科技有限公司;TritonX-100:Amresco公司。
超净工作台:VS-840K-U,苏州安泰空气技术有限公司;倒置显微镜:XDS-1B,COIC公司;低速台式离心机:TD24-WS,湘仪离心机有限公司;二氧化碳细胞培养箱:HF-90,上海力申科学仪器有限公司;酶标仪:model 550,美国Bio-Ran公司。
1.2 凝胶溶液的制备
1.2.1 凝胶溶液的制备
在室温下,将葡萄糖磷酸二钠溶液在搅拌条件下滴入壳聚糖溶液中,得到的混合溶液继续搅拌10 min得到均一澄清透明的溶液。
1.2.2 载药凝胶溶液的制备
在室温下,将计算量的鲑鱼降钙素分散于壳聚糖溶液中,制得含药的壳聚糖溶液。将葡萄糖磷酸二钠溶液在搅拌条件下滴入含药壳聚糖溶液中,得到的混合溶液继续搅拌10 min得到载药凝胶溶液。
1.3 胶凝温度及胶凝时间的测定
采用试管翻转法来考察不同比例壳聚糖、葡萄糖磷酸二钠溶液的溶液-凝胶相变[5]。将装有聚合物溶液的试管浸入恒温水浴中,在30~45 ℃范围内观察溶液的胶凝温度,升温间隔为1 ℃。溶液在每个温度下放置20 min后,通过翻转试管观察溶液的状态来确定溶液是否胶凝,当溶液不可流动时的温度即为胶凝温度,从试管放入水浴中到达到胶凝点所经历的时间即为胶凝时间。
1.4 ρ(鲑鱼降钙素)测定方法的建立
样品采用鲑鱼降钙素酶免分析试剂盒进行定量分析[6]。精密称取鲑鱼降钙素5 mg,置于25 mL的棕色容量瓶中,加入适量注射用水溶解,定容即得ρ(鲑鱼降钙素)为200 μg/mL的溶液;精密量取250 μL的上述溶液,置于25 mL的棕色容量瓶中,加入适量注射用水溶解,定容即得ρ(鲑鱼降钙素)为2 μg/mL的标准品溶液。加入稀释好后的标准品50 μL于反应孔、加入待测样品50 μL于反应孔内。立即加入50 μL的生物素标记的抗体。盖上膜板,轻轻振荡混匀,37 ℃温育1 h。清洗酶标板5次,每孔加入80 μL的亲和链酶素-HRP,轻轻振荡混匀,37 ℃温育30 min。清洗酶标板5次,每孔加入底物显色剂和终止液各50 μL,轻轻振荡混匀,37 ℃温育15 min。取出酶标板,迅速加入50 μL终止液,加入终止液后应立即在450 nm波长处测定各孔的OD值。用ELISA法检测样品时均扣除了空白溶液样品本底。
1.5 温敏凝胶的处方筛选
以累积释放度为指标,以对体外释放度影响较大的因素壳聚糖黏度(A)、ρ(壳聚糖)(B)、ρ(葡萄糖磷酸二钠)(C)为考察因素进行三因素三水平的正交试验,采用综合评分法对正交实验的结果进行分析,进行温敏凝胶的处方筛选。
1.5.1 累积释放度的测定方法
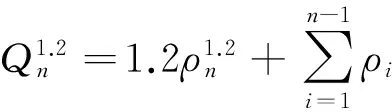
计算累积释药量,计算累积释放度。其中,ρ为样品浓度,Q为累积释放量,i和n分别为取样次数。
1.5.2 正交实验
选择对体外释放度影响较大的因素壳聚糖黏度(A)、ρ(壳聚糖)(B)、ρ(葡萄糖磷酸二钠)(C)为考察因素进行三因素三水平的正交实验,采用综合评分法对正交实验的结果进行分析(是实验对不同处方1、6、12 h的释放度进行评价),再将评分结果进行加权相加后得出总分,各点的评分标准如下:1 h为|Q1 h-15%|,6 h为|Q6 h-45%|,12 h为|Q12 h-90%|,计算公式为:Y=|Q1 h-15%|+|Q6 h-45%|+|Q12 h-90%|,Y小者为优,最小时最佳[8]。最后采用直观分析和方差分析的方法对结果进行分析,因素水平见表1。

表1 因素及水平
1.6 体外释药
按1.5.1项下的累积释放度测定方法,以最优处方为凝胶基质,考察了载有不同ρ(鲑鱼降钙素的凝胶)(10、15、20 mg/mL)在PBS溶液中的释放情况,以各处方累积释放百分率对时间作图,绘制释放曲线。
1.7 生物相容性研究
1.7.1 凝胶浸提液的制备
于6孔细胞培养板中,每孔加入1 mL的溶液,置于37 ℃、体积分数5% CO2培养箱中,待其形成凝胶后,每孔加入2 mL的DMEM完全培养基作为浸提介质,分别浸提24、48、72 h,取出6孔细胞培养板,吸取凝胶上清液,即为浸提液。ρ(浸提液)按比例稀释成为100、50、10、1 mg/mL的浸提液,备用。
1.7.2 凝胶浸提液细胞毒性的测定
SRB法检测水凝胶浸提液的细胞相容性[9]。取传至第4代的胎鼠成纤维细胞,调整细胞为4×104个/mL,制成细胞悬液。将配制好的细胞悬液接种于96孔板中,100 μL/孔,置37 ℃、体积分数5% CO2培养箱中培养24 h,于细胞培养的第3天进行浸提液毒性的测定。取出细胞培养板,加入200 μL DMEM培养基作为空白对照组,10 mg/mL TritonX-100为阳性对照,加入浸提3 d的一系列浓度的浸提液作为实验组,每组6孔,继续培养24 h。取出培养板,PBS清洗一遍,加入200 μL预冷的φ(三氯醋酸)=10%固定,将培养板移至4 ℃放置1 h。倒掉固定液,每孔用去离子水洗5遍,甩干,37 ℃烘干。每孔加入100 μL SRB液,在室温放置10 min,未与蛋白质结合的SRB用质量分数1%醋酸洗5遍,空气干燥。结合的SRB用200 μL 10 mmol/L非缓冲Tris碱液(pH=10.5)振荡溶解。于BIO-TEK酶标仪测定各孔的OD值,测定波长为540 nm。根据各孔OD值计算细胞的存活率。计算公式如下:细胞相对存活率%=OD实验组/OD对照组×100%。
2 结果与讨论
2.1 结果
2.1.1 ρ(鲑鱼降钙素)测定标准曲线的制备
取空白溶液0.2 mL,分别加入鲑鱼降钙素标准品适量,使其质量浓度分别为5、10、20、40、80、120、160、200 μg/L;按2.2中所述方法,进行分析测定,每一质量浓度进行5个样本分析,记录光密度OD,以光密度OD对质量浓度ρ做线性回归分析,得回归方程为:OD=0.038 58ρ-0.539 7,r2=0.996 5。鲑鱼降钙素浓度检测方法的检测范围为5~200 μg/L,最低检测浓度为5 μg/L。
2.1.2 正交实验结果
正交实验及结果见表2,方差分析见表3。

表2 正交实验及结果
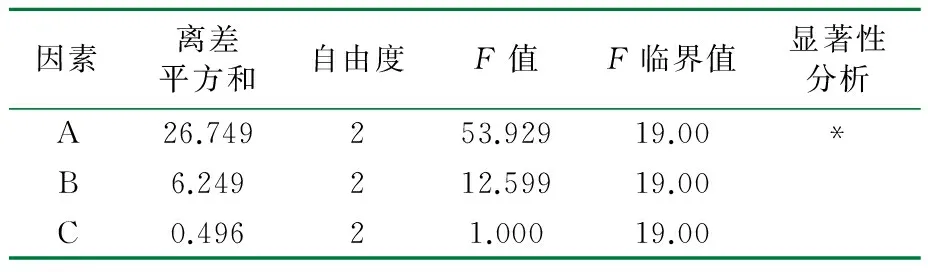
表3 方差分析1)
1)F0.1(2,2)=9.00,F0.05(2,2 )=19.00,F0.01(2,2)=99.00。
由表2、表3可见,各因素对凝胶体外释药的影响程度依次为A>B>C,且A对体外累积释放度有显著影响(P<0.05)。从实验结果来看,温敏凝胶的最优处方为A2B2C1,即壳聚糖黏度为200~400 mPa·s,ρ(壳聚糖)=12 mg/mL,ρ(葡萄糖磷酸二钠)=100 mg/mL。
2.1.3 验证实验
按A2B2C1最优处方制备温敏凝胶,各平行制备3份,测定其胶凝温度、胶凝时间和体外累积释放度,结果见表4。

表4 验证实验结果
验证性实验结果表明,以最优处方制备的温敏凝胶胶凝温度为(35.3±0.2)℃,胶凝时间为(13.7±0.6)min,1 h体外累积释放度为(13.9±0.1)%,没有药物的突释现象,6 h时累积释放度为(42.9±0.2)%,具有缓释效果,12 h时累积释放度为(90.2±0.3)%,释放较完全,综合评分为3.8±0.1,该值比所有的正交实验值都要小,说明处方优化结果较好。
2.1.4 体外释药
不同ρ(鲑鱼降钙素的凝胶)(20、15、10 mg/mL)的释放曲线见图1。

t/h图1 不同载药量凝胶处方的体外释药曲线
从体外释放曲线可以看出,在释放开始的前1 h内,各处方凝胶分别释放了(14.46±1.91)%,(13.12±1.63)%,(10.57±2.02)%的鲑鱼降钙素,显示了较快的药物释放速率,随后的释放减缓,在6 h的释放时间内,各处方最终都只有不到50%的药物从凝胶中释放,说明所制备的凝胶具有良好的缓释效果。在6 h的释放过程中,载10和15 mg/mL鲑鱼降钙素的凝胶分别累积释放了(38.14±6.44)%和(42.14±6.80)%的药物,两组间不存在显著性的差异(P>0.05);而载20 mg/mL鲑鱼降钙素的凝胶累积释放了(48.93±3.34)%的药物,且每个时间点20 mg/mL鲑鱼降钙素凝胶的释药量均高于另外两组。12 h后,各处方凝胶分别释放了(93.70±4.38)%,(89.31±4.60)%,(85.32±4.90)%的鲑鱼降钙素,均体现出较好的缓释效果。
2.1.5 生物相容性研究
不同浓度凝胶浸提液细胞毒性的测定结果见图2。
由图2可见,随着凝胶浸提液浓度的增大,细胞存活率随之降低。但是,当ρ(凝胶浸提液)范围在1~50 mg/mL时,细胞存活率没有显著性差异(P>0.05);当ρ(凝胶浸提液)=1 mg/mL时,细胞存活率为96.9%;当ρ(凝胶浸提液)=50 mg/mL时,细胞存活率为92.1%;当ρ(凝胶浸提液)=10 mg/mL时,细胞存活率仍高于80%,为87.4%,但显著低于ρ(凝胶浸提液)=1 mg/mL时的细胞存活率(P<0.05),作为阳性对照的10 mg/mL Triton X-100,其细胞存活率低于26%,具有显著的细胞毒性。结果说明凝胶浸提液在所测定的浓度范围内基本没有细胞毒性。

ρ(凝胶浸提液)/(mg·mL-1)图2 不同浓度凝胶浸提液的细胞毒性测定结果(n=6)
2.2 讨论
壳聚糖是一种具有生物相容性、生物可降解性以及粘膜黏附性的阳离子生物高分子,以其低免疫原性及低细胞毒性而受到广泛关注[10-11]。壳聚糖可溶解在酸性溶液中,在 pH>6 时发生相分离形成凝胶样沉淀。然而,具有单阴离子基团的多元醇盐(如多元醇或糖的磷酸盐)的加入可以将单纯 pH 依赖胶凝的壳聚糖溶液,转变为温度敏感型的溶液,使其成为温敏原位凝胶非常有潜力的材料之一,并在蛋白多肽类药物缓控释系统的研究方面取得了一定进展[12]。
近年来,新型生物材料的毒性问题备受关注,聚合物材料由于在制备过程中会有有机溶解残留以及聚合物材料缓慢降解,因此可能造成蓄积毒性[13]。由于凝胶的降解产物微量存在,因此浸提液的细胞毒性应该大大低于材料溶液的毒性,实验结果也证实了这一点。由生物相容性实验数据可看出,浸提3 d后,ρ(浸提液)=100 mg/mL的细胞存活率仍然为87.4%,而阳性对照组10 mg/mL TritonX-100的细胞存活率仅为25.3%。由浸提液的结果来看,凝胶的毒性相当低,在药物释放领域具有一定的应用前景。
3 结 论
正交实验法优化的处方为壳聚糖黏度为200~400 mPa·s,ρ(壳聚糖)=12 mg/mL,ρ(葡萄糖磷酸二钠)=100 mg/mL。不同载药量处方体外释药结果显示,在6 h的释放时间内,各处方都只有不到50%的药物从凝胶中释放,显示了较好的缓释效果。生物相容性研究结果显示,凝胶浸提液在所测定的浓度范围内基本没有细胞毒性,说明此凝胶系统生物相容性好,可应用于药物释放领域。
[1] HANSEN J M,ASHINA M.Calcitonin gene-related peptide and migraine with aura:A systematic review[J].Cephalalgia,2014,34(9):695-707.
[2] 郑林,肖涟波.鲑鱼降钙素治疗骨质疏松症的临床应用进展[J].风湿病与关节炎,2014,3(10):64-66.
[3] 赵宇,王晓波,张治然,等.温敏凝胶的研究与应用进展[J].中国药房,2015,26(1):132-135.
[4] DAI PHU HUYNH,GUANG JIN IM,SU YOUNG CHAE,et al.Controlled release of insulin from pH/temperature-sensitive injectable pentablock copolymer hydrogel[J].Journal of Controlled Release,2009,137(1):20-24.
[5] JEONG B,BAE YH,KIM SW.Thermoreversible gelation of PEG-PLGA-PEG triblock copolymer aqueous solutions[J].Macromolecules,1999,32(21):7064-7069.
[6] 宋益民,杨青,苏传东,等.酵母表达鲑鱼降钙素的降血钙活性和药动学研究[J].药物分析杂志,2010,30(5):775-779.
[7] 张田野,王垚,李蒙,等.叶黄素眼用温敏型原位凝胶的制备及体外释放研究[J].中国药学杂志,2015,50(21):1880-1884.
[8] 岑菁.水飞蓟宾双层缓释片的研究[D].四川:成都中医药大学,2013.
[9] WANG X,LI X,LI Y,et al.Synthesis,characterization and biocompatibility of poly(2-ethyl-2-oxazoline)-poly(D,L-lactide)-poly(2-ethyl-2-oxazoline)hydrogels[J].Acta Biomaterialia,2011,7:4149-4159.
[10] 吴湛霞,潘江球,蔡鹰,等.近年壳聚糖在医药上的应用研究进展[J].山东化工,2016,45(2):55-56,59.
[11] 张程亮,孙纳.壳聚糖用于抗肿瘤治疗的研究进展[J].中国药房,2005,16(7):549-550.
[12] 汪林,吴霞,马龙,等.温敏型壳聚糖/甘油磷酸钠缓释胰岛素凝胶系统的制备[J].口腔颌面修复学杂志,2012,13(2):65-67.
[13] 彭伟,穆玉.羧甲基壳聚糖温敏凝胶的制备及其毒性实验[J].中国组织工程研究与临床康复,2010,14(51):9591-9594.
