机器人胃切除术与腹腔镜胃切除术治疗胃癌近期疗效的Meta分析
2017-03-08楼茜洁刘芳腾罗洪亮南昌大学第二附属医院手术室胃肠外科南昌330006
楼茜洁,刘芳腾,潘 华,邱 铖,黄 俊,罗洪亮(南昌大学第二附属医院.手术室; .胃肠外科,南昌 330006)
胃癌是我国最常见的恶性肿瘤疾病之一,其发病率和病死率在全球所有恶性肿瘤中分别位居第4位和第2位,严重危害人类的生命健康[1-2]。目前,外科手术仍是目前治疗胃癌最有效的方法。近年来,随着微创技术的快速发展,胃癌根治手术已由传统的开腹手术向具有创伤小、术后恢复快等特点的微创手术普及。腹腔镜胃切除术(LG)是目前治疗胃癌应用最多的手术方式,已被证实比开腹手术具有更好的近期疗效[3-4]。然而,LG存在一些缺陷,如显示界面为二维成像、手术器械操作灵活性较差、有效操作范围有限等。自从2001年Giulianotti实施第1例机器人胃切除术(RG)以来,有关RG的病例陆续有文献[5-6]报道。由于相关研究样本量较小,对于RG能否取得与LG相当或更好的手术疗效问题仍需进一步研究来确认。本文收集了2004年7月至2015年7月公开发表的中、英文全文文献,通过荟萃分析方法系统评价RG在治疗胃癌方面的有效性、安全性和近期疗效,以期为临床治疗提供依据。
1 资料与方法
1.1 检索策略
检索Pubmed、Elsevier、Cochrane Library、SPRINGER以及中国期刊全文数据库(CNKI)、数字化期刊全文数据库(万方)、维普中文科技期刊全文数据库中有关研究RG和LG治疗胃癌的文献,时间为2004年7月至2017年1月,英文检索词为“robotic OR robot OR da vinci”“laparoscopic OR laparoscopic”“gastrectomy”“cancer OR carcinoma”,中文检索词为“腹腔镜”“机器人OR达芬奇”“胃切除术”,并通过人工检索等方法进一步拓宽检索范围,浏览相关文献的摘要及参考文献,保证文献的查全率。
1.2 纳入、排除标准
1.2.1 纳入标准
1)2004年7月至2017年1月公开发表的研究RG与LG手术的中文和英文文献;2)所有样本病理组织学为胃癌;3)文献包含评价指标的原始数据及原始的均数和标准差、优势比值;4)同一作者的文献,选取质量更高的研究。
1.2.2 排除标准
1)研究只包含RG或LG一种手术疗效的文献;2)文献中含有非胃癌或非原发性胃癌的病例;3)数据太少或者描述不祥的文献;4)文献为病例报道、综述或评论。
1.3 文献信息提取及质量评价
1.3.1 信息提取
由2位研究组的成员根据统一表格独立进行信息数据提取。对于有争议的问题,通过共同讨论或者与第3位研究者商讨决定。提取的信息数据包括第1作者、发表时间、国家、病例年限、病例数、研究样本量、手术时间、手术出血量、近和远端切缘距离、淋巴结清扫数目、术后首次排气时间、术后首次进食时间、住院时间以及术后并发症(包括吻合口瘘、肠梗阻、胃肠排空障碍、肺部感染等)。
1.3.2 纳入文献的质量评价
对于非随机对照实验(RCT)的研究文献,通过Kim等[7]方法对纳入文献进行质量评价。评价指标共计3方面9项,即研究设计(包括是否随机、是否符合纳入标准、研究样本总量是否≥100例)、组间可比性(包括性别、年龄、肿瘤部位、大小及危险度)以及结果评估(是否描述淋巴结清扫数目)。所纳入的研究若满足以上指标1项则计1分,否则计0分;如纳入文献所获分数≥6分,则表示该文献质量好。
1.4 统计学方法
采用Review Manager 5.3统计软件(Cochrane协作网提供)进行Meta分析。对无明显异型性(I2≤50%)的数据和存在异型性(I2>50%)的数据,分别采用固定效应模型(fixed effects model)和随机效应模型(random effects model)计算合并统计效应量;对二分类变量资料和连续变量资料分别采用比值比和加权均数差值合并统计效应量,各效应量均以95%CI表示。以P<0.05为差异有统计学意义。
2 结果
2.1 纳入文献信息情况
依据纳入标准和排除标准,经全文筛选后,共入选22篇文献,共计7252例患者进入荟萃分析,其中RG组2111例,LG组5141例。入选文献质量评分均≥6分。纳入文献的基本信息及质量评价见表1。

表1 纳入文献的基本信息和质量评价
Ⅰ为是否随机对照研究,Ⅱ为是否具有纳入标准,Ⅲ为总样本量是否>100 例;a 为性别,b 为年龄,c 为体质指数(BMI),d 为肿瘤部位,e 为肿瘤分期。
2.2 纳入研究的Meta分析结果
2.2.1 2组手术时间的比较
22篇文献中的21篇文献对手术时间进行了研究,异质性检验结果为I2=90%,采用随机效应模型。结果显示,与LG组比较,RG 组手术时间更长(WMD=41.04,95%CI31.68~50.39,P<0.01)。见图1。
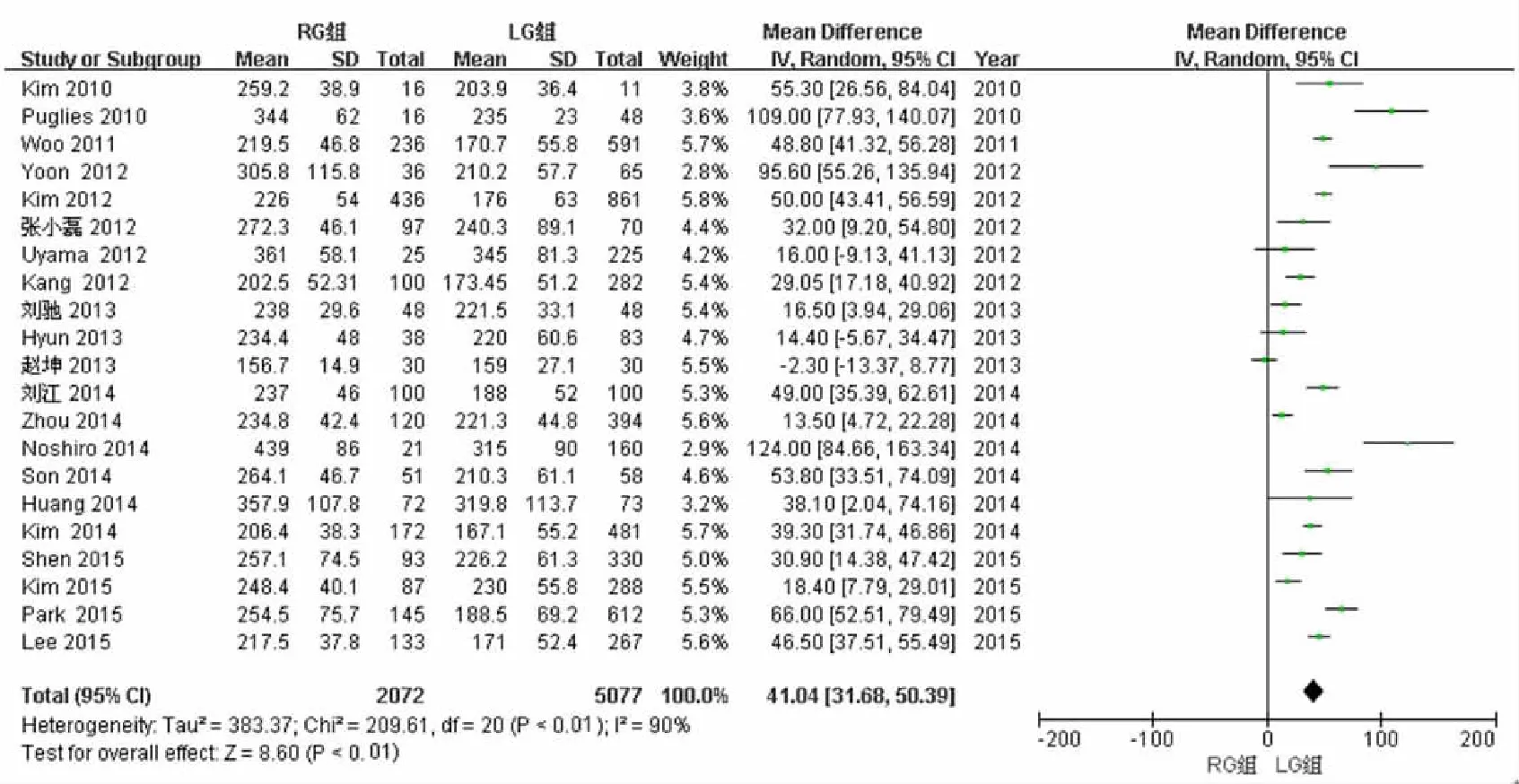
图1 2组手术时间的Meta分析结果
2.2.2 2组术中出血量的比较
22篇文献中的19篇文献对术中出血量进行了研究,异质性检验结果为I2=93%,采用随机效应模型。结果显示,与LG组比较,RG组术中出血量更少(WMD=-36.20,95%CI-49.65~-22.75,P<0.01)。见图2。
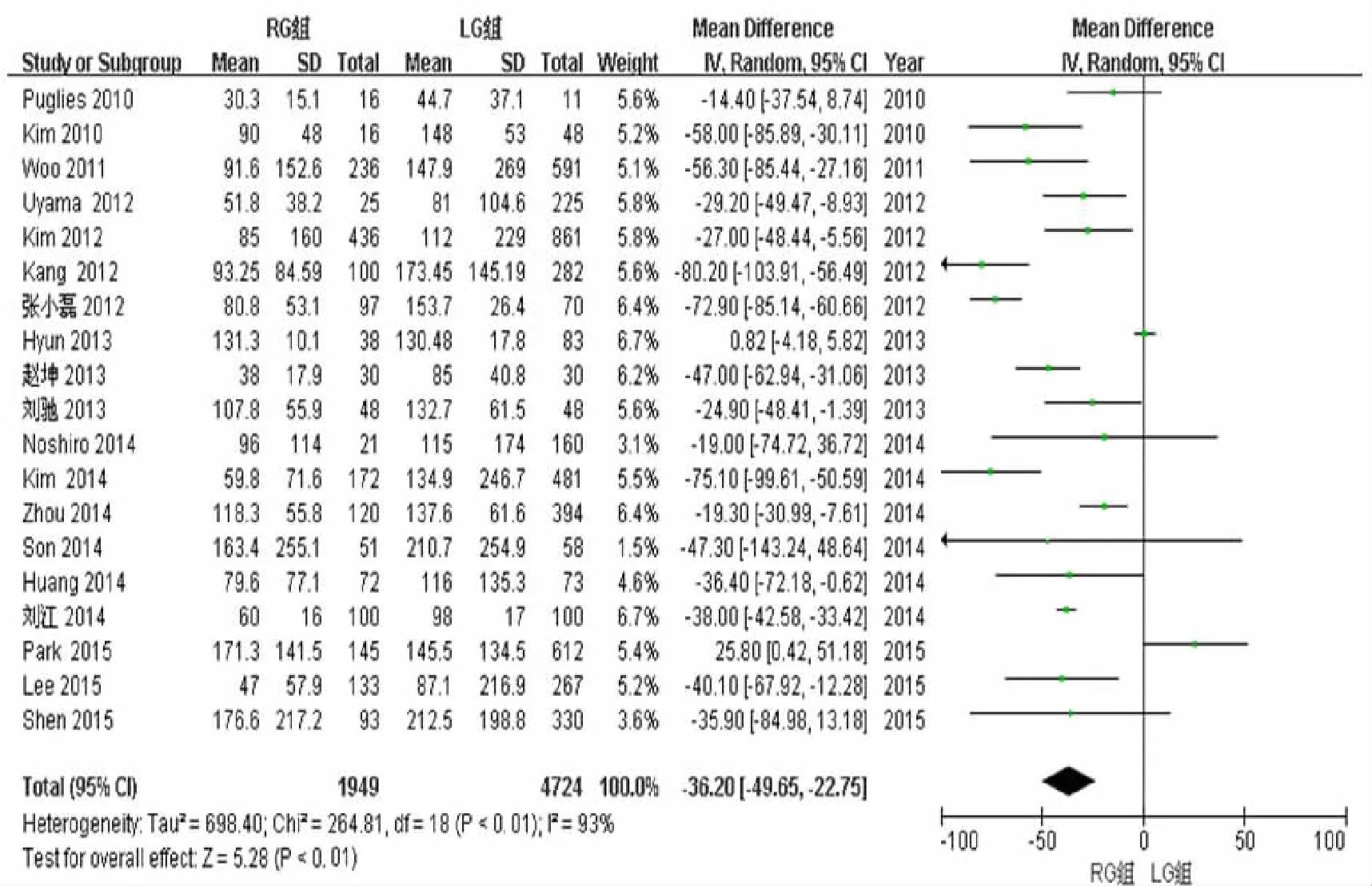
图2 2组术中出血量的Meta分析结果
2.2.3 2组近端切缘距离的比较
22篇文献中的11篇文献对近端切缘距离进行了研究,异质性检验结果为I2=0%,采用固定效应模型。结果显示,RG组近端切缘距离与LG组比较差异无统计学意义(WMD=0.10,95%CI-0.03~-0.24,P>0.05)。见图3。
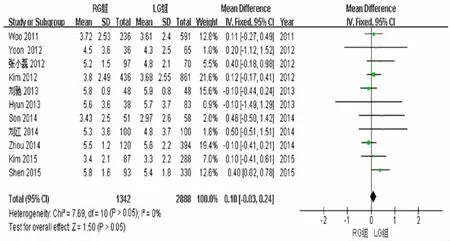
图3 2组近端切缘距离的Meta分析结果
2.2.4 2组远端切缘距离的比较
22篇文献中的10 篇文献对远端切缘距离进行了研究,异质性检验结果为I2=84%,采用随机效应模型。结果显示,LG组远端切缘距离与RG组比较差异无统计学意义(WMD=0.22,95%CI-0.28~-0.71,P>0.05)。见图4。
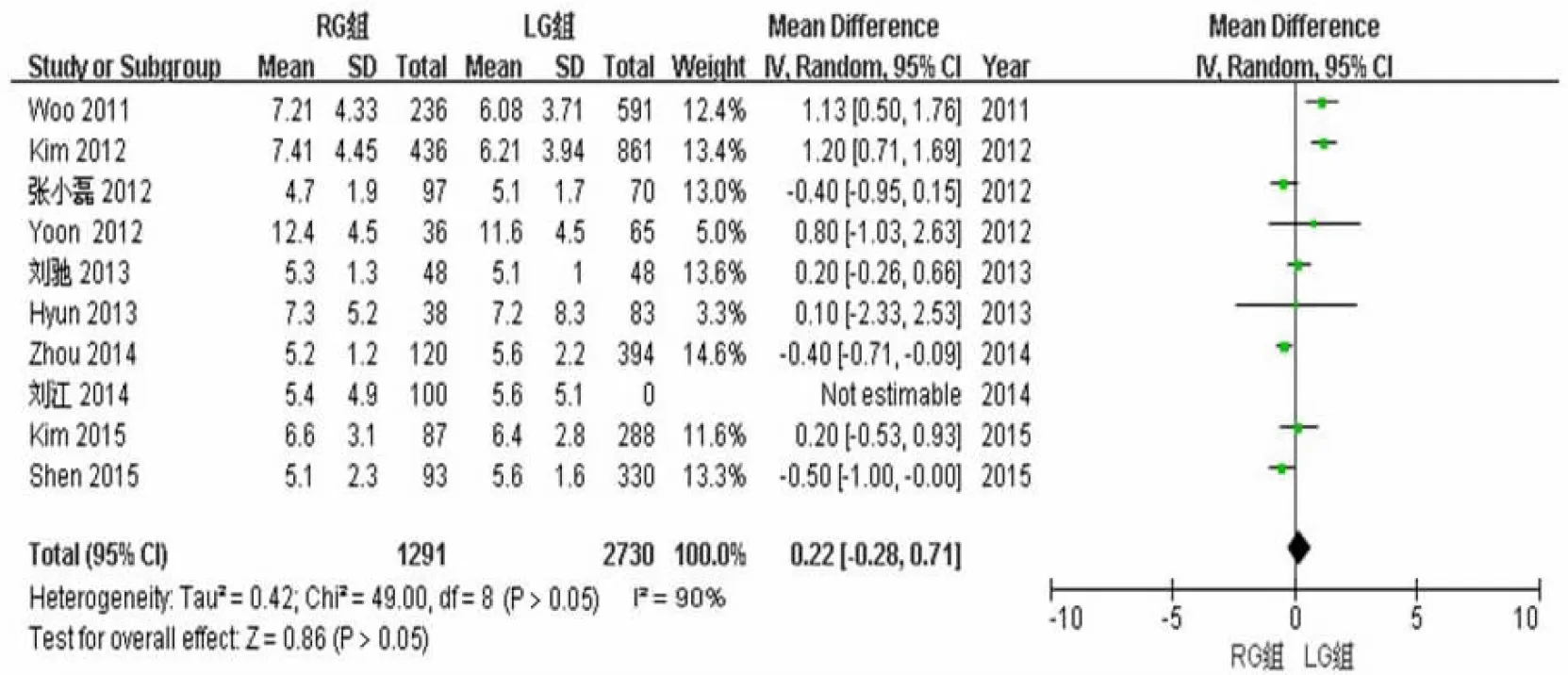
图4 2组远端切缘距离的Meta分析结果
2.2.5 2组淋巴结清扫数目的比较
22篇文献中的19篇文献对淋巴结清扫数目进行了研究,异质性检验结果为I2=47%,采用固定效应模型。结果显示,与LG组比较,RG组淋巴结清扫数目更多(WMD=1.89,95%CI1.28~2.49,P<0.01)。见图5。
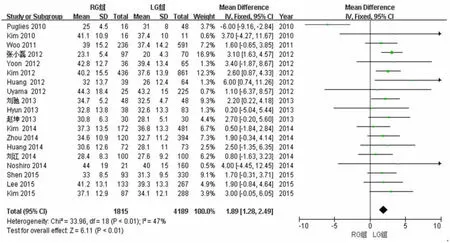
图5 2组淋巴结清扫数目的Meta分析结果
2.2.6 2组术后首次排气时间的比较
22篇文献中的10篇文献对术后首次排气时间进行了研究,异质性检验结果为I2=0%,采用固定效应模型。结果显示,与LG组比较,RG组术后首次排气时间更短(WMD=-0.27,95%CI-0.36~-0.18,P<0.01)。见图6。
2.2.7 2组术后首次进食时间的比较
22篇文献中的9篇文献对术后首次进食时间进行了研究,异质性检验结果为I2=0%,采用固定效应模型。结果显示,与LG组比较,RG组术后首次进食时间明显更早(WMD=-0.24,95%CI-0.35~-0.13,P<0.01)。见图7。
2.2.8 2组术后住院时间的比较
22篇文献中的20篇文献对术后住院时间进行了研究,异质性检验结果为I2=64%,采用随机效应模型。结果显示,与LG组比较,RG组术后住院时间更短(WMD=-0.74,95%CI-1.11~-0.36,P<0.01)。见图8。

图6 2组术后首次排气时间的Meta分析结果

图7 2组术后首次进食时间的Meta分析结果

图8 2组术后住院时间的Meta分析结果
2.2.9 2组术后总并发症发生率的比较
22篇文献均对术后并发症进行了研究,异质性检验结果为I2=0%,采用固定效应模型。结果显示,RG组术后总并发症发生率与LG组比较差异无统计学意义(WMD=0.96,95%CI0.81~1.15,P>0.05)。见图9。
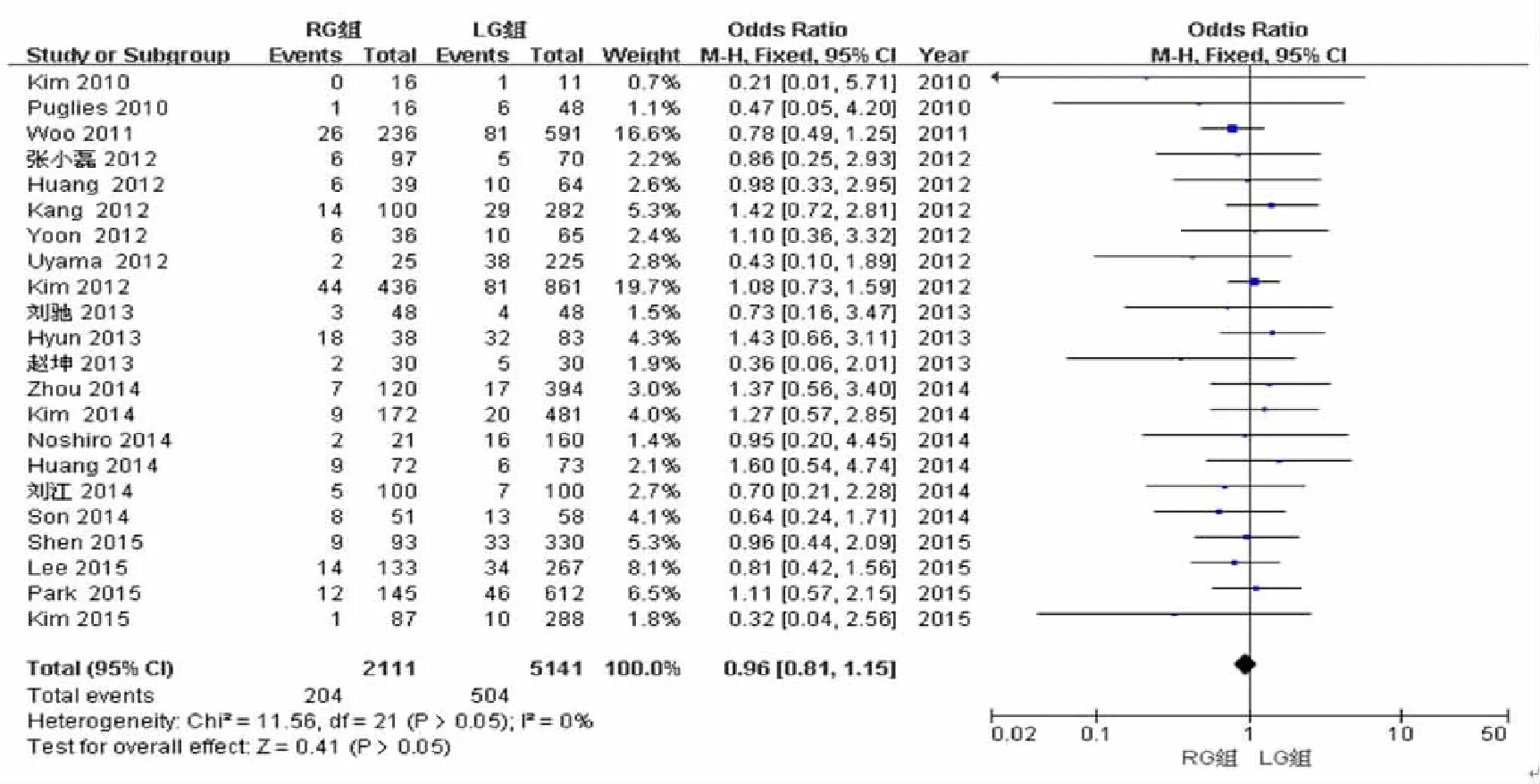
图9 2组术后总并发症发生率的Meta分析结果
3 讨论
机器人辅助手术作为一种新的微创技术,目前已被应用于医学治疗的多个领域,而对比机器人系统和腹腔镜手术在治疗胃癌疗效方面一直是该研究领域的热点。本研究在广泛临床研究的基础上,运用循证医学方法,综合分析近11年已发表的中、英文文献,对RG治疗胃癌的近期疗效作出较客观、全面的评估。虽然目前该领域的研究报道逐渐增多,但多为回顾性研究,且文献质量参差不齐。对于RG的长期疗效问题的研究仍较少,今后更高质量的大样本、多中心的随机对照试验仍是必需的。
本Meta分析结果显示,与LG组比较,RG组手术时间更长、术中出血量更少(均P<0.01)。对于RG手术时间更长的原因主要有:1)机器人系统需要较长的时间去额外调试器械,从而导致总体手术时间延长;2)机器人手术作为一种近年来的新兴技术,大多数外科医师尚需较长时间的训炼,才能达到熟练操作的水平。由此可见,随着机器人操作系统的不断技术改良,以及外科医师机器人手术操作经验的积累,RG手术时间将会缩短。对于RG术中出血量更少的原因有:1)机器人手术系统是一种良好稳定的三维操作视野的手术平台,显示画面立体清晰、不颤动,使手术操作更为灵活;2)高倍放大的操作视野能更准确显示较小的解剖结构,增加解剖的层次感,进而避免血管等组织损伤。
本Meta分析结果显示,与LG组比较,RG组淋巴结清扫数目更多(P<0.01)。机器人胃切除术由于比腹腔镜具有更好的手术视野以及高仿真手腕的灵活操作,可获得更多的浸润性淋巴结,这对于以淋巴结转移为主要转移途径的胃癌而言,淋巴结获取数目与预后密切相关,因而显示出RG可能具有更好的肿瘤根治优势。
RG不仅在手术安全、有效方面显示出一定的优势,在术后恢复方面也具有优势。本Meta分析结果显示,与LG组比较,RG组术后首次排气时间、术后首次进食时间、术后住院时间均明显缩短(均P<0.01);2组术后总并发症发生率比较差异无统计学意义(P>0.05),提示RG并不会提高患者的术后并发症发生率,其有利于患者术后的康复。
[1] Torre L A,Bray F,Siegel R L,et al.Global cancer statistics,2012[J].CA Cancer J Clin,2015,65(2):87-108.
[2] Chen W,Zheng R,Zhang S,et al.Report of incidence and mortality in China cancer registries,2009[J].Chin J Cancer Res,2013,25(1):10-21.
[3] Hur H,Jeon H M,Kim W.Laparoscopy-assisted distal gastrectomy with D2 lymphadenectomy for T2b advanced gastric cancers:three years’experience[J].J Surg Oncol,2008,98(7):515-519.
[4] Hwang S I,Kim H O,Yoo C H,et al.Laparoscopic-assisted distal gastrectomy versus open distal gastrectomy for advanced gastric cancer[J].Surg Endosc,2009,23(6):1252-1258.
[5] Giulianotti P C,Coratti A,Angelini M,et al.Robotics in general surgery:personal experience in a large community hospital[J].Arch Surg,2003,138(7):777-784.
[6] Giulianotti P C,Angelini M,Coratti A,et al.Technique de la gastrectomie subtotale robotique[J].J Coelio-Chirurgie,2002,43:55-60.
[7] Kim M C,Heo G U,Jung G J.Robotic gastrectomy for gastric cancer:surgical techniques and clinical merits[J].Surg Endosc,2010,24(3):610-615.
[8] Pugliese R,Maggioni D,Sansonna F,et al.Subtotal gastrectomy with D2 dissection by minimally invasive surgery for distal adenocarcinoma of the stomach: results and 5-year survival[J].Surg Endosc,2010,24(10):2594-2602.
[9] Woo Y,Hyung W J,Pak K H,et al.Robotic gastrectomy as an oncologically sound alternative to laparoscopic resections for the treatment of early-stage gastric cancers[J].Arch Surg,2011,146(9):1086-1092.
[10] Uyama I,Kanaya S,Ishida Y,et al.Novel integrated robotic approach for suprapancreatic D2 nodal dissection for treating gastric cancer:technique and initial experience[J].World J Surg,2012,36(2):331-337.
[11] Yoon H M,Kim Y W,Lee J H,et al.Robot-assisted total gastrectomy is comparable with laparoscopically assisted total gastrectomy for early gastric cancer[J].Surg Endosc,2012,26(5):1377-1381.
[12] Huang K H,Lan Y T,Fang W L,et al.Initial experience of robotic gastrectomy and comparison with open and laparoscopic gastrectomy for gastric cancer[J].J Gastrointest Surg,2012,16(7):1303-1310.
[13] 张小磊,江志伟,赵坤.手术机器人系统与腹腔镜辅助胃癌切除术的临床疗效对比[J].中华胃肠外科杂志,2012,15(8):804-806.
[14] Kim K M,An J Y,Kim H I,et al.Major early complications following open,laparoscopic and robotic gastrectomy[J].Br J Surg,2012,99(12):1681-1687.
[15] Kang B H,Xuan Y,Hur H,et al.Comparison of surgical outcomes between robotic and laparoscopic gastrectomy for gastric cancer:the learning curve of robotic surgery[J].J Gastric Cancer,2012,12(3):156-163.
[16] 刘驰,唐波,郝迎学,等.达芬奇机器人与腹腔镜胃癌手术近期疗效的对照研究[J].第三军医大学学报,2013,35(11):1164-1166.
[17] 赵坤,潘华峰,王刚,等.达芬奇手术机器人与腹腔镜行远端胃癌根治术近期疗效对照研究[J].中国实用外科杂志,2013,33(4):325-327.
[18] Hyun M H,Lee C H,Kwon Y J,et al.Robot versus laparoscopic gastrectomy for cancer by an experienced surgeon:comparisons of surgery,complications,and surgical stress[J].Ann Surg Oncol,2013,20(4):1258-1265.
[19] Zhou J F,Shi Y,Tang B,et al.Robotic gastrectomy versus laparoscopic gastrectomy for gastric cancer:comparison of surgical performance and short-term outcomes[J].Surg Endosc,2014,28(6):1779-1787.
[20] Noshiro H,Ikeda O,Urata M.Robotically-enhanced surgical anatomy enables surgeons to perform distal gastrectomy for gastric cancer using electric cautery devices alone[J].Surg Endosc,2014,28(4):1180-1187.
[21] Kim H I,Park M S,Song K J,et al.Rapid and safe learning of robotic gastrectomy for gastric cancer: multidimensional analysis in a comparison with laparoscopic gastrectomy[J].Eur J Surg Oncol,2014,40(10):1346-1354.
[22] 刘江,阮虎,赵坤,等.达芬奇机器人与腹腔镜行胃癌根治术的对照研究[J].中华胃肠外科杂志,2014,17(5):461-464.
[23] Huang K H,Lan Y T,Fang W L,et al.Comparison of the operative outcomes and learning curves between laparoscopic and robotic gastrectomy for gastric cancer[J].PLoS One,2014,9(10):e111499.
[24] Son T,Lee J H,Kim Y M,et al.Robotic spleen-preserving total gastrectomy for gastric cancer: comparison with conventional laparoscopic procedure[J].Surg Endosc,2014,28(9):2606-2615.
[25] Lee J,Kim Y M,Woo Y,et al.Robotic distal subtotal gastrectomy with D2 lymphadenectomy for gastric cancer patients with high body mass index:comparison with conventional laparoscopic distal subtotal gastrectomy with D2 lymphadenectomy[J].Surg Endosc,2015,29(11):3251-3260.
[26] Kim Y W,Reim D,Park J Y,et al.Role of robot-assisted distal gastrectomy compared to laparoscopy-assisted distal gastrectomy in suprapancreatic nodal dissection for gastric cancer[J].Surg Endosc,2016,30(4):1547-1552.
[27] Shen W,Xi H,Wei B,et al.Robotic versus laparoscopic gastrectomy for gastric cancer:comparison of short-term surgical outcomes[J].Surg Endosc,2016,30(2):574-580.
[28] Park J Y,Ryu K W,Reim D,et al.Robot-assisted gastrectomy for early gastric cancer:is it beneficial in viscerally obese patients compared to laparoscopic gastrectomy?[J].World J Surg,2015,39(7):1789-1797.
