影响γ-Al2O3负载纳米级SO42-/TiO2固体超强酸催化活性的因素的研究
2017-02-27王甫丽薛红丹
王甫丽 张 萍 王 克 刘 朴 薛红丹
(1.河北建筑工程学院,河北 张家口 075000;2.石家庄学院,石家庄 050035)
0 引 言
固体超强酸具有较高的催化活性和选择性,与反应混合物易于分离,无腐蚀、污染少;纳米级材料比表面积大、催化活性高,纳米级固体超强酸兼有固体超强酸和纳米材料二者的优势.笔者在不同硫酸浓度、焙烧温度下制备了γ-Al2O3负载纳米级SO42-/TiO2固体超强酸,并用做乙酸和正丁醇酯化反应催化剂,考察了不同硫酸浓度、焙烧温度对γ-Al2O3负载纳米级SO42-/TiO2固体超强酸比表面积和酸强度的影响.
1 材料与方法
1.1 主要仪器与试剂
表面与孔径测定仪(北京分析仪器厂ST-03A型);傅立叶变换红外光谱仪(日本SHIMADZU 8900型).
冰醋酸,正丁醇,氢氧化钠,硫酸,无水乙醇,氨水,钛酸丁酯,酚酞试液(均为分析纯).γ-Al2O3(直径2 mm,圆柱状).
1.2 制备γ-Al2O3负载纳米级SO42-/TiO2固体超强酸
按照文献[1],制备11.5% TiO2溶胶包覆的γ-Al2O3负载TiO2.首先,将制备的包覆物分别在浓度为0.50 mol/L、0.75 mol/L、1.00 mol/L、2.00 mol/L的硫酸溶液中浸泡1 h;然后,在远红外干燥箱中控制温度为100 ℃干燥1 h;再在马弗炉中分别在350 ℃、450 ℃、550 ℃、650 ℃焙烧3 h,制得γ-Al2O3负载纳米级SO42-/TiO2固体超强酸.
2 结果讨论
2.1 焙烧温度的影响
2.1.1 焙烧温度对酸强度的影响
控制硫酸浓度为1.0 mol/L,分别在350 ℃,400 ℃,450 ℃,500 ℃,550 ℃,650 ℃焙烧制得γ-Al2O3负载SO42-/TiO2样品,检测样品的酸强度.结果见表1.

表1 不同温度下焙烧制得的γ-Al2O3负载纳米级SO42-/TiO2的酸强度
注:1~8号指示剂及其pKa值分别为:1.蒽醌(-8.2)、2.对硝基甲苯(-11.35)、3.间硝基甲苯(-11.99)、4.硝基苯(-12.14)、5.对硝基氯化苯(-12.70)、6.间硝基氯化苯(-13.16)、7. 2,4-二硝基甲苯(-13.80)、8. 2,4-二硝基氟苯(-14.52).
“+”表示指示剂由无色变为黄色,“-”表示指示剂颜色不变,“±”表示指示剂变色不明显
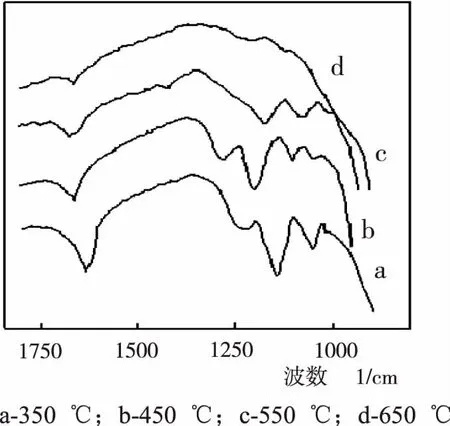
图1 不同焙烧温度SO42- /TiO2的红外光谱图
由表1数据可以看出,在450 ℃时SO42-/TiO2的酸强度最强.究其原因:一方面,焙烧温度太低,材料吸附水含量会增多[2];同时,可能会有不止一个羟基与金属离子连接,分散了诱导效应作用效果,削弱了强质子酸中心的产生.因此,对于确定氧化物,适当提高焙烧温度有助于酸中心集中.另一方面,提高焙烧温度又会使结合不牢固的SO42-脱去,导致酸中心数目减少.所以,焙烧温度过高或过低都对提高酸强度不利,需要选择、控制在合适温度下焙烧.对于二氧化钛,最合适的焙烧温度是450 ℃.
图1是不同焙烧温度下制得的样品的红外光谱.由图1可以看出,b曲线在1 225 cm-1处吸收峰强,说明:焙烧温度是450 ℃时,与TiO2成键的SO42-数目最多.
2.1.2 焙烧温度对比表面积的影响
控制硫酸浓度为1.0 mol/L,分别在焙烧温度350 ℃,450 ℃,550 ℃,650 ℃制得γ-Al2O3负载SO42-/TiO2固体超强酸样品,用表面与孔径测定仪检测样品的比表面积.结果见表2.

表2 不同温度下焙烧制得的γ-Al2O3负载纳米级SO42-/TiO2的比表面积
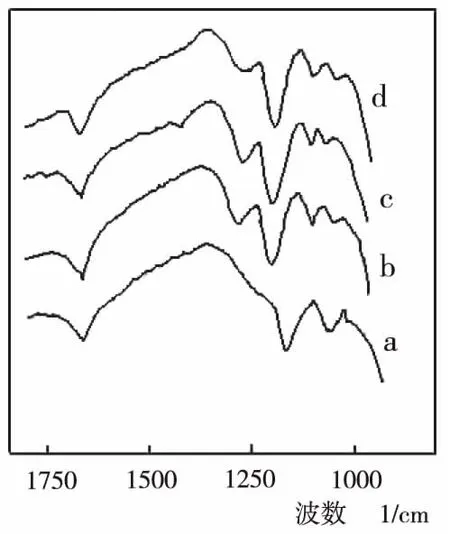
a-0.5 mol/L;b-0.75 mol/L;c-1.0 mol/L;d-2.0 mol/L 图2 不同浓度H2SO4 SO42- /TiO2的红外光谱
由表2可以看出:随着焙烧温度由350 ℃升高到650 ℃,样品的比表面积大幅度减小.这是因为:1、焙烧温度越高,样品聚集度越高,样品粒度增大,从而样品的比表面积大幅度减小.2、随着氧化物TiO2吸附的SO42-数目的增多,氧化物载体的比表面积会增大[3].然而,焙烧温度升高,作用于TiO2表面的部分SO42-会脱附,作用于TiO2表面的SO42-数目减少,所以,焙烧温度升高样品比表面积减小.
2.2 硫酸浓度的影响
2.2.1 硫酸浓度对酸强度的影响
选择焙烧温度为450 ℃,分别用0.5 mol/L、0.75 mol/L、1.0 mol/L、2.0 mol/L浓度的硫酸浸渍,制得γ-Al2O3负载纳米级SO42-/TiO2固体超强酸,用傅立叶变换红外光谱仪测得样品的红外光谱,结果见图2.
由图2可见:1、a、b、c、d四条谱线在980~1 225 cm-1附近处均有四个吸收峰,且谱线b、c较样品谱线a、d在1 225 cm-1处的吸收峰强.这说明:当H2SO4浓度在0.75~1.0 mol/L范围时,有较多的SO42-与金属Ti原子以螯合双配位形式结合[4],形成稳定的超强酸.换言之,当用0.75~1.0 mol/L H2SO4浸渍时SO42-/TiO2的酸强度更大.2、谱线c、d在1 139 cm-1峰强度较大,表明c、d两样品表面酸中心数目更多,主要是因为制备c、d两样品时浸渍用硫酸浓度大[4].综上所述,样品c中,与金属Ti原子结合的SO42-多,且表面酸中心数目也多.所以,制备γ-Al2O3负载SO42-/TiO2固体超强酸合适的H2SO4浓度是1.0 mol/L.
2.2.2 硫酸浓度对比表面积的影响
分别用0.5 mol/L、0.75 mol/L、1.0 mol/L、2.0 mol/L浓度的硫酸浸渍,在450 ℃焙烧,制得γ-Al2O3负载纳米级SO42-/TiO2固体超强酸,用表面与孔径测定仪测定样品的比表面积,结果见表3.
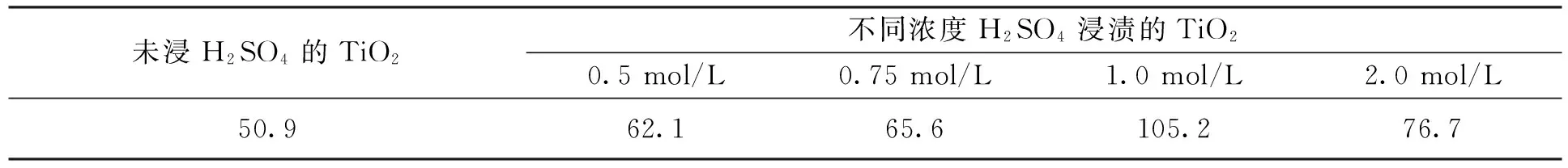
表3 不同浓度H2SO4时γ-Al2O3负载纳米级SO42-/TiO2的比表面积(m2/g)
注:未浸H2SO4的TiO2也在马弗炉内450 ℃焙烧3 h
从表3数据可以看出,用H2SO4浸渍过的样品比未用H2SO4浸渍过的样品的比表面积明显增大;并且,H2SO4浓度由0.5 mol/L增加到1.0 mol/L,样品比表面积由62.1 m2/g增大到105.2 m2/g,但继续增大硫酸浓度,由1.0 mol/L增加到2.0 mol/L,样品比表面积又明显减小,由105.2 m2/g减小到76.7 m2/g.原因可能是:由于TiO2与SO42-结合后SO42-/TiO2表面呈现多孔状结构,所以比表面积增大.但是,当硫酸浓度超过1.0 mol/L时,生成的硫酸盐又堵塞了SO42-/TiO2表面的孔道,导致H2SO4浓度增大到2.0 mol/L,比表面积大幅度地减小到76.7 m2/g.
3 γ-Al2O3负载纳米级SO42-/TiO2超强酸的催化活性
用上述方法制得的γ-Al2O3负载SO42-/TiO2固体超强酸为催化剂,催化冰醋酸和正丁醇的酯化反应.控制醇/酸摩尔比为1.22:1,催化剂用量为4.5%(质量百分数),在120 ℃回流3 h[1],检测乙酸转化率,借助乙酸转化率评价催化剂的催化活性.进一步考察硫酸浓度和焙烧温度对γ-Al2O3负载纳米级SO42-/TiO2的催化活性的影响.
3.1 焙烧温度对γ-Al2O3负载纳米级SO42-/TiO2的催化活性的影响
用1.0 mol/L硫酸浸渍,分别在350 ℃,450 ℃,550 ℃,650 ℃温度下焙烧制得的γ-Al2O3负载纳米级SO42-/TiO2固体超强酸作催化剂,检测乙酸转化率.结果见表4.

表4 不同焙烧温度下制备的γ-Al2O3负载SO42-/TiO2的催化活性
由表4数据可以看出:用450 ℃焙烧制得的γ-Al2O3负载纳米级SO42-/TiO2固体超强酸作催化剂,乙酸转化率最高.结合2.1考察结果,即:用450 ℃焙烧制得的γ-Al2O3负载纳米级SO42-/TiO2固体超强酸比表面积大,酸强度高,催化活性高.
3.2 硫酸浓度对γ-Al2O3负载纳米级SO42-/TiO2的催化活性的影响
分别用焙烧温度为450 ℃、硫酸浓度为0.5 mol/L,0.75 mol/L,1.0 mol/L,2.0 mol/L制得的γ-Al2O3负载纳米级SO42-/TiO2固体超强酸催化乙酸和正丁醇酯化反应,结果见表5.

表5 不同浓度H2SO4浸渍制备的γ-Al2O3负载纳米级SO42-/TiO2的催化活性
由表5数据可以看出:用1.0 mol/L H2SO4浸渍制得的γ-Al2O3负载纳米级SO42-/TiO2固体超强酸作催化剂,乙酸转化率最高.结合2.2考察结果,即:用1.0 mol/L H2SO4浸渍制得的γ-Al2O3负载纳米级SO42-/TiO2固体超强酸比表面积大,酸强度高,催化活性高.
4 结 论
材料的比表面积和酸强度大小直接决定了固体超强酸的催化活性,而焙烧温度和硫酸浓度是影响γ-Al2O3负载SO42-/TiO2固体超强酸的比表面积和酸强度的关键因素.用1.0 mol/L硫酸浸渍、在450 ℃焙烧制得的γ-Al2O3负载纳米级SO42-/TiO2固体超强酸比表面积和酸强度大,催化活性高.
[1]王甫丽,张萍,薛红丹.γ-Al2O3负载纳米级SO42-/TiO2固体超强酸催化合成乙酸正丁酯[J].食品研究与开发,2013,34(9):57~59
[2]唐新硕,王新平,金松寿.SO42-/ZrO2型超强酸中心形成机理研究[J].中国科学(B辑),1994,24(6):584~595
[3]战永复,战瑞瑞.纳米固体超酸SO42-/TiO2的研究[J].无机化学学报,2002,18(5):505~508
[4]张萍,李平,贾振斌,等.纳米级SO42-/TiO2固体超强酸的红外光谱及催化活性[J].精细化工,2003,20(3):160~162
