氘代替代物结合UPLC—MS/MS同步检测去卵巢大鼠血浆中22种内源性大麻素
2017-02-16向世勰徐颖朱晶晶王智民张东陈两
向世勰+徐颖+朱晶晶+王智民+张东+陈两绵+冯伟红

[摘要]该文旨在建立一种超高效液相色谱-串联质谱(UPLC-MS/MS)同步检测去卵巢大鼠血浆中22种内源性大麻素类物质的新方法。首先血浆样品经固相小柱(SPE柱)萃取,然后利用UPLC-MS/MS进行检测。采用ACQUITY UPLC BEH C18色谱柱,以0.1%乙酸溶液为流动相A,乙腈-异丙醇(9∶1)溶液为流动相B,进行梯度洗脱,采用正离子多反应离子监测模式,以氘代试剂作为对照品的替代物计算回收率,同步定量22种内源性大麻素。其中,22种内源性大麻素类物质的线性相关系数均大于0.99,定量限(LOQs)为0.089 6~1.965 2 nmol·L-1;5个氘代替代物的相对回收率为11.40%~129.9%;重复性考察结果显示,RSD均小于8.0%。所建立的方法,可以用于去卵巢大鼠血浆样品中PGF2α EA,AEA等多种内源性大麻素类物质的定性与定量分析,验证了该方法的可行性及实用性。总之,该方法灵敏度高、重复性好、实用性强,可以用于大鼠血浆样品脂质代谢组学研究。
[关键词]高效液相色谱-串联质谱; 内源性大麻素; 氘代替代物
[Abstract]A new method based on ultraperformance liquid chromatography-tandem mass spectrometry(UPLC-MS/MS) was developed for the simultaneous determination of 22 endocannabinoids(eCBs) and relevant compounds in ovariectomized rat plasma. After being extracted by solid-phase column(SPE), the plasma samples were detected by using UPLC-MS/MS. Analysis was carried out with ACQUITY UPLC BEH C18 column. The mobile phase was 0.1% acetic acid solution(A)-acetonitrile and isopropanol(9∶1, B) for the gradient elution. In the positive ion multiple reaction monitoring(MRM) mode, deuterated reagents were taken as standard alternatives to calculate recoveries and simultaneously quantify 22 endocannabinoids. The established method provided a good linearity for the 22 eCBs, and their linearly dependent coefficients were all higher than 0.99. The limits of quantitation(LOQs) ranged from 0.089 6 to 1.965 2 nmol·L-1. Relative recoveries of 5 deuterated surrogates ranged between 11.40% and 129.9%. The repeatability study results showed that RSD was all less than 8.0%. The established method could be used to analyze PGF2a EA, AEA and other endogenous cannabinoids in plasma samples of ovariectomized rats. In summary, this method was proved to boast a high sensitivity, repeatability and practicability, and thus could be used in rat plasma lipid metabolomics study.
[Key words]UPLS-MS/MS; endocannabinoids; deuterated surrogate
doi:10.4268/cjcmm20162122
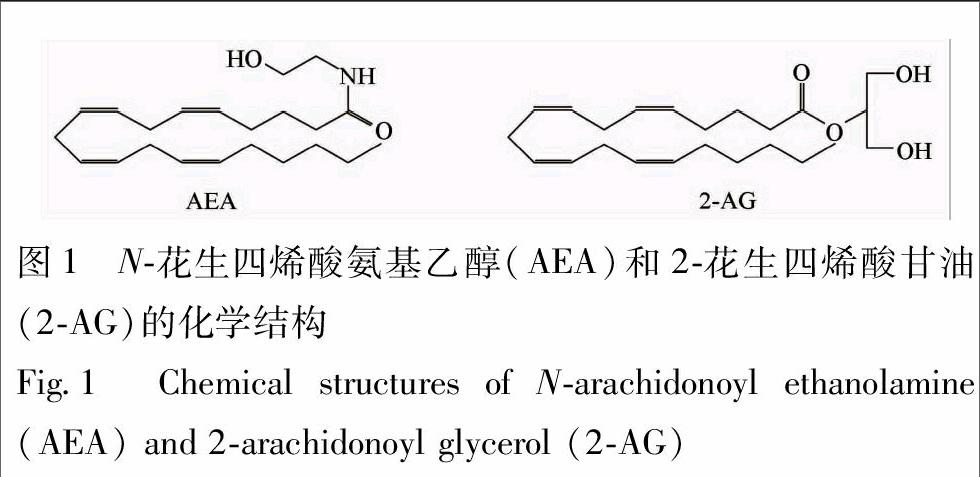
內源性大麻素(endocannabinoids,eCBs)作为内源性脂质介质,能结合和激活大麻素受体(CB1与CB2),在各种不同的生理和病理过程中具有重要作用。与神经保护、记忆、肿瘤、肥胖、免疫功能调节和心血管系统疾病等多种病理、药理作用均有关[1]。eCBs主要是N-花生四烯酸氨基乙醇(anandamine)和2-花生四烯酸甘油(2-AG)2种(化学结构见图1),还包括长链饱和或不饱和脂肪酰胺、酯和醚等不同种类,如:O-花生四烯酸乙醇胺(O-arachidonoyl ethanolamine,O-AEA)[2],2-花生四烯酸甘油酯(2-arachidonoyl glycerol ether,2-AGE)[3]和N-花生四烯酸多巴胺(N-arachidonoyl dopamide,NADA)[4]等。其中AEA和2-AG的生物活性最强,且两者均是环加氧酶(COX-2)作用的底物,在COX-2的氧化下分别形成不同于经典前列腺素的新型前列腺素,如前列腺素甘油酯(prostaglandin glycerol esters, PG-Gs)和前列腺素乙醇胺(prostaglandin ethanolamides, PG-EAs)[5]。PG-Gs包括PGE2-G,PGI2-G,PGD2-G,PGF2α-G和TXA2-G。而PG-EAs由PGE2-EA,PGI2-EA,PGD2-EA,PGF2α-EA和TXA2-EA等组成。
目前,生物样品中内源性大麻素及其代谢产物的分析方法主要有液相色谱-紫外检测法(HPLC-UV),液相色谱-荧光检测法(HPLC-FD)[6-8],气相色谱-质谱法(GC-MS)[9-10],气相色谱串联质谱法(GC-MS/MS)[11],液相色谱-质谱法(LC-MS)[12-13],液相色谱串联质谱法(LC-MS/MS)[14-16]等。内源性大麻素在生物样品中含量很低,而且其化学结构特殊,缺乏必需的发色基团或荧光基团,因此不适于使用紫外或荧光检测器进行分析。GC-MS和GC-MS/MS分析前一般要求样品具有较好的挥发性,且前处理过程复杂,样品回收率低,不适用于生物样品等热不稳定物质的分析。目前,LC-MS和LC-MS/MS仍然是分析生物样品中内源性大麻素及其主要代谢产物的最主要方法。因此,本文采用LC-MS/MS分析技术,采用固相小柱萃取样品前处理方法,并首次使用氘代试剂作为对照品的替代物计算回收率,建立了一种基于UPLC-MS/MS同时定性/定量检测去卵巢大鼠血浆中多种内源性大麻素类物质的新方法。
1 材料
Waters ACQUITY超高效液相色谱仪(美国Waters公司);AB 5500三重四级杆质谱仪(美国AB SCIEX公司);台式高速冷冻离心机(TGL 20MW,湖南赫西仪器装备有限公司);METTLER TOLEDO XSE 105DU型电子分析天平(瑞士梅特勒公司);QL-901型涡旋仪(海门市其林贝尔仪器制造有限公司);PSAN-8氮气发生器(北京中惠普分析技术研究所);GM-1.0A两用型隔膜真空泵(天津津腾公司);Visiprep 24管防交叉污染固相萃取裝置(美国Supelco公司);Oasis HLB 1cc(10 mg)固相萃取小柱(美国Waters公司)。甲醇、乙腈、异丙醇、乙酸(色谱纯,美国Fisher公司);抗氧化剂BHT/EDTA(美国Sigma公司);甘油(美国Sigma公司);内源性大麻素类对照品(美国Cayman公司)。试验用水均为Milli-Q纯水仪制得的双蒸水(德国默克密理博公司)。样品为去卵巢组、假手术组、阳性给药组、七宝美髯方给药组(低、中、高剂量)大鼠血浆。
2 方法
2.1 对照溶液的配制 内标1-cyclohexyl urea 3-dodecanoic acid(CUDA)溶液的配制:精密称取一定量的CUDA于5 mL量瓶中,甲醇定容,作为内标储备液。精密量取上述内标储备液21 μL于10 mL量瓶中,甲醇定容,制备终浓度为6 167.40 nmol·L-1的CUDA内标溶液A,精密量取CUDA内标溶液A 160 μL于10 mL量瓶中,甲醇-乙腈(1∶1)定容,制备得到终浓度为100 nmol·L-1的CUDA内标溶液B,-80 ℃冰箱保存,备用。
内源性大麻素氘代替代物混合液的配制:精密吸取一定量的d8-NA-Gly,d5-2-AG,d4-PGF2α EA,d4-PEA,d8-AEA原液于同一5 mL量瓶中,甲醇定容,得到各物质终浓度分别为6.49,6.26,6.23,6.59,6.19 μmol·L-1,作为混合氘代储备液C,-80 ℃冰箱保存,备用。精密量取1.6 mL上述混合氘代储备液于10 mL量瓶中,甲醇定容,制备终浓度为1 000 nmol·L-1的氘代替代物混合液D,-80 ℃冰箱保存,备用。
内源性大麻素混合对照品溶液的配制:分别精密称取适量的PEA,SEA等7种内源性大麻素类对照品,甲醇定容,配成单标溶液,备用。分别精密量取适量上述7种单标溶液以及LEA,αLEA等15种对照品原液于同一10 mL量瓶中,甲醇定容,得到22个内源性大麻素混合对照品储备液。分别精密吸取上述内源性大麻素混合对照品储备液3,1,0.3,0.08,0.008,0.001 mL,置于10 mL量瓶中,再分别加入适量且等量的CUDA内标溶液A,氘代替代物混合液C,甲醇定容,使各浓度梯度混合对照品溶液中CUDA内标和氘代替代物混合液的终浓度都为100 nmol·L-1,-80 ℃冰箱保存,备用。
2.2 样品预处理 固相萃取小柱(SPE柱)的准备:分别使用乙酸乙酯1 mL,甲醇2 mL对SPE柱进行活化,然后用2 mL酸水溶液1(0.1%乙酸水-甲醇 95∶5)对其进行平衡,备用。样品的准备:精密量取血浆样品100 μL,分别加入抗氧化剂(0.1 g·L-1BHT-EDTA 1∶1)5 μL,5种氘代替代物混合液C 10 μL(浓度为1 000 nmol·L-1),混合均匀后,备用。
样品的处理:上样,加入1 mL酸水1稀释,在自身重力作用下自然洗脱;加入酸水溶液2(0.1%乙酸水-甲醇 7∶3)1 mL,在自身重力作用下自然洗脱;连续抽真空20 min,弃去滤液;分别使用甲醇0.2 mL,乙腈0.5 mL,乙酸乙酯0.7 mL依次冲洗小柱,合并滤液,并加入20%甘油甲醇溶液10 μL,氮气吹干,残留物用100 μL CUDA内标溶液B复溶,6 ℃,12 000 r·min-1离心10 min,吸取上清液,-80 ℃冰箱保存,备用。
2.3 液相色谱及质谱条件 色谱条件:ACQUITY UPLC BEH C18色谱柱(2.1 mm×100 mm,1.7 μm, Part No.186002352);流动相:A相为0.1%乙酸水,B相为乙腈-异丙醇 9∶1,梯度洗脱,0~0.25 min,25%B,0.25~0.5 min,25%~40%B,0.5~1.5 min,40%~50%B,1.5~3 min,50%~55%B,3~3.5 min,55%~80%B,3.5~8 min,80%~85%B,8~9 min,85%~95%B,9~9.25 min,95%B,9.25~9.35 min,95%~100%B,9.35~10.35 min,100%B,10.35~10.5 min,100%~25%B,10.5~12 min,25%B,流速0.25 mL·min-1;柱温60 ℃;进样量5 μL。
質谱条件:离子源为电喷雾离子源(ESI),扫描模式为正离子多反应离子监测(MRM),检测窗口时间范围为0~12 min;碰撞气(CAD)为9 psi(1 psi=6.895 kPa),雾化气(Gas 1)为40 psi,辅助加热气(Gas 2)为40 psi,气帘气(CUR)为30 psi,离子源温度(TEM)为500 ℃,喷雾电压(IS)为-4 500 kV。使用Analyst 1.6软件进行数据采集及处理。
2.4 精密度试验 按照2.1项下方法操作,配制一定浓度的混合对照品溶液,同1 d连续进样3次,记录氘代替代物的峰面积,计算相对标准偏差。
2.5 回收率试验 本试验采用氘代替代物计算回收率。按照2.2项下方法操作,记录样品中氘代替代物的峰面积A,按照2.1项下方法操作,配制一定浓度的混合对照品溶液,检测并记录纯溶剂中氘代替代物的峰面积B,通过比较相同量的氘代替代物在实际样品与纯溶剂中的峰面积之比来考察回收率,即提取回收率=A/B×100%。
3 结果
3.1 方法专属性 分别取加标样品溶液在上述液相色谱-质谱条件下进行检测,22种内源性大麻素、5种氘代替代物及1种内标的提取离子色谱图见图2。d4-PGF2αEA作为PGF2α EA,PGE2 EA,PGD2 EA,PGF2α 1G,PGE2 1G的内标,d8-AEA作为AEA,LEA的内标,d5-2-AG作为2-AG的内标,d8-NA-GLY作为NA-Gly,Dihomo GLA EA,1-AG,2-LG的内标,d4-PEA则为22个中除以上几种内源性大麻素的内标。
3.2 标准曲线与定量限 按上述色谱质谱条件测定所配制的系列对照溶液,标准曲线以待测物浓度为横坐标,待测物与内标峰面积的比值为纵坐标,用加权最小二乘法进行线性回归运算,求得直线回归方程,线性方程、相关系数及线性范围见表1。以大于10倍信噪比(S/N)得出22种内源性大麻素类的定量限。
3.3 精密度和回收率 配制一定质量浓度的混合对照品溶液,同1 d连续进样3次,记录氘代替代物峰面积,计算3次不同测定值的相对标准偏差,结果显示,日内精密度的RSD低于8.0%。通过比较相同量的氘代替代物在实际样品与纯溶剂中的峰面积之比来考察回收率,结果显示,除d8-NA-Gly与d4-PEA回收率较低外,其他氘代替代物回收率都在80%以上,结果见表2。
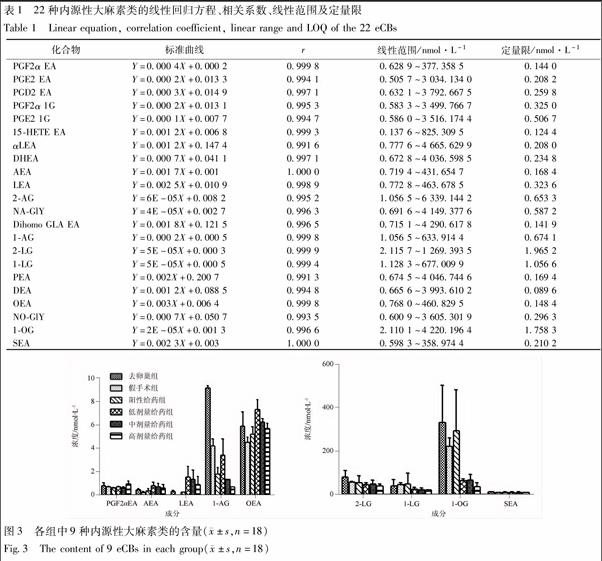
3.4 方法的应用 用上述方法定性定量分析了去卵巢组、假手术组、阳性给药组、七宝美髯方给药组(低、中、高剂量组)大鼠血浆中的内源性大麻素类代谢产物。各组中22种内源性大麻素类的含量结果见图3。在对内源性大麻素类物质定量分析的基础上,采用SIMCA-P 12.0软件,对所测样品数据进行主成分分析(PCA)与偏最小二乘判别(PLS-DA)分析,见图4。试验结果表明,共定性检测到PGF2a EA,PGF2a 1G,αLEA,DHEA,AEA,LEA,2-AG,dihomo GLA EA,1-AG,2-LG,1-LG,PEA,DEA,OEA,NO-Gly,1-OG,SEA等17种内源性大麻素类物质,其中对PGF2a EA,AEA,LEA,1-AG,2-LG,1-LG,OEA,1-OG,SEA等8种物质进行了定量分析。其中1-OG,2-LG,1-LG含量相对较高;且去卵巢组内源性大麻素明显高于其他组。PCA分析与PLS-DA判别分析中可知,去卵巢组与假手术组明显聚为2类,经七宝美髯方给药治疗后,各组中内源性大麻素的成分有不同变化,且给药剂量越高,越接近阳性给药组与假手术组,这些结果表明七宝美髯方具有雌激素样作用,能改善脂质代谢,降低血浆中内源性大麻素的含量。
4 讨论
4.1 样品前处理方法的优化 目前血浆样品的前处理方法有蛋白质沉淀法和固相萃取法,蛋白质沉淀法又叫液液萃取法,其优点是操作简单、快速,缺点是在使用有机溶剂沉淀血浆中蛋白质的同时,部分待测物会包裹其中,与蛋白发生共沉淀,造成待测物的损失。固相萃取法具有回收率高、除杂效果好等优点,不足的是操作相对复杂,而且成本较高。试验比较了利用乙腈、甲醇等作为萃取剂的蛋白质沉淀法和固相萃取法,结果表明固相萃取法对极性较大的内源性大麻素类物质(如DHEA,AEA,LEA)有较高的萃取率,而经乙腈和甲醇处理后的样品中,这3种物质损失较为严重。综合考虑,选择固相萃取进行样品前处理的方法。
4.2 应用氘代替代物 进行内源性物质的检测与分析时,如何准确的计算回收率是一个必须解决的问题。如果采用常规的对照品法进行回收率计算,样品中自身存在的内源性目标分析物会干扰回收率的结果,无法计算得到真实的样品回收率。尤其是当样品中分析物浓度比较低的时候,干扰更大,其回收率计算值往往会高于100%。本试验采用氘代对照品替代实际对照品,进行回收率的考察,有效解决了上述干扰问题。氘代对照品的优势在于它们在样品中不存在,不受样品中本底的干扰,其化学结构、化学性质以及质谱裂解方式均与实际对照品相似,可以用来代替对照品计算回收率。同时还可以有效地消除基质的干扰,降低基质效应的影响,简化试验过程。另外,本试验氘代替代物回收率试验与样品测定试验同步进行,所有样品信息只需采集1次,在完成样品测定的同时,也采集到回收率数据,大大提高了试验效率,也降低了试验
成本,为内源性物质代谢组学的方法学研究提供了一个新的思路。
[参考文献]
[1]Zhou G H, Jin S N, Wen J F. The endocannabinoid system in regulation of cardiovascular function [J].Chin Pharmacol Bull, 2011, 27(7):903.
[2]Porter A C, Sauer J M, Knierman M D, et al. Characterization of a novel endocannabinoid, virodhamine, with antagonist activity at the CB1 receptor [J]. Pharmacol Exp Ther, 2002, 301: 1020.
[3]Hanus L, Abu-Lafi S, Fride E, et al. 2-arachidonyl glyceryl ether, an endogenous agonist of the cannabinoid CB1 receptor [J]. Proc Natl Acad Sci USA, 2001, 98: 3662.
[4]Bisogno T, Melck D, Bobrov M, et al.N-acyl-dopamines: novel synthetic CB(1) cannabinoid-receptor ligands and inhibitors of anandamide inactivation with cannabimimetic activity in vitroandin vivo[J]. Biochem, 2000, 315: 817.
[5]Kozak K R, Prusakiewicz J L, Marnett L J. Oxidative metabolism of endocannabinoids by COX-2 [J]. Curr Pharmaceut Design, 2004, 10: 659.
[6]Arai Y, Fukushima T, Shirao M, et al. Sensitive determination of anandamide in rat brain utilizing a coupled-column HPLC with fluorimetric detection[J].Biomed Chromatogr, 2000, 14:118.
[7]Pisani A, Fezza F, Galati S, et al. High endogenous cannabinoid levels in the cerebrospinal fluid of untreated Parkinson′s disease patients [J]. Ann Neurol, 2005, 57: 777.
[8]Schmidt A, Brune K, Hinz B. Determination of the endocannabinoid anandamide in human plasma by high performance liquid chromatography [J]. Biomed Chromatogr, 2006, 20: 336.
[9]Di Marzo V, Breivogel C S, Tao Q, et al. Levels, metabolism, and pharmacological activity of anandamide in CB(1) cannabinoid receptor knockout mice: evidence for non-CB(1),non-CB(2) receptor-mediated actions of anandamide in mouse brain [J]. Neurochem, 2000, 75: 2434.
[10]Obata T, Sakurai Y, Kase Y, et al. Simultaneous determination of endocannabinoids (arachidonylethanolamide and 2-arachidonylglycerol) and isoprostane (8-epiprostaglandin F2alpha) by gas chromatography-mass spectrometry-selected ion monitoring for medical samples [J]. J Chromatogr B, 2003, 792: 131.
[11]Zoerner A A, Gutzki F M, Suchy M T, et al. Targeted stable-isotope dilution GC-MS/MS analysis of the endocannabinoid anandamide and other fatty acid ethanol amides in human plasma [J]. J Chromatogr B, 2009, 877:2909.
[12]Annuzzi G, Piscitelli F, Di Marino L, et al. Differential alterations of the concentrations of endocannabinoids and related lipids in the subcutaneous adipose tissue of obese diabetic patients [J]. Lipids Health Dis, 2010, 9: 43.
[13]Di Marzo V, Verrijken A, Hakkarainen A, et al. Role of insulin as a negative regulator of plasma endocannabinoid levels in obese and nonobese subjects [J]. Eur J Endocrinol, 2009, 161: 715.
[14]Salomé Gachet M, Gertsch Jürg. Quantitative analysis of arachidonic acid, endocannabinoids,N-acylethanolamines and steroids in biological samples by LC-MS/MS: fit to purpose [J]. J Chromatogr B, 2016, 1012: 215.
[15]Qi Ming, Morena Maria, Vecchiarelli Haley A, et al. A robust capillary liquid chromatography/tandem mass spectrometry method for quantitation of neuromodulatory endocannabinoids [J].Rapid Commun Mass Spectrom, 2015, 29:1889.
[16]Amoako A A, Marczylo T H, Lam P M, et al. Quantitative analysis of anandamide and related acylethanolamides in human seminal plasma by ultra performance liquid chromatography tandem mass spectrometry [J]. J Chromatogr B, 2010, 878: 3231.
[責任编辑 曹阳阳]
