卡巴匹林钙对猪的解热效果及靶动物安全性试验
2017-02-06牛华星冯言言吴连勇
孟 芳 , 牛华星 , 郑 莉 , 林 红 , 冯言言 , 孔 梅 , 吴连勇 , 陈 玲
(1.齐鲁动物保健品有限公司 , 山东 济南 250100 ;2.山东省兽药质量检验所 山东省畜禽产品质量安全监测与风险评估重点实验室 , 山东 济南 250022)
卡巴匹林钙(Carbasalate calcium)为阿司匹林衍生物,最初由荷兰DSM公司研制开发,于1974年由荷兰卫生当局批准生产,目前在国外已批准用于猪、牛、鸡等食品动物的解热镇痛,其安全性高,无残留,无休药期,食品动物可以放心使用[1]。我国于2010年批准用于鸡,2016年批准用于猪,是目前国内惟一获批畜禽专用可口服的解热、镇痛、消炎药[2-3]。本试验研究了卡巴匹林钙在猪上的解热效果,并进行了卡巴匹林钙可溶性粉对猪的靶动物安全性研究。
1 材料与方法
1.1 试验材料 卡巴匹林钙可溶性粉,含量50%,批号1405014,由齐鲁动物保健品有限公司提供;内服给药。阿司匹林片,0.5 g,批号140301,由四川巴尔动物药业有限公司生产。MEK-6138K全自动血液分析仪,魅力1800自动血液生化分析仪。
1.2 解热效果研究方法 选取50头内毒素发热模型造模成功的猪,随机分为5组:发热对照组、卡巴匹林钙可溶性粉低剂量组(20 mg/kg体重)、中剂量组(40 mg/kg体重)、高剂量组(80 mg/kg体重)、阿司匹林对照组,另选10头猪不攻毒为健康对照组,于接种前、用药前、用药后的2、4、6、8、10、12 h分别测量体温,并观察临床症状。
1.3 靶动物安全性评价试验方法
1.3.1 动物分组及给药 选择24头2.5月龄体重25 kg左右的健康长白×大白二元杂交猪随机分为4组,每组6头,分别设为空白对照组,1倍推荐剂量组(40 mg/kg体重)、3倍推荐剂量组(120 mg/kg体重)、5倍推荐剂量组(200 mg/kg体重),对动物进行卡巴匹林钙可溶性粉内服给药,每日1次,连续给药5日。
1.3.2 临床观察 试验期间每天定时观察猪的精神状态、采食饮水、行为、呼吸及粪便等情况,并记录是否有猪只死亡。
1.3.3 血液生理指标检查 给药前、给药结束后1日、10日前腔静脉采血,测定以下血液学指标:红细胞数(RBC)、白细胞数(WBC)、血红蛋白含量(HGB)、血细胞比容(HCT)、平均红细胞体积(MCV)、平均红细胞血红蛋白含量(MCH)、平均红细胞血红蛋白浓度(MCHC)和血小板计数(PLT)。
1.3.4 血液生化指标检查 给药前、给药结束后1日、10日前腔静脉采血,测定以下血液生化指标。包括:丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、总胆红素(T-BIL)、尿酸(UA)、尿素氮(BUN)、肌酐(CREA)、血葡萄糖(GLU)、肌酸激酶(CK)。
1.3.5 病理组织学检查 给药结束后1 d随机宰杀5倍剂量组猪1头,在给药结束后10日随机宰杀1倍剂量组猪、3倍剂量组猪、5倍剂量组猪各1头,采集多种组织器官(肝、肾、胃、肠、心脏、脾脏)制作病理切片,进行肉眼和组织病理学观察。
1.4 数据的分析处理 采用SPSS17.0统计分析软件对猪体温变化、血液生理指标、血液生化指标进行显著性检验。采用t检验比较试验组与对照组间体温、血液生理指标、血液生化指标的差异性。判定标准:P<0.05有显著性差异;P<0.01有极显著差异。
2 结果与分析
2.1 解热效果研究结果 发热对照组在试验过程中表现的主要临床症状是:体温升高,精神沉郁,食欲下降,部分猪只下痢。发热猪内服卡巴匹林钙可溶性粉或阿司匹林后,与发热对照组比较,能迅速解热,体温下降。在内服给药后2 h,大多数猪只的体温显著降低,恢复至较接近正常体温,食欲亦有所恢复。各组猪的体温变化见图1。
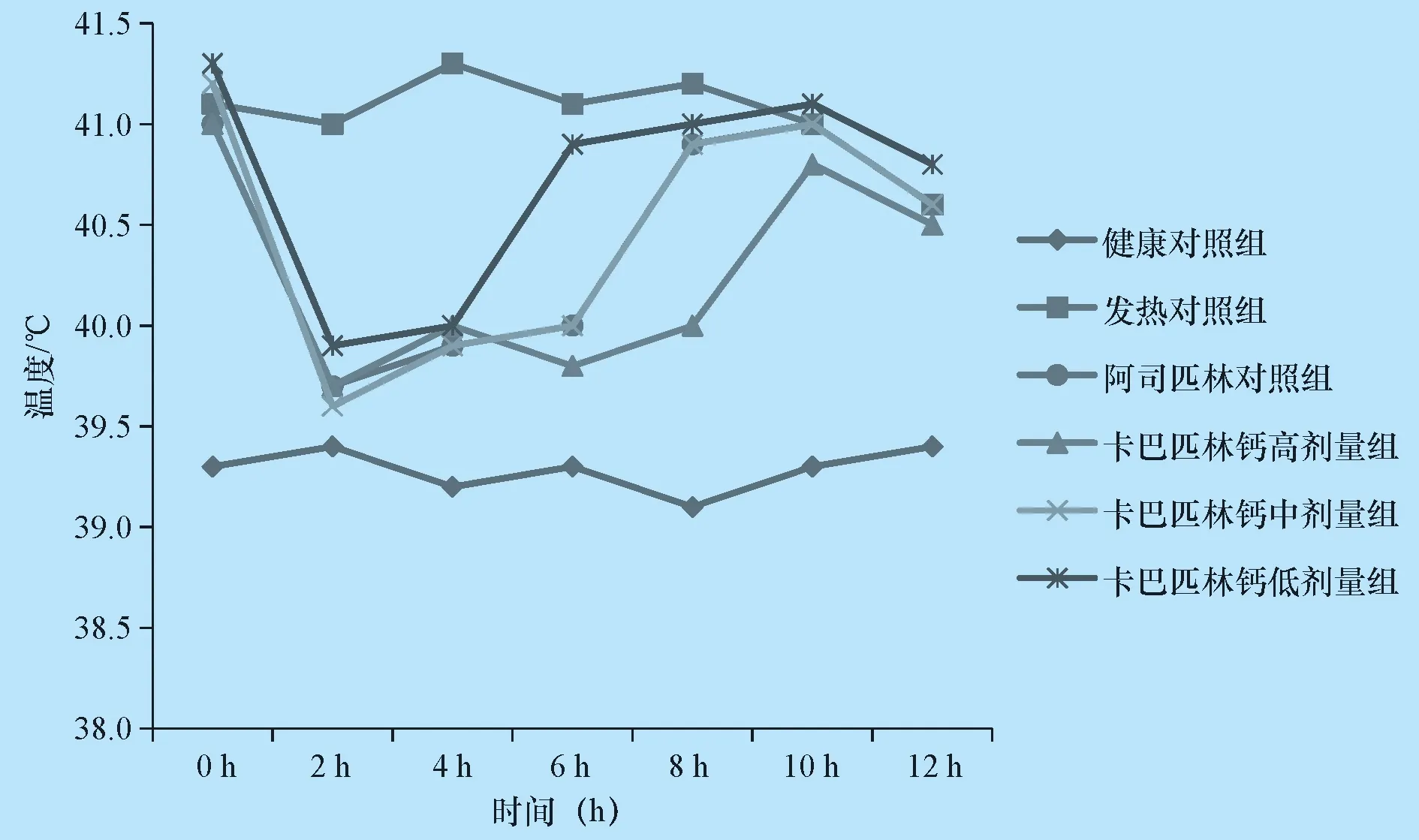
图1 卡巴匹林钙可溶性粉内服给药后发热猪的体温变化
经统计学分析,发热猪内服高剂量卡巴匹林钙(80 mg/kg体重)可溶性粉后2~8 h,其体温显著或极显著低于发热对照组(P<0.05或P<0.01);发热猪内服中剂量卡巴匹林钙(40 mg/kg体重)可溶性粉或阿司匹林(40 mg/kg体重)片后2~6 h,其体温显著或极显著低于发热对照组(P<0.05或P<0.01);发热猪内服低剂量的卡巴匹林钙(20 mg/kg体重)可溶性粉后2~4 h,其体温显著或极显著低于发热对照组(P<0.05或P<0.01)。结果表明,卡巴匹林钙(40 mg/kg体重)可溶性粉及阿司匹林(40 mg/kg体重)片内服给药均对发热猪有较好的解热作用,这种作用至少可维持6 h,二者效果相当,没有显著性差异。
2.2 靶动物安全性评价结果
2.2.1 临床观察结果 从给药第1天到第5天,空白对照组、1倍推荐剂量组猪、3倍推荐剂量组猪、5倍推荐剂量组猪的采食饮水均正常,精神状态正常,未见中毒症状及不良反应,无死亡情况出现。
2.2.2 血液生理指标检测结果
最后一次给药后1日、10日,各剂量组动物与对照组相比,各项指标差异均不显著(表1,表2)。
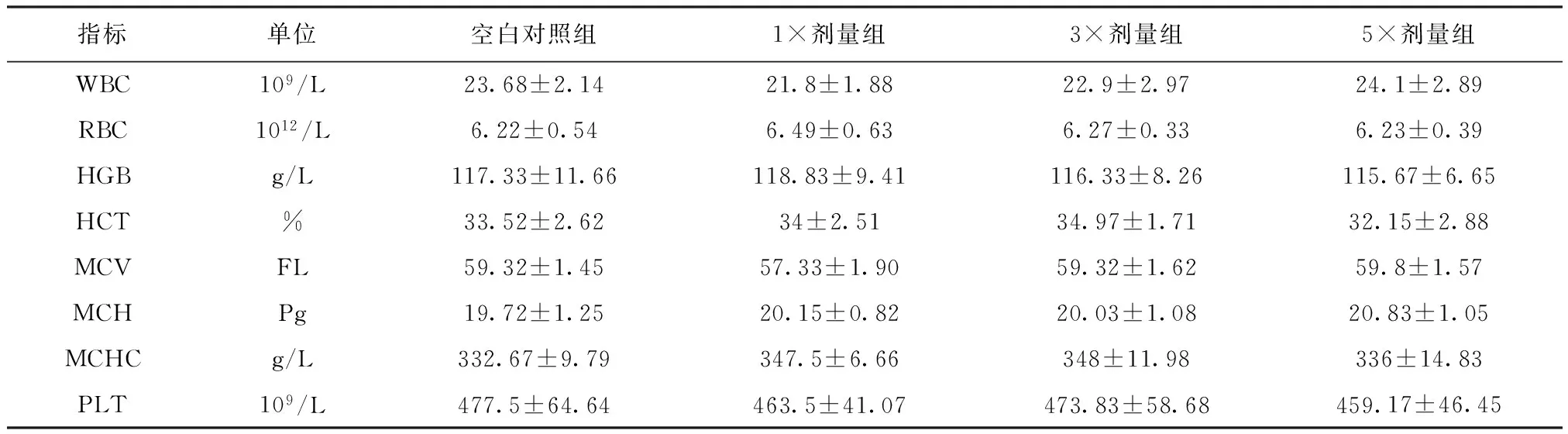
表1 给药后1日各组猪的血液生理指标平均值 (n=6)
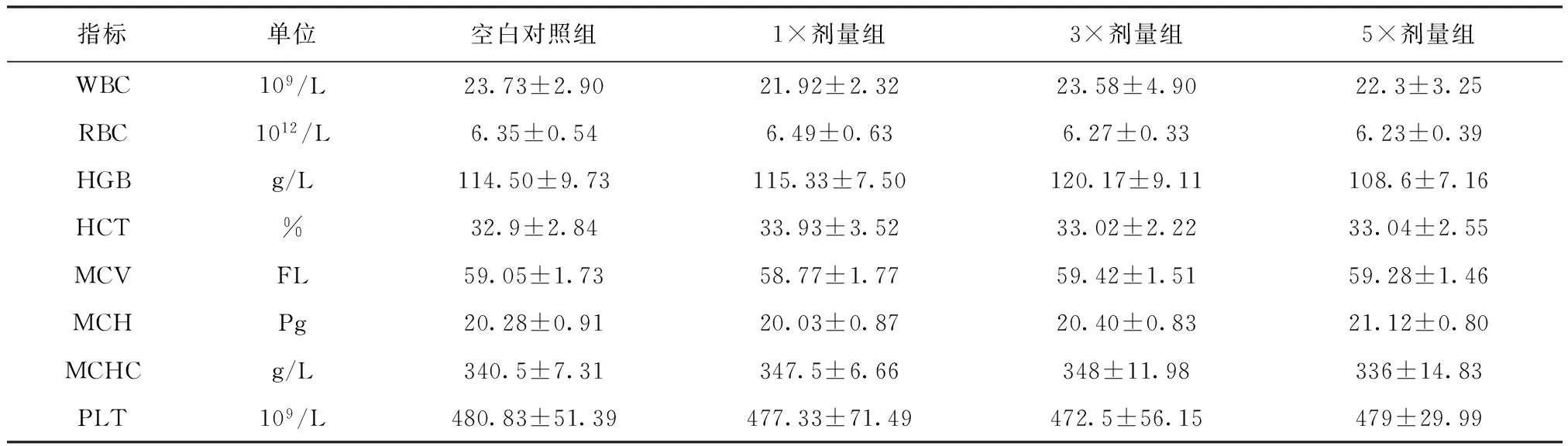
表2 给药后10日各组猪的血液生理指标平均值 (n=6)
2.2.3 血液生化指标检测结果 血液生化指标检测结果见表3、4,统计分析表明,各给药剂量组与空白对照组相比各指标均无显著差异,各剂量组之间差异也不显著。表明卡巴匹林钙可溶性粉对靶动物猪肝脏、肾脏功能无不良影响。
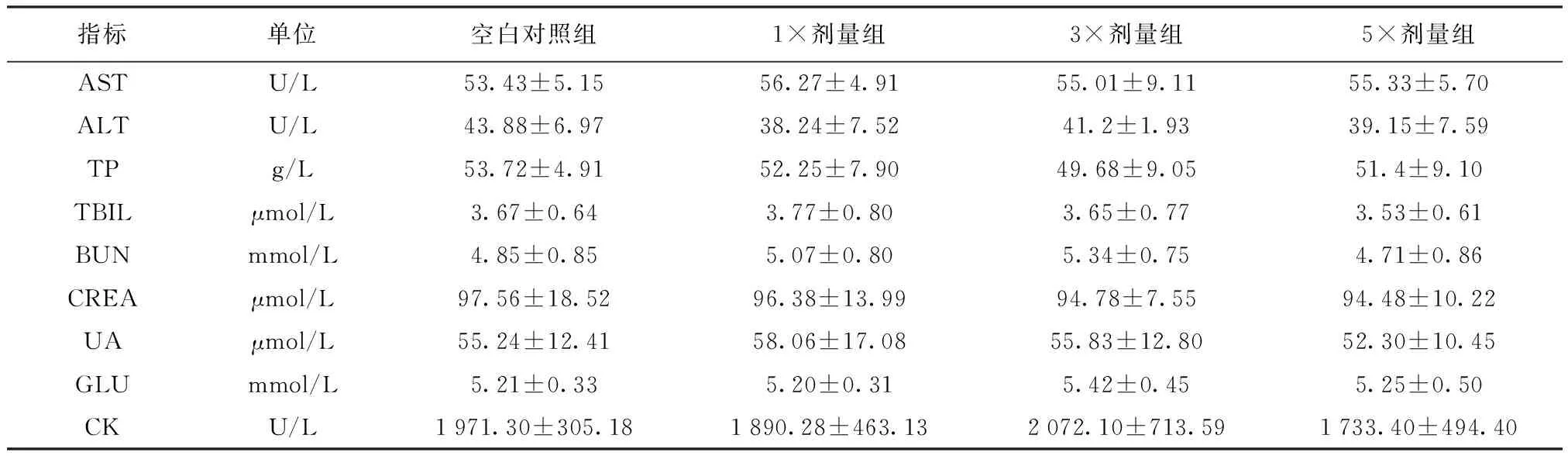
表3 给药后1日各组猪的血液生化指标平均值 (n=6)
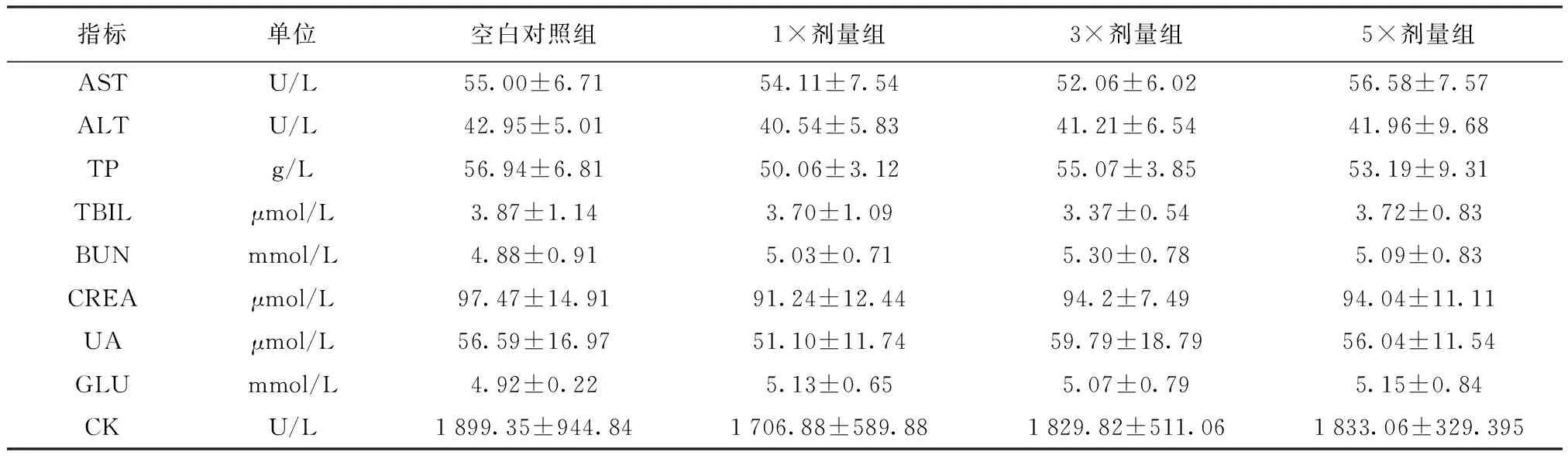
表4 给药后10日各组猪的血液生化指标平均值 (n=6)
2.2.4 病理组织学检查 给药结束后1日,5倍推荐剂量组中随机选取1头猪,剖检采集心、肝、脾、肾、胃、小肠等各部位组织,肉眼观察无病理变化。将各组织切片进行H.E.染色,显微镜镜检观察也无病理变化。给药结束后10日,分别对空白对照组猪、推荐剂量组猪、3倍推荐剂量组猪、5倍推荐剂量组猪中随机选取一头猪,采集心、肝、脾、肾、胃、小肠等各部位组织,肉眼观察无病理变化。将各组织切片进行H.E.染色,显微镜镜检观察也无病理变化。
3 结论与讨论
VMD/HMA批准的产品‘Suispirin,1 000 mg/g,oral powder for pigs’[7]是乙酰水杨酸预混剂,是德国aniMedica GmbH公司于2011.10.18批准上市(上市国家有英国、比利时、法国、德国)用于缓解靶动物猪的发热,其规格为1 g药品含1 000 mg乙酰水杨酸,单次给药剂量为30 mg/kg体重。卡巴匹林钙为乙酰水杨酸衍生物,吸收进入体内之后分解为乙酰水杨酸发挥药效,一分子卡巴匹林钙含两分子乙酰水杨酸,卡巴匹林钙分子量为458.434,乙酰水杨酸分子量为180.16,根据卡巴匹林钙和乙酰水杨酸的分子量折算出卡巴匹林钙的用药量为37.97 mg/kg体重,与本试验结果一致。结合欧盟评估报告[1]中报道的卡巴匹林钙用于猪给药剂量为40~130 mg/kg体重和‘Suispirin,1 000 mg/g,oral powder for pigs’的给药剂量,卡巴匹林钙可溶性粉用于猪的解热,建议临床使用时,以40 mg/kg体重的剂量(以卡巴匹林钙计)内服给药。
该研究中进行卡巴匹林钙可溶性粉连续给药5日后,推荐剂量的1倍、3倍、5倍剂量组与对照组相比,血液生理指标、血液生化指标均无显著性差异,各剂量组之间差异不显著。临床未观察到不良反应,5倍给药组猪剖检,胃肠黏膜、心脏、肾脏、脾脏等组织未见病变。试验表明,卡巴匹林钙可溶性粉对猪的安全性良好。
[1] EMEA/MRL/695/99-FINAL November 1999 COMMITTEE FOR VETERINARY MEDI-CINAL PRODUCTS ACETYLSALICYLIC ACID,SODIUM ACETYLSALICYLATE,ACET-YLSALICYLIC ACID dl-LYSINE AND CARBASALATE CALCIUM SUMMARY REPORT(1).
[2] 中华人民共和国农业部公告第1433号公告.
[3] 中华人民共和国农业部公告第2479号公告.
[4] 陈洪亮,郑文,曾凡宝,等。卡巴匹林钙可溶性粉对内毒素致热肉鸡的解热作用研究[J].中国兽药杂志,2011,45(1):25-27.
[5] 抗菌药物Ⅱ、Ⅲ期临床药效评价试验指导原则.
[6] VICH GL43 GUIDELINE ON TARGET ANIMAL SAFETY FOR VETERINARY PHARMACEUTIDAL PRODUCTS.
[7] PUBLICLY AVAILABLE ASSESSMENT REPORT FOR A VETERINARY MEDICINAL PRODUCT Suispirin,1000 mg/g Oral Powder for pigs.
