甘蔗独脚金内酯生物合成关键基因ScD27的克隆与表达分析
2017-02-05吴转娣刘新龙刘家勇昝逢刚李旭娟刘洪博林秀琴陈学宽苏火生赵培方吴才文
吴转娣刘新龙刘家勇 昝逢刚 李旭娟 刘洪博 林秀琴陈学宽 苏火生 赵培方 吴才文
云南省农业科学院甘蔗研究所 / 云南省甘蔗遗传改良重点实验室, 云南开远661699
甘蔗独脚金内酯生物合成关键基因ScD27的克隆与表达分析
吴转娣**刘新龙**刘家勇 昝逢刚 李旭娟 刘洪博 林秀琴陈学宽 苏火生 赵培方 吴才文*
云南省农业科学院甘蔗研究所 / 云南省甘蔗遗传改良重点实验室, 云南开远661699
独脚金内酯(strigolactones, SLs)是一类新型植物激素, D27基因是独脚金内酯生物合成途径中最上游的调控基因, 且该基因调控SLs的合成是一个可逆的过程。本研究根据水稻、玉米、高粱、二穗短柄草4种禾本科作物的D27基因核苷酸序列保守区域设计引物, 以甘蔗品种ROC22的cDNA为模板, 利用RT-PCR和RACE技术, 从甘蔗中克隆出D27基因的cDNA全长序列, 命名为ScD27, GenBank登录号为KP987221.1。该基因序列全长1379 bp, 包含一个867 bp的完整开放阅读框(ORF), 编码288个氨基酸残基。ScD27编码的蛋白质分子量为71.58 kD, 理论等电点为5.04, 是一种非分泌性蛋白, 主要分布于叶绿体上, 该蛋白的保守区可能具有2个锌指蛋白结构域(ZnF_TAZ和ZnF_A20), 且不存在信号肽; 该基因编码的氨基酸序列具有较高的保守性, 与高粱、谷子、大麦、短穗二柄草等禾本科植物的D27氨基酸序列相似性在70%以上; ScD27基因在甘蔗各组织部位均有表达, 其中茎尖和腋芽中表达量较高,叶、茎和根中的表达较低。此外, ScD27基因在甘蔗茎尖中的表达受PEG、盐胁迫、磷缺乏和营养缺乏的诱导, 推测ScD27基因是甘蔗独脚金内酯生物合成途径中响应非生物胁迫的关键基因。
甘蔗; ScD27; 同源克隆; 生物信息学; q-PCR
农作物的生长发育主要受植物激素的调控, 如作物的株型、水分和营养的利用以及对生物和非生物胁迫的适应性等, 因此植物激素对作物产量的形成与品质的保持发挥至关重要的作用[1]。甘蔗(Saccharum spp.)是世界上最重要的糖料作物, 在其生长发育和逆境胁迫适应过程中受到多种激素信号的调控作用[2-3]。因此, 研究植物激素调控甘蔗重要农艺性状、抗逆性状表现的生理分子机制对于甘蔗品种产量性状的改良具有重要的理论和实践意义。
独脚金内酯(strigolactones, SLs)属于类萜内酯类植物激素, 该激素能够促进寄生植物种子的萌发和植物与共生真菌之间的相互作用, 对于植物的分枝和逆境胁迫调控也具有重要作用[4-6], 前人研究表明, 独脚金内酯是作为第二信使在抑制植物分枝上发挥作用, 当植物营养受到限制时, SLs会在植物的根部生成并促进侧根和根毛的生长, 同时 SLs被运输至植物的出芽位置, 抑制侧芽生长, 从而增加植物根部对无机营养物质的捕获, 减少分蘖对营养的需求[7]。
此外, SLs还具有促进节伸长、加快叶片衰老、促进根毛伸长和次生根生长、增加茎粗度诱导二次生长、响应逆境胁迫等作用[8-10]。迄今, 通过对多种模式植物如拟南芥[11-12]、矮牵牛[13-15]、豌豆[16]、水稻[17-20]等的研究, 初步明确 SLs的合成及信号传导途径在调控植物分枝形成和响应逆境胁迫的功能作用。一系列相关基因也被陆续克隆出来, 如CCD7/D17/HTD1[21]、CCD8/D10[22-23]、D27[20,24-25]、MAX1[26]等基因主要参与独脚金内酯的合成[27]。D14[26,28]、D3[29-30]、D53[31]主要参与独脚金内酯的信号传导途径[32-35], 当具有活性的独脚金内酯与 D14蛋白结合, 诱导D14的构象变化, 使D3和D53结合,以促进 D53蛋白的泛素化, 最终使 D53蛋白降解,独脚金内酯得以正常应答。
在独脚金内酯合成途径中, D27 (DWARF27)是一个叶绿体定位的铁结合蛋白, 为独角金内酯生物合成的一个重要成员, 当D27基因突变后生长素的极性运输增强, 根部分泌液中检测不到独角金内酯,导致分蘖芽向外生长的抑制作用被解除而呈多分蘖表型[18,20]。对水稻 D27基因的研究表明, 它被定位于水稻的第11染色体, 主要在幼叶、腋芽、花序原基、侧根和冠状根中表达, 尤其是在主茎地上部顶端和幼叶以及节和节间的维管束细胞中表达[20]。氨基酸序列的比对分析发现, 从低等的藻类到高等植物广泛存在D27的同源蛋白。
SLs的生物合成受其自身和外部环境条件的共同调节, 植物可能通过调节 SLs合成基因的转录水平来调控SLs的合成和分泌[36-37], SLs还可能通过调控植物的分枝来响应外部环境的胁迫, 如磷胁迫[38]等。研究发现, 在磷缺乏条件下, 三叶草[39]和番茄[40]中SLs的生物合成量大幅提高, 进而导致分枝减少。另有研究发现, 磷缺乏还可能影响SLs的生物活性[6,37]。从拟南芥 max2突变体对干旱胁迫敏感性的研究发现, SLs类似物GR24能够提高SLs缺失突变体对干旱的抵抗能力, 同时也能提高野生型植株的耐旱性[41-42]。SLs不仅可以调控芽的生长, 还能调控初生根、侧根的发育以及根毛的延长, 在逆境条件下(如磷缺乏、干旱和盐胁迫), 植物会通过抑制芽的生长, 增强根系生长, 从而提高植物应对逆境的能力, 最终影响整个植物的形态建成[43-44]。
甘蔗D27基因是否也参与甘蔗品种分蘖形成、形态构建和逆境胁迫响应, 依然是不清楚的。本研究利用基因克隆技术, 从甘蔗中克隆出 D27基因的同系物, 并通过生物信息学和实时荧光定量PCR技术分析其序列结构特点和表达模式, 以期为 SLs对甘蔗品种发育和重要性状的分子调控功能的研究奠定基础。
1 材料与方法
1.1 试验材料及处理
选用我国蔗区种植面积最大的主栽品种ROC22,剪取处于分蘖期的甘蔗茎尖, 提取其总RNA。甘蔗品种 ROC22由云南省甘蔗遗传改良重点实验室提供。大田中选取生长健壮并长势一致的ROC22蔗茎,砍成单芽茎段, 洗净并52℃温水脱毒处理30 min。温室中取 45 d的甘蔗幼苗, 参考李晓君的方法[45],设置6种处理: 即以10% (w/v) PEG-6000的MS培养基; 20% (w/v) PEG-6000的MS培养基; 200 mmol L-1NaCl的MS培养基; 300 mmol L-1NaCl的MS培养基; 1/8 mmol L-1的磷缺乏; 纯水培养(营养缺乏)。于不同处理的不同时间0 (对照)、6、12、24、48、72和96 h取茎尖, 立即投入液氮速冻, 并保存于-80℃, 用于提取总RNA。
1.2 甘蔗茎尖总RNA的提取和cDNA第1链的合成
提取总RNA参照全式金公司RNA Plant Kit说明书, 以RNAase-Free H2O溶解RNA, NanoDrop测定RNA浓度, 根据OD260/OD280和OD260/OD230评估RNA质量, 通过 1%琼脂糖凝胶电泳的结果判断RNA的完整性, 存于-70℃备用。取1 μg茎尖总RNA按照TaKaRa公司的RNA PCR Kit试剂盒说明书合成 cDNA。
1.3 甘蔗ScD27基因同源片段的克隆
以NCBI检索的二穗短柄草(Brachypodium distachyon)、玉米(Zea mays)、高粱(Sorghum bicolor)、水稻(Oryza sativa)的 D27基因序列为模板, 以 DNAman软件分析D27保守区。用Primer5.0软件设计RT-PCR引物(表1)。以cDNA为模板, 使用全式金Trans Taq HiFi DNA Polymerase进行RT-PCR, PCR运行程序为94℃, 3 min预变性, 94℃ 30 s, 56℃ 30 s, 72℃ 45 s, 30个循环, 72℃延伸10 min。PCR产物经1.2%的琼脂糖凝胶电泳检测, 以全式金公司的凝胶回收试剂盒回收、纯化扩增条带, 并连接到pEASYTM-T5 Zero-Vector载体中, 转入DH5α大肠杆菌, 阳性克隆经PCR鉴定后, 送上海生工测序,测序结果经Blast和DNAman 6.0验证比对分析。
1.4 5′和3′端的RACE克隆
根据1.3中的甘蔗ScD27基因同源片段序列设计内外巢基因特异性引物(表1)。按照Clontech Smart Race cDNA Amplification Kit说明书扩增目的基因的 3′和 5′末端。以拼接获得的全长序列为模板, 设计引物扩增 ScD27基因的编码区序列, 扩增条件为94℃, 3 min预变性, 94℃ 30 s, 57℃ 30 s, 72℃ 45 s, 30个循环, 72℃延伸10 min。参见1.3的检测、回收、测序、验证比对分析。
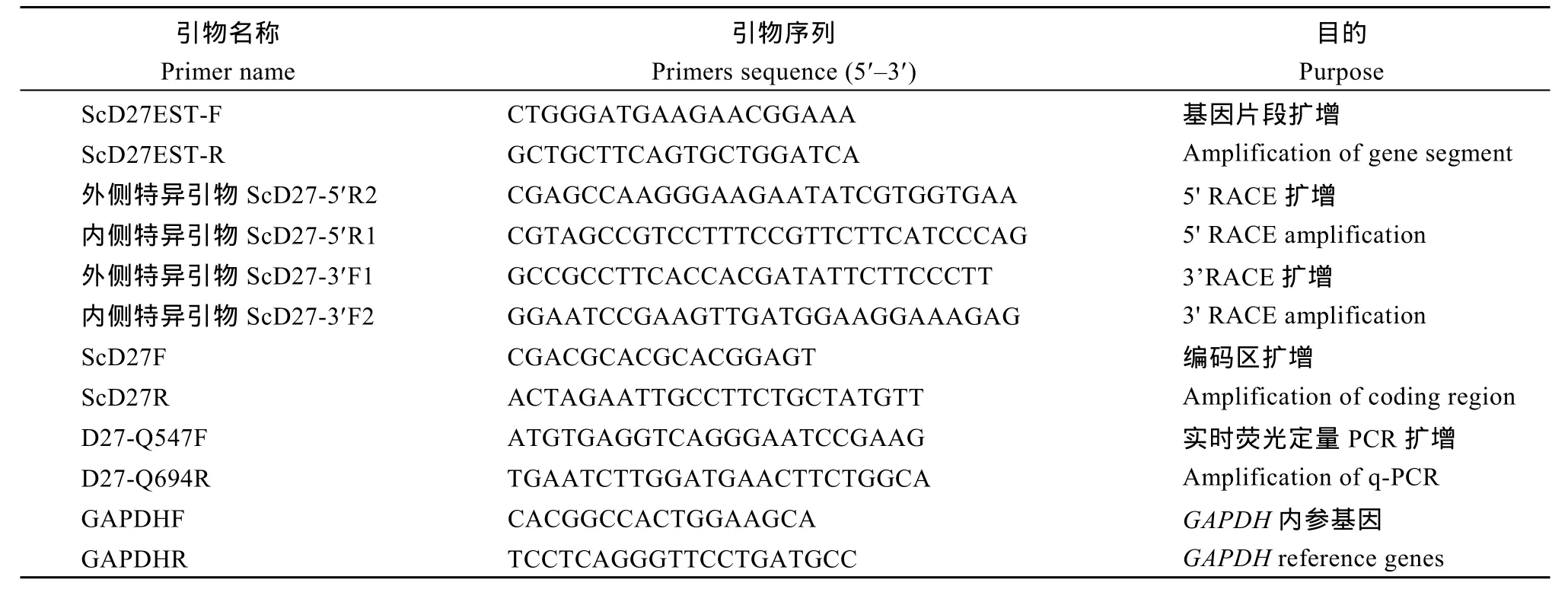
表1 RT-PCR、RACE、荧光定量PCR扩增引物Table 1 Primers used for RT-PCR, RACE, and Q-PCR experiments
1.5 甘蔗ScD27基因的生物信息学分析
使用ORF Finer在线工具寻找编码框; ProtParam (http://web.expasy.ory/ProtParam/)和Smart (http://smart. embl-heidelberg.de/)在线软件分析蛋白的基本理论性质和保守结构域; ProtScale分析蛋白质疏水性; SignalP4.1 (http://www.cbs.dtu.dk/services/SignalP/)、TMHMM Sever2.0 (http://www.cbs.dtu.dk/services/ TMHMM/)和PSORT (http://psort.hgc.jp/)分析蛋白的信号肽和亚细胞定位预测; SOPMA软件预测蛋白的二级结构; NCBI平台进行 Blast同源比对分析, ClustalW软件进行多序列对齐和排序, MEGA5.0构建NJ系统进化树。
1.6 甘蔗 ScD27基因表达的实时荧光定量 PCR分析
取甘蔗的分蘖芽、腋芽、茎尖、根尖、老根、嫩叶、老叶(第四叶中段)、节(第三节)和叶鞘, 提取RNA (方法参考1.2)。根据ScD27基因序列设计荧光定量 PCR引物, 使用 GAPDH作为内参基因[46](表1)。选用TaKaRa公司的PrimeScript RT reagent Kit with gDNA Eraser和SYBR Premix Ex Taq II试剂盒,按其说明书, 定量PCR体系20 μL, 用ABI Vii7Real time PCR System (Applied Biosystems, USA)检测ScD27基因的表达。设置3个重复样品, 利用2-ΔΔCT法计算基因的相对表达量[47]。
2 结果与分析
2.1 甘蔗ScD27基因全长cDNA序列
图1所示, RT-PCR扩增得到长度为477 bp的甘蔗D27基因片段; RACE扩增获得479 bp的3′端序列和670 bp的5′端序列。通过将中间片段、3′端序列和5′端序列拼接, 得到全长为1379 bp的甘蔗D27基因全长 cDNA序列, 使用编码区引物扩增获得867 bp的编码区序列。该基因包含127 bp的5′非编码区、385 bp的3′非编码区和867 bp的编码区, 可编码288个氨基酸, 被命名为ScD27, 并将基因序列提交GenBank数据库, 登录号为KP987221.1。
2.2 甘蔗ScD27的生物信息学分析

图1 PCR产物琼脂糖凝胶电泳图Fig. 1 Agarose gel electrophoresis of PCR products

图2 ScD27基因的编码区序列及推导出的氨基酸序列Fig. 2 Leotide and predicted amino acid sequences of ScD27 gene
2.2.1 ScD27蛋白基本理化性质和保守结构域分析通过ORF Finer在线工具找到ScD27的ORF框,并翻译成氨基酸序列(图2)。使用ProtParam在线软件分析该蛋白序列的理化性质表明, ScD27蛋白的分子式为C2539H4205N867O1033S255, 分子量为71.58 kD,等电点为5.04, Ala、Pro、Ser在氨基酸序列组成中出现频率较高, 分别占10.1%、9.4%、7.3%和8.1%,而一些氨基酸如Pyl、Sec在氨基酸序列中则没有出现。稳定性系数为50.16, 表明为不稳定蛋白(不稳定系数<40是稳定蛋白, >40是不稳定蛋白); 总平均亲水性(GRAVY)为-0.308, 脂肪系数(AI)为 68.79, 说明该蛋白质亲水区域多于疏水区域, 为亲水蛋白。
通过Smart分析表明甘蔗ScD27蛋白在氨基酸序列第190~234之间可能含有一个ZnF_TAZ锌指结构域, 在氨基酸序列第 199~224之间有一个类ZnF_A20锌指结构域, 由于具有相同结构的蛋白往往行使相似的功能[48], 因此推测ScD27蛋白可能参与了其他生物学通路, 与植物调节分蘖来响应非生物胁迫有关。
2.2.2 ScD27蛋白磷酸化和糖基化位点 蛋白质的修饰方式包括蛋白质的磷酸化和糖基化, 它可以调节蛋白质的活力和功能。分别运用DictyOGlyc 1.1 Server 和NetPhos 2.0 Serve在线软件预测ScD27基因翻译后磷酸化、O-糖基化修饰情况。结果显示, ScD27蛋白有可能发生磷酸化修饰的位点有16个,其中色氨酸(Ser)、苏氨酸(Thr)、酪氨酸(Tyr)可能发生磷酸化修饰的位点分别有8、5、3个(图3); 有可能发生 O-糖基化修饰的位点有0个(图4)。磷酸化位点均集中分布在中间亲水区。

图3 ScD27蛋白氨基酸序列翻译后磷酸化修饰位点预测Fig. 3 Prediction of phosphorylation site modification in amino acid sequence of ScD27 protein

图4 ScD27蛋白氨基酸序列翻译后O-糖基化修饰位点预测Fig. 4 Prediction of O-glycosylation site modification in amino acid sequence of ScD27 protein
2.2.3 ScD27蛋白信号肽预测、亚细胞定位和蛋白的二级结构预测 根据 SignalP4.1 server软件预测可知, 该蛋白的信号肽平均值较小, 为 0.217 (远远小于 0.500), 因此推测 ScD27蛋白无信号肽及切割位点, 属于非分泌蛋白, 说明该蛋白在细胞质中合成后不能被转运。根据PSORT II在线软件预测表明ScD27蛋白主要定位于叶绿体上。使用SOPMA软件预测 ScD27蛋白的二级结构(图 5), 该蛋白 α-螺旋(h)占33.6%、β-折叠(e)占14.24%、β-转角(t)占4.86%和无规则卷曲(c) 47.22%。可见α-螺旋和无规则卷曲占据了该蛋白质二级结构的大部分, 进一步分析发现α-螺旋在N端与中部所占分量较大, 延伸链主要集中在中部及 C端, β-转角则主要在中部和前部, 无规则卷曲的分布则比较平均(图 5)。Motif Scan软件在线软件分析该基因含有一个异戊烯化作用位点和一个CAAX BOX结构, 这可能是蛋白质翻译后修饰并正确定位的重要作用元件。
作为蛋白质折叠的主要驱动力, 蛋白质的亲水、疏水氨基酸的组成能够影响蛋白质的结构和特性, 经在线软件 ProtScale采用 Hyhob/Kyte & Doolittle的方法分析显示(图6), 第130位具有最高分值, 为2.367, 疏水性最强; 第36和第37位最低分值, 为-3.067, 亲水性最强。整条多肽链表现为亲水性, 没有明显的疏水区, 故推测甘蔗 ScD27蛋白是一种亲水蛋白。
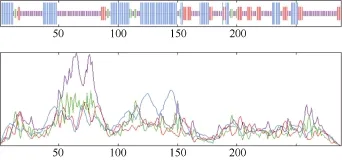
图5 ScD27蛋白质二级结构分析Fig. 5 Secondary structure analysis of ScD27 protein
2.2.4 ScD27蛋白氨基酸序列的同源比对及进化树分析 在NCBI上筛选出与甘蔗ScD27基因氨基酸序列相似性较高的5个不同物种的D27蛋白, 并将其与甘蔗ScD27基因预测的氨基酸序列进行多序列比对。结果显示, ScD27蛋白氨基酸序列与其他D27氨基酸序列有较高的保守性(图7)。
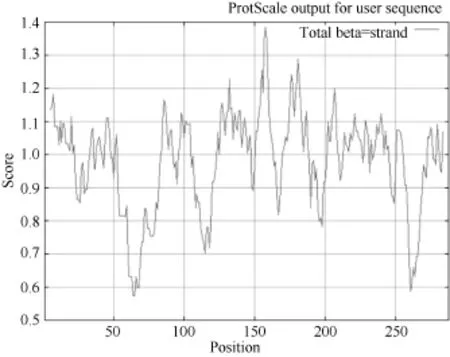
图6 ScD27蛋白的亲水性/疏水性预测Fig. 6 Hydrophobicity/hydrophilicity prediction of ScD27

图7 ScD27与其他五种作物同源蛋白的氨基酸序列比对结果Fig. 7 Structure and sequence alignment analysis among ScD27 and D27 homologs of five cropsgi326492644: 大麦; gi357156309: 二穗短柄草; >gi242068981: 高粱; gi514809530: 谷子; gi226501302: 玉米。gi326492644: Hordeum vulgare subsp. vulgare; gi357156309: Brachypodium distachyon; gi242068981: Sorghum bicolor; gi514809530: Setaria italica; gi226501302: Zea mays.
氨基酸同源比对分析表明 ScD27蛋白与玉米D27蛋白氨基酸序列相似性达到82% (图8), 与单子叶植物高粱(Sorghum bicolor)、谷子(Setaria italicaBeauv.)、大麦(Hordeum vulgare subsp. vulgare)、二穗短柄草(Brachypodium distachyon)和山羊草(Aegilops umbellulata)的相似性分别高达78%、76%、73%、71%和 64%, 与双子叶植物海枣(Phoenix dactylifera)和甜橙(Citrus aurantium)的相似性分别为57%和58%。使用MEGA5.0构建的NJ进化树(图8)显示单子叶植物和双子叶植物D27蛋白同系物分别聚在2个不同的分支, 表明D27蛋白在单双子叶植物间存在一定的分化, 在同类型植物间表现出较高的保守型。在单子叶植物分支群中, ScD27蛋白与谷子、高粱聚为一个小分支, 表现出较高的同源性。

图8 不同物种D27氨基酸序列的聚类分析Fig. 8 Phylogenetic analysis of D27 gene homologs in different plant species
2.3 ScD27基因组织特异性表达分析
qRT-PCR分析表明(图9), 甘蔗ScD27基因在各器官中差异表达, 在分蘖芽、腋芽、茎尖中的表达量相对较高, 根尖、老根、嫩叶、老叶、节和叶鞘中的表达量相对较少。因此, ScD27基因在甘蔗中具有组织特异性, 主要是在甘蔗的幼嫩组织中强表达。
2.4 ScD27基因不同胁迫下的表达分析
q-PCR (quantitative PCR, q-PCR)分析结果表明,在不同胁迫条件下, ScD27基因均被诱导表达, 而响应的方式有一定的差异(图10)。ScD27基因的表达受到PEG强烈诱导, 10% (w/v) PEG-6000的MS培养基处理, 在6个时间点(6、12、24、48、72和96 h)中甘蔗 ScD27基因表达以24 h达最高; 20% (w/v) PEG-6000的MS培养基胁迫下12 h达最高的4倍的表达量, 并在整个处理周期, 96 h内均维持较高的表达水平(3倍以上)。
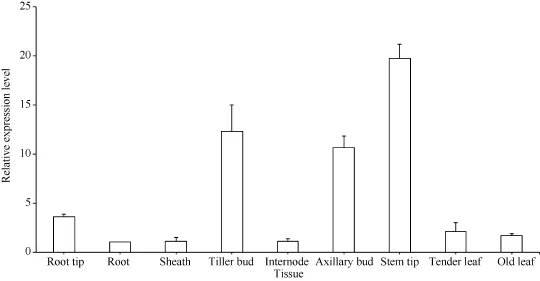
图9 ScD27基因在甘蔗不同组织中的表达Fig. 9 Expression of ScD27 gene in different sugarcane tissues analyzed with q-PCR technique
总体上看, ScD27基因在受到模拟干旱胁迫和中度盐胁迫(以200 mmol L-1NaCl的MS培养基处理)的诱导表达增强, 处理24 h后表达量均出现明显增强, 但在重度盐胁迫(以300 mmol L-1NaCl的MS培养基处理)处理后, ScD27基因的表达量相对增加较少, 可能与蔗苗受极端胁迫有关, 而后期蔗苗出现死亡现象。在磷缺乏和营养缺乏时, ScD27基因同样表现出表达增强, 但与响应模拟干旱和盐胁迫相比, 其表达量增长较少。

图10 ScD27基因在不同胁迫条件下的表达量Fig. 10 Expression level of ScD27 gene under different stress conditions using q-PCR technique
3 讨论
植物激素作为调节植物的分枝数量和模式的重要因素, 其受体鉴定、代谢调控、信号转导和调控发育一直是重要的研究前沿课题。虽然SLs调控植物分蘖的特性研究已经取得了较大的进展, 但更多的调控因子、未知来源的SLs, 和SLs类似物的出现及其重要信号功能, 可能的新的 SLs合成途径的存在, 以及相关基因的调控分子机制还有待进一步阐明[49]。
本研究从甘蔗主栽品种 ROC22中克隆获得了与甘蔗分蘖相关的基因 ScD27基因, 该基因序列全长1379 bp, 其开放阅读框为867 bp, 编码288个氨基酸的蛋白质。研究表明水稻D27基因是一个定位于叶绿体中的含铁蛋白质, 在甘蔗中的 ScD27通过在线分析表明其同样定位于叶绿体[17,54], 该推断还需要进一步的验证。通过同源性分析和进化树分析表明, 甘蔗 ScD27基因的氨基酸序列与谷子、高粱和水稻中 D27蛋白的氨基酸序列同源性较高, 达80%左右, 但与甜橙等双子叶植物的同源性只有58%, 这也从另一方面证明本研究分离获得的ScD27基因序列是正确的, 但氨基酸序列的保守性一般, 推测来源于不同作物的 D27基因在功能上可能存在差异。
植物锌指蛋白是一类庞大的转录调控因子家族,可以通过与核酸或蛋白质结合来行使功能, 参与多个生理过程, 其中植物A20/AN1型锌指蛋白与植物的非生物逆境应答密切相关[50]。甘蔗ScD27基因保守区中含有一个 ZnF_TAZ锌指结构域和一个类ZnF_A20锌指结构域, 推测该结构域的存在与甘蔗ScD27基因参与其他生物学通路相关, 也可能与甘蔗调节分蘖来响应非生物胁迫有关。D27基因是位于独脚金内酯生物合成最上游位置的一个调控基因,其调控作用是一个可逆的过程, 预计基因的研究对于了解独脚金内酯生物合成与植物响应非生物逆境胁迫之间的关系十分重要[44,51], 同时该基因还可能对SLs合成的新途径的研究有重要的作用。
ScD27基因是甘蔗合成独脚金内酯所必需的[25],通过对 ScD27基因在甘蔗组织中的表达, 发现在甘蔗的不同组织部分均能检测到 ScD27基因的表达,但其表达具有较强的组织特异性。在甘蔗茎尖中的表达量最高, 在腋芽、分蘖芽中的表达量次之, 根尖、老根、节和叶鞘中的表达量相对较少。总之, 主要是在幼嫩分生组织处表达。与水稻D27基因的表达较相似[20]。在受到非生物胁迫(PEG、盐、磷、营养)的情况下, 该基因均受到诱导而高表达, 独脚金内酯的生物合成量增多, 地上分蘖减少, 这与前人的研究结果一致[52]。尤其是在受到PEG模拟的干旱胁迫作用下, 其表达量被诱导高达 4倍, 说明该基因可能与干旱或渗透胁迫响应有关, 推测 ScD27基因是甘蔗独脚金内酯响应非生物胁迫的关键基因。
在水稻中D27的表达量可影响SLs对水稻分蘖的调控[18]。d27突变体中D27基因的第4外显子发生4 bp缺失, 提前形成终止密码子, d27突变体株高矮化, 分蘖数增多, 多达野生型的3倍, d27突变体的表型与生长素极性运输增强有关。D27突变之后生长素极性运输增强, 根部分泌液中检测不到独角金内酯 2’-epi-5-deoxystrigol, 导致分蘖芽向外生长的抑制作用被解除, 因此表现出多分蘖表型。d27d10双突变体的表型与水稻突变体d10的表型类似, d27的表型可以被人工合成的独脚金内酯类似物GR24所恢复[20]。ScD27基因在甘蔗中的功能鉴定、亚细胞定位将是本研究的后续的工作, 本课题组已经构建了相应的过表达和RNAi干扰植物表达载体,并开展了农杆菌介导的甘蔗遗传转化的相关工作。通过对转基因甘蔗的非生物胁迫处理可进一步鉴定ScD27在甘蔗SLs生物合成途径中的作用。
4 结论
克隆获得一个全长ORF为867 bp, 编码288个氨基酸的 ScD27基因的全长序列, 该基因编码的蛋白属于亲水性蛋白, 且不存在信号肽。ScD27基因含有一个ZnF_TAZ锌指结构域和一个类ZnF_A20锌指结构域。该基因在甘蔗不同部位的表达具有组织特异性, 在受到多种非生物胁迫的作用下均被诱导表达, 表明它与甘蔗SLs响应非生物胁迫密切相关。
[1] 许智宏, 李家洋. 中国植物激素研究: 过去、现在和未来. 植物学通报, 2006, 23: 433-442
Xu Z H, Li J Y. Plant hormones research in china: past, present and future. Chin Bull Bot, 2006, 23: 433-442 (in Chinese with English abstract)
[2] 王威豪, 王一丁, 莫云川, 叶燕萍, 李杨瑞. 水分胁迫下喷施乙烯利对甘蔗分蘖及农艺性状的影响. 广西农业科学, 2007, (2): 148-151
Wang W H, Wang Y D, Mo Y C, Ye Y P, Li Y Y. Studies on effects of etheph on physiological, biochemical and agronomical characters in sugarcane during tillering stage under water stress. Guangxi Agric Sci, 2007, (2): 148-151 (in Chinese with English abstract)
[3] Vasantha S, Shekinah D E, Gupta C, Rakkiyappan P. Tiller production, regulation and senescence in sugarcane (Saccharum species hybrid) genotypes. Sugar Tech, 2012, 14: 156-160
[4] Gomez-Roldan V, Fermas S, Brewer P B, Puech-Pages V, Dun E A, Pillot J P, Letisse F, Matusova R, Danoun S, Portais J C, Bouwmeester H, Becard G, Beveridge C A, Rameau C, Rochange S F. Strigolactone inhibition of shoot branching. Nature, 2008, 455: 189-194
[5] Klee H. Plant biology: hormones branch out. Nature, 2008, 455: 176-177
[6] Umehara M, Hanada A, Yoshida S, Akiyama K, Arite T, Takeda-Kamiya N, Magome H, Kamiya Y, Shirasu K, Yoneyama K, Kyozuka J, Yamaguchi S. Inhibition of shoot branching by new terpenoid plant hormones. Nature, 2008, 455: 195-200
[7] Koltai H. Strigolactones are regulators of root development. New Phytol, 2011, 190: 545-549
[8] Al-Babili S, Bouwmeester H J. Strigolactones, a novel carotenoid-derived plant hormone. Annu Rev Plant Biol, 2015, 66: 161-186
[9] Rasmussen A, Hosseini S A, Hajirezaei M R, Druege U, Geelen D. Adventitious rooting declines with the vegetative to reproductive switch and involves a changed auxin homeostasis. J Exp Bot, 2015, 66: 1437-1452
[10] Andreo-Jimenez B, Ruyter-Spira C, Bouwmeester H J, Lopez-Raez J A. Ecological relevance of strigolactones in nutrient uptake and other abiotic stresses, and in plant-microbe interactions below-ground. Plant Soil, 2015, 394: 1-19
[11] Alder A, Jamil M, Marzorati M, Bruno M, Vermathen M, Bigler P, Ghisla S, Bouwmeester H, Beyer P, Al-Babili S. The path from beta-carotene to carlactone, a strigolactone-like plant hormone. Science, 2012, 335: 1348-1351
[12] Booker J, Sieberer T, Wright W, Williamson L, Willett B, Stirnberg P, Turnbull C, Srinivasan M, Goddard P, Leyser O. MAX1 encodes a cytochrome P450 family member that acts downstream of MAX3/4 to produce a carotenoid-derived branch-inhibiting hormone. Dev Cell, 2005, 8: 443-449
[13] Simons J L, Napoli C A, Janssen B J, Plummer K M, Snowden K C. Analysis of the DECREASED APICAL DOMINANCE genes of petunia in the control of axillary branching. Plant Physiol, 2007, 143: 697-706
[14] Drummond R S, Martinez-Sanchez N M, Janssen B J, Templeton K R, Simons J L, Quinn B D, Karunairetnam S, Snowden K C. Petunia hybrida CAROTENOID CLEAVAGE DIOXYGENASE 7 is involved in the production of negative and positive branching signals in petunia. Plant Physiol, 2009, 151: 1867-1877
[15] Drummond R S, Sheehan H, Simons J L, Martinez-Sanchez N M, Turner R M, Putterill J, Snowden K C. The expression of petunia strigolactone pathway genes is altered as part of the endogenous developmental program. Front Plant Sci, 2011, 2: 115
[16] Sorefan K, Booker J, Haurogne K, Goussot M, Bainbridge K, Foo E, Chatfield S, Ward S, Beveridge C, Rameau C, Leyser O. MAX4 and RMS1 are orthologous dioxygenase-like genes that regulate shoot branching in Arabidopsis and pea. Genes Dev, 2003, 17: 1469-1474
[17] 王涛. 水稻独脚金内酯相关基因的图位克隆与功能分析. 中国农业科学院博士学位论文, 北京, 2012
Wang T. Map-Based Cloning and Functional Analysis of the Strigolactones-Related Genes in Rice (Orzya sativa L.). PhD Dissertation of Chinese Academy of Agriculture Science, Beijing, China, 2012 (in Chinese with English abstract)
[18] Waters M T, Brewer P B, Bussell J D, Smith S M, Beveridge C A. The Arabidopsis ortholog of rice DWARF27 acts upstream of MAX1 in the control of plant development by strigolactones. Plant Physiol, 2012, 159: 1073-1085
[19] Zhang Y, van Dijk A D, Scaffidi A, Flematti G R, Hofmann M, Charnikhova T, Verstappen F, Hepworth J, van der Krol S, Leyser O, Smith S M, Zwanenburg B, Al-Babili S, Ruyter-Spira C, Bouwmeester H J. Rice cytochrome P450 MAX1 homologs catalyze distinct steps in strigolactone biosynthesis. Nat Chem Biol, 2014, 10: 1028-1033
[20] Lin H, Wang R, Qian Q, Yan M, Meng X, Fu Z, Yan C, Jiang B, Su Z, Li J, Wang Y. DWARF27, an iron-containing protein required for the biosynthesis of strigolactones, regulates rice tiller bud outgrowth. Plant Cell, 2009, 21: 1512-1525
[21] Rubio-Moraga A, Ahrazem O, Perez-Clemente R M, Gomez-Cadenas A, Yoneyama K, Lopez-Raez J A, Molina R V, Gomez-Gomez L. Apical dominance in saffron and the involvement of the branching enzymes CCD7 and CCD8 in the control of bud sprouting. BMC Plant Biol, 2014, 14: 171
[22] 陈芳育, 江良荣, 郑景生, 黄荣裕, 王侯聪. 用蛋白质组遗传方法分析水稻多蘖矮秆突变体的共分离蛋白. 中国遗传学会大会, 厦门大学, 福建厦门, 2011
Chen F Y, Jiang L R, Zheng J S, Huang R Y, Wang H C. Fine mapping and proteomics analysis of a high-tillering dwarf mutant in rice. Congress of Chinese Genetic Society, Xiamen University, Xiamen, China, 2010
[23] Arite T, Iwata H, Ohshima K, Maekawa M, Nakajima M, Kojima M, Sakakibara H, Kyozuka J. DWARF10, an RMS1/MAX4/ DAD1 ortholog, controls lateral bud outgrowth in rice. Plant J, 2007, 51: 1019-1029
[24] Harrison P J, Newgas S A, Descombes F, Shepherd S A, Thompson A J, Bugg T D. Biochemical characterization and selective inhibition of beta-carotene cis-trans isomerase D27 and carotenoid cleavage dioxygenase CCD8 on the strigolactone biosynthetic pathway. FEBS J, 2015, 282: 3986-4000
[25] Wen C, Zhao Q, Nie J, Liu G, Shen L, Cheng C, Xi L, Ma N, Zhao L. Physiological controls of chrysanthemum DgD27 gene expression in regulation of shoot branching. Plant Cell Rep, 2016
[26] Abe S, Sado A, Tanaka K, Kisugi T, Asami K, Ota S, Kim H I, Yoneyama K, Xie X, Ohnishi T, Seto Y, Yamaguchi S, Akiyama K, Yoneyama K, Nomura T. Carlactone is converted to carlactonoic acid by MAX1 in Arabidopsis and its methyl ester can directly interact with AtD14 in vitro. Proc Natl Acad Sci USA, 2014, 111: 18084-18089
[27] Zou J, Zhang S, Zhang W, Li G, Chen Z, Zhai W, Zhao X, Pan X, Xie Q, Zhu L. The rice HIGH-TILLERING DWARF1 encoding an ortholog of Arabidopsis MAX3 is required for negative regulation of the outgrowth of axillary buds. Plant J, 2006, 48: 687-698
[28] 王闵霞, 白玉路, 王平, 向跃武, 蔡平钟, 张志雄. 水稻Dwarf 14(D14)基因的生物信息学分析. 西南农业学报. 2014, 27: 1347-1352
Wang M X, Bai Y L, Wang P, Xiang Y W, Cai P Z, Zhang Z X. Bioinformatics analysis of D14 (dwarf 14) in rice. Southwest China J Agric Sci, 2014, 27: 1347-1352 (in Chinese with English abstract)
[29] Zhao J, Wang T, Wang M, Liu Y, Yuan S, Gao Y, Yin L, Sun W, Peng L, Zhang W, Wan J, Li X. DWARF3 participates in an SCF complex and associates with DWARF14 to suppress rice shoot branching. Plant Cell Physiol, 2014, 55: 1096-1109
[30] Zhao L H, Zhou X E, Yi W, Wu Z, Liu Y, Kang Y, Hou L, de Waal P W, Li S, Jiang Y, Scaffidi A, Flematti G R, Smith S M, Lam V Q, Griffin P R, Wang Y, Li J, Melcher K, Xu H E. Destabilization of strigolactone receptor DWARF14 by binding of ligand and E3-ligase signaling effector DWARF3. Cell Res, 2015, 25: 1219-1236
[31] Soundappan I, Bennett T, Morffy N, Liang Y, Stanga J P, Abbas A, Leyser O, Nelson D C. SMAX1-LIKE/D53 family members enable distinct MAX2-dependent responses to strigolactones and karrikins in Arabidopsis. Plant Cell, 2015, 27: 3143-3159
[32] Arite T, Umehara M, Ishikawa S, Hanada A, Maekawa M, Yamaguchi S, Kyozuka J. d14, a strigolactone-insensitive mutant of rice, shows an accelerated outgrowth of tillers. Plant Cell Physiol, 2009, 50: 1416-1424
[33] Ishikawa S, Maekawa M, Arite T, Onishi K, Takamure I, Kyozuka J. Suppression of tiller bud activity in tillering dwarf mutants of rice. Plant Cell Physiol, 2005, 46: 79-86
[34] Zhou F, Lin Q, Zhu L, Ren Y, Zhou K, Shabek N, Wu F, Mao H, Dong W, Gan L, Ma W, Gao H, Chen J, Yang C, Wang D, Tan J, Zhang X, Guo X, Wang J, Jiang L, Liu X, Chen W, Chu J, Yan C, Ueno K, Ito S, Asami T, Cheng Z, Wang J, Lei C, Zhai H, Wu C, Wang H, Zheng N, Wan J. D14-SCFD3-dependent degradation of D53 regulates strigolactone signalling. Nature, 2013, 504: 406-410
[35] Jiang L, Liu X, Xiong G, Liu H, Chen F, Wang L, Meng X, Liu G, Yu H, Yuan Y, Yi W, Zhao L, Ma H, He Y, Wu Z, Melcher K, Qian Q, Xu H E, Wang Y, Li J. DWARF 53 acts as a repressor of strigolactone signalling in rice. Nature, 2013, 504: 401-405
[36] Brewer P B, Dun E A, Ferguson B J, Rameau C, Beveridge C A.Strigolactone acts downstream of auxin to regulate bud outgrowth in pea and Arabidopsis. Plant Physiol, 2009, 150: 482-493
[37] 贾昆鹏. 植物激素独脚金内酯和茉莉酸信号与光信号互作的分子机制研究. 上海交通大学博士学位论文, 上海, 2014
Jia K P. The Molecular Mechanism of Cross Talking between Light and Phytohormones Strigolactone and Jasmonate Signaling. PhD Dissertation of Shanghai Jiao Tong University, Shanghai, China, 2014 (in Chinese with English abstract)
[38] Kumar M, Pandya-Kumar N, Dam A, Haor H, Mayzlish-Gati E, Belausov E, Wininger S, Abu-Abied M, McErlean C S, Bromhead L J, Prandi C, Kapulnik Y, Koltai H. Arabidopsis response to low-phosphate conditions includes active changes in actin filaments and PIN2 polarization and is dependent on strigolactone signalling. J Exp Bot, 2015, 66: 1499-1510
[39] Yoneyama K, Xie X, Kusumoto D, Sekimoto H, Sugimoto Y, Takeuchi Y, Yoneyama K. Nitrogen deficiency as well as phosphorus deficiency in sorghum promotes the production and exudation of 5-deoxystrigol, the host recognition signal for arbuscular mycorrhizal fungi and root parasites. Planta, 2007, 227: 125-132
[40] Lopez-Raez J A, Charnikhova T, Gomez-Roldan V, Matusova R, Kohlen W, De Vos R, Verstappen F, Puech-Pages V, Becard G, Mulder P, Bouwmeester H. Tomato strigolactones are derived from carotenoids and their biosynthesis is promoted by phosphate starvation. New Phytol, 2008, 178: 863-874
[41] Bu Q, Lv T, Shen H, Luong P, Wang J, Wang Z, Huang Z, Xiao L, Engineer C, Kim T H, Schroeder J I, Huq E. Regulation of drought tolerance by the F-box protein MAX2 in Arabidopsis. Plant Physiol, 2014, 164: 424-439
[42] Ha C V, Leyva-Gonzalez M A, Osakabe Y, Tran U T, Nishiyama R, Watanabe Y, Tanaka M, Seki M, Yamaguchi S, Dong N V, Yamaguchi-Shinozaki K, Shinozaki K, Herrera-Estrella L, Tran L S. Positive regulatory role of strigolactone in plant responses to drought and salt stress. Proc Natl Acad Sci USA, 2014, 111: 851-856
[43] Yamaguchi S, Kyozuka J. Branching hormone is busy both underground and overground. Plant Cell Physiol, 2010, 51: 1091-1094
[44] Sun H, Tao J, Liu S, Huang S, Chen S, Xie X, Yoneyama K, Zhang Y, Xu G. Strigolactones are involved in phosphate- and nitrate-deficiency-induced root development and auxin transport in rice. J Exp Bot, 2014, 65: 6735-6746
[45] 李晓君. 甘蔗逆境相关锌指蛋白基因ShSAP1的功能研究. 海南大学博士学位论文, 海南海口, 2012
Li X J. Functional Analysis of Stress Associated Zinc Finger Protein Gene ShSAP1 from Sugarcane. PhD Dissertation of Hainan University, Haikou, China, 2012 (in Chinese with English abstract)
[46] 阙友雄, 许莉萍, 徐景升, 张积森, 张木清, 陈如凯. 甘蔗基因表达定量PCR分析中内参基因的选择. 热带作物学报, 2009, 30(3): 274-278
Que Y X, Xu L P, Xu J S, Zhang J S, Zhang M Q, Chen R K. Selection of control genes in Real-time qPCR analysis of gene expression in sugarcane. Chin J Trop Crops, 2009, 30(3): 274-278 (in Chinese with English abstract)
[47] 谢晓娜, 杨丽涛, 王盛, 张小秋, 李杨瑞. 甘蔗 NADP异柠檬酸脱氢酶基因(SoNADP-IDH)的克隆与表达分析. 中国农业科学, 2015, 48: 185-196
Xie X N, Yang L T, Wang S, Zhang X Q, Li Y Y. Cloning and expression analysis of sugarcane NADP+-dependent isocitrate dehydrogenase (SoNADP-IDH) gene. Sci Agric Sin, 2015, 48: 185-196 (in Chinese with English abstract)
[48] Vij S, Tyagi A K. Genome-wide analysis of the stress associated protein (SAP) gene family containing A20/AN1 zinc-finger(s) in rice and their phylogenetic relationship with Arabidopsis. Mol Genet Genom, 2006, 276: 565-575
[49] Waldie T, Mcculloch H, Leyser O. Strigolactones and the control of plant development: lessons from shoot branching. Plant J, 2014, 79: 607-622
[50] 李晓君, 武媛丽, 孔冉, 杨本鹏, 张树珍. 植物A20/AN1型锌指蛋白基因功能研究进展. 生物技术通报, 2013, 29(12): 6-14
Li X J, Wu Y L, Kong R, Yang B P, Zhang S Z. Functional Research of A20/AN1 type zinc finger protein gene in plants. Biotechnol Bull, 2013, 29(12): 6-14 (in Chinese with English abstract)
[51] Mayzlish-Gati E, De-Cuyper C, Goormachtig S, Beeckman T, Vuylsteke M, Brewer P B, Beveridge C A, Yermiyahu U, Kaplan Y, Enzer Y, Wininger S, Resnick N, Cohen M, Kapulnik Y, Koltai H. Strigolactones are involved in root response to low phosphate conditions in Arabidopsis. Plant Physiol, 2012, 160: 1329-1341
[52] Yoneyama K, Yoneyama K, Takeuchi Y, Sekimoto H. Phosphorus deficiency in red clover promotes exudation of orobanchol, the signal for mycorrhizal symbionts and germination stimulant for root parasites. Planta, 2007, 225: 1031-1038
Cloning and Expression Analysis of Key Gene ScD27 in Strigolactones Biosynthesis Pathway
WU Zhuan-Di**, LIU Xin-Long**, LIU Jia-Yong, ZAN Feng-Gang, LI Xu-Juan, LIU Hong-Bo, LIN Xiu-Qin, CHEN Xue-Kuan, SU Huo-Sheng, ZHAO Pei-Fang, and WU Cai-Wen*
Sugarcane Research Institute, Yunnan Academy of Agricultural Sciences / Yunnan Key Laboratory of Sugarcane Genetic Improvement, Kaiyuan 661699, China
Strigolactones (SLs) is a novel class of plant hormones. D27 regulating reversible metabolic process is located in up-stream of strigolactones biosynthesis pathway. In this study, primers were designed based on the conserved domains from four species inluding Oryza sativa, Zea mays, Sorghum bicolor, and Brachypodium distachyon. Using cDNA from sugarcane cultivar ROC22 as the template, the full-length cDNA sequence of D27 gene from sugarcane was cloned by RT-PCR and RACE method. This gene is named as ScD27, with the GenBank accession number of KP987221.1. Its length is 1379 bp, and it contains an 867 bp open reading frame (ORF), encoding 288 amino acid residues. ScD27 is not a secretory protein and has a molecular weight of 71.58 kD, with a theoretical isoelectric point of 5.04. ScD27 is mainly located in chloroplast and the conserved domains of this protein involve two zinc finger protein structures (ZnF_TAZ and ZnF_A20). Amino acid sequences encoded by ScD27 shared more than 70% similarity with the reported amino acid sequences encoded by D27 of Sorghum bicolor, Setaria italica Beauv.,Hordeum vulgare subsp. vulgare and Brachypodium distachyon. ScD27 gene was differentially expressed in different parts of sugarcane plant, with higher level of transcript in stem tip and axillary bud but much lower level in leaf, stem and root. Furthermore, the expression of ScD27 could be induced by the stresses of PEG, salt and the deficiencies of phosphorus and nutrition. These results demonstrated that ScD27 might be a key gene participating in the response to abiotic stresses during sugarcane SLs biosynthesis pathway.
Sugarcane; ScD27; Homology cloning; Bioinformatics; q-PCR
10.3724/SP.J.1006.2017.00031
本研究由国家自然科学基金项目(31360359), 国家现代农业产业技术体系建设专项(CARS-20-1-1), 云南省中青年学术技术带头人后备人才(2014HB038), 云南省应用基础研究计划项目(2016FB071), 重大科技专项-生物(2015ZA001)和科技创新人才计划(2014HC015)资助。
This study was supported by the National Natural Science Foundation of China (31360359), the National Modern Agricultural Industry Technology System Construction Project (CARS-20-1-1), the Young and Middle-aged Academic Technology Leaders Reserve Talented Person in Yunnan Province (2014HB038), the Applied Basic Research Projects in Yunnan Province (2016FB071), the Major Science and Technology Projects - Biology (2015ZA001), and the Science and Technology Innovation Talents Project (2014HC015).
*通讯作者(Corresponding author): 吴才文, E-mail: gksky_wcw@163.com**同等贡献(Contributed equally to the work)
联系方式: 吴转娣, E-mail: judith1123@126.com; 刘新龙, E-mail: lxlgood868@163.com
稿日期): 2016-01-11; Accepted(接受日期): 2016-09-18; Published online(
日期): 2016-09-28.
URL: http://www.cnki.net/kcms/detail/11.1809.S.20160928.0948.006.html
