重组人白介素-11治疗化疗引起的血小板减少症的临床观察
2017-01-06李建华唐小万陈莉莉台州市第一人民医院血液肿瘤内科浙江台州318020
黄 辉,章 展,李建华,唐小万,陈莉莉(台州市第一人民医院血液肿瘤内科,浙江台州 318020)
重组人白介素-11治疗化疗引起的血小板减少症的临床观察
黄 辉*,章 展,李建华,唐小万,陈莉莉(台州市第一人民医院血液肿瘤内科,浙江台州 318020)
目的:观察重组人白介素-11治疗由化疗引起的血小板减少症的临床疗效及安全性。方法:选取化疗引起的血小板减少症患者86例,按随机数字表法分为对照组和观察组,各43例。对照组患者输注血小板10 IU,2~3 d 1次;观察组患者给予注射用重组人白介素-11,25~50 μg/kg,qd。两组患者均治疗14 d。观察两组患者临床疗效及治疗前后血小板计数,并比较两组患者血小板减少持续与恢复时间,以及不良反应发生情况。结果:观察组患者临床总有效率为81.40%,显著高于对照组的62.79%,差异有统计学意义(P<0.05)。两组患者治疗前血小板计数比较,差异无统计学意义(P>0.05);治疗后,两组患者血小板计数均显著升高,且观察组显著高于对照组,差异均有统计学意义(P<0.05)。观察组患者血小板<50×109L-1持续时间,恢复至70×109L-1和100×109L-1时间均显著短于对照组,差异均有统计学意义(P<0.05)。两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。结论:重组人白介素-11治疗化疗引起的血小板减少症有较好的疗效,能明显改善患者血小板计数,缩短血小板减少持续与恢复时间,且安全性较好。
血小板减少症;重组人白介素-11;临床疗效;安全性
化疗是各种肿瘤术后治疗的有效方式,大部分细胞毒性化疗药物单用或者联用都会引起不同程度的不良反应[1]。其中多数药物会造成骨髓抑制,导致患者白细胞、中性粒细胞、血小板等血细胞计数的减少,从而使机体抵抗力下降,这些不良反应都会直接或者间接地影响患者的化疗效果和预后[2]。重组人白介素-11(rhIL-11)属于一种促血小板生长因子,可直接刺激造血干细胞和巨核细胞的增殖分化,增加体内血小板的生成,从而提高血液中血小板计数,而血小板功能无明显改变[3]。rhIL-11用于血小板减少症是临床治疗化疗引起骨髓抑制的主要手段之一。本研究观察了rhIL-11治疗由化疗引起的血小板减少症的临床疗效及安全性,以期为临床提供参考。
1 资料与方法
1.1 纳入与排除标准
纳入标准:(1)化疗所致血小板减少者;(2)血小板减少分级为Ⅲ、Ⅳ级;(3)卡氏(KPS)评分>70分,预计生存期>3个月。
排除标准:(1)无骨髓抑制表现者;(2)血液疾病患者;(3)肝肾功能不全者;(3)明显心肺疾病者;(4)对本研究药物过敏者。
1.2 研究对象
选择我院2014年1月-2015年11月化疗引起的血小板减少症患者86例,按随机数字表法分为对照组和观察组,各组43例。两组患者性别、年龄、体质量、血小板减少分级等一般资料比较,差异均无统计学意义(P>0.05),具有可比性,详见表1。本研究方案经医院医学伦理委员会批准,患者知情同意并签署知情同意书。
1.3 治疗方法
对照组患者输注血小板每次10 IU,2~3 d 1次;观察组患者给予注射用重组人白介素-11(齐鲁制药有限公司,批准文号:国药准字S20030016,规格:1.5 mg/支)每次25~50 μg/kg,qd。两组患者均治疗14 d后评价疗效。
表1 两组患者一般资料比较(±s)Tab 1 Comparison of general information between 2 groups(±s)

表1 两组患者一般资料比较(±s)Tab 1 Comparison of general information between 2 groups(±s)
组别对照组观察组t/χ2P n 43 43性别,例男22 23 0.332>0.05女21 20年龄,岁51.34±4.32 52.11±3.12 3.632>0.05体质量,kg 63.82±7.35 62.42±6.26 5.235>0.05血小板减少分级,例Ⅲ级28 30 2.342>0.05Ⅳ级15 13
1.4 观察指标及疗效评价标准
(1)观察两组患者临床疗效。疗效评价标准[4]——完全反应(CR):治疗后血小板计数≥100×109L-1且没有出血;有效(R):治疗后血小板计数≥30×109L-1,至少比基础血小板数量增加2倍,且没有出血;无效(NR):治疗后血小板计数<30× 109L-1或者血小板计数增加不到基础值的2倍或者有出血;复发:有以下情况之一者,①患者CR后,血小板计数<100×109L-1或者出血;②患者CR后,血小板计数<30×109L-1或者血小板计数增加不到基础值的2倍或者有出血。总有效=完全反应(CR)+有效(R)。(2)观察两组患者治疗前后血小板计数及血小板减少持续与恢复时间,并观察治疗期间不良反应发生情况。
1.5 统计学方法
采用SPSS 20.0软件对数据进行统计分析。计数资料以例或率表示,采用χ2检验;计量资料以±s表示,采用t检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较
观察组患者总有效率为81.40%,显著高于对照组的62.79%,差异有统计学意义(P<0.05),详见表2。

表2 两组患者临床疗效比较Tab 2 Comparison of clinical efficacies between 2 groups
2.2 两组患者治疗前后血小板计数比较
治疗前,两组患者血小板计数比较,差异无统计学意义(P>0.05);治疗后,两组患者血小板计数显著升高,且观察组显著高于对照组,差异均有统计学意义(P<0.05),详见表3。
表3 两组患者治疗前后血小板计数比较(±s ,×109L-1)Tab 3 Comparison of platelet count between 2 groups before and after treatment(±s ,×109L-1)
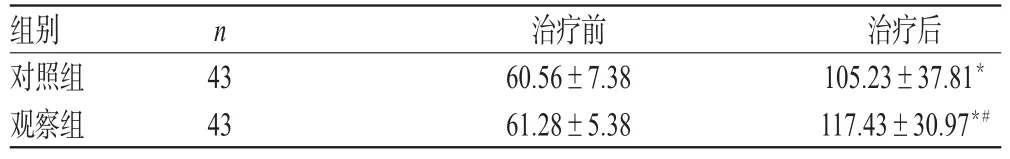
表3 两组患者治疗前后血小板计数比较(±s ,×109L-1)Tab 3 Comparison of platelet count between 2 groups before and after treatment(±s ,×109L-1)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.control group,#P<0.05
治疗后105.23±37.81*117.43±30.97*#组别对照组观察组n 43 43治疗前60.56±7.38 61.28±5.38
2.3 两组患者血小板减少持续时间比较
观察组患者血小板<50×109L-1持续时间、恢复至70×109L-1和100×109L-1时间均显著短于对照组,差异均有统计学意义(P<0.05),详见表4。
2.4 不良反应
观察组患者有低热表现2例、眩晕头昏4例、轻度皮疹1例,不良反应发生率为16.28%;对照组患者发热3例、轻度皮疹3例,不良反应发生率为13.95%。两组患者不良反应发生率比较,差异无统计学意义(P>0.05)。上述不良反应程度均较轻,停药后均能自行恢复正常。
表4 两组血小板减少持续时间比较(±s ,d)Tab 4 Comparison of the duration of platelet decreasing between 2 groups(±s,d)

表4 两组血小板减少持续时间比较(±s ,d)Tab 4 Comparison of the duration of platelet decreasing between 2 groups(±s,d)
组别对照组观察组n 43 43 t P<50×109L-17.11±1.57 5.35±1.34 2.123<0.05 70×109L-111.85±2.53 7.11±3.12 4.342<0.05 100×109L-120.32±4.51 15.16±3.87 6.324<0.05
3 讨论
癌症患者术后化疗中极易发生骨髓抑制现象,临床表现为中性粒细胞、白细胞、血小板等血细胞计数不同程度地减少。骨髓抑制是剂量限制性毒性,发生率为50.0%~91.3%[5],而血小板减少会引起全身皮肤紫癜、鼻衄或女性月经过多、疲乏无力、面色苍白、尿色加深,偶尔还可见肾脏受损征象如血尿、氮质血症等[6]。
白细胞介素(IL)-11是骨髓基质细胞产生的一种多功能细胞因子,具有促进造血干细胞和巨核祖细胞增殖、诱导巨核细胞成熟、促进血小板生成等作用[7-8]。近年来研发的rhIL-11是一种具有178个氨基酸的活性蛋白。已经有研究证明,rhIL-11能有效治疗各种原因诱发的骨髓巨核系造血功能不良或衰竭所致的血小板减少[6],且在其作用下,体内发育成熟的巨核细胞超微结构是正常的,形成的血小板的形态、功能和寿命均与正常的血小板相同。目前,rhIL-11已获得美国食品与药物管理局(FDA)的批准,用于治疗接受化疗的实体瘤和淋巴瘤患者,促进其血小板生成[2]。rhIL-11用于治疗恶性肿瘤或急性白血病患者化疗后血小板减少症,可以减轻化疗后血小板减少的程度,缩短血小板减少持续时间,加快血小板恢复速度,从而减少患者对血小板输注的需求[9-10]。
本研究结果显示,观察组患者总有效率显著高于对照组,说明rhIL-11治疗血小板减少症具有良好的疗效;治疗后,观察组患者血小板计数显著高于对照组,观察组血小板<50×109L-1持续时间、恢复至70×109L-1和100×109L-1时间均明显短于对照组,差异均有统计学意义(P<0.05),提示rhIL-11能增加血小板计数,缩短血小板恢复时间,从而减少相关出血并发症的发生。
应用rhIL-11治疗血小板减少症,常见的不良反应有全身性副作用(如水肿、头痛、中性粒细胞减少性发热)、心血管系统副作用(如心动过速、血管扩张、心悸、晕厥等)、神经系统副作用(如眩晕、失眠)、呼吸系统副作用(如呼吸困难、咽炎等)及其他(如皮疹、视力减退、视物模糊等)[2]。本研究中,两组患者不良反应发生情况比较,差异无统计学意义(P>0.05),且程度均较轻,说明其安全性较好。
综上所述,rhIL-11治疗化疗引起的血小板减少症有较好的疗效,能明显改善患者血小板计数,缩短血小板减少持续与恢复时间,且安全性较好。但本研究样本较小,观察时间较短,有待大样本、多中心、较长随访时间的试验观察其远期疗效。
[1] 詹启敏,陈杰.细胞周期与肿瘤转化医学[J].中国肿瘤临床,2014,41(1):1.
[2] Nash RA,Seidel K,Storb R,et al.Effects of rhIL-11 on normal dogs and after sublethal radiation[J].Exp Hematol,1995,23(5):389.
[3] 毛建平,王莹,贾韬,等.重组人白细胞介素-11治疗重型再生障碍性贫血血小板减少的临床观察[J].中国现代医学杂志,2016,26(7):116.
[4] 杨仁池.免疫性血小板减少症的命名、定义与疗效评价的标准化:关于ITP国际工作组报告的解读[J].中华血液学杂志,2009,30(3):215.
[5] Paul SR,Benett F,Calvetti JA,et al.Molecular cloning of a cDNA encoding interleukin-11,a stromal cell-derived lymphopoietic and hematopoietic cytokine[J].Proc Natl Acad Sci U S A,1990,87(19):7 512.
[6] 郭立仪,邓明辉.重组人粒细胞集落刺激因子治疗化疗后骨髓抑制的疗效分析[J].中国现代药物应用,2014,8(4):106.
[7] 刘霄,彭睿,柳海燕,等.重组人白介素-11治疗放化疗后血小板减少的临床观察[J].贵州医药,2015,39(9):806.
[8] 袁振宁.肿瘤化疗前应用重组人粒细胞集落刺激因子预防白细胞减少临床研究[J].生物技术世界,2015(9):18.
[9] 刘红,赵挺.重组人白介素-11治疗急性髓系白血病化疗后血小板减少的疗效观察[J].陕西医学杂志,2014,43(6):747.
[10] Taguchi K,Saitoh M,Arai Y,et al.Disparate effects of interleukin-11 and thrombopoietin on megakaryocytopoiesis in vitro[J].Cytokine,2001,15(15):241.
Clinical Observation of Recombinant Human Interleukin-11 in the Treatment of Chemotherapy-induced Thrombocytopenia
HUANG Hui,ZHANG Zhan,LI Jianhua,TANG Xiaowan,CHEN Lili(Dept.of Hemntology and Onclology,Taizhou First People’s Hospital,Zhejiang Taizhou 318020,China)
OBJECTIVE:To observe clinical efficacy and safety of recombinant human interleukin-11(rhIL-11)in the treatment of chemotherapy-induced thrombocytopenia.METHODS:86 patients with thrombocytopenia induced by chemotherapy were selected and divided into control group and observation group according to random number table,with 43 cases in each group.Control group was given platelet transfusion 10 IU,once every 2-3 d;observation group was given Recombinant human IL-11 for injection 25-50 μg/kg,qd.Both groups received treatment for 14 d.Clinical efficacies of 2 groups were observed as well as platelet count before and after treatment.The duration of platelet decrease and recovery,the occurrence of ADR were compared between 2 groups.RESULTS:The total effective rate of observation group was 81.40%,which was significantly higher than 62.79%of control group,with statistical significance(P<0.05).There was no statistical significance in platelet count between 2 groups before treatment(P>0.05);after treatment,platelet count of 2 groups increased significantly,and the observation group was significantly higher than the control group,with statistical significance(P<0.05).The duration of platelet count<50×109L-1,the time of platelet count recovering to 70×109L-1and 100×109L-1in observation group were significantly shorter than in control group,with statistical significance(P<0.05).There was no statistical significance in the incidence of ADR between 2 groups(P>0.05).CONCLUSIONS:rhIL-11 shows good therapeutic efficacy in the treatment of chemotherapy-induced thrombocytopenia,and can significantly improve platelet count,shorten the duratione of platelet decrease and recovery with good safety.
Thrombocytopenia;Recombinant human interleukin-11;Clinical efficacy;Safety
R558+.2
A
1001-0408(2016)35-4998-03
*住院医师。研究方向:恶性血液病的诊治及研究。电话:0576-84230185。E-mail:souleren@163.com
2016-01-02
2016-06-20)
(编辑:黄 欢)
DOI10.6039/j.issn.1001-0408.2016.35.34
