聚乳酸两亲性共聚物的研究进展
2017-01-03张玡珂张婧伟胡志国
张玡珂,张婧伟,胡志国*
(1.河南师范大学 化学化工学院,河南 新乡 453007; 2.河南师范大学 环境学院,河南 新乡 453007))
聚乳酸两亲性共聚物的研究进展
张玡珂1,张婧伟2,胡志国1*
(1.河南师范大学 化学化工学院,河南 新乡 453007; 2.河南师范大学 环境学院,河南 新乡 453007))
聚乳酸是一种具有良好的生物相容性和可降解性高分子材料,也是被美国食品和药品管理局(FDA)批准的生物医用材料.但它本身的疏水性使其在医用方面受到限制.为克服其缺陷,人们对聚乳酸做了大量改性修饰的工作以提高亲水性,如将其与各种亲水性聚合物进行聚合制得不同结构类型的两亲性共聚物.本文中我们对聚乳酸两亲性共聚物的研究进展做了综述,并讨论了它的应用现状及前景.
聚乳酸;两亲性共聚物;生物医用材料
聚乳酸(PLA)由于其可降解性和生物相容性且降解产物能参与人体的新陈代谢,以及其性能可在大范围内通过与其他单体共聚得到调节等特点,已成为生物降解医用材料领域中最受重视的材料之一.但PLA 材料具有以下缺点:1)含有大量的酯基,使其表现出高疏水性,材料表面缺少可反应的活性基团,对细胞的粘附能力差;2)由于其降解速度受很多条件的影响,使其降解速度难以控制,同时其降解产物乳酸偏酸性,对细胞的亲和性差,在人体内降解后,会造成肌体局部酸性积累等现象[1];3)由于其载药微粒在经静脉注射入血液中后会被单核吞噬细胞系统(MPS)中的巨噬细胞吞噬,会影响其血液循环的时间.这些限制了聚乳酸在生物医用材料领域的的应用.为了调节其物理化学性能,增加亲水性,人们通过在 PLA 分子链中引入亲水性的单体或聚合物单元进行共聚改性,合成了一系列线形和非线形具有特定结构的聚乳酸两亲性共聚物,这极大地拓宽聚乳酸的应用范围,具有重要的现实意义.
1 聚乳酸两亲共聚物结构类型
聚乳酸两亲性嵌段共聚物是目前研究热点,其中亲水性链段需要具有生物相容性好、柔性、低毒及低免疫原性等特性.常用的亲水性链段有聚乙二醇(PEG)、葡聚糖(Dextran)、壳聚糖衍生物马来酰化壳聚糖(NMCS)、聚乙烯吡咯烷酮(PVP)等.其中聚乙二醇(PEG)是最常用的,是被FDA认可的医用聚合物材料.常用的制备方法[2]包括活性阴离子聚合、基团转移聚合、开环歧化聚合、活性阳离子聚合、活性/可控自由基聚合以及活性中心转变法和嵌段共聚物化学改性法.通过控制嵌段共聚物亲水链段和PLA链段的比例可调节共聚物的HLB值、降解速度以及在选择性溶剂中的自组装性能.
1.1 线形聚合物
1.1.1 两嵌段聚合物
GOPFERICH等[3]用聚乙二醇单甲醚与聚乳酸聚合得到了二嵌段的共聚物,研究了成骨细胞在材料上的粘附、增殖、分化等行为,发现亲水的链段能够调节蛋白质的吸附,从而改善细胞繁殖能力.宋继彬等[4]合成了一端具有氨基,可修饰靶向分子的功能化端氨基聚乙二醇-聚乳酸嵌段共聚物(α-H2N-PEG-b-PLA).他们采用阴离子开环聚合,酸解去除氨基保护基团后成功得到了一系列端氨基聚乙二醇-聚乳酸嵌段共聚物(α-H2N-PEG-b-PLA),随后用界面沉积法制备了H2N-PEG-b-PLA胶束和负载噻唑烷酮药物(CDBT)的聚合物胶束,通过表征发现其有规则的球形核壳结构,药物缓释实验表明载药聚合物胶束具有良好的缓释作用.此外也发现H2N-PEG-b-PLA经修饰后具有极好的多重靶向功能.
WU等[5]通过D,L-PLA的开环聚合,N-乙烯基己内酰胺(NVCL)的自由基聚合,以及随后的点击反应合成了热敏性嵌段共聚物PNVCL-b-PLA.荧光技术表明这种聚合物可自组装为纳米胶束,并且随疏水嵌段的增加溶液的CMC值降低,胶束变小,另外,透射电子显微镜显示胶束呈球形.
TUCKING等[6]报道了一种新型的透明质酸HYA和PLA的两亲嵌段共聚物.其合成是由铜催化的1, 3偶极环加成进行的.HYA-PLA在水中可自组装成囊泡结构,原发性皮肤微血管内皮细胞的细胞毒性实验证实这种两嵌段纳米微粒具有生物相容性.
1.1.2 三嵌段聚合物
三嵌段聚合物目前也有很多研究成果,ABEBE等[7]合成了ABA型的聚合物PLLA-PEG-PLLA.GANG等[8]采用油/水型溶剂挥发法制备了含紫杉醇的PLA、PLGA和PLA-PEG-PLA微球,具体步骤是先将紫杉醇溶解于PLA或PLGA的二氯甲烷溶液中,将此溶液迅速倾入2%的PVA水溶液中,磁力搅拌(800 r/ min) 2 h,使二氯甲烷完全挥发、过滤、收集形成的微球,用蒸馏水洗涤,干燥即得.
YANG等[9]制备了三嵌段聚合物PLLA-b-PEG-b-PLLA的花状胶束(图1),这种花状胶束可由三嵌共聚物PLLA-b-PEG-b-PLLA在主链上与双硫键自组装而成.三嵌段共聚物PLA3000-PEG2000-PLA3000和PLA3000-PEG4000-PLA3000在水中分别可以自组装为平均直径是110 nm和43 nm的胶束,与双嵌段共聚物相比,它们的临界胶束浓度(CMC)较低,分别是0.017 g/L和0.014 g/L.此外,以DOX为模型药物,体外药物释放分析表明该还原环境可导致靶向药物释放.MTT法体外检测结果表明即使浓度高达1 000 g/L,胶束内孵育的NIH3T3细胞仍未表现出明显的细胞毒性.另外,荧光显微镜测试和MTT法测试均表明与二嵌段共聚物相比,对于细胞内的还原响应,三嵌段共聚物自组装成的胶束表现出更快的药物释放速度和更高的细胞增殖抑制能力.
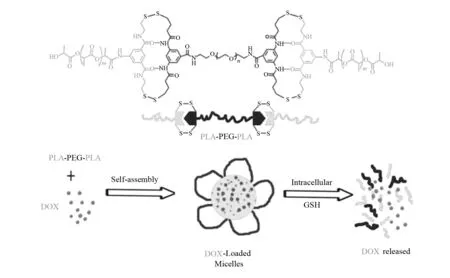
图1 PLLA-b-PEG-b-PLLA 的花状胶束
LI等[10]以羟基化的PEG为前体,采用原位依次加入法,通过开环聚合反应制得了ABC型共聚物PEG-b-PDLLA-b-PMPC.他们的合成中没有选择传统的Sn(Oct)2或 Zn(Et)2作为催化系统,而是使用Salan型稀土金属烷基催化剂,发现催化效果更优.研究发现经叠氮化修饰后聚合物具有聚集诱导发光效应(AIE),聚合物可进行自组装,并且有良好的光学性能,因此可应用于生物成像技术和化学传感器.
1.1.3 多嵌段聚合物
LI等[11]以己二酰氯为偶联剂制备了聚乙二醇-聚乳酸多嵌段共聚物,它具有较高的相对分子质量和PEG含量,有较强的力学性能和较高的吸水量,可用来制备水凝胶.
CRAPARO等[12]制备了一种半乳糖基化多嵌段两亲聚合物.首先以RhB,PLA以及荧光衍生物α,β-聚丙烯酸-2-羟乙酯(PHEA)反应得PHEA-RhB-PLA.然后PHEA-RhB-PLA与GAL-PEG-NH2反应得PHEA-RhB-PLA-PEG-GAL.
1.2 非线形聚合物
非线形两亲聚合物以其独特的结构和化学性质在各个方面得到广泛应用.下面将对比较有代表性的星形、树枝形和超支化类型聚合物作介绍.
1.2.1 多臂星型聚合物
星型聚合物是一种支化聚合物,各条链之间无主、支链区分.星型共聚物与线型相比,由于其三维立体结构,具有较小的流体力学体积,因此其溶液具有更低的黏度,并且有望解决胶束尺寸与稳定性不可兼得的问题[13].
SALAAM 等[14]研究表明聚乙二醇-聚乳酸四臂星型共聚物具有比线型共聚物更好的热稳定性和更快的降解速率.因此这种结构的两亲性共聚物制备的胶束也具有较低的临界胶束浓度,从而更加稳定.LU等[15]分别以多羟基(2、4和8)封端的 PEG 为引发剂,合成了一系列杠铃型的共聚物(PLGA)n-b-PEG-b-(PLGA)n(n=1,2,4).研究结果显示,随着这种共聚物中 PLGA 臂数的增加或臂长的降低, 共聚物的降解速率会加快, 其热性能也随结构的变化而改变.另外,HU等[16]合成了以β-环糊精为中心的三臂星形聚合物(mPEG2k-PLA3k)3-CD,以DOX-HCl为模型药物,发现这种结构聚合物具有低渗透性和高负载能力,在水溶性药物运输中将发挥巨大作用.其合成路线如图2所示.
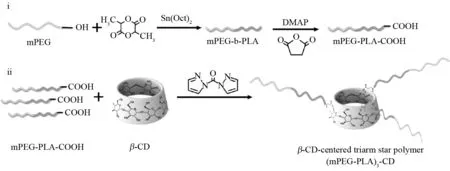
(i) Ring-opening polymerization and carboxylation to get mPEG-PLA-COOH; (ii) Conjugation of mPEG-b-PLA-COOH to β-CD.图2 (mPEG-PLA)3-CD的合成路线
PAN等[17]通过聚乳酸和环氧乙烷的开环聚合构建四臂星形聚合物(star-PLA-PEO)包载紫杉醇,与同相对分子质量的线形聚合物胶束相比,特殊的星形结构使该载药胶束具有更高的稳定性、更长的降解时间(超过3 w),更持续的药物释放(超过2 w)和更彻底的体内清除.
张安强等[18]以不同臂数和相对分子质量的星型聚乙二醇(sPEG)和L-丙交酯为原料, 采用开环聚合法合成以星型聚乙二醇为内部嵌段、聚乳酸为外部嵌段的三臂、四臂星形聚乙二醇-聚乳酸嵌段共聚物(sPEG-b-PLLA), 探讨了其结构与性能之间的关系.合成路线如图3所示.

图3 sPEG-b-PLLA的合成路线
DSC 和XRD 结果均表明产物为结晶性聚合物, 且表现出与PLLA 相似的晶型, 随着PLA 链段的增加, 产物的结晶度也呈增大的趋势.接触角测试结果表明, 共聚物的亲水性较sPLLA的亲水性有明显改善, 且随着PEG 链段的增多, 共聚物的亲水性增强.
JAIN等[19]制备了(PEG)3-PLA聚合物囊泡.他们通过酯化反应将三个甲氧基(PEG1100)链连接在柠檬酸上,然后(MeOPEG11003)-柠檬酸上的-OH引发不同物质的量的D,L-乳酸开环聚合得到PEG/PLA10∶90~90∶10 5种不同比例的嵌段共聚物.其中PEG含量为10%~30%的聚合物可自组装为囊泡.疏水燃料荧光素能相对快速的从囊泡的壳上释放,而亲水性染料碘化丙啶在18 d才释放.由于其可同时运载油溶性和水溶性药物分子,因此囊泡载药系统预计将成为一种合适的载体在未来得到广泛的应用.

图4 两亲性聚合物(PEG)3-PLA的自组装
1.2.2 树枝状聚合物
树枝状聚合物是一类高度支化、具有树枝状三维结构的大分子,表面堆砌致密,内部有空隙,分子尺度在纳米级,结构有着极好的几何对称性,而且分子的体积、形状可以得到精确控制.与线性结构的聚合物相比,树枝状聚合物具有良好的溶解性和较低的粘度,而且其分子表面丰富的端基能够使其引入较多的功能性分子,因而有望在生物、分子识别、医药、催化和光电功能材料等不同领域得到广泛的应用[20].
FAN等[21]通过单电子转移自由基聚合,开环聚合和硫代-溴点击反应合成了新型树突状的两亲性共聚物PLA-b-PAA,表征发现其囊泡型胶束对pH变化有响应,在载药方面将会有潜在的应用.合成路线图如图5所示.
CAO等[ 22]报道了以疏水性的星型PLLA为核,以亲水性PAMAM为壳的两亲性树枝状聚合物的合成.他们首先将L-丙交酯与琥珀酸酐开环聚合合成了羧酸官能化PLLA星型聚合物,然后再制备了在树突根部有伯氨,外围有苄基酯保护的1, 2, 3代PAMAM.最后将PLLA和6个PAMAM树突进行耦合,合成了两亲性的树枝状DLSPs.实验结果表明,这种聚合物在水溶液中溶解度很好,约10~25 g/L.预计这种聚合物将应用于疏水性药物的运载.

图5 树突状的两亲性共聚物PL(D)LA-b-PAA的合成路线
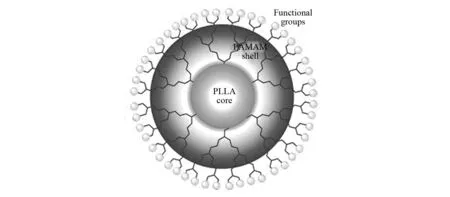
图6 树枝状星型两亲聚合物胶束
GONG等[23]通过线形PEG 两端连接着的树枝PLA引发丙交酯开环聚合,设计合成了一类哑铃形类树枝状三嵌段共聚物.这种共聚物的溶液经浇铸成膜和溶剂挥发后, 可以观察到自组装形成的多孔结构,通过改变PLLA 链段的长度, 则可以得到蜂窝状的孔结构.此外,随着PLLA链长的增加,聚合物膜的表面疏水性和蛋白质吸附能力随之增加.
我们实验室合成了新型的两亲聚合物POSS-(G3-PLLA-b-PEO-COOH)8,核为疏水的树枝状PLLA,壳为羧基官能化的亲水PEO[24].首先通过L-丙交酯的开环聚合和分支链反应合成核POSS-(G3-PLLA-OH)8,随后通过酯化反应将烯丙基-PEO-COOH链和POSS-(G3-PLLA-OH)8耦合.随后外围的羧基官能团与巯基丙酸反应即可制得.通过动态光散射和扫描电镜可知,在水中它以单分子微粒稳定存在.根据其独特的结构,预计可在载药方面得到应用.
1.2.3 超支化聚合物
超支化聚合物,属于树枝型聚合物同系物中的一种,三维结构决定了它的特殊性能, 如高溶解度、低黏度、高化学反应活性等[25].在具有相同重复单元的线性聚合物,树形分子和超支化聚合物中,超支化聚合物的溶解性几乎是线性聚合物的50 倍,而树枝型聚合物和超支化聚合物的溶解性相当.但由于超支化聚合物的支化度(DB 在0~0.5 左右),相对树枝型聚合物(DB=1)要低得多,支化结构具有可控性、分子表面官能度高、化学反应活性强、易于端基改性、且合成比较容易,具有某些跟树枝型聚合物相似的物理和化学性质[26],因此常用来代替树枝型聚合物研究应用于许多功能材料领域方面.
YANG 等[27]用一步酯化法将超支化聚缩水甘油醚和聚乳酸合成了共聚物( PLA-HPG).将纳米粒子加入到PLAHPG乳液中,制得共聚物包覆的纳米粒子( PLA-HPG NPs),其能够高效地将抗肿瘤剂喜树碱包覆在其中.此外,该材料具有稳定性好、在血液中循环时间长、肝脏毒素积累少等优点,其对肿瘤有更好的治疗效果.
LIU等[28]合成了一种新型两亲性超支化多臂共聚物[H40-star-(PLA-b-PEP-OH)].它是通过两步开环聚合反应(ROP)合成的.首先以Boltorn H40 为大分子引发剂与L-丙交酯形成中间体(H40-star-PLA-OH).然后与乙基乙烯酯进一步反应生成[H40-star-(PLA-b-PEP-OH)].通过表征发现[H40-star-(PLA-b-PEP-OH)]在水中可自组装成平均直径为130 nm的胶束,如图7,体外检测表明它们有良好的生物相容性和高效的细胞摄入能力,有望构建极有前景的载药系统.

图7 两亲性超支化多臂聚合物[H40-star-(PLA-b-PEP-OH)]
2 应用方向
聚乳酸两亲共聚物的应用研究范围很广,可与乙烯、淀粉等共混作包装材料及农膜,可作化妆品的添加成分,但更多研究集中在药物控制释放体系、组织工程及体内药物探针等生物医学工程领域[29].
2.1 药物缓释
在聚乳酸两亲共聚物的研究刚兴起的时候多用于研制载药系统.以聚乳酸-聚乙二醇共聚物应用的居多,因为聚乙二醇具有良好的生物相容性,同时柔软易组装.通过改变共聚物组成,可大幅度调节材料的亲疏水性能和人体内降解速率.通常用于负载一些易降解,稳定性差,半衰期短,同时毒副作用大的药物.由其所制成具有特定粒径及分布的载药纳米微球,以亲水性、无毒、无免疫原性的 PEG 链段作为壳层,注射进入人体后可避免被人体内网状内皮系统及肝、脾、肾等器官识别捕获,具有较长的血液循环时间,降解后可通过肾排出体外[30].
LI等[31]制备了载牛血清白蛋白(BSA)的MPEG -PLGA 纳米粒子.结果发现在给大鼠静脉注射该粒子后, BSA 粒子半衰期为4.5 h, 而未经修饰的PLGA 粒子半衰期仅为13.6 min.可见, 经修饰的纳米粒子能增加在血中的半衰期.
TOBIO 等[32]研究了口服后消化液中 PEG 的稳定性及 PLA-PEG 纳米粒子的行为.发现PEG 可减少纳米粒子与消化液酶的相互作用,在消化液中 4 h 后,破伤风疫苗大部分仍与纳米粒子相连.PLA-PEG-PLA 水凝胶在蛋白质药物缓释方面的研究,尤其值得关注.HMDI扩链法获得的 PLA-PEG-PLA 应用时,不必使用有机溶剂,成型简单,特别适用于一些扩散系数低而且在使用有机溶剂制作微球时容易失活的蛋白质类大分子药物的控制缓释[33].
聚乳酸两亲共聚物除了用于载药系统还可用于体内药物检测.在化疗的过程中,检测药物在体内的位置及浓度变化是成功治疗的关键.对此,CHEN等[34]报道了一种新型载药系统,它由作为肿瘤靶向性配体的叶酸和被空心X射线和上变频纳米荧光粉包覆的PLA-PEG结合.与之前报道过的以PLA-PEG为基础或包覆无机纳米粒子的PLA-PEG相比,他们的的载药系统可通过X射线,近红外光和核磁共振激发的光释放,在作为药物载体的同时也能做跟踪药物的探针.此外,中空的空间结构可以大大增加载药量,而且,纳米荧光粉上负载的药物表面有叶酸,这增加了细胞的摄取,从而显著增强了药物的疗效.因此,在可预见的未来里,这种多功能纳米载体系统在载药领域将成为重大的改进.

图8 PLA-PEG涂层多功能影像探针药物靶向输送
2.2 组织工程
聚乳酸两亲共聚物可作为修复、改善、替代人体组织或功能的生物装置应用于组织工程,与传统的金属制品相比,其优势在于可降解,有良好的力学性能,同时具有压电特性,即受压后能产生电压,从而促进细胞增殖,组织愈合,然后聚乳酸材料在体内会被吸收,周围组织器官会得到完全修复.
聚乳酸两亲共聚物在生物医学领域可注射水凝胶一直担任着为组织工程或细胞封装载体提供三维(3D)结构仿生支架的功能.CUI等[35]研制了可注射电活性水凝胶材料(IEHs),带羧基的苯胺四聚体(CTA)被作为官能团加到聚合物PLA-PFE-PLA上,通过混合的对映体聚合物CTA-PLLA-PEG-PLLA-CTA和CTA-PDLA-PEG-PDLA-CTA水溶液制得电活性水凝胶.此凝胶材料具有良好的生物相容性和很高的封装效率.皮下注射时用苏木精-伊红(H&E)染色表明此材料在体内具有生物相容性,并且这些可注射材料用脉冲电刺激时显现出更活跃的功能,同时能加速封装成纤维细胞、心肌细胞、成骨细胞的增殖.因此IEHs所拥有的这些卓越性能在将来可应用于制备体内组织工程的支架材料.

图9 PLA-PEG-PLA及其苯胺四聚体活性共聚物
2.3 免疫治疗佐剂
癌症治疗方法按时间顺序依次为手术、放疗、传统化疗、靶向疗法以及免疫疗法.其中免疫疗法将是继手术、放疗、化疗之后的新支柱,已经在多种肿瘤临床试验中取得良好效果.然而,现阶段人们对于很多机制了解不够,已经面世的免疫疗法仍有诸多不足之处尚需改进,需要引入新的技术和疗法来增进其治疗效果.
COUMES等[36]介绍了一种癌症免疫治疗的佐剂.他们将免疫调节因子LD-indolicidin偶联到作为乳化剂的聚合物PEG-PLA的亲水链上,使调剂因子位于接近乳液表面的位置,这样,合成了肽/聚合物LD-indolicidin-PEG-PLA.作为癌症治疗使用的佐剂,用肿瘤相关抗原TAA配置的LD-indolicidin-PEG-PLA和角鲨烯-水乳液利用卵清蛋白(OVA)/EG7细胞可有效地引发显性抗原特异性免疫反应.这个结果打开了针对疫苗佐剂和癌症免疫治疗的免疫抗原运载系统的崭新局面.
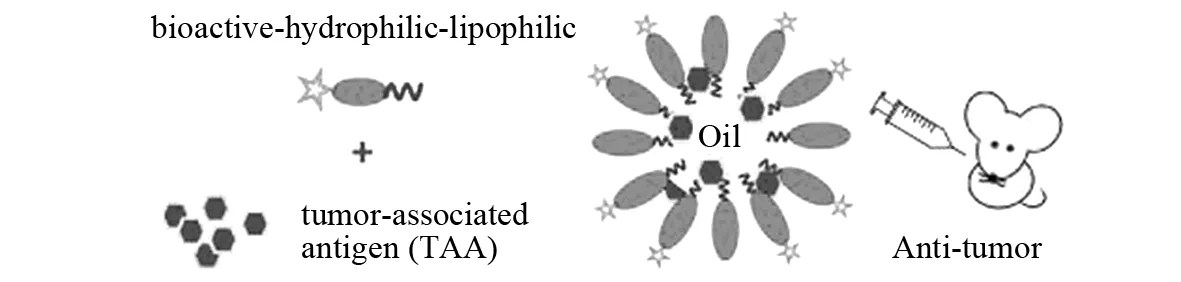
图10 免疫治疗系统癌症疫苗
2.4 其他医药方面
聚乳酸-聚乙烯基吡咯烷酮具有显著的络合能力,可与许多不同的化合物生成络合物,具有增溶作用,能增加某些基本不溶于水而有药理活性的物质的水溶性,因此广泛用作医药的粘结剂、包衣剂、缓释剂、胶囊助剂等[37].
3 前景展望
在医用高分子领域内,高分子药物控制释放体系的研究和开发方兴未艾,近30年来,PLA及其共聚物被用作一些半衰期短、稳定性差、易降解及毒副作用大的药物控释制剂的可溶蚀基材,减轻了药物对患者全身特别是对肝、肾的毒副作用.利用嵌段共聚物的自组装特性制备出共聚物微球或微囊可以包覆或包埋药物,具有载药能力强、粒径小、体内循环时间长、主动靶向性和被动靶向性等特点.具有一定组成的PLA-PEG嵌段共聚物微粒可逃逸体内网状内皮系统吸收,延长其在体内的循环时间,到达一般聚合物微粒难以到达的靶区.PLA-PEG嵌段共聚物目前已经在组织工程、药物载体、靶向和基因传输载体等研究方面显示出独特的作用.制成纳米颗粒的PLA 可运载抗肿瘤药如顺铂,抗寄生虫药如戊烷脒、阿苯达唑等.虽然人们对聚乳酸纳米控释系统进行了大量的研究,但成功上市的产品不多.制约此类药物制剂商品化的因素有聚乳酸的生产规模小、品种不全、价格昂贵, 制剂的制备工艺较为复杂等.随着聚乳酸纳米控释制剂的不断生产上市,特别是蛋白质、DNA和多肽药物迅猛发展及其特殊需要, 促进了在这一方面的研究工作, 上述影响因素有望得到克服,因此, 聚乳酸及其共聚物在纳米控释制剂方面有希望获得应用.
结构较复杂的树枝型和超支化型聚合物,由于其独特的结构和性质吸引许多研究者的兴趣,然而合成过程较复杂,分离提纯较困难,现研究成果十分有限.今后如何通过合理设计来简洁高效地合成具有特殊功能的聚乳酸树枝状共聚物, 是研究中应该努力的方向.
在目前,人们的研究方向依然是设计特定结构以提高载药率以及采用计算机模拟与实验相结合的方法探究不同结构类型的共聚物的性状,在计算机上建立模型,这样既提高了效率,也能给人们提供其他应用方向的思路.聚乳酸类纳米粒子的修饰方面的工作也存在着许多待深入之处,使聚乳酸共聚物在医学上发挥充分作用,研究者们未来要走的路依然很长.
[1] 路德待, 张小伟, 周添红, 等.可降解乳酸共聚物[J].化学进展, 2008, 20(2): 339-350.
[2] 程蓉, 钱欣.聚乳酸的改性及应用进展[J].化工进展, 2002, 21(11): 824-826.
[3] GOPFERICH A, PETER S J, LUCKE A, et al.Modulation of marrow stromal cell function using poly(D,L-lactic acid)-block-poly(ethylene glycol)-monomethyl ether surfaces [J].J Bio Mater Res, 1999, 46(3): 390-398.
[4] 宋继彬.α-氨基聚乙二醇-聚乳酸嵌段共聚物的合成(α-H2N-PEG-b-PLA)的合成及其医用研究[D].济南: 山东大学, 2010: 1-2.
[5] WU Q H, YI J, WANG S Y, et al.Synthesis and self-assembly of new amphiphilic thermosensitive poly(N-vinylcaprolactam)/poly (D,L-lactide) block copolymers via the combination of ring-opening polymerization and click chemistry [J].Polym Bull, 2015, 72(6): 1449-1466.
[6] TUCKING K S, GRUETZNER V, UNGER R E, et al.Dual enzyme-responsive capsules of hyaluronic acid-block-poly(Lactic Acid) for sensing bacterial enzymes [J].Macro Rap Comm, 2015, 36(13): 1248-1254.
[7] ABEBE D G, KANDIL R, KRAUS T, et al.Three-Layered biodegradable micelles prepared by two-step self-assembly of PLA-PEI-PLA and PLA-PEG-PLA triblock copolymers as efficient gene delivery system [J].Macromol Biosci, 2015, 15(5): 689-711.
[8] GANG R, SI S F.Preparation and characterization of poly(lacticacid)-poly(ethylene glycol)-poly(lactic acid) (PLA-PEG-PLA)m icrospheres for controlled release of paclitaxel [J].Biomaterials, 2003, 24(27): 5037-5044.
[9] YANG Q L, HE C Y, ZHANG Z, et al.Redox-responsive flower-like micelles of poly(L-lactic acid)-b-poly(ethylene glycol)-b-poly(L-lactic acid) for intracellular drug delivery [J].Polymer, 2016, 90: 351-362.
[10] LI C Y, LIU X L, HE S S, et al.Synthesis and AIE properties of PEG-PLA-PMPC based triblock amphiphilic biodegradable polymers [J].Polym Chem, 2016, 7(5): 1121-1126.
[11] 李晓然, 袁晓燕.聚乙二醇-聚乳酸共聚物药物载体[J].化学进展, 2007, 19(6): 973-981.
[12] CRAPARO E F, LICCIARDI M, CONIGLIARO A, et al.Hepatocyte-targeted fluorescent nanoparticles based on a polyaspartamide for potential theranostic applications [J].Polymer, 2015, 70: 257-270.
[13] LUO J, GIGUERE G, ZHU X.Asymmetric poly(ethylene glycol) star polymers with a cholic acid core and their aggregation properties [J].Biomacromolecules, 2009, 10(4): 900-906.
[14] SALAAM L E, DEAN D, BRAY T L.In vitro degradation behavior of biodegradable 4-star micelles [J].Polymer, 2006, 47: 310-318.
[15] LU D D, YUAN J C, LI H G, et al.Synthesis and characterization of a series of biodegradable and biocompatible PEG-supported poly(lactic-ran-glycolic acid) amphiphilic barbell-like copolymers [J].J Polym Sci Part A, 2008, 46(11): 3802-3812.
[16] HU M Y, SHEN Y R, ZHANG L, et al.Polymersomes via self-assembly of amphiphilic beta-cyclodextrin-centered triarm star polymers for enhanced oral bioavailability of water-soluble chemotherapeutics [J].Biomacromolecules, 2016, 17(3): 1026-1039.
[17] PAN J, SUBBUS, FENG M, et al.Micelle-like nanoparticles of star-branched PEO-PLA copolymers as chemotherapeutic carrier [J].Control Release, 2005, 110(1): 20-33.
[18] 张安强, 林雅铃, 魏芬芬, 等.星形聚乙二醇-聚乳酸嵌段共聚物的合成与表征[J].高分子材料科学与工程, 2011, 27(11): 83-88.
[19] JAIN J P, KUMAR N.Self-assembly of amphiphilic (PEG)3-PLA copolymer as polymersomes: preparation, characterization, and their evaluation as drug carrier [J].Biomacromolecules, 2010, 11(4): 1027-1035.
[20] KIM Y S, GIL E S, LOWE T L.Synthesis and characterization of thermoresponsive-co-biodegradable linear-dendritic copolymers [J].Macromolecules, 2006, 39(23): 7805-7811.
[21] FAN X S, WANG Z, YUAN D, et al.Novel linear-dendritic-like amphiphilic copolymers: synthesis and self-assembly characteristics [J].Polym Chem, 2014, 5: 4069-4075.
[22] CAO W Q, ZHU L.Synthesis and unimolecular micelles of amphiphilic dendrimer-like star polymer with various functional surface groups [J].Macromolecules, 2011, 44 (6): 1500-1512.
[23] GONG F R, CHENG X Y, WANG S F, et al.Biodegradable comb-dendritic tri-block copolymers consisting of poly(ethylene glycol) and poly(L-lactide): synthesis, characterizations, and regulation of surface morphology and cell responses [J].Polymer, 2009, 50(13): 2775-2785.
[24] FAN X S, HU Z G, WANG G W.Synthesis and unimolecular micelles of amphiphiliccopolymer with dendritic poly(L-lactide) core and poly(ethylene oxide) shell for drug delivery [J].RSC Adv, 2015, 5, 100816-100823.
[25] SANDA F, FUJIYAMA T, ENDO T.Chemical synthesis of poly-γ-glutamic acid by polycondensation ofγ-glutamic acid dimer: synthesis and reaction of poly-γ-glutamic acid methyl ester[J].J Polym Sci, Part A, 2001, 39(5): 732-741.
[26] 刁建志, 周炬, 彭政.超支化聚合物应用研究进展[J].现代塑料加工应用, 2008, 20(6): 55-58.
[27] YANG D, JENNIFER K S, CHRISTOPHER J H, et al. The effect of hyperbranched polyglycerol coatings on drug delivery using degradable polymer nanoparticles[J]. Biomaterials, 2014, 35: 6595-6602.
[28] LIU J Y, HUANG W, PANG Y, et al.Self-assembled micelles from an amphiphilic hyperbranched copolymer with polyphosphate arms for drug delivery [J].Langmuir, 2010, 26(13): 10585-10592.
[29] 郁志芳, 朱康杰.一种两亲生物降解高分子-聚丙交酯-聚乙二醇嵌段共聚物的研究进展[J].功能高分子学报, 2003, 16: 417-422.
[30] HARIHARAN S, BHARDWAJ V, BALA I, et al.Design of estradiol loaded PLGA nanoparticulate formulation: a potential oral delivery system for hormone therapy [J].Pharm Res, 2006, 23: 184-195.
[31] LI Y P, PEI Y Y, ZHANG X Y, et al.PEGylated PLGA nanoparticles as proteincarriers: synthesis, preparation and biodistribution in rats[J].J Control Release, 2001, 71(2): 203-211.
[32] TOBIO M, SANCHEZ A, VILA A, et al.The role of PEG on the stability in digestive fluids and in vivo fate of PEG-PLA nanoparticles following oral administration[J].Collo Sur Biointerfaces, 2000, 18: 215-323.
[33] BAE Y H, HUH K M, KIM Y, et al.Biodegradable amphiphilic multiblock copolymers and their implications for biomedical applications[J].Control Release, 2000, 64: 3-13.
[34] CHEN H Y, HE S S.PLA-PEG coated multifunctional imaging probe for targeted drug delivery [J].Pharmaceutics, 2015, 12(6): 1885-1892.
[35] CUI H T, SHAO J, WANG Y, et al.PLA-PEG-PLA and its electroactive tetraaniline copolymer as multi-interactive injectable hydrogels for tissue engineering [J].Biomacromolecules, 2013, 14(6): 1904-1912.
[36] COUMES F, HUANG C Y, HUANG C H, et al.Design and development of immunomodulatory antigen delivery systems based on peptide/PEG-PLA conjugate for tuning immunity [J].Biomacromolecules, 2015, 16(11): 3666-3673.
[37] WANG C H, HSIUE G H.New amphiphilic poly(2-ethyl-2-oxazoline) poly(L-lactide) triblock copolymer [J].Biomacromolecules, 2003, 4(6): 1487-1490.
[责任编辑:张普玉]
Research progress on amphiphilic polylactide copolymers
ZHANG Yake1, ZHANG Jingwei2, HU Zhiguo1*
(1.SchoolofChemistryandChemicalEngineering,HenanNormalUniversity,Xinxiang453007,Henan,China;2.SchoolofEnvironment,HenanNormalUniversity,Xinxiang453007,Henan,China)
Polylactic acid (PLA) is an excellent polymer material with good properties of biocompatibility and biodegradation, and is also approved as biomedical materials by Food and Drug Administration (FDA) of the United States.But its application in medical material is limited because of its hydrophobicity.In order to enhance its hydrophilicity, PLA has been modificated, for example PLA copolymerized with hydrophilic polymers to produce different types of amphiphilic copolymers.In this article, the research progress of amphiphilic copolymers of polyactic acid is reviewed, and its status and prospects of application are discussed.
polylactide; amphiphilic copolymers; biomedical materials
2016-10-17.
国家自然科学基金项目(21271066).
张玡珂(1994-),女,硕士生,研究方向为两亲聚合物的设计、合成及性能.*
O633.14
A
1008-1011(2016)06-0671-10
