新化合物ZM对大鼠血压的影响和对肠系膜上动脉的舒张作用
2016-12-25,
,
(1.西安交通大学医学院附属红会医院临床药学科,陕西 西安710054;2.西安交通大学第二附属医院药剂科)
·基础医学·
新化合物ZM对大鼠血压的影响和对肠系膜上动脉的舒张作用
张丽心1*,周凯2
(1.西安交通大学医学院附属红会医院临床药学科,陕西 西安710054;2.西安交通大学第二附属医院药剂科)
目的研究新合成的二氢吡啶类化合物ZM对大鼠血压的影响和对肠系膜上动脉的舒张作用及机制。方法自发性高血压大鼠(SHR)分为溶媒组6只,给药组各8只(ZM 0.2 mg/kg组,ZM 0.4 mg/kg组),采用鼠尾无创血压测量法测量给药前及ZM灌胃给药1 h后大鼠收缩压和舒张压的变化。SD大鼠32只用于体外实验,利用小血管张力测量系统研究ZM对SD大鼠完整内皮及去内皮肠系膜上动脉的扩张作用;研究ZM对KCl、CaCl2、苯肾上腺素和U46619收缩血管量效曲线的影响;研究在不含钙的缓冲液中ZM对苯肾上腺素、CaCl2及咖啡因收缩血管的影响。
ZM; 大鼠; 血压; 肠系膜动脉; 舒张
1982年,Hantzsch 合成了第一个1,4二氢吡啶类化合物,1975年第一个二氢吡啶类化合物硝苯地平上市[1]。其后30多年间,药物学家以硝苯地平结构为基本框架进行改造,合成了数以千计的二氢吡啶类化合物,并筛选出许多在药效学、药动学及器官选择性方面有明显特点的药物,并应用于临床。
拉西地平是第三代1,4二氢吡啶类钙离子拮抗剂的代表,也是在硝苯地平结构基础上进行改进而成,硝苯地平二氢吡啶环的3,5甲酯被乙酯基取代,苯环2位的硝基被一丙烯酸叔丁酯长链取代,由于其结构上的特点,拉西地平具有高度的脂溶性,虽然半衰期较短,但具有较高的膜分配系数,可以聚集在细胞膜脂质双层中[2],缓慢释放,从而平稳降压,自上市以来,成为治疗轻中度原发性高血压的首选药物之一[3]。以拉西地平的化学结构为母版,自我研发,采用电子等排原理,设计合成了一系列新的1,4二氢吡啶类衍生物,并不断筛选,用丙烯酰胺代替丙烯酸叔丁酯,通过对其不同结构和降压效果初步筛选并考查N(氮)上不同的取代基对降压活性的影响,经初步的降压实验,筛选出其中较好的一种化合物ZM,对其进行系统的药理学研究,期望获得具有高效、长效、选择性突出、副作用少的候选药物。本研究希望通过考察新合成化合物ZM的降压作用和对肠系膜上动脉血管的舒张作用,对其降压作用和特点及机制进行系统的研究。
1 材料与方法
1.1新化合物的结构将拉西地平4-苯基2位的叔丁基变为叔戊基而成,具体结构见图1。
1.2动物SD (Sprague-Dawley) 大鼠32只,体重250~300 g,雌雄兼用,购于西安交通大学医学院实验动物中心,实验动物许可证号:SYXK(陕)2007-2003。自发性高血压大鼠(spontaneously hypertensive rats,SHR)22只,雄性,20周龄,购于北京维通利华科技有限公司。所有动物按性别分笼饲养,室温25±3 ℃,相对湿度50%~70%,自然光照12 h,颗粒饲料、自来水喂养,适应性喂养一周后用于实验研究。
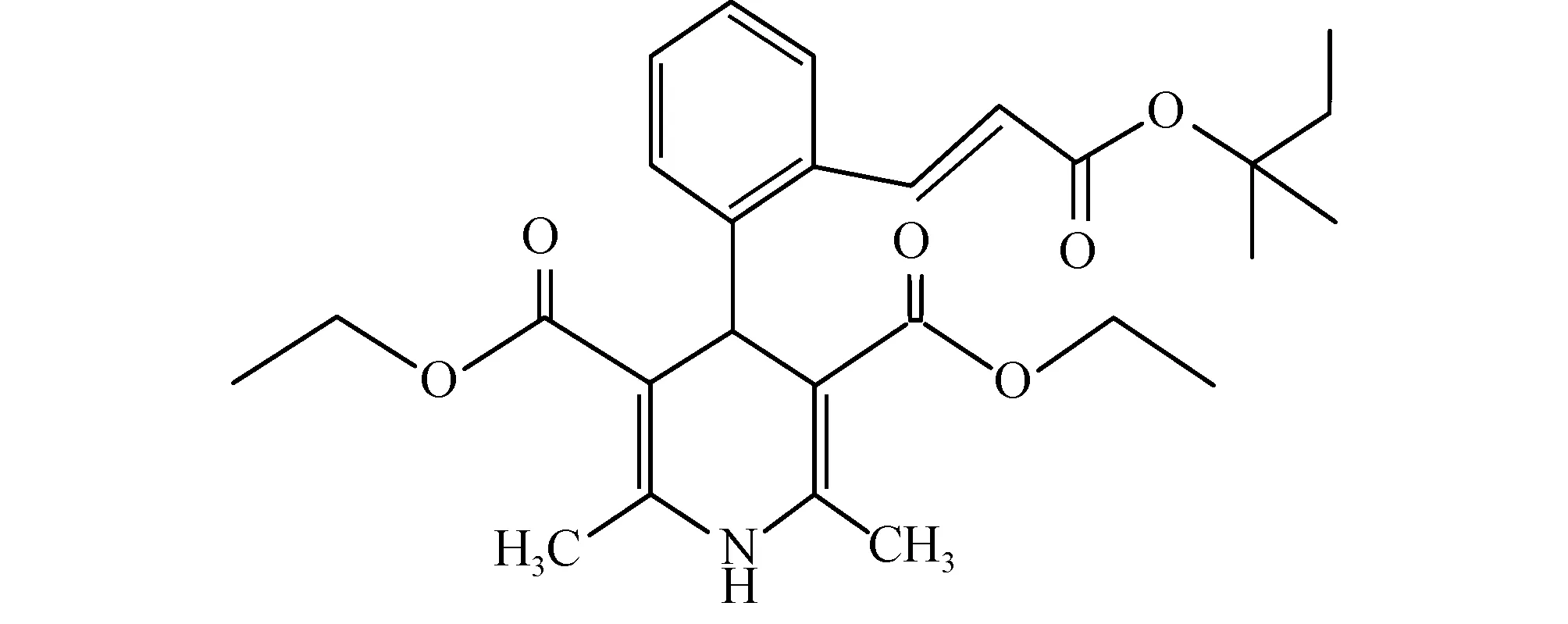
图1 ZM化合物分子结构 (E)-4-(2-(3-叔戊氧基-3-氧-1-丙烯基)苯基-2,6-二甲基-1,4-二氢吡啶-3,5-二羧酸二乙酯(ZM)
1.3主要试剂苯肾上腺素、氯化乙酰胆碱、咖啡因、Triton X-100、DMSO购于Sigma公司。U46619购于Cayman Chemical,USA;其他试剂均为国产分析纯试剂。U46619溶于乙醇,用于体外实验的新化合物ZM溶于DMSO配成母液备用。
1.4主要仪器BP-6无创血压仪(成都泰盟科技有限公司,中国)序号:TM009-0609-05-010-008,包括8通道生物机能实验系统。Myograph 恒温离体器官浴槽(DMT-610,Danish Myo Technology,Denmark),PowerLab 数据采集分析系统 (ADIstruments Co.,Australia)。
1.5血压测定SHR大鼠分为三组,溶媒组(30%吐温-80+30%无水乙醇+40%双蒸水)6只,给药组每组8只,分别为ZM 0.2 mg/kg组,ZM 0.4 mg/kg组。给药前测定基础血压后,灌胃给药,1h后用BP-6无创血压仪测量给药前后动脉血压的变化。记录大鼠的收缩压和舒张压,每个时间点重复测量3~5次,取平均值。给药前测出每只大鼠的正常收缩压和舒张压,给药后1 h再次测定收缩压和舒张压,计算给药前后血压的变化率,采用以下公式:
血压的降低率=(给药前血压-给药后血压)/给药前血压×100%。
1.6肌张力测定SD大鼠用二氧化碳麻醉致死,取出肠系膜上动脉,体视显微镜下剥离干净周围组织,剪成长3 mm的环段。将动脉环浸入37 ℃ DMT恒温浴槽中,将2根直径40 μm的不锈钢丝穿过动脉环,不锈钢丝两端与张力换能器和微调装置相连,张力换能器连接肌张力描记系统,记录肌张力的变化。浴槽中持续通入95%氧气和5%的二氧化碳,pH值保持在7.4。去内皮血管环用0.1%Triton X-100灌注10 s,随即用Krebs液冲洗10 s[4]。
1.7数据分析及统计通过累加激动剂获得血管环收缩或舒张曲线。血管环收缩反应以对60 mmol/L K+预收缩的相对百分比表示,舒张反应以激动剂诱导预收缩的百分比表示。Emax、Rmax分别指最大收缩率和最大舒张率;pEC50(产生最大效应的50%时激动剂摩尔浓度的负对数),采用Graphpad prism 5.0(San Diego,CA,USA)进行曲线回归得出。pA2’为拮抗剂的解离常数,用以下公式得出:
pA2’=-log([B]/(r-1)),其中[B]表示拮抗剂的摩尔浓度,r表示加入激动剂前后EC50值的比率。
所有实验数据均用均数±标准差表示,均数之间的差异用SPSS13.0进行统计,涉及多组数据,用多因素方差分析Post-hoc test法进行检验,两组之间数据比较用非配对t检验。P<0.05为差异有显著性。
2 结 果
2.1对大鼠血压的影响结果显示(表1)溶媒组SHR灌胃给药后血压无明显变化;新化合物ZM 0.2 mg/kg降低SHR大鼠收缩压和舒张压分别为16%和17%;0.4 mg/kg ZM降低SHR大鼠收缩压和舒张压分别为24%和25%。结果显示:新合成化合物ZM有降低自发性高血压大鼠收缩压和舒张压的作用,且呈现剂量依赖性。
表1ZM灌胃给药对自发性高血压大鼠血压的影响
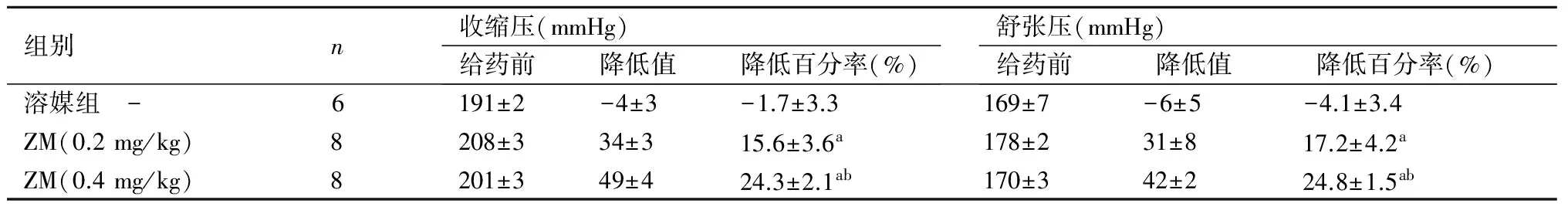
组别n收缩压(mmHg)给药前降低值降低百分率(%)舒张压(mmHg)给药前降低值降低百分率(%)溶媒组 -6191±2-4±3-1.7±3.3169±7-6±5-4.1±3.4ZM(0.2mg/kg)8208±334±315.6±3.6a178±231±817.2±4.2aZM(0.4mg/kg)8201±349±424.3±2.1ab170±342±224.8±1.5ab
与溶媒组相比,a:P<0.01;与低剂量组相比,b:P<0.05
2.2 ZM对完整内皮和去内皮的大鼠肠系膜上动脉的作用内皮完整和去除内皮的肠系膜上动脉用60 mmol/L K+预收缩,待曲线稳定后累加浓度法在浴槽中加入ZM(10-9~10-4mol/L)。结果显示(图2):化合物ZM呈浓度依赖性地舒张肠系膜动脉;最大舒张率(Rmax)在完整内皮动脉和去内皮动脉分别为80%±5%和82%±5%,pEC50值在完整内皮动脉和去内皮动脉分别为5.40±0.17和5.31±0.13。结果显示,最大舒张率(Rmax)和pEC50值在去内皮动脉和完整内皮动脉之间比较差异无显著性。
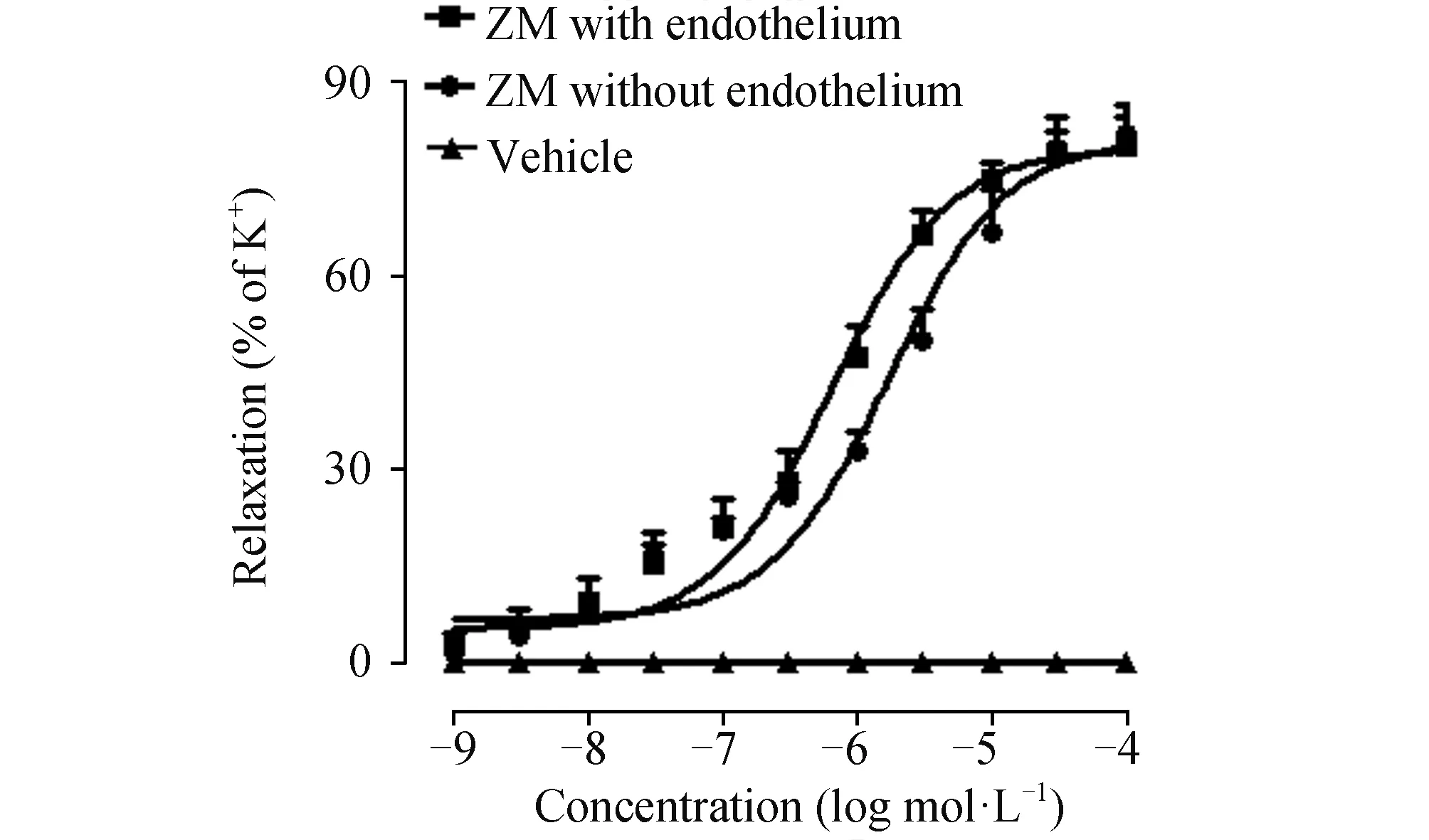
图2 ZM对完整肠系膜上动脉及去内皮肠系膜上动脉舒张作用的影响(n=8)
2.3 ZM对KCl和CaCl2收缩血管的量效曲线的影响进一步考察化合物舒张血管的作用是否涉及电压依赖性Ca2+离子通道,观察其对KCl和CaCl2收缩血管的量效曲线的影响。血管环用ZM(3×10-8mol/L,3×10-7mol/L)孵育40 min,浴槽中的溶液每20 min替换1次。孵育结束后,用含KCl(10、20、40和80 mol/L)的Krebs液相继替换浴槽中的溶液,观察孵育后血管环的反应。结果显示(图3),KCl诱导了一个浓度依赖性的收缩;ZM在3×10-8mol/L和3×10-7mol/L浓度下使KCl的浓度依赖型曲线以非平行方式右移,KCl的相对最大收缩率从110%±4%分别降低到49%±5%和34%±4%,ZM抑制KCl收缩血管的pA2’值为7.88。
同上法孵育,孵育结束后,浴槽中液体换成含60 mmol/L K+和10-4mol/L EDTA,不含Ca2+的Krebs液,稳定20 min后,用累加浓度法加入CaCl2(10-5~10-2mol/L),建立CaCl2收缩血管的量效曲线。由图4可见ZM使CaCl2收缩血管的量效曲线非平行右移,ZM 3×10-8mol/L,3×10-7mol/L分别使CaCl2的相对最大收缩率从107%±10%降至56%±8%和44%±5%,ZM抑制CaCl2收缩血管的pA2’值为7.31。
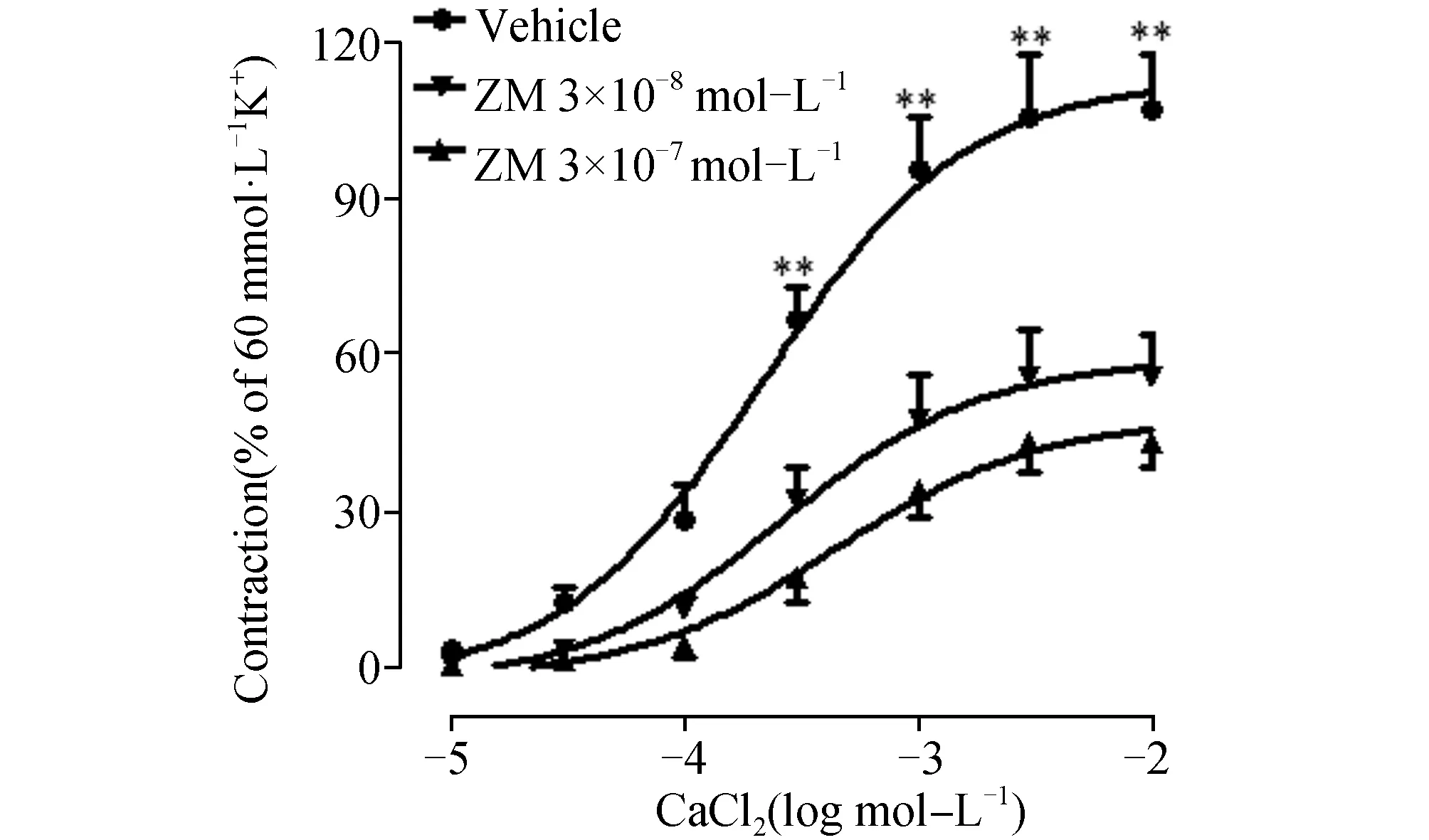
图3 ZM对KCl诱导的大鼠肠系膜上动脉收缩量效曲线的影响(n=8) 与溶媒组相比,a:P<0.01
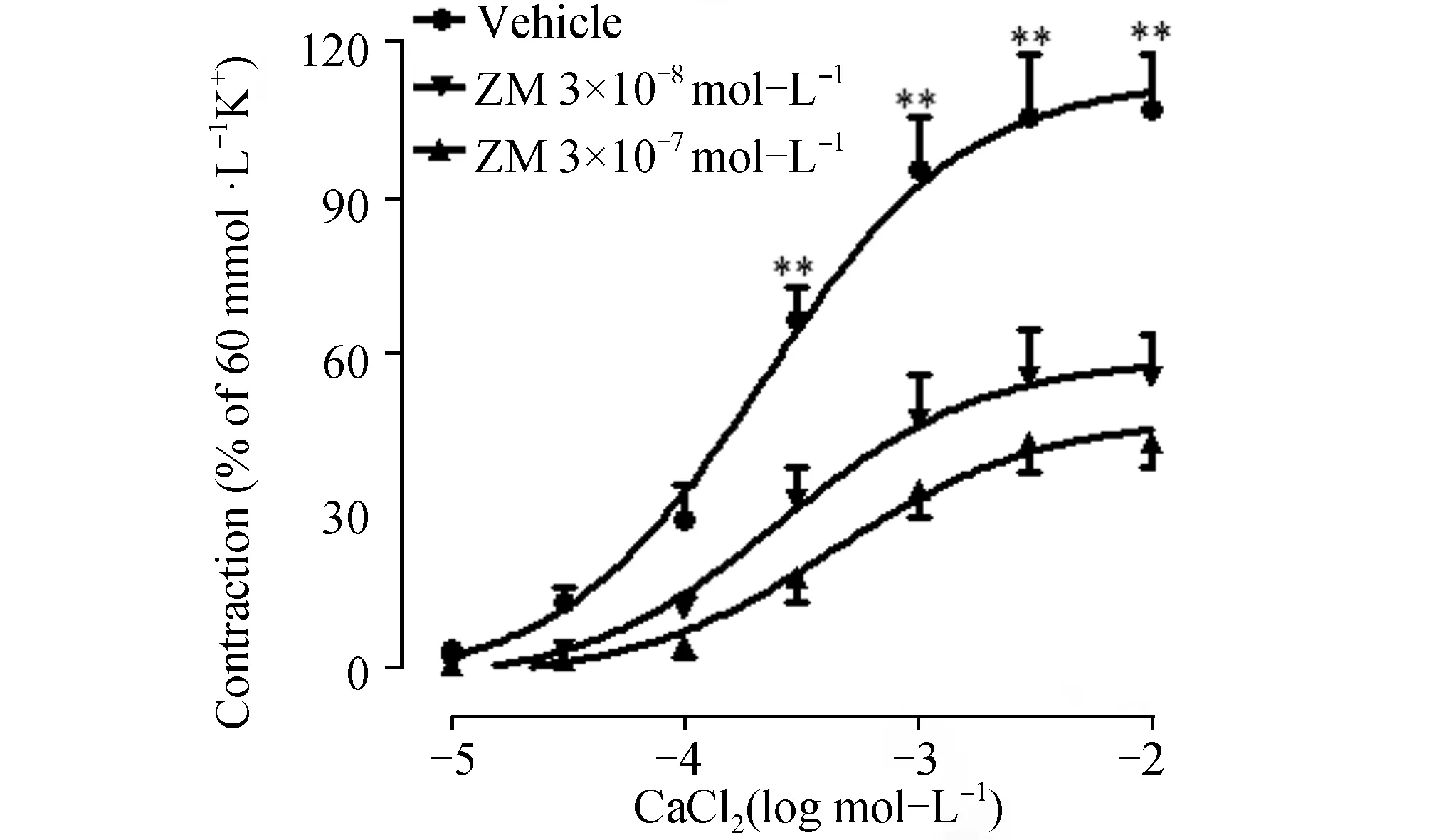
图4 ZM对CaCl2诱导的大鼠肠系膜上动脉收缩量效曲线的影响(n=8) 与溶媒组相比,a:P<0.01
2.4 ZM对苯肾上腺素和U46619量效曲线的影响进一步研究ZM的舒张血管作用是否涉及α肾上腺素受体和血栓素受体,用ZM(3×10-8mol/L,3×10-7mol/L)孵育大鼠肠系膜上动脉40 min后,累加浓度法依次在浴槽中加入苯肾上腺素(10-9mol/L~3×10-5mol/L),得到苯肾上腺素收缩血管的量效曲线。结果显示(图5):ZM在3×10-8mol/L和3×10-7mol/L浓度下使苯肾上腺素收缩血管的量效曲线的相对最大收缩率从103%±9%分别降为49%±6%和40%±5%,ZM抑制苯肾上腺素收缩血管的pA2’值为7.69。
同法研究ZM对U46619收缩血管的量效曲线的影响。结果显示(图6):ZM在3×10-8mol/L和3×10-7mol/L浓度下使U46619收缩血管的量效曲线的相对最大收缩率从139%±9%分别降为115%±5%和62%±8%,ZM抑制U46619收缩血管的pA2’值为6.70。
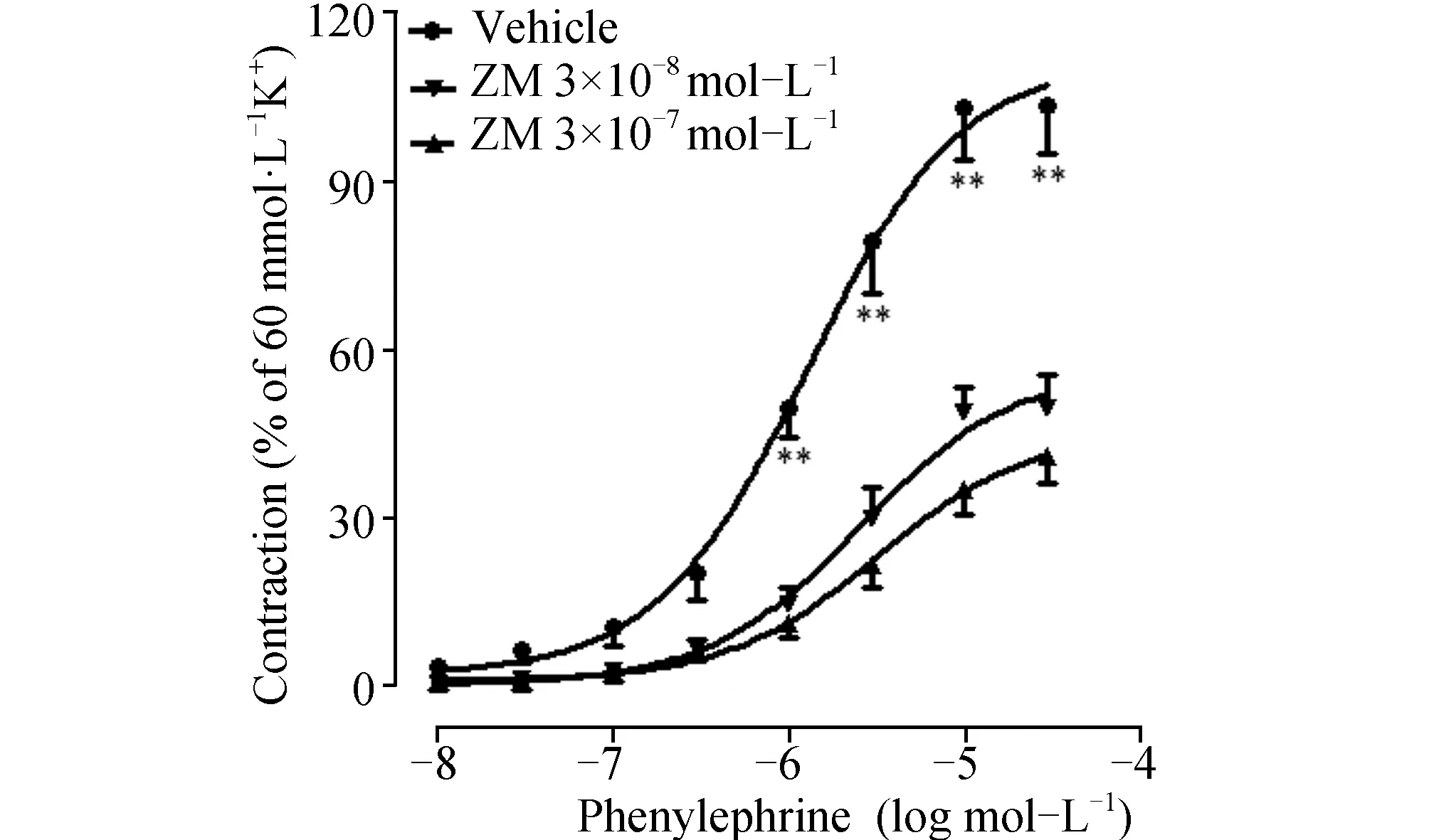
图5 ZM对苯肾上腺素诱导的大鼠肠系膜上动脉收缩量效曲线的影响(n=8) 与溶媒组相比,a:P<0.01
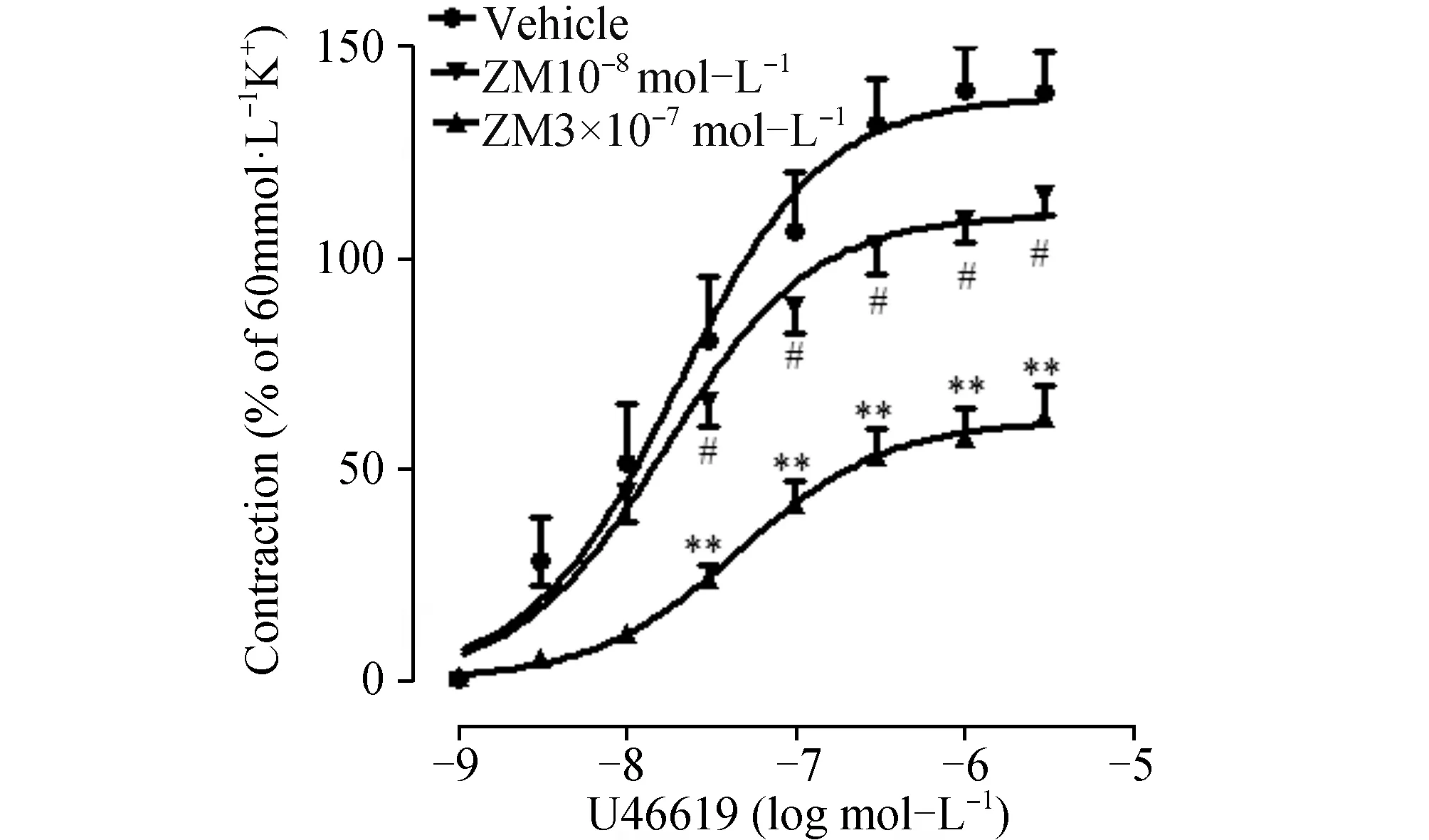
图6 ZM对U46619诱导的大鼠肠系膜上动脉收缩量效曲线的影响(n=8) 与溶媒组相比,a:P<0.01;与低浓度组相比,b:P<0.05
2.5在无Ca2+液中对苯肾上腺素和CaCl2收缩血管的影响为了研究ZM对血管内钙释放和外钙内流的影响,肠系膜上动脉在无钙的Krebs液(含EDTA 10-4mol/L)中加入ZM(3×10-8mol/L,3×10-7mol/L和3×10-6mol/L)进行孵育,孵育完成后,浴槽中加入苯肾上腺素(10-5mol/L),可见动脉环产生一个迅速而短暂的收缩,紧接着浴槽中加入CaCl2(2×10-3mol/L),可见动脉环再次收缩并达峰值。
结果显示(图7),在ZM处理过的血管对苯肾上腺素诱导的收缩反应与溶媒无显著性差别;在溶媒组CaCl2诱导的血管收缩反应相对最大收缩率达88%±10%,在ZM(3×10-8mol/L,3×10-7mol/L和3×10-6mol/L)处理过的血管相对最大收缩率分别为81%±13%,63%±7%和44%±5%,提示ZM对CaCl2诱导的收缩反应有抑制作用。
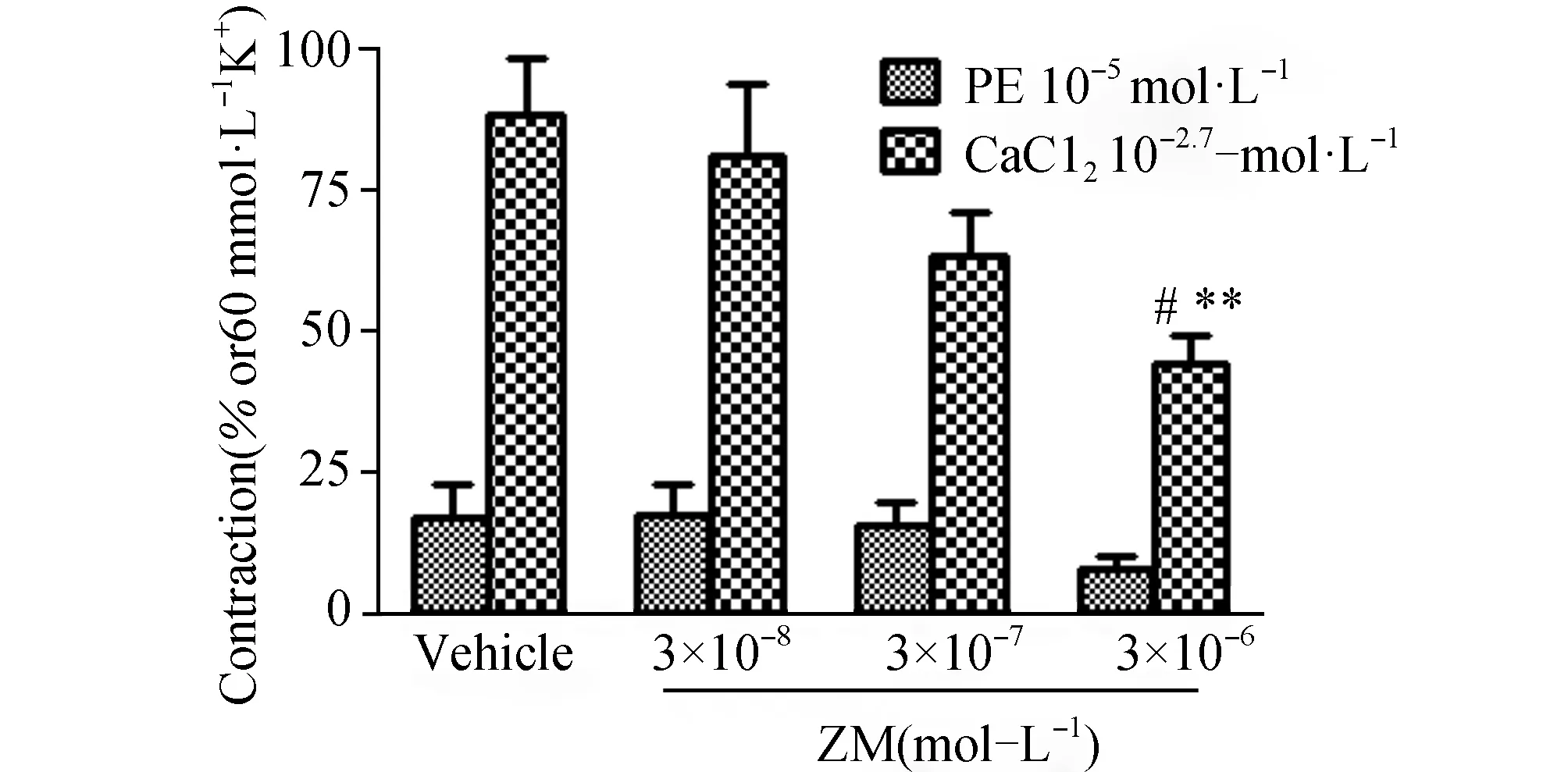
图7 在无钙液中ZM对苯肾上腺素及CaCl2诱导的血管收缩的影响(n=6) 与溶媒组相比,a:P<0.01;与低浓度组相比,b:P<0.05
2.6 ZM对无钙液中咖啡因收缩血管的影响为进一步研究ZM对内钙释放的影响,肠系膜上动脉在不含钙的Krebs液(含EDTA 10-4mol/L)中用ZM(3×10-6mol/L)进行孵育后,浴槽中加入咖啡因(3×10-2mol/L)诱导血管收缩。结果显示,在溶媒组咖啡因诱导了一个快速短暂的收缩(Emax分别为11%±2%,13%±2%);在ZM孵育的血管,咖啡因诱导的血管收缩反应Emax分别为9%±1%和11%±1%,与对照组比较差异无显著性。
3 讨 论
钙通道阻滞剂主要通过阻滞细胞外钙离子的内流,使血管平滑肌舒张,外周血管阻力下降,从而使系统血压降低。实验发现,在0.2 mg/kg的剂量下,ZM降低SHR大鼠收缩压和舒张压分别为16%和17%,提示新化合物ZM具有明显的降压作用。
血管平滑肌细胞内的钙离子水平是引起血管收缩舒张的关键和最终因素之一。当细胞内K+浓度增高时,细胞膜去极化,这时电压依赖性的钙离子通道开放,细胞外的钙离子流入,引起血管平滑肌收缩[5],导致血管平滑肌张力异常增高,成为高血压的主要病理特征之一[6]。在离体血管实验中,ZM浓度依赖性地舒张高浓度K+诱导的血管收缩,并且使KCl和CaCl2诱导的血管收缩量效曲线非平行性向右移动,提示阻断电压依赖性钙通道可能是ZM舒张血管的途径之一[7]。在血管舒张过程中除平滑肌扩张外,血管内皮也可合成并释放内皮源性超极化因子、前列腺素、一氧化氮等物质引起血管扩张[8],在ZM对高浓度K+预收缩的舒张血管量效关系研究中,对完整内皮的肠系膜上动脉和用Triton X-100去除内皮的肠系膜上动脉分别进行比较,发现去除内皮并不影响ZM的血管舒张效应,表明内皮对ZM的舒张血管作用无影响,这一点可能与内皮细胞上较少表达电压依赖性钙离子通道有关。
苯肾上腺素通过与细胞膜上α1肾上腺素受体结合,使细胞膜上受体操纵性钙通道开放,同时磷酸化电压依赖性钙离子通道,引起细胞内钙离子浓度升高,导致血管收缩[9],在实验研究中,ZM使苯肾上腺素诱导的血管收缩量效曲线非平行右移,同时使血管量效曲线的最大收缩率降低,提示阻断受体操纵性钙离子通道有可能是ZM舒张血管的另一条作用途径。苯肾上腺素还可以通过与细胞膜上α1肾上腺素受体结合,激活磷脂酶C,产生三磷酸肌醇,导致对三磷酸肌醇敏感的细胞内钙池释放内钙,诱发血管收缩[10],但实验中,在不含钙的缓冲液中,ZM对苯肾上腺素引起的内钙释放诱导的血管收缩没有明显的抑制作用,而明显抑制了由CaCl2引起的细胞外钙离子的内流而诱导的血管收缩;咖啡因激活Ryanodine受体引起内钙释放是内钙释放的另一条途径[11],在实验中ZM对咖啡因引起的血管收缩亦无明显抑制,这些结果提示ZM舒张血管的作用可能主要是通过抑制细胞外钙离子的内流,对细胞内钙离子的释放无明显抑制作用。U46619为血栓素受体激动剂,通过与细胞膜上的血栓素受体结合而具有强烈的缩血管作用,U46619还依赖于细胞膜上的电压依赖性钙离子通道[12],引起细胞外的钙离子内流,信号转导途径可能与蛋白激酶C有关,实验可见,ZM对U46619的血管收缩量效曲线也呈现浓度依赖性地抑制作用。这些实验结果均提示,ZM对大鼠肠系膜上动脉的舒张作用可能主要通过抑制细胞外的钙离子内流。实验研究表明:新化合物ZM可以呈剂量依赖性地降低大鼠血压,其降压作用可能通过抑制细胞外的钙离子内流。
[1] 郭鹏程,黄红林.二氢吡啶类钙通道阻滞剂及其药物手性研究[J].现代生物医学进展,2009,9(1):181-185.
[2] Kawada T,Sun HT,Nakazawa M,et al.In vitro effects of the new calcium antagonist lacidipine[J].Jpn J Pharmacol,1993,62(3):289-296.
[3] 刘运阳,秦玲,吴海帝,等.国产拉西地平治疗原发性轻中度高血压的Mata分析[J].中国老年学杂志,2012,32(6):2242-2244.
[4] Ping NN,Cao L,Xiao X,et al.The determination of optimal initial tension in rat coronary Artery using wire myography[J].Physiol Res,2014,63(1):143-146.
[5] Cao YX,Zhang W,He JY,et al.Ligustilide induces vasodilatation via inhibiting voltage dependent calcium channel and receptor-mediated Ca2+influx and release[J].Vascul Pharmacol,2006,45,171-176.
[6] 曾国伟,刘波,赵国政,等.高血压促进血管平滑肌细胞L型钙离子通道重塑的研究进展[J].解放军医学院学报,2015,36(2):190-192.
[7] Ping NN,Li S,Mi YN,Cao L,Cao YX.Hydrogen sulphide induces vasoconstriction of rat corOnary artery via activation of Ca2+influx[J].Acta Physiol (Oxf),2015,214(1):88-96.
[8] Andresen J,Shafi NI,Bryan RM,Jr.Endothelial influences on cerebrovascular tone[J].J Appl Physiol,2006,100(1):428-431.
[9] Wettschureck N,Offermanns S.Mammalian G proteins and their cell type specific functions[J].Physical Review,2005,85(4):1159-1204.
[10] He JY,Zhang W,He LC,et al.Imperatorin induces vasodilatation possibly via inhibiting voltage dependent calcium channel and receptor-mediated Ca2+influx and release[J].Eur J Pharmacol,2007,573,170-175.
[11] Ahn HY,Karaki H,Urakawa N.Inhibitory effects of caffeine on contractions and calcium movement in vascular and intestinal smooth muscle[J].Br J Pharmacol,1988,93,267-274.
[12] Yamagishi T,Yanagisawa T,Taira N.Ca2+influx induced by the agonist U46619 is inhibited by hyperpolarization induced by the K+ channel opener cromakalim in canine coronary artery[J].Jpn J Pharmacol,1992,59(3):291-299.
EffectsofaNewCompoundZMonBloodPressureandMesentericArteryinRats
ZHANG Lixin,ZHOU Kai
(HonghuiHospital,Xi’anJiaotongUniversityHealthScienceCenter,Xi’an,Shanxi710054,China)
ObjectiveThe aim of this study was to assess the effects of a new synthetic dihydropyridines compound (ZM) on rat blood pressure and vasodilation of superior mesenteric artery and its mechanism.MethodSpontaneously hypertensive rats were divided into the vehicle group,administration group (ZM 0.2 mg/kg,ZM 0.4 mg/kg).The blood pressure of rats was measured using a non-invasive tail cuff blood pressure system in vivo before administration and 1 h after gavage.32 SD(Sprague-Dawley)rats were used in vitro,Isometric tension of artery ring segments was recorded by myography system in vitro for the estimation of the effects of ZM on the vasoconstriction dose-response curves of KCl,CaCl2,phenylephrine and U46619.Effects of ZM on the contraction of artery ring segments in calcium-free Krebs solution with phenylephrine,CaCl2and caffine added were also evaluated.ResultsZM (0.2 mg/kg) decreased the systolic and diastolic blood pressure of spontaneously hypertensive rats 1h after gavage by 16% and 17%.ZM (0.4 mg/kg) decreased by 24% and 25% respectively.There was no obvious difference of the vasorelaxation between intact and denuced endothelium mesenteric arterial ring segments in ZM(10-9~10-4mol/L).ZM(3×10-8mol/L,3×10-7mol/L)shifted the concentration-contratile curves induced by KCl,CaCl2,phenylephrine and U46619 towards the right in a non-parallel manner with the decreasedEmax.ZM(3×10-8mol/L,3×10-7mol/L,3×10-6mol/L)obviously inhibited the contraction induced by CaCl2,but did not inhibit the contraction induced by phenylephrine and caffine in calcium-free Krebs solution.ConclusionZM can lower blood pressure of rats in vivo and concentration-dependently relax the mesenteric artery in vitro.The mechanism of the effects of ZM was mainly through inhibiting extracellar calcium of artery muscle.
ZM; rat; blood pressure; mesenteric artery;vasodilation
10.15972/j.cnki.43-1509/r.2016.05.007
2016-06-08;
2016-08-28
*通讯作者,E-mail:zlx_good@163.com.
结果ZM灌胃给药0.2 mg/kg降低自发性高血压大鼠收缩压和舒张压分别为16%和17%;0.4 mg/kg降低收缩压和舒张压分别为24%和25%。ZM(10-9~10-4mol/L)呈浓度依赖性地舒张大鼠肠系膜上动脉,去内皮动脉和完整内皮动脉相比较舒张作用间差异无显著性;ZM(3×10-8mol/L,3×10-7mol/L)使KCl、CaCl2、苯肾上腺素和U46619收缩血管量效曲线非平行右移;在不含钙的缓冲液中ZM(3×10-8mol/L,3×10-7mol/L,3×10-6mol/L)可以抑制CaCl2引起的血管收缩,对苯肾上腺素及咖啡因引起的收缩血管无影响。结论ZM可以降低大鼠血压,呈浓度依赖性地扩张大鼠肠系膜上动脉,其主要作用机制可能与抑制血管平滑肌细胞钙离子内流有关。
R972
A
蒋湘莲)
