LC-MS/MS法测定人尿液中他唑巴坦钠浓度及其尿药排泄动力学研究Δ
2016-12-19任立玲王源园孙鲁宁张宏文谢利军王永庆1南京医科大学药学院南京1009南京医科大学第一附属医院药学部南京1009
任立玲,王源园,孙鲁宁,张宏文,谢利军,刘 云,王永庆1,#(1.南京医科大学药学院,南京 1009;.南京医科大学第一附属医院药学部,南京 1009)
·临床药学与研究·
LC-MS/MS法测定人尿液中他唑巴坦钠浓度及其尿药排泄动力学研究Δ
任立玲1*,王源园2,孙鲁宁2,张宏文2,谢利军2,刘云2,王永庆1,2#(1.南京医科大学药学院,南京210029;2.南京医科大学第一附属医院药学部,南京210029)
目的:建立测定人尿液中他唑巴坦钠浓度的方法,并进行尿药排泄动力学研究。方法:尿液样品经10%高氯酸沉淀后,采用高效液相色谱-串联质谱(LC-MS/MS)法测定尿液中他唑巴坦钠的浓度。色谱柱为Hypersil GOLD C18,流动相为甲醇-水(30∶70,V/V),流速为0.2 ml/min,柱温为30℃,进样量为5 μl;采用电喷雾离子源,以多反应监测方式进行正离子扫描,用于定量分析的离子对为m/z 301→168。入组8名健康受试者,静脉滴注注射用头孢噻肟钠他唑巴坦钠(6∶1,m/m)2.34 g,收集其给药前和给药后0~2、2~5、5~8、8~12和12~16 h的尿液研究其尿液排泄动力学。结果:他唑巴坦钠尿药浓度在0.25~500 μg/ml范围内线性关系良好(r=0.999 9),定量下限为0.25 μg/ml,批内、批间RSD<10%,方法回收率为93.8%~111.8%,提取回收率为93.9%~99.7%,介质效应为87.6%~107.2%。受试者用药16 h后,他唑巴坦钠的尿累积排泄量为(209.70±39.24)mg,累积排泄率为(61.7±11.5)%。结论:LC-MS/MS法用于人尿液中他唑巴坦钠浓度的测定和排泄动力学的研究简便、快捷、灵敏度高;他唑巴坦钠主要经肾脏排泻。
高相液相色谱-串联质谱法;他唑巴坦钠;尿液;尿药浓度;排泄动力学
头孢噻肟钠是第三代头孢菌素类抗菌药物,通过破坏细菌细胞壁的合成来发挥广谱抗菌作用,对革兰氏阴性杆菌和革兰氏阳性球菌均具有较强的抗菌活性。随着临床使用越来越广泛,其耐药率逐年递增[1]。他唑巴坦钠是舒巴坦的衍生物,为不可逆的β-内酰胺酶竞争性抑制剂。两者组成的复方制剂可增强头孢菌素类抗菌药物对β-内酰胺酶的稳定性,扩大抗菌谱范围,从而避免或减少耐药性的发生,可用于各种敏感菌、多重耐药菌、耐甲氧西林金黄色葡萄球菌(MRSA)、铜绿假单胞菌、产超广谱β-内酰胺酶(ESBLs)的大肠埃希菌、肺炎克雷伯菌和阴沟肠杆菌引起的感染[2]。不同配比的头孢噻肟钠他唑巴坦钠的杀菌作用明显强于头孢噻肟钠单药。前期体外抗菌研究表明,头孢噻肟钠他唑巴坦钠具有较强的体外抗菌作用,综合考虑药物疗效和不良反应、生产和使用成本等多方面因素,6∶1(m/m,下同)为较合理的配方组合[3]。目前,国内测定人尿液中他唑巴坦钠主要采用高效液相色谱(HPLC)法[4-5],但操作烦琐、分析时间长。本研究建立了简便、快速的高效液相色谱-串联质谱(LC-MS/MS)法,用于测定人体内他唑巴坦钠的尿药浓度,并研究健康受试者使用头孢噻肟钠他唑巴坦钠(6∶1)后他唑巴坦钠的尿药排泄特征,现报道如下。
1 材料
1.1仪器
TSQ Ultra EMR型三重四极杆串联质谱仪、Surveyor型HPLC系统(包括四元梯度泵、温控自动进样器和在线脱气机)和Xcalibur V2.0软件(美国Finnigan公司);Milli-Q Gradient A10型超纯水器(美国Millipore公司);TGL-16G型低温高速离心机(上海安亭科学仪器厂);BP-211D型电子天平(德国Storius公司);LP2000-P2型恒速输液泵(北京鑫禾丰医疗技术有限公司);PCB-11型涡旋仪(德国Eppendorf公司);30AK型氮吹仪(北京八方世纪科技有限公司)。
1.2药品与试剂
注射用头孢噻肟钠他唑巴坦钠(6∶1)(南京信业医药技术有限公司,批号:20090802,规格:2.34 g);他唑巴坦钠对照品(齐鲁制药有限公司,批号:9030064JE,纯度:92.0%);甲醇为色谱纯,高氯酸为分析纯,水为纯净水。空白尿液由健康受试者提供。
2 方法
2.1色谱与质谱条件
色谱柱:Hypersil GOLD C18(150 mm×2.1 mm,5µm);流动相:甲醇-水(30∶70,V/V);流速:0.2 ml/min;柱温:30℃;进样量:5µl。
采用电喷雾离子源(ESI);检测方式:正离子检测;扫描方式:多反应选择监测(MRM);喷雾电压:4 500 V;金属毛细管温度:350℃;鞘气(N2)压力:25 Arb;辅助气(N2)压力:25 Arb;碰撞气(Ar)压力:1.5 mTorr;源内碰撞诱导解离(CID)电压:2 V;用于定量分析的离子对:m/z 301→168(他唑巴坦钠)。
2.2标准溶液的配制
精密称取他唑巴坦钠对照品适量于量瓶中,用水溶解并定容,摇匀,配制成他唑巴坦钠质量浓度为5 000 μg/ml的贮备液。取上述贮备液适量,加水配制成质量浓度分别为2.5、5、10、50、100、500、1 000和5 000 μg/ml的系列标准溶液。
2.3尿液样品的处理
取尿液50µl,加入10%高氯酸25µl,加水450µl,涡旋混匀10 s,于4℃下以离心半径3.5 cm、转速15 000 r/min离心10 min,取上清液,经0.2µm微孔滤膜滤过,取续滤液5 μl进样分析。
2.4方法学考察
2.4.1专属性在“2.1”项色谱与质谱条件下,他唑巴坦钠的保留时间约为2.45 min。尿液中他唑巴坦钠的色谱图见图1。2.4.2标准曲线的绘制与定量下限的考察取空白尿液50 μl,分别加入相应质量浓度的他唑巴坦钠标准溶液各适量,涡旋混匀,配制成相当于他唑巴坦钠质量浓度分别为0.25、0.5、1、5、10、50、100、500 μg/ml的含药尿液样品,按“2.3”项下方法处理后,进样分析,记录色谱图。以峰面积(As)为纵坐标、待测物质量浓度(c)为横坐标,进行线性回归(权重系数为w=1/c),得回归方程为As=42 900c+1 520(r=0.999 9)。结果显示,他唑巴坦钠尿药浓度在0.25~500 μg/ml范围内线性关系良好,定量下限为0.25 μg/ml。
2.4.3精密度与准确度试验参照《化学药物制剂人体生物利用度和生物等效性研究技术指导原则》[6],分别配制他唑巴坦钠低、中、高质量浓度(0.5、10和500 μg/ml)的含药尿液样品各5份,按“2.3”项下方法处理后,进样分析;测定3个分析批,根据当批标准曲线计算各样品的实测质量浓度,考察方法的精密度和准确度。结果显示,批内、批间RSD<10%,方法回收率为93.8%~111.8%,详见表1。

图1 尿液中他唑巴坦钠的色谱图A.空白尿液;B.空白尿液+他唑巴坦钠(10 μg/ml);C.受试者静脉滴注注射用头孢噻肟钠他唑巴坦钠5~8 h的尿液样本;1.他唑巴坦钠;2.空白尿液干扰峰Fig 1 Chromatograms of tazobactam sodium in urineA.blank urine;B.blank urine+tazobactam sodium(10 μg/m);C.urine sample from healthy volunteers 5-8 h after intravenous drip of Cefotaxime sodium tazobactam sodium for injection;1.tazobactam sodium;2. interference peak of blank urine
表1 精密度与准确度试验结果(±s,n=5)Tab 1 Results of recovery and precision tests(±s,n=5)

表1 精密度与准确度试验结果(±s,n=5)Tab 1 Results of recovery and precision tests(±s,n=5)
加入质量浓度,μg/ml方法回收率,% 0.5 10.500.批内精密度实测质量浓度,μg/ml 0.50±0.02 10.29±0.68 494.09±19.61 RSD,% 4.5 6.6 4.0批间精密度实测质量浓度,μg/ml 0.51±0.03 10.73±0.57 493.62±17.06 RSD,% 5.7 5.3 3.5 99.9±4.5 102.9±6.6 98.8±4.0
2.4.4提取回收率试验分别配制他唑巴坦钠低、中、高质量浓度(0.5、10和500µg/ml)的含药尿液样品各5份,按“2.3”项下方法处理后,进样分析,记录他唑巴坦钠峰面积(B1)。取空白尿液50 μl,按“2.3”项下方法处理后,得空白尿液提取液。分别取他唑巴坦钠标准溶液(5、100和5 000 μg/ml)5µl于离心管中,于37℃水浴中以氮气流吹干,残渣用适量空白尿液提取液复溶,涡旋混匀1 min,于4℃下以离心半径3.5 cm、转速15 000 r/min离心10 min,取上清液,经0.2µm微孔滤膜滤过后,取续滤液5µl进样分析,记录他唑巴坦钠峰面积(A1),上述样品分别配制5份(最终质量浓度与前者对应)。提取回收率(%)=B1/A1×100%。结果显示,各样品的提取回收率为93.9%~99.7%。
2.4.5稳定性考察分别配制他唑巴坦钠低、中、高质量浓度(0.5、10和500 μg/ml)的含药尿液样品各适量,考察各样品在室温放置2 h、4℃自动进样器内放置24 h、冷冻(-70℃)保存15 d(经历冻融1次)、30 d(经历冻融2次)等条件下的稳定性。结果显示,各样品在上述条件下稳定性均良好,RSD<8%。稳定性试验结果见表2。
2.4.6介质效应取空白尿液和水各适量,分别按“2.3”项下方法操作后,得空白尿液提取液和水提取液。采用文献[7]报道的方法,分别取他唑巴坦钠标准溶液(5、100和5 000 μg/ml)5 µl于离心管中,于37℃水浴中以氮气流吹干,残渣用空白尿液提取液取或水提取液525µl复溶,涡旋混匀1 min,于4℃下以离心半径3.5 cm、转速15 000 r/min离心10 min,取上清液,经0.2µm微孔滤膜滤过后,取续滤液5µl进样分析,记录他唑巴坦钠峰面积(A2或B2),各质量浓度分别配制5份。介质效应(%)=A2/B2×100%。结果显示,他唑巴坦钠的介质效应为87.6%~107.2%,表明在本试验条件下,他唑巴坦钠的测定不受介质效应的干扰[8]。
2.5尿药排泄动力学研究
2.5.1临床试验方案本试验经国家食品药品监督管理局批准、经南京医科大学第一附属医院医学伦理委员会审批同意,在药物临床试验机构进行。所有受试者签署知情同意书后接受全面体检,共入组健康受试者8例,其中男性和女性各4例,年龄20~38岁,身高156~178 cm,体质量50~68 kg。受试者在给药前一天晚上统一进食清淡饮食后,禁食10 h,不禁水过夜。于次日单次静脉滴注注射用头孢噻肟钠他唑巴坦钠2.34 g,以0.9%氯化钠注射液250 ml为溶剂,采用恒速输液泵给药,滴注时间为60 min。用药后2 h可进水,进食统一餐。试验期间受试者均住在病房内,禁服浓茶、咖啡和其他含咖啡因及醇类的饮料。收集各受试者给药前和给药后0~2、2~5、5~8、8~12和12~16 h的尿液,记录每个时间段尿量。
2.5.2计算方法采用Excel 2007计算:各时间段尿液样品中的药物浓度测定值与该时间段尿液体积相乘为该时间段药物排泄量;各时间段药物排泄量之和为药物的累积排泄量,其与给药剂量相比即得相应时间内的药物累积排泄率。
2.5.3试验结果8例健康受试者单次给予注射用头孢噻肟钠他唑巴坦钠2.34 g后,尿液中他唑巴坦钠的排泄量、累积排泄量和累积排泄率见表3,平均累积排泄量-时间曲线见图2,平均累积排泄率-时间曲线见图3。结果表明,他唑巴坦钠在给药后0~2 h的尿排泄量最大,8 h后基本排泄完全,16 h内尿液中的累积排泄量为(209.70±39.24)mg,累积排泄率为(61.7±11.5)%。
表2 稳定性试验结果(±s,n=5)Tab 2 Results of stability tests(±s,n=5)
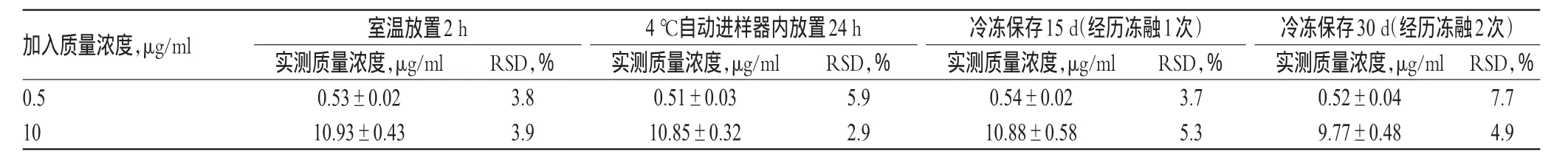
表2 稳定性试验结果(±s,n=5)Tab 2 Results of stability tests(±s,n=5)
加入质量浓度,μg/ml 0.5 10.室温放置2 h实测质量浓度,μg/ml 0.53±0.02 10.93±0.43 RSD,% 3.8 3.9 4℃自动进样器内放置24 h实测质量浓度,μg/ml 0.51±0.03 10.85±0.32 RSD,% 5.9 2.9冷冻保存15 d(经历冻融1次)实测质量浓度,μg/ml 0.54±0.02 10.88±0.58 RSD,% 3.7 5.3冷冻保存30 d(经历冻融2次)实测质量浓度,μg/ml 0.52±0.04 9.77±0.48 RSD,% 7.7 4.9
表3 他唑巴坦钠的排泄量、累积排泄量和累积排泄率(±s)Tab 3 Excretion amount,amount and accumulative excretion rate of tazobactam sodium(±s)
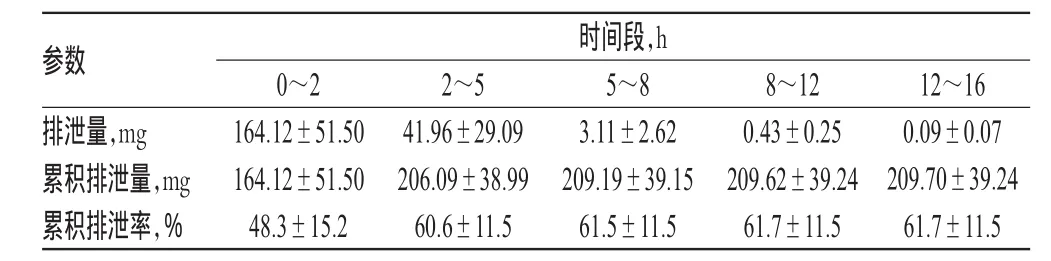
表3 他唑巴坦钠的排泄量、累积排泄量和累积排泄率(±s)Tab 3 Excretion amount,amount and accumulative excretion rate of tazobactam sodium(±s)
参数排泄量,mg累积排泄量,mg累积排泄率,%时间段,h 0~2 164.12±51.50 164.12±51.50 48.3±15.2 2~5 41.96±29.09 206.09±38.99 60.6±11.5 5~8 3.11±2.62 209.19±39.15 61.5±11.5 8~12 0.43±0.25 209.62±39.24 61.7±11.5 12~16 0.09±0.07 209.70±39.24 61.7±11.5
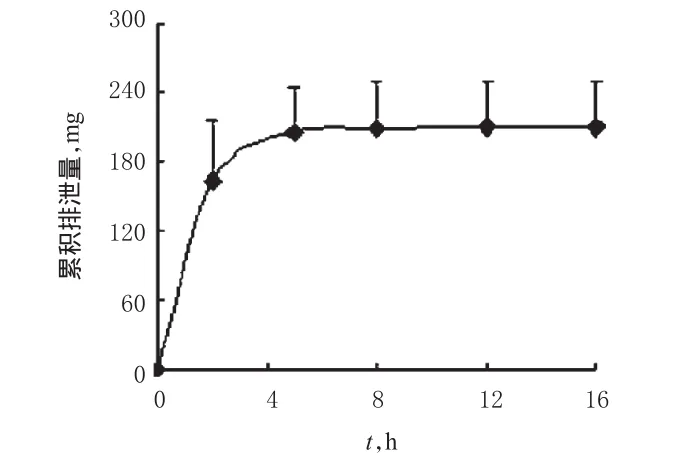
图2 他唑巴坦钠的平均累积排泄量-时间曲线Fig 2 Average accumulative excretion amount-time curve of tazobactam sodium
3 讨论
采用LC-MS/MS法测定人尿液中他唑巴坦钠的质量浓度已有文献报道,但其中并无详细的方法学考察过程及结果[9]。故本研究在已有文献的基础上,对所建立的LC-MS/MS法进行方法学考察。结果显示,该方法特异性好、灵敏度高。与文献报道的HPLC-紫外检测法[4-5]比较,该方法分析时间更短(<5 min)、线性范围更宽(0.25~500 μg/ml)。此外,方法学考察结果还显示,尿液中杂质均不干扰样本的测定,并可忽略介质效应的影响;批内、批间RSD<10%,提取回收率为93.9~99.7%;在室温放置2 h、4℃自动进样器内放置24 h、冷冻保存15 d和30 d等条件下均稳定,符合生物样品定量分析的要求[7],可用于人尿液中他唑巴坦钠浓度的测定和尿药排泄动力学的研究。
他唑巴坦钠在正离子条件下有较强且稳定的质谱效应,故以正离子方式进行检测。结果显示,以ESI为离子源,分子离子峰m/z 301和碎片离子峰m/z 168响应较强,故将定量离子对确定为m/z 301→168。为选择合适的鞘气、辅助气、碰撞气和CID电压,笔者分别对不同条件下他唑巴坦钠离子对的响应值进行了比较,选择了离子对响应最强的条件为最终的试验条件。质谱条件经优化后,他唑巴坦钠离子对响应强、灵敏度高。专属性考察过程中,笔者发现在,空白尿液的色谱图(见图1A)中,2.25 min处有一干扰峰,疑似为空白尿液的内源性物质,但该峰保留时间与他唑巴坦钠不同,且两者基线分离。在进行定量分析时,统一了积分参数,在此条件下标准曲线及各样本的结果均在可接受的范围内,故该干扰峰对测定结果的影响是可接受的。
本研究根据前期耐受性试验结果和Ⅱ期临床试验可能采用的剂量,将受试者的给药剂量确定为2.34 g。临床试验结果表明,健康受试者单次使用头孢噻肟钠他唑巴坦钠16 h后,他唑巴坦钠累积排泄率为(61.7±11.5)%,且主要经肾脏排泄,与文献[5-6]的结果相似。头孢噻肟钠他唑巴坦钠(6∶1)制剂尚未在肾功能不全的患者中进行尿药排泄动力学研究,故在后续试验中,应根据患者肾功能损害程度调整本制剂的给药剂量和间隔时间,为临床应用提供参考。
(本研究经国家食品药品监督管理局批准,临床试验批件号:2005L02508)
[1]梅亚宁,童明庆.2011年度卫生部全国细菌耐药监测网报告:成年患者分离菌的耐药监测[J].中国临床药理学杂志,2014,30(2):94.
[2]王霆,张春慧.头孢噻肟钠与β-内酰胺酶抑制剂复方研究进展[J].中国新药杂志,2010,19(5):377.
[3]陈苏婉,张守钗,王晓娟,等.不同配比的头孢噻肟/他唑巴坦的体外抗菌作用[J].华西药学杂志,2009,24(1):38.
[4]孙路路,单爱莲,吕媛.注射用头孢他啶/他唑巴坦(3∶1)在中国健康人体的单剂量药代动力学研究[J].中国临床药理学杂志,2012,28(8):584.
[5]孙路路,单爱莲,吕媛.注射用头孢他啶/他唑巴坦(5∶1)在中国健康人体的单次给药的药代动力学[J].中国临床药理学杂志,2013,29(9):669.
[6]国家食品药品监督管理局.化学药物制剂人体生物利用度和生物等效性研究技术指导原则[S].2005-03-18.
[7]叶显撑,范国荣,祝德秋.LC-MS/MS法测定人尿液中舒巴坦钠的浓度及其动力学研究[J].中国药房,2012,23(6):531.
[8]国家药典委员会.中国人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2010:363-368.
[9]许羚,盛玉成,郑青山.头孢噻肟钠他唑巴坦钠注射液静脉滴注在健康志愿者的临床药代动力学研究及其算法探讨[J].中国临床药理学与治疗学,2005,10(11):1 225.
(编辑:张元媛)
Concentration Determination of Tazobactam Sodium in Human Urine by LC-MS/MS and Urinary Excretion Dynamics Study
REN Liling1,WANG Yuanyuan2,SUN Luning2,ZHANG Hongwen2,XIE Lijun2,LIU Yun2,WANG Yongqing1,(21. College of Pharmacy,Nanjing Medical University,Nanjing 210029,China;2.Dept.of Pharmacy,the First Affiliated Hospital of Nanjing Medical University,Nanjing 210029,China)
OBJECTIVE:To establish a method for the concentration determination of tazobactam sodium in human urine,and to study urinary excretion pharmacokinetics.METHODS:The urine samples were extracted by 10%perchloric acid,and then determined by LC-MS/MS.The separation was performed on a Hypersil GOLD C18column with mobile phase consisted of ethanol-water(30∶70,V/V)at flow rate of 0.2 ml/min;the column temperature was set at 30℃,and sample size was 5 μl.ESI was used,and positive ion scanning was conducted in MRM mode;ion pair for quantitative analysis was m/z 301→168.8 healthy volunteers were given Cefotaxime sodium and tazobactam sodium for injection(6∶1,m/m)2.34 g intravenously,and then urine samples were collected before medication,0-2,2-5,5-8,8-12 and 12-16 h after medication.RESULTS:The linear range of tazobactam sodium was 0.25-500 μg/ml(r=0.999 9).The limit of quantitation was 0.25 μg/ml;RSDs of inter-batch and intra-batch were all lower than 10%;method recoveries were 93.8%-111.8%;extraction recoveries were 93.9%-99.7%;medium effect ranged 87.6%-107.2%.16 h after medication,accumulative excretion amount of tazobactam sodium in urine was(209.70±39.24)mg and accumulative excretion rate was(61.7±11.5)%.CONCLUSIONS:LC-MS/MS method can be used for the concentration determination of tazobactam sodium in human urine and excretion kinetics study.It is simple,rapid and sensitivity;tazobactam sodium mainly excrete viareral tissue.
LC-MS/MS;Tazobactam sodium;Urine;Urine concentration;Excretion pharmacokinetics
R969.1
A
1001-0408(2016)32-4501-04
10.6039/j.issn.1001-0408.2016.32.12
国家自然科学基金(面上项目)(No.81673515);国家自然科学基金(青年基金项目)(No.81503160);江苏省自然科学基金(青年科技人才专项资金)(No.BK20161591);江苏省“六大人才高峰”项目(No.2014-YY-001);江苏省卫生厅面上科研课题(No.H201108)
*硕士研究生。研究方向:临床药学。电话:025-86816192。E-mail:renliling6@126.com
主任药师,博士。研究方向:临床药学和临床药理学。电话:025-68136984。E-mail:wyqjsph@163.com
(2016-03-08
2016-08-20)
