防护口罩中甲醛及微生物检测方法的探讨
2016-12-13魏峰朱晓军王玥
魏峰++++朱晓军++++王玥


摘要:分析防护口罩测试标准中甲醛和微生物测试过程中可能存在的问题,结合现有技术和口罩实际使用过程,提出口罩测试标准中甲醛和微生物测试过程需要完善的地方,为更为正确地描述防护口罩的安全性和实用性提供数据支撑,为更好地保护消费者身体健康提供标准保障。
关键词:防护口罩;重点关注项目;甲醛;微生物
我国目前在防护口罩尤其是PM2.5防护口罩的销售市场高速增长。为监测防护口罩的质量,保护消费者的身体健康,以更为有效地防止雾霾的侵扰,国家相继出台了相关标准,主要有GB 2626—2006《呼吸防护用品 自吸过滤式防颗粒物呼吸器》,TAJ001—2015《PM2.5防护口罩》和GB/T 32610—2016《日常防护型口罩技术规范》等。这些标准在口罩的防护效率、泄漏率、防护效果、偶氮、pH值、微生物等方面规定了限值和测试方法,但是通过分析研判这些标准,结合现有口罩实际情况,本文认为国内出台的口罩防护标准中在甲醛和微生物测试方面仍存在着一定的不足之处,难以正确合理地评估防护口罩在实际佩戴过程中由于产品本身的问题给消费者带来的潜在危害。由此,本文提出了在口罩测试标准中需要完善的部分,以更为准确地评价产品的性能。
1 甲醛
1.1 甲醛危害及防护用品中甲醛检测依据
20世纪20年代以来,纺织用甲醛树脂开始在面料整理中使用,在纺织印染行业助剂中添加甲醛,可以达到防缩水、抗皱、防水、防褪色、阻燃等功能[1]。此外,在助剂中添加甲醛还能够满足保持印花、染色的耐久性和改善手感等需求。甲醛是一类致癌和致畸性物质,会对人体健康造成危害。因此,国家对纺织品中的甲醛含量进行了严格规定,分别针对儿童、成人非直接接触衣物和成人直接接触衣物等进行了限值规定[2]。
近年来,口罩中采用棉纱布或无纺布制造口罩时,也同样面临着甲醛超标问题。因此,在这两年新出台的口罩标准TAJ 1001—2015和GB/T 32610—2016中均对口罩中甲醛的含量进行了限定。这两份标准中规定甲醛的测试采用GB/T 2912.1—2009《纺织品 甲醛的测定 第1部分:游离和水解的甲醛(水萃取法)》标准执行,甲醛含量的测定采用乙酰丙酮比色法。但是,尽管该方法具有很强的实用性,但在实际测定过程中,仍然存在着一些问题,会影响到样品中甲醛含量的测定结果。主要问题为:
一是分光光度计的吸光度范围问题,分光光度法中吸光度在0.2~0.8之间时数据采信度较高,被测试试样的吸光度太大或太小,都可能会产生比尔定律偏离。因此在吸光度测定时,还需考虑到吸光度问题,浓度过高时需进行溶液稀释;而浓度过低时,则需要加大取样量,以获得满意的精度。无疑,这会增加测试过程的工作量以及实验室成本。
二是双甲酮的确认问题,在标准中规定,如果怀疑吸收不是来自于甲醛而是受其他因素影响,则需用双甲酮进行确认试验[3]。因此,对于样品中出现的甲醛是否需要进行确认试验,则是由检测人员自行决定。同样地,对于实验室之间数据的一致性和人力物力的成本都会带来一定的麻烦。
三是萃取过程中样品的褪色问题,如果在萃取过程中产品出现褪色现象,会污染到萃取液并干扰到检测结果,使得测试结果发生偏离[1,4]。
四是干扰物质存在问题,在萃取过程中,比色法会受到一些化学物质如酚、SO2、胺等物质的干扰,进而影响到测试结果的准确性[4]。
五是乙醛等物质存在的问题。通常来说,在产品处理过程中加入甲醛进行整理时,会引入到乙醛等物质,而乙醛同样会对人体产生危害,低浓度的甲醛同样会引起眼、鼻及上呼吸道刺激症状及支气管炎。高浓度吸入则会有一定的麻醉作用,对皮肤也存在有致敏性。采用比色法无法对乙醛等其他有害物质的存在进行检测。
基于此,本文采取了高效液相色谱法检测口罩中甲醛的含量,以有效地排除在比色法萃取及测量过程中产生的各种干扰,以更快更准确地测试出口罩中所含有甲醛的真实含量。
1.2 试验部分
(1)仪器与试剂
Agilent 1260高效液相色谱仪,检测器为DAD检测器(安捷伦科技有限公司);Milli-Q超纯水仪(美国Millipore公司);DKZ-450B型电热恒温振荡水槽(上海森信实验仪器有限公司);XS205DU电子天平(梅特勒—托利多仪器有限公司)。
甲醛标准品:10500 mg/L,购买于中国计量科学研究院。乙腈(HPLC级,德国Merck公司);DNPH(分析纯,国药集团化学试剂有限公司);磷酸(优级纯,国药集团化学试剂有限公司);超纯水(18.2 MΩ·cm)。
(2) 标准溶液的配制
DNPH溶液的配制:1.2g DNPH加入到30 mL水和170mL浓磷酸中,溶解后得到DNPH溶液。
取0.1mL甲醛标准溶液,移入装有20mL蒸馏水的50mL容量瓶中,振荡摇匀后用蒸馏水稀释至刻度,即为甲醛标准母液。随后,在8个10mL容量瓶中,分别加入4 mL乙腈,然后分别加入0.005mL、0.025mL、0.05mL、0.25mL、0.50mL、1.0mL、2.5mL和5.0 mL的甲醛标准母液,立即加入0.5 mLDNPH溶液,摇匀后用蒸馏水稀释至刻度,放置60min后经0.45μm滤膜过滤后上机分析,制作甲醛标准曲线。
(3) 样品的处理
准确称取2g试样(精确至0.1 mg),放入到100 mL锥形瓶中,加入50 mL去离子水后在40℃水浴中振荡60 min后过滤至锥形瓶中,冷却至室温后备用。
将4 mL乙腈、5 mL过滤后萃取液和0.5 mL二硝基苯肼溶液加入到10 mL容量瓶中,蒸馏水定容后,放置衍生60 min后经0.45 μm滤膜过滤后上机分析。
(4)液相色谱条件
色谱柱:Eclipse XDB C18 (4.6mm×250mm,5μm);进样量:20μL;柱温:30 ℃;检测波长:350nm;流速:1mL/min;流动相A:超纯水;流动相B:乙腈。洗脱程序:40% A;运行时间10min。
1.3 结果与讨论
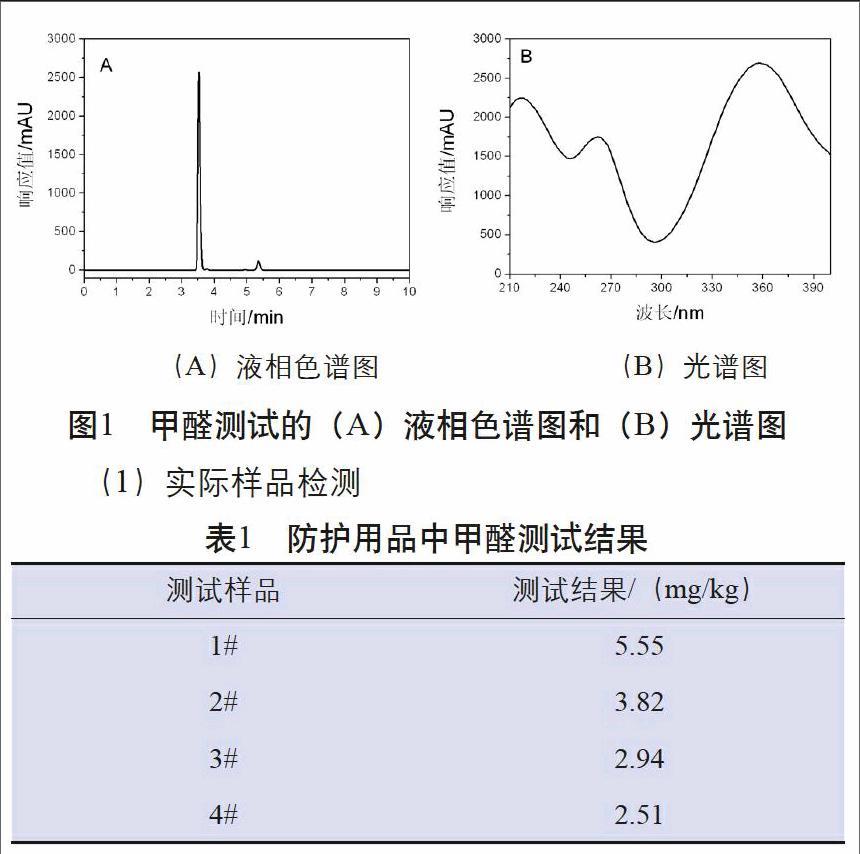
甲醛经衍生后通过高效液相色谱分析后的色谱图和光谱图见图1。其中色谱图上3.5min处为DNPH色谱峰,5.25min处为甲醛-DNPH色谱峰。标准曲线在0.01mg/L~10mg/L范围内与峰面积呈现线性关系,线性相关系数为0.99973。
(1)实际样品检测
通过本文所采用方法对4种防护用品分别进行检测,测试结果见表1。从表中可以明显可出,4种防护口罩均检测出少量的甲醛,尽管含量低于标准中要求的甲醛检出值,但是当使用比色法进行防护口罩中甲醛的检测时,测试过程中的干扰极有可能会影响到最终的判定。与此同时,图2给出了其中一个样品的测试色谱图,峰1为甲醛,峰2和峰3分别为乙醛和丙酮与DNPH的衍生物。在测试过程中,有少量的乙醛和丙酮被检测出,也说明防护口罩中确实是会存在着其他的有毒有害物质。
(2)方法回收率与精密度
对样品进行添加回收试验,共选取两个浓度进行试验,每个浓度水平进行5次重复试验,方法回收率和精密度见表2。结果表明,加标回收率范围在88.80% ~ 102.5%之间,相对标准偏差(RSD)为1.5% ~ 6.2%。
2 微生物
2.1 微生物危害及防护用品中微生物的限值
雾霾天气微生物会附着在颗粒物上,目前已知的雾霾空气中大约有1300种微生物[5],其中有部分已知微生物会引发人类的过敏和肺部疾病。在新颁布的防护口罩标准TAJ 1001—2015和GB/T 32610—2016中均对防护口罩中微生物进行了限值规定,其中大肠菌群和致病性化脓菌不得检出,真菌菌落总数和细菌菌落总数分别不大于100 cfu/g 和200 cfu/g。
值得注意的是,由于佩戴防护口罩的雾霾空气中往往会存在着一定量的微生物,但目前市售的防护口罩中大部分都不具有抗菌性,因此这就会使得在使用过程中附着在颗粒物上的微生物被吸附过滤在防护口罩上。消费者佩戴防护口罩时的局部微环境为微生物的生长提供了合适的温湿度,在吸气过程中就极有可能将微生物吸入呼吸道,从而带来二次污染。鉴于此,针对防护口罩在附着有一定微生物时,在一定温度和时间下,微生物是否还存在就成为一个值得研究的问题。
2.2 试验部分
(1) 仪器与试剂
恒温培养箱(上海一恒科学仪器有限公司);水浴锅(上海森信实验仪器有限公司,DKZ-450B型);恒温调速摇瓶柜(上海知楚仪器有限公司,ZQTY-70S型);高压灭菌锅(上海申安医疗器械厂,LDZM-60KCS型);二级生物安全柜(美国Thermo,1300-A2型)。
大豆蛋白胨肉汤(TSB);大豆蛋白胨琼脂培养基(TSA);营养肉汤(NB);SCDLP液体培养基;稀释液;计数培养基(EA),均采购于北京陆桥技术有限责任公司。
菌种:大肠杆菌 (ATCC 11229)。
(2)冻干菌的活化
将冻干菌融化分散在5 mL的TSB中呈悬浮状,在37℃下培养24 h;用接种环取菌悬液以划线法接种到TSA平皿上,在37℃下培养24 h;从培养皿上取典型菌落接种在TSA斜面试管内,在37℃下培养24 h,斜面试管储存于冰箱内(5℃~10℃)作为保存菌。
(3) 试验菌液的培养和制备
培养A:用接种环取保存菌,以划线法接种EA平面皿上,在37℃下培养24 h。
培养B:取20 mL肉汤NB放入到100 mL的锥形瓶内,用接种环取培养A的典型菌落接种在肉汤内培养,培养条件为温度37℃,振动频率为110 min-1,时间为24 h。
培养C:取20 mL肉汤NB放入到100mL的锥形瓶内,取0.4mL培养B菌液加入瓶内培养,培养后菌浓度为107cfu/mL。培养条件为温度37℃,振动频率为110min-1,时间为3h。
试样菌液的制备:用水对肉汤NB进行稀释,调节培养C的菌液浓度为103 cfu/mL,作为试验菌液。
采用分光光度计测定菌液浓度。
(4)样品的处理
试样的接种:取0.2 mL试验菌液分散接种在小瓶内的试样(试样质量4.00 g)上。
培养及洗脱:将已接种试验菌液的小瓶在37℃下分别培养0h、24h、144h和168h。随后在培养后小瓶中分别加入20mL SCDLP培养基,振荡器振荡5次后将细菌洗下。
菌落数的测定:取1 mL上述溶液分别注入两个平皿内,各加入15 mLEA,室温下放置至培养基凝固后,将平皿倒置放置在37℃下培养48 h,随后对菌落总数进行计数。
2.3 结果与讨论
常用防护口罩主要分为一次性防护口罩和可更换性防护口罩。由于一次性防护口罩使用周期较短,因此本试验只针对4种防护口罩开展了0 h和24 h微生物生长情况培养。对于可更换性防护口罩,则将时间分别设定为0h、24h、144h和168h。
图3给出了一次性防护口罩在0 h和24 h的微生物生长情况,从图中可以明显看出,4种一次性防护口罩在0 h时菌落总数较少,约为5~12 个;经过24 h后,菌落总数有了显著的增加,增长为300~400个左右(表3),充分表明当微生物附着在口罩上时,合适的温度会促进菌群的生长。
可更换性防护口罩的结果也表明了相同的趋势(图4),即24 h后菌落总数增长明显,但144 h和168 h的菌落总数有所回落(表3),这可能是时间较长,部分菌出现凋亡所致。
3 结语
(1)在测试口罩中甲醛的含量时,采用比色法会对最终结果带来一定的干扰,而选择采用高效液相色谱法时,则会弥补比色法的诸多缺陷,能够更为准确地给出口罩中甲醛的真实含量;因此,本文建议在口罩中甲醛的测试方法标准应修订为液相色谱法,以避免假阳性样品的检出。
(2)即使新购买的防护口罩在测试时微生物指标是合格的,但是由于空气中存在着微生物,在使用者佩戴口罩的微环境中,仍可以检测到微生物的增殖,从而为消费者带来二次污染。因此,建议防护口罩能够采用抗菌性技术,并且在防护口罩的测试标准中增加抗菌性能测试,以更为有效地保护公众健康。
参考文献:
[1]谢思瑶. 消除纺织品甲醛检测中褪色干扰的研究[J].山西大同大学学报:自然科学版, 2016, 32(1): 45-47.
[2] GB 18401—2010《国家纺织产品基本安全技术规范》[S].
[3] GB/T 2912.1—2009《纺织品 甲醛的测定 第1部分:游离和水解的甲醛(水萃取法)》[S].
[4]张春玲. 高效液相色谱法测定纺织品中游离甲醛含量[J].现代测量与实验室管理, 2007, (4): 11-13.
[5] 田埂. 雾霾中的“危险分子”[J].生命世界, 2014, (6): 54-57.
(作者单位:无锡出入境检验检疫局)
