HABR反应器硫酸盐型厌氧氨氧化启动特性研究
2016-12-07李军向韬郑驰骏
李军,向韬,郑驰骏
(沈阳建筑大学市政与环境工程学院,辽宁沈阳110168)
Li Jun,Xiang Tao,Zheng Chijun
(SchoolofMunicipaland EnvironmentalEngineering,Shenyang Jianzhu University,Shenyang110168,China)
HABR反应器硫酸盐型厌氧氨氧化启动特性研究
李军,向韬,郑驰骏
(沈阳建筑大学市政与环境工程学院,辽宁沈阳110168)
试验探讨了复合式厌氧折流板反应器(HABR)里硫酸盐型厌氧氨氧化启动特性及不同COD对系统的影响。通过提升进水基质浓度成功启动硫酸盐型厌氧氨氧化。结果表明,硫酸盐型厌氧氨氧化是分步进行的,一号、三号和四号隔室所进行的主要反应各不相同。NH4+-N、SO42-、COD去除效果稳定,最高值分别为52.2%、53.7%、60.9%。较低的COD(60~150mg/L)能促进硫酸盐型厌氧氨氧化的进行,COD过高会抑制厌氧氨氧化菌活性。
硫酸盐型厌氧氨氧化;复合式厌氧折流板反应器;颗粒污泥
Li Jun,Xiang Tao,Zheng Chijun
(SchoolofMunicipaland EnvironmentalEngineering,Shenyang Jianzhu University,Shenyang110168,China)
工业废水中常含有大量的氨氮和硫化物,传统的生物脱氮技术能完成脱氮的任务,但不能有效处理硫酸盐。因此寻找有效的同步脱氮、除硫方法便成为废水处理领域普遍关注的问题。
2001年,F.Fdz-Polanco等〔1〕在处理甜菜酒糟废水的试验中首次发现了硫酸盐和氨氮的同步去除现象,并伴有元素硫和氮气的生成,通过推测,认为发生了以下反应:

国内外相关研究表明〔2-4〕,硫酸盐型厌氧氨氧化反应确实存在,它能够较好地解决同时含有氨氮和硫酸盐废水的处理问题,且不需要有机碳源介入,污泥产率低、节约能源、运行费用低,能够同步脱氮除硫,反应产物可回收,无二次污染。
目前在不同的反应器里都实现了硫酸盐型厌氧氨氧化的启动,如利用上流式厌氧污泥床(UASB)〔5〕、序批式厌氧反应器(ASBR)〔6〕、上流式厌氧附着膜膨胀床〔7〕成功启动硫酸盐型厌氧氨氧化。另外。蔡靖等〔8-9〕研究发现,芽孢杆菌是硫酸盐型厌氧氨氧化的优势菌种。但是在复合式厌氧折流板反应器(HABR)里进行硫酸盐型厌氧氨氧化启动的研究还比较少,而且对于启动机理的探究多从单一菌种的整体反应出发,对于过程中发生分步反应的研究还不够深入。
试验通过检测HABR中不同隔室的硫酸盐、氨氮、有机物等的降解情况,从硫酸盐厌氧氨氧化分步反应的机理出发,探究了硫酸盐型厌氧氨氧化的启动特性,还研究了COD对系统的影响,以期为硫酸盐型厌氧氨氧化的应用提供参考。
1 材料与方法
1.1 试验装置
试验采用HABR复合式厌氧折流板反应器,反应器的体积为9.3 L,有效体积为8.4 L,分为4个格室。每个格室的尺寸为20.00 cm×5.00 cm×6.75 cm,折板的有效高度为18 cm。各隔室中加入软性纤维填料,填充比为30%。反应器主体包裹有恒温水浴外层,外层中设有加热棒保证适宜温度。通过氮气瓶每天向进水水箱曝氮气15~20min,保证试验所需的厌氧环境。
1.2 试验用水
试验用水为人工配制模拟废水,模拟废水成分为:CH3COONa、NH4Cl、Na2SO4(按需配制)、NaHCO3(1 000 mg/L)、KH2PO4(27 mg/L)、CaCl2·2H2O(136 mg/L)、MgCl2·2H2O(200mg/L),微量元素1(1mL/L)、微量元素2(1mL/L)。其中微量元素1组成:EDTA(5 000mg/L)、FeSO4(5 000mg/L);微量元素2组成:EDTA(5 000mg/L)、ZnSO4·7H2O(430mg/L)、CoCl2· 6H2O(240mg/L)、MnCl2·4H2O(990mg/L)、CuSO4· 5H2O(250 mg/L)、NiCl2·6H2O(190 mg/L)、H3BO4(14 mg/L)。用碳酸氢钠调节模拟废水pH 7.0~8.5,温度(32±1)℃,溶解氧<0.5mg/L。
1.3 接种污泥
接种污泥为实验前期已经驯化成熟的硫酸盐还原菌颗粒污泥,MLSS为8 300mg/L。
1.4 分析项目和方法
SO42-:铬酸钡光度法,T6新世纪紫外/可见分光光度计;NH4+-N:纳氏试剂光度法,T6新世纪紫外/可见分光光度计;COD:快速密闭催化消解法,T6新世纪紫外/可见分光光度计;NO3--N:酚二磺酸光度法,T6新世纪紫外/可见分光光度计;NO2--N:N-(1-萘基)-乙二胺光度法,T6新世纪紫外/可见分光光度计;S2-:对氨基二甲基苯胺光度法,T6新世纪紫外/可见分光光度计;DO:上海雷磁JPB-607A便携式溶解氧仪;pH:pHS-25型便携式pH计;温度:普通温度计;MLSS:重量法,上海精宏DHG-9240A电热干燥箱。
1.5 试验方法
前30 d将NH4+-N与SO42-分别控制在50、150 mg/L左右,之后将它们的质量浓度同时提升至原来的2倍,COD始终控制在50mg/L左右。研究不同隔室中NH4+-N、COD、SO42-、S2-、S0、NO2--N、NO3--N等指标的变化情况,分析启动过程中HABR反应器各个隔室中所进行的分步反应,最后逐步提高COD研究其对整个系统的影响。
2 结果与讨论
2.1 HABR各隔室去除效果与分析
2.1.1 HABR各隔室去除结果
HABR各隔室去除NH4+-N结果如图1所示。
反应器启动前30 d NH4+-N进水及各隔室浓度几乎保持一致,NH4+-N去除率不高,第30天起,将NH4+-N浓度提升为原来的2倍,各隔室浓度曲线逐渐分离,总体趋势沿水流方向逐隔室减少,其中一、二号隔室NH4+-N浓度曲线较接近,明显高于相互
接近的三、四号隔室曲线,这表明NH4+-N的降解主要发生在一号隔室和三号隔室。NH4+-N进水浓度和一号隔室浓度之差随进水负荷的增高而增大,二号隔室与三号隔室NH4+-N浓度之差亦随之不断增大直至稳定。试验表明,随着反应的进行,一、三号隔室中降解NH4+-N的菌种逐渐适应了环境。一、三号隔室对NH4+-N去除量比约为2∶1。NH4+-N去除率稳定在50%左右,最高达52.2%。
各隔室中SO42-含量变化如图2所示。

图1 各隔室中NH4+-N含量变化
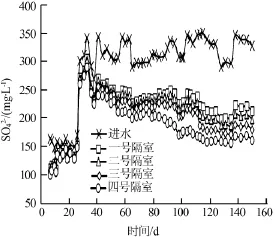
图2 各隔室中SO42-含量变化
由图2可见,试验前30 d,一号隔室SO42-浓度略小于进水浓度,其余隔室浓度与一号隔室相差不大。从第30天开始,提高进水SO42-浓度为初始时的2倍,随反应器的运行SO42-进水浓度曲线逐渐与各隔室浓度曲线分离,一、二、三号隔室中SO42-浓度曲线相差较小,三号隔室与四号隔室SO42-浓度曲线在反应器运行稳定阶段逐渐分离。SO42-进水浓度与一号隔室浓度之差不断增大。试验表明,SO42-的降解大部分发生在一号隔室,反应后期四号隔室也出现了部分SO42-的降解。SO42-去除率最后稳定在50%左右,最高达53.7%。
图3所示的是各隔室COD变化情况。

图3 各隔室中COD含量变化
与SO42-浓度曲线变化相类似,前30 d进水COD稍高于各隔室COD,各隔室COD基本持平。从第30天起,各隔室COD曲线与进水COD曲线逐渐分离,进水COD与一号隔室COD之差随反应进行逐渐增大直至稳定。从第40天起,四号隔室COD曲线也与一、二、三号隔室曲线分离。整个过程中,一、二、三号隔室COD曲线分离程度不大,以一号隔室去除的COD为多,四号隔室中COD的降解量平均为8.1 mg/L。这表明COD的降解去除主要发生在一号隔室,四号隔室也出现了较明显的COD降解。反应器运行至第150天时,各隔室去除效果基本稳定。COD最大去除率为60.9%,反应器运行稳定。
各隔室中NO2--N含量变化如图4所示。

图4 各隔室中NO2--N含量变化
由图4可见,试验前30 d各隔室中NO2--N含量很低。第30天到第50天,反应器内4个隔室都出现了NO2--N积累,且各隔室积累量大致相同。第50天到第73天,4个隔室NO2--N浓度曲线出现了明
显的分离,且都呈现出上升趋势,一、二号隔室曲线上升幅度最大,且相互接近;三号隔室NO2--N浓度曲线次之;四号隔室NO2--N浓度曲线上升幅度最小。第73天到第150天,一、二号隔室曲线依然保持相近的变化趋势,三号隔室开始下降,二号隔室与三号隔室浓度之差随着反应进行而不断增大,直至趋于稳定,平均质量浓度差约为16.5mg/L。四号隔室NO2--N质量浓度呈下降趋势,至反应器运行稳定时四号隔室NO2--N质量浓度平均为1.3mg/L。以上现象说明,NO2--N的积累主要发生在一号和二号隔室内,三号隔室与四号隔室内发生以NO2--N为底物的转化反应,两个隔室转化量比约为1.33∶1。
另外,反应器前30 d没有检测到NO3--N的积累,从第30天到第80天,四个隔室中均检测到NO3--N浓度变化,且从第30天开始,各隔室NO3--N浓度曲线出现分离,一、二、三隔室中NO3--N浓度曲线几乎重合,第30天至第50天,三个隔室中NO3--N都出现了快速累积,最大积累量为15.1mg/L,第50天到第80天,NO3--N积累量迅速下降,至第80天时NO3--N积累情况消失。四号隔室NO3--N浓度曲线变化不大,没有出现大量积累。以上现象表明,反应器前3个隔室中出现了NO3--N的积累,四号隔室发生了以NO3--N为底物的转化反应。
反应器中S2-浓度变化情况与SO42-浓度变化相类似,前30 d硫酸盐还原菌有一定优势,S2-呈现下降趋势,之后,各隔室S2-浓度曲线发生分离,一、二、三号隔室呈上升趋势且浓度曲线很接近,四号隔室S2-浓度曲线上升幅度小,与其余隔室逐渐分离。三号隔室与四号隔室曲线浓度之差逐渐变大并最终稳定。说明一号隔室中S2-正在积累,四号隔室降解转化了部分S2-,一号隔室S2-最大生成量为73.1mg/L,四号隔室最大转化量为33.1mg/L。
2.1.2 HABR中各隔室分步反应分析
一号隔室:由前面分析可知,反应器运行稳定阶段,一号隔室中NH4+-N与SO42-同时被去除,且由分析可见,在反应器进水并未添加NO2--N和S2-的情况下,两者均出现一定积累,说明式(1)所示的反应主要发生在一号隔室。图3中COD的降解,以及反应器中NO3--N含量的上升表明还存在着部分硫酸盐还原反应和硝化反应。第50天至第80天时NO3--N积累量下降,硫酸盐型厌氧氨氧化逐渐占据主导地位,发生了式(2)所示反应。
二号隔室:各项指标在二号隔室中的浓度曲线
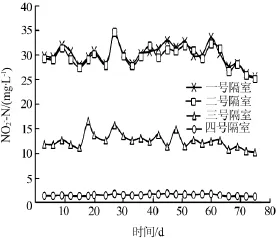
图5 不同COD下NO2--N含量变化
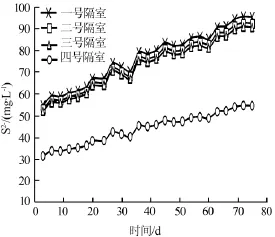
图6 不同COD下S2-含量变化
本阶段反应第1天—第15天,第15天—第30几乎与一号隔室中的浓度曲线相重合,表明二号隔室中没有出现各个指标的大量降解,一些微小变化也应该是其中的细胞内源呼吸、生长过程的代谢消耗所致。
三号隔室:由前面的分析可知,三号隔室中NH4+-N与NO2--N去除量之比约为1.16∶1,与理论去除量比1.32∶1接近,主要发生了式(3)所示厌氧氨氧化反应。考虑到HABR中复杂的菌群环境,笔者认为在三号隔室中除厌氧氨氧化反应之外,还发生了其他反应,也可能存在着微生物自身的代谢消耗。
四号隔室:由图2、图3可见,三号隔室的COD、SO42-浓度曲线与四号隔室出现分离,表明四号隔室同时去除了COD、SO42-,发生了硫酸盐还原反应。另外NO2--N和S2-的浓度曲线也出现分离,说明四号隔室同时去除了NO2--N和S2-,发生式(2)所示的反应。
2.2 不同COD下各隔室NO2--N、S2-变化情况分析
图5、图6所示为不同COD梯度下各隔室NO2--N、S2-变化情况。
天阶段分别对应的进水COD为60、90mg/L。此时各隔室NO2--N浓度与前一阶段启动末期NO2--N浓度总体相差不大,表现为一号隔室生成NO2--N,三、四号隔室去除NO2--N。此时COD相对较低,硫酸盐还原菌活性变化不大,还原S2-量变化也不大,对式(2)发生的反应过程影响不显著,反应器总体去除效果上表现为NH4+-N、SO42-去除率变化较小。由于COD呈梯度提升,则此时反应器中各隔室中S2-浓度表现为缓慢上升趋势,体系内S2-不断积累。试验第30天—第45天、第45天—第60天阶段,此时COD进水分别为120、150mg/L,图6中各隔室S2-浓度继续上升,表明一号隔室中硫酸盐还原菌活性有所增强,且三号隔室与四号隔室浓度曲线之差有所增大,表明四号隔室中发生的式(2)反应因为S2-浓度的增加而得到了促进,从整体上表现为NH4+-N、SO42-去除率均有所上升,硫酸盐型厌氧氨氧化反应得到了促进。
试验第60天—第75天阶段,COD进水提升至为180mg/L,图5中一号隔室NO2--N浓度曲线呈下降趋势,这是因为由于COD的持续提升,一号隔室中硫酸盐还原菌活性增强,逐渐占据优势地位,SO42-还原量加大,与一号隔室中式(1)所示硫酸盐型厌氧氨氧化过程形成对底物SO42-的基质竞争关系,并占据竞争优势,从而对一号隔室中的硫酸盐型厌氧氨氧化产生了抑制,由NH4+-N转化产生的NO2--N的量减少。图6中S2-浓度在此时依然保持上升的趋势,也佐证了一号隔室中硫酸盐还原菌成为优势菌这一观点。从整体反应体系上看NH4+-N转化效果受到抑制,NH4+-N去除率下降,相应的SO42-去除率也有所下降。
3 结论
通过对HABR中各隔室内NH4+-N、SO42-、COD、NO2--N、NO3--N、S2-等指标的分析,结果表明HABR中硫酸盐型厌氧氨氧化反应是分隔室、分步骤进行的,一号隔室中主要进行式(1)中所示反应;三号隔室中主要进行式(3)所示厌氧氨氧化过程;四号隔室中主要进行式(2)中所示反应。一号隔室中细菌种群组成复杂,沿反应器水平方向隔室细菌种群逐渐减少,呈现单一化趋势。硫酸盐型厌氧氨氧化启动成功。
硫酸盐型厌氧氨氧化适宜在低COD下进行,较低的COD使硫酸盐型厌氧氨氧化菌群与其他伴生菌群互惠互利,协同共生,促进反应进行,但较高的COD使硫酸盐型厌氧氨氧化菌群与伴生菌群关系变为竞争抑制。适当提高NH4+-N、SO42-浓度,对反应器运行效果有促进作用。
[1]Fdz-Polanco F,Fdz-Polanco M,Fernandez N,et al.New process for simultaneous removalofnitrogen and sulphurunderanaerobic conditions[J].WaterResearch,2001,35(4):1111-1114.
[2]Liu Sitong,YangFenglin,Gong Zheng,etal.Application ofanaerobic ammonium-oxidizing consortium to achieve comp letely autotrophic ammonium and sulfate removal[J].Bioresource Technology,2008,99(15):6817-6825.
[3]Yang Zhiquan,Zhou Shaoqi,Sun Yanbo.Start-up of simultaneous removalofammonium and sulfate from an anaerobic ammonium oxidation(ANAMMOX)process in an anaerobic up-flow bioreactor[J]. Journalof HazardousMaterials,2009,169(13):113-118.
[4]赵庆良,李巍,徐永波,等.厌氧附着生长反应器处理氨氮和硫酸盐废水的研究[J].黑龙江大学:自然科学学报,2007,24(4):421-426.
[5]赖杨岚.硫酸盐型厌氧氨氧化的启动特性与影响因素研究[D].广州:华南理工大学,2011.
[6]李祥,黄勇,袁怡,等.自养厌氧硫酸盐还原/氨氧化反应器启动特性[J].化工学报,2012,63(8):2606-2611.
[7]张蕾,郑平,何玉辉,等.硫酸盐型厌氧氨氧化性能的研究[J].中国科学:B辑,2008,38(12):1113-1119.
[8]蔡靖,蒋坚祥,郑平.一株硫酸盐型厌氧氨氧化菌的分离和鉴定[J].中国科学:化学,2010,40(4):421-426
[9]刘正川,袁林江,周国标,等.从亚硝酸还原厌氧氨氧化转变为硫酸盐型厌氧氨氧化[J].环境科学,2015(9):3345-3351.
Research on the start-up characteristics ofsulfate-dependent anaerobic ammonium oxidation in HABR
The influences of the start-up characteristics ofsulfate-dependentanaerobic ammonium oxidation in hybrid anaerobic baffle reactor(HABR)and differentCOD on the system havebeen tested and discussed.The sulfatedependentanaerobic ammonium oxidation hassuccessfully been started up by upgrading the concentration of influent substrates.The resultsshow thatsulfate-dependentanaerobic ammonium oxidation proceeds step by step.Themain reactions proceeding in Compartment No.l,3 and 4 are different.The removing rates of NH4+-N,SO42-,and COD keep stable and themaximum values are 52.2%,53.7%,60.9%,respectively.Lower COD(60-150mg/L)can promote the proceeding of the sulfate-dependent anaerobic ammonium oxidation.However,if its COD is too high,the activity ofanaerobic ammonium oxidation bacteria can be inhibited.
sulfate-dependentanaerobicammonium oxidation;hybrid anaerobicbaffle reactor;particlesludge
X703.3
A
1005-829X(2016)11-0024-05
李军(1978—),博士,副教授。电话:024-24690710,E-mail:junlee@sjzu.edu.cn。
2016-09-18(修改稿)
国家自然科学基金项目(51108277);辽宁省高等学校优秀人才支持计划项目(LJQ2012051);辽宁省科学技术计划项目(2012225086)
