钴掺杂Sr1.5La0.5M nO4的合成及高温电化学性能研究
2016-12-05范宇航孙丽萍霍丽华赵辉JeanMarcBassatAlineRougierSbastienFourcadeJeanClaudeGrenier
范宇航 孙丽萍 霍丽华 赵辉*,Jean-Marc BassatAline RougierSébastien FourcadeJean-Claude Grenier
(1黑龙江大学化学化工与材料学院,功能无机材料化学教育部重点实验室,哈尔滨150080)
(2CNRS,Universitéde Bordeaux,ICMCB,87 avenue du Dr.A.Schweitzer,F-33608 Pessac-Cedex,France)
钴掺杂Sr1.5La0.5M nO4的合成及高温电化学性能研究
范宇航1孙丽萍1霍丽华1赵辉*,1Jean-Marc Bassat2Aline Rougier2Sébastien Fourcade2Jean-Claude Grenier2
(1黑龙江大学化学化工与材料学院,功能无机材料化学教育部重点实验室,哈尔滨150080)
(2CNRS,Universitéde Bordeaux,ICMCB,87 avenue du Dr.A.Schweitzer,F-33608 Pessac-Cedex,France)
采用EDTA-柠檬酸法合成了中温固体氧化物燃料电池阴极材料Sr1.5La0.5Mn1-xCoxO4(SLMCO x),并利用粉末X射线衍射XRD)、X射线光电子能谱(XPS)以及电化学交流阻抗谱(EIS)进行表征。结果表明,该材料与Ce0.9Gd0.1O1.95(CGO)在1 200℃烧结2 h不发生化学反应。随着Co掺入量的增加,氧化物中Mn3+和Co2+含量增多,晶格氧含量降低,晶格畸变率增大。交流阻抗谱EIS)测试结果显示,钴的掺杂明显降低电极的极化电阻,其中Sr1.5La0.5Mn0.7Co0.3O4阴极在700℃空气中的极化电阻为0.62Ω· m2,明显小于Sr1.5La0.5MnO4阴极在750℃的极化电阻(1.5Ω·cm2),表明钴掺杂的Sr1.5La0.5Mn1-xCoxO4是一种潜在的IT-SOFC阴极材料。
中温固体氧化物;燃料电池;阴极材料
0 引言
固体氧化物燃料电池(SOFC)是一种将化学能直接转化为电能的全固态能量转换装置,具有转换率高、燃料来源广泛、不需要使用贵金属催化剂等优点[1-2]。研究和开发中温固体氧化物燃料电池(ITSOFC)是目前SOFC发展的主要趋势。降低工作温度不仅能克服系统密封以及组件热稳定性问题,而且还能降低连接材料的开发成本及开发难度,提高电池的使用寿命[3-5]。
离子-电子混合导电材料Sr2MnO4具有较高电催化活性和良好的热稳定性,是一种潜在的ITSOFC阴极材料[6-12]。Sr2MnO4的性能优化研究主要集中在A位的掺杂改性[13-17]。例如Munning等通过La离子掺杂引入间隙氧,增强La2-xSrxMnO4+δ(0.6≤x≤2)氧化物的导电率[13]。Broux等[14,18]利用中子衍射(NPD)研究了La1.2Sr0.8MnO4+δ材料的相变对氧空位的形成及氧交换能力的影响。Sun等[15]探索了Sr2-xLaxMnO4+δ(x=0.4,0.5,0.6)的高温电化学性质,发现氧在Sr2-xLaxMnO4+δ电极表面主要发生解离吸附和电荷转移反应;随着La掺杂量的增加,电极极化电阻逐渐降低,800℃的阻抗值Rp为0.87Ω·cm2。相比于A位掺杂体系,B位掺杂的Sr2MnO4主要涉及晶体结构以及磁性能方面的研究[19-20],其高温电化学性质还未见报道。已有的研究结果表明,B位掺杂可以显著增加(类)钙钛矿材料的氧缺陷浓度,改善氧离子输送能力。Kharton[21-22]发现B位掺Cu和Co可以降低La2Ni1-xMxO4(M=Cu,Co)系列氧化物电极的极化电阻。李强[23]报道Cu的掺杂能够增加La1.6Sr0.4Ni1-xCuxO4中氧缺陷浓度,进而提高电催化活性。Munning[24]对Co掺杂的La2Ni1-xCoxO4+δ材料进行了氧扩散性能测试。结果表明相比于La2NiO4,Co的掺杂能显著提高氧扩散系数和改善氧表面交换能力。
基于以上研究报道,本文在前期工作基础上[15],采用EDTA-柠檬酸法制备了Co掺杂的Sr1.5La0.5Mn1-xCoxO4材料,研究了材料的电化学性能,考察其作为中温固体氧化物燃料电池阴极材料的可行性。
1 实验部分
1.1 电极材料的合成
Sr1.5La0.5Mn1-xCoxO4(SLMCO x,x=0.0,0.1,0.3,0.5)采用EDTA-柠檬酸法制备。按照化学计量比将La(NO3)3、Sr(NO3)2、Mn(NO3)2和Co(NO3)2加入到30 mL去离子水中配置成溶液,逐次加入柠檬酸和EDTA,使得金属离子、柠檬酸和EDTA的物质的量比为1∶2∶1,以氨水调节溶液pH值至8,得到的溶胶在180℃干燥24 h,600℃煅烧10 h,所得粉末经过研磨压片再于1 200℃焙烧12 h,得到Sr1.5La0.5Mn1-xCoxO4材料。为检测该材料与电解质材料的高温化学相容性,将SLMCO x与CGO粉体按照质量比6∶4均匀混合,在1 200℃煅烧12 h。产物相纯度以及高温化学相容性通过粉末X射线衍射(XRD)进行检测。
1.2 电极的制备
两电极测试电池的制备:Sr1.5La0.5Mn1-xCoxO4粉体中加入适量含5%乙基纤维素的松油醇,研磨得到的阴极浆料均匀刷涂在CGO电解质圆片两侧,空气中1 000~1 200℃烧结4 h。三电极测试电池的制备:将阴极浆料均匀刷涂在CGO电解质基片的一侧,1 100℃煅烧4 h形成工作电极,另一侧对称地涂上铂浆作为对电极,铂丝粘接在工作电极一侧作为参比电极。
1.3 材料结构及电化学性能表征
采用Bruker D8-Advance型X射线粉末衍射仪对所合成材料进行物相与结构分析。测试条件:Cu靶Kα射线,波长0.154 nm;射线管电压为40 kV,电流为40 mA;测试角度范围为10°~80°,扫描步长0.02°,扫描速度10°·min-1。
Sr1.5La0.5Mn1-xCoxO4粉料在210 MPa下加压成型,于1 300℃烧结12 h,得到相对密度大于90%,尺寸为3mm×5 mm×50 mm的条形试样,用于热膨胀和电导率测试。
电极的电化学性能采用AUTOLAB PGStat30电化学工作站进行测试。激励电压振幅10 mV,扫描频率1MHz~10-2Hz,测试温度500~700℃。阴极过电位采用以下公式计算:ηWE=ΔUWE-iRel,式中ηWE为阴极过电位,ΔUWE为工作电极相对于参比电极的电压,i为流过电池的电流,Rel为电解质电阻。
2 结果与讨论
2.1 物相分析
图1为Sr1.5La0.5Mn1-xCoxO4在1 200℃煅烧12 h的XRD图。可见随着Co离子的掺杂量从0.1增加至0.5,XRD衍射峰与PDF标准数据库83-1897的数据基本一致,表明钴掺杂化合物仍保持原有Sr1.5La0.5MnO4的类钙钛矿结构,没有其它第二相生成。采用Rielveld精修的方法对不同钴掺杂量样品的XRD数据进行拟合并计算晶胞参数,结果列于表1。对比发现随Co掺入量的增加,晶格常数a和晶胞体积V均减少,而晶格常数c增大,相应的畸变率(c/a)也增大。这表明在SLMCO x的[BO6]八面体结构中,Co离子掺杂引起ab平面的Mn/Co-O2Ⅱ键长缩短,c轴方向的Mn/Co-O1Ⅰ键长增大,钙钛矿结构沿c轴方向伸长(O2Ⅱ代表ab平面上的氧,O1Ⅰ为c轴上的氧),即Co的掺杂引起[BO6]八面体发生畸变。相关研究发现,[BO6]的畸变与氧化物中氧的活性有关[25]。在A2BO4结构中B-O2Ⅱ-B平面(即ab平面)是载流子的主要迁移通道,B-O2Ⅱ键的性质将决定载流子传导特性。而B位离子的价态以及B-O1Ⅰ键强度对晶格氧和吸附氧的活性及材料的催化性质有很大影响。畸变率增大导致轴向氧的活动能力增强,有利于岩盐层中的氧迁移扩散。
为了考察SLMCO x和CGO电解质的高温化学相容性,将Sr1.5La0.5Mn0.7Co0.3O4与CGO粉体按质量比6∶4进行充分混合,在1 200℃空气中煅烧12 h,并用XRD检测物相。由图2可见混合烧结粉体的衍射峰均可归属于Sr1.5La0.5Mn0.7Co0.3O4与CGO的特征衍射峰,没有其它杂相峰出现,表明Sr1.5La0.5Mn0.7Co0.3O4与CGO在1 200℃不发生化学反应,表现出良好的高温化学相容性。
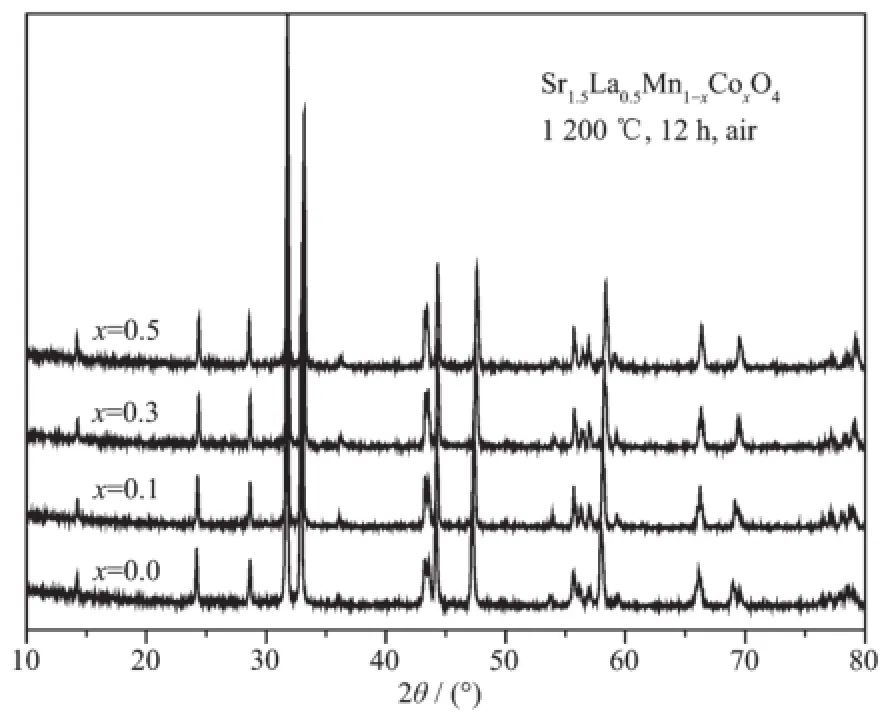
图1 Sr1.5La0.5Mn1-xCoxO4(x=0.1~0.5)1 200℃煅烧12 h后的XRD图Fig.1 XRD patterns of Sr1.5La0.5Mn1-xCoxO4(x=0.0~0.5) after calcined at1 200℃for 12 h
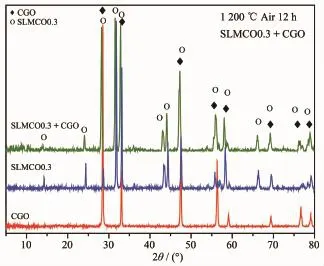
图2 Sr1.5La0.5Mn0.7Co0.3O4-CGO粉末在1 200℃空气中烧结12 h后的XRD图Fig.2 Sr1.5La0.5Mn0.7Co0.3O4-CGO after sintered at 1 200℃for 12 h in air
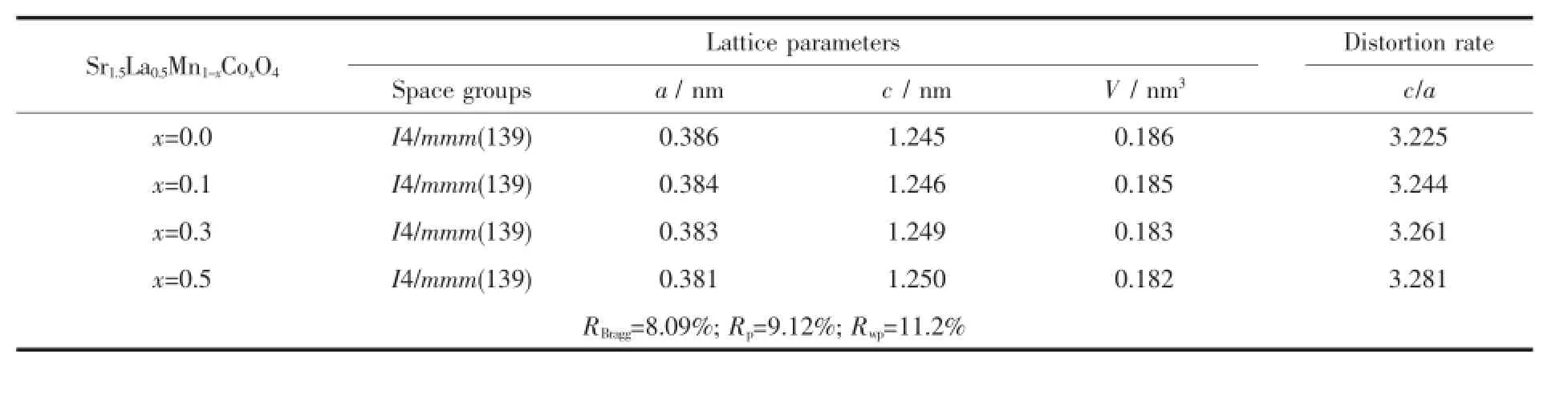
表1 Sr1.5La0.5M n1-xCoxO4的晶胞参数Table 1 Lattice parameters for the Sr1.5La0.5M n1-xCoxO4
2.2 Sr1.5La0.5Mn1-xCoxO4的XPS表征
X射线光电子谱(XPS)技术被广泛用于材料性质、化合物价态以及元素含量测定。键合能及峰面积可以为XPS测定元素种类和相对含量提供相关信息[26]。图3为Sr1.5La0.5Mn0.7Co0.3O4的Mn2p XPS光
谱图。采用Casa XPS软件对光谱进行分峰拟合(光谱精度在0.1 eV,Shirley型线为背底),Mn2p谱可拟合为2个峰,其中641.9~642.6 eV区域的谱峰符合Mn2O3中Mn3+的光谱峰[26-28],而结合能在643.2~644.2 eV区域的峰符合MnO2中Mn4+光谱峰[27-28]。表2为SLMCO x系列氧化物中Mn的2p光谱的分峰拟合结果,可见锰元素的平均价态变化处于Mn3+~Mn4+之间,且随着Co掺杂量增多,Mn3+含量增加而Mn4+减少。
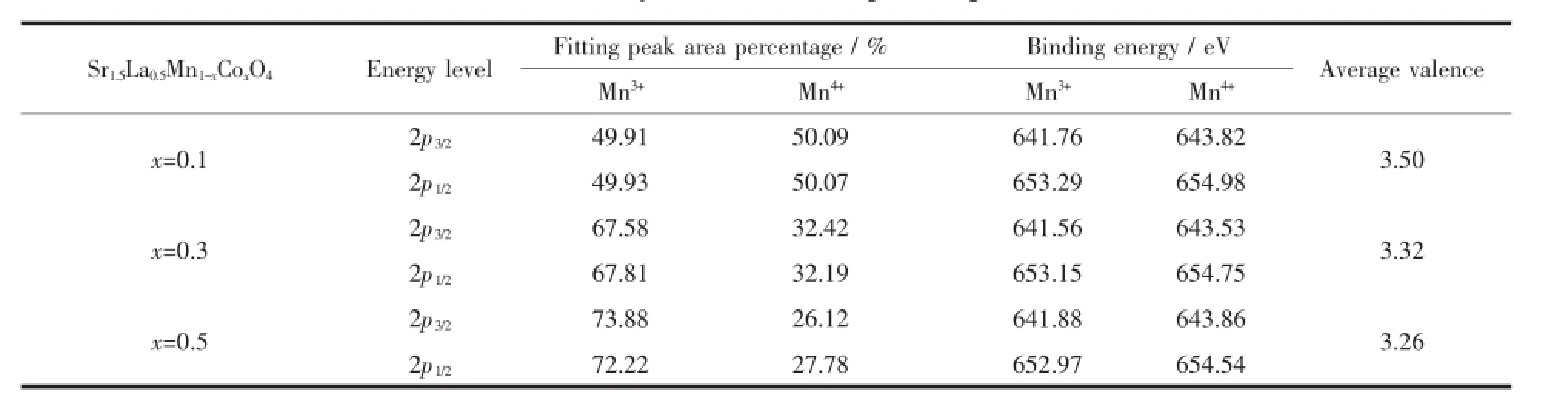
表2 Mn2p的XPS光谱数据分析Table 2 Analysis resu lts of M n2p XPS spectrum
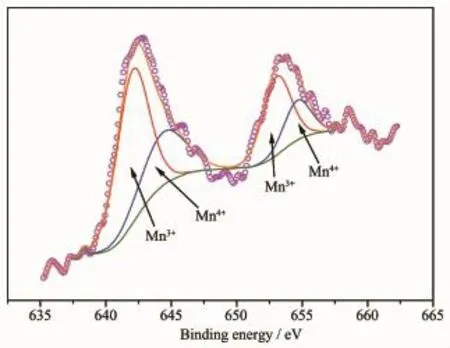
图3 Sr1.5La0.5Mn0.7Co0.3O4的Mn2p XPS谱图Fig.3 Mn2p spectrum of Sr1.5La0.5Mn0.7Co0.3O4
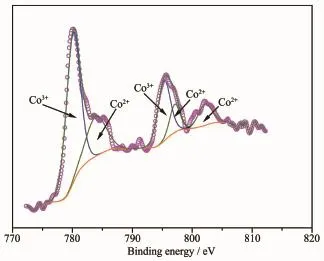
图4 Sr1.5La0.5Mn0.7Co0.3O4的Co2p XPS谱图Fig.4 Co2p spectrum of Sr1.5La0.5Mn0.7Co0.3O4
图4 为Co2p的XPS光谱。Co的2个自旋轨道的主峰分别位于780eV(2p3/2)和795.5eV(2p1/2),这与LixCoO2中Co3+2p光谱峰相符,证明材料中Co的价态主要以Co3+为主[29]。而在802.15 eV存在一个卫星峰。Galakhov等[30]对比分析了CoO与LiCoO2在不同氧分压下测定的XPS光谱,认为Co2p1/2主峰后的卫星峰归属为Co2+,其强度受氧空位浓度的影响。据此我们认为在SLMCO x氧化物中Co以+2和+3形式存在。通过拟合分峰处理,可以计算出Co3+与Co2+的相对百分含量(见表3)。可见随着钴掺杂量的增加,Co离子平均价态降低,表明Sr1.5La0.5Mn1-xCoxO4化合物中具有较低的氧含量及高的氧空位浓度,这对于氧离子的迁移起着重要的作用。图5为Sr1.5La0.5Mn0.6Co0.4O4的O1s XPS谱图。O1s光谱可以拟合为3个主峰[31~37]:(O1sⅠ)529.09~529.68 eV,(O1sⅡ)530.91~531.50 eV,(O1sⅢ)532.08~533.25 eV。其中O1sⅡ,O1sⅢ归属于材料表面吸附的氢氧化物[31]以及碳酸盐[35-36]中的氧,属于化学吸附氧;O1sⅠ则属
于钙钛矿结构中的晶格氧[33-34]。化学吸附氧的存在证明化合物中存在氧空位[37]。由表4可见,随着Co掺入量的增加,表面吸附氧与晶格氧拟合峰面积之比逐渐增大,表明氧空位的含量逐渐增大。
总结上述XPS光谱数据分析结果,可知随着Co掺杂量增多,氧化物中的Mn4+和Co3+逐渐减少,Mn3+和Co2+含量逐渐增多,晶格氧含量不断降低,吸附氧含量不断增加。以上结果表明,为保持体系的电中性,随着钴掺杂量的增加,SLMCO x氧化物主要通过产生氧空位补偿减少的正电荷。
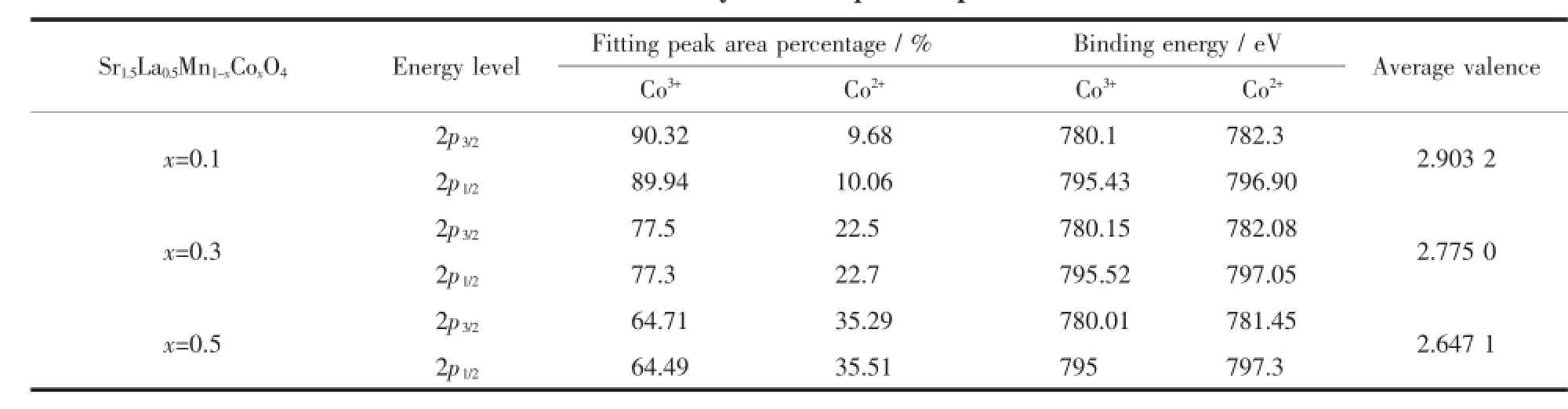
表3 Co2p光谱数据分析Table 3 Analysis of Co2p XPS spectrum
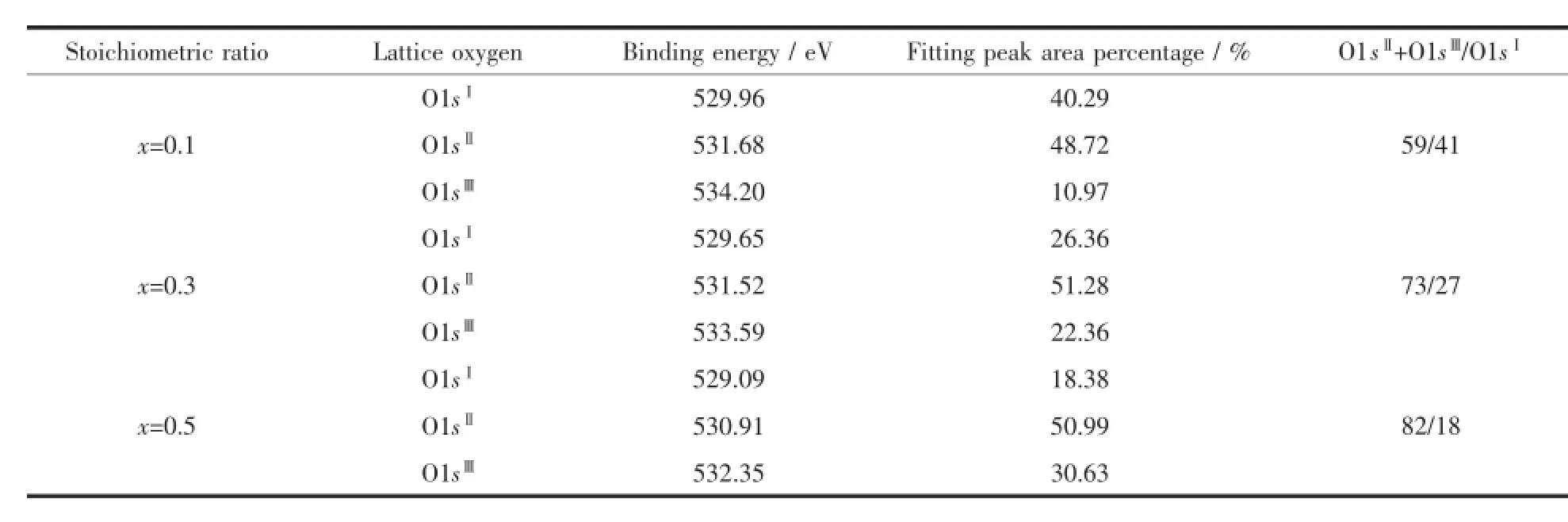
表4 O1s光谱数据分析Table 4 Analysis of O1s XPS spectrum
2.3 热膨胀系数
图6为SLMCO x的线性热膨胀曲线与温度的关系图。由图可见,当钴掺杂量较低时,材料的热膨胀系数变化不明显。考虑到钙钛矿复合氧化物中B位金属元素与氧(B-O)之间的化学键能随着过渡金属离子半径的增大而增大[38],而Mn3+离子的半径(0.064 nm,HS)大于Co3+离子半径(0.054 nm,LS),因而Mn-O的键能大于Co-O的键能,这使得MnO6八面体较难发生热膨胀,因此低Co含量样品的热膨胀系数改变较小。随着B位Co掺杂量的增多,根据XPS研究结果可知,为保持体系的电中性,SLMCO x中主要存在氧空位补偿机制。Tai等[39]认为材料的晶格膨胀跟氧空位的生成有关:氧离子从晶格中解离出来,使得相互暴露的阳离子之间的斥力增加。所以随着Co含量进一步增加,体系中产生大量氧空位,导致Sr1.5La0.5Mn1-xCoxO4的热膨胀系数显著增加。
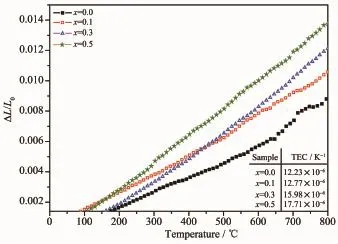
图6 Sr1.5La0.5Mn1-xCoxO4(x=0.0,0.1,0.3,0.5)热膨胀曲线Fig.6 Thermal expansion curves of Sr1.5La0.5Mn1-xCoxO4(x=0.0,0.1,0.3,0.5)
2.4 电导率
图7为Sr1.5La0.5Mn1-xCoxO4在空气中的电导率随温度变化曲线图。材料的电导率随温度升高而增大,样品的ln(σT)与1 000/T近似满足直线关系,表现出半导体导电特性,其导电行为符合小极化子导电机制,可归属于小极化子跃迁热激活材料[40]。根据Arrhenius关系式,可计算载流子输运的活化能(见图8中表格所示)。从图中可以发现,当B位掺杂Co后,SLMCO x氧化物的电导率随着钴掺杂量的增加有明显提高。x=0.3及0.5的样品在800℃空气下的电导率分别为13.03和15.92 S·cm-1。相关研究认为[41-42],钙钛矿晶体进行异价态阳离子(如Al、Co、Ni等)掺杂,会对晶体中电荷平衡产生影响;为维持电中性,结构中将产生电子-空穴或氧缺陷以维持电荷平衡。通过对XPS数据的分析可知,随着钴掺杂量的增大,SLMCO x氧化物的晶格氧逐渐失去,体系中形成大量氧空位;在空气气氛中,晶体中存在着如下反应:

Oo×表示晶格氧,h′表示电子空穴[43]。可见随着氧空位增多,体系中的电子空穴浓度增大,因此材料的电导率随着钴掺杂量增大而逐渐升高。

图8 Sr1.5La0.5Mn0.7Co0.3O4阴极在不同温度下烧结后的SEM图像:表面(a)1 000℃,(b)1 100℃,(c)1 200℃, (d)1 100℃烧结的电极横断面Fig.8 SEM images of the Sr1.5La0.5Mn0.7Co0.3O4electrode sintered at1 000℃(a);1 100℃(b);1 200℃(c);and the cross-section image at 1 100℃(d)
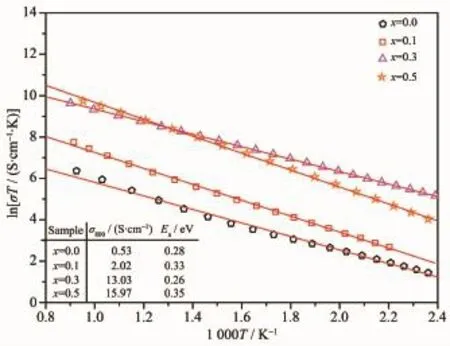
图7 Sr1.5La0.5Mn1-xCoxO4(x=0~0.5)电导率的Arrhenius曲线Fig.7 Arrhenius plots of the electrical conductivity for Sr1.5La0.5Mn1-xCoxO4(x=0~0.5)
2.5 电化学性能
电极材料的性能与电极的微观结构和孔隙度有关。图8为不同温度烧结的电极表面和横断面的SEM图像。随着烧结温度的升高,粒子尺寸增大。1 100℃烧结的电极材料颗粒之间出现一定的烧结连接,形成较好的多孔结构,有利于气体的传输,从而降低界面极化电阻。从SEM横断面图(图
d)可见,1 100℃烧结的阴极材料与电解质的界面结合良好,电极平均厚度约为2.5μm。
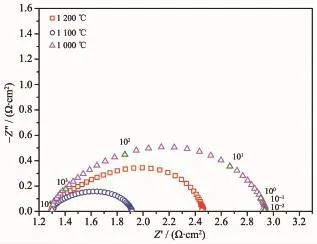
图9 不同温度下烧结的Sr1.5La0.5Mn0.7Co0.3O4电极在700℃空气中测得的阻抗谱Fig.9 Impedance spectra of Sr1.5La0.5Mn0.7Co0.3O4cathode sintered at different temperatures for 4 h and then measured at700℃in air
不同烧结温度形成的电极微观结构对电极性能有很大的影响。图9为不同温度下烧结4 h得到的Sr1.5La0.5Mn0.7Co0.3O4电极在700℃空气中的阻抗谱。可以看出,经过1 200℃烧结的电极,其极化电阻相对较大。这是由于烧结温度过高导致粒子过度生长和粘结,减少了氧气的扩散通道,使气相输运过程受阻,导致界面电阻的增加,这一点可以从图c得到验证。当烧结温度为1 100℃时,电极的极化电阻达到最小值。而烧结温度降低到1 000℃的电极极化电阻又进一步增大,这是由于较低的烧结温度不能使电极粒子之间及与电解质界面形成良好的接触,从而产生较高的接触电阻(图8a)。类似的现象在其它A2BO4型阴极材料体系也有所发现[44-45]。根据以上结果,可以确定Sr1.5La0.5Mn0.7Co0.3O4电极在CGO固体电解质上最佳的烧结温度为1 100℃。
从图10可以看到,随着Co掺杂量的增加,电极的极化电阻逐渐降低。当Co的掺杂量为0.3时,Sr1.5La0.5Mn0.7Co0.3O4电极的极化电阻达到最小值,700℃的极化电阻为0.63Ω·cm2,明显小于Sr1.5La0.5MnO阴极在750℃的极化电阻(1.5Ω·cm2)[46]。这是由于Co的掺杂增大了电极材料的氧空位浓度,从而改善了电极的电催化活性。类似的结果在Ba0.5Sr0.5Fe1-xCuxO3、La1-xSrxCo1-yFeyO3等阴极材料中也有报道[47-48]。随着钴的掺杂量达到0.5,电极的极化电阻又开始增大,700℃的极化电阻为0.86Ω·cm2。这可能是由于Sr1.5La0.5Mn0.5Co0.5O4的热膨胀系数较大,与CGO电解质的热匹配性质较差导致的。
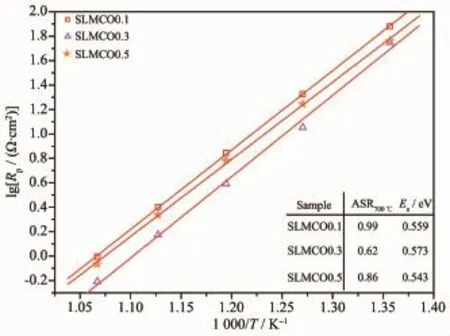
图10 Sr1.5La0.5Mn1-xCoxO4(x=0.1~0.5)电极的极化电阻随温度变化的Arrhenius曲线Fig.10 Arrhenius plots of the polarization resistances of Sr1.5La0.5Mn1-xCoxO4(x=0.1~0.5)electrodes under air
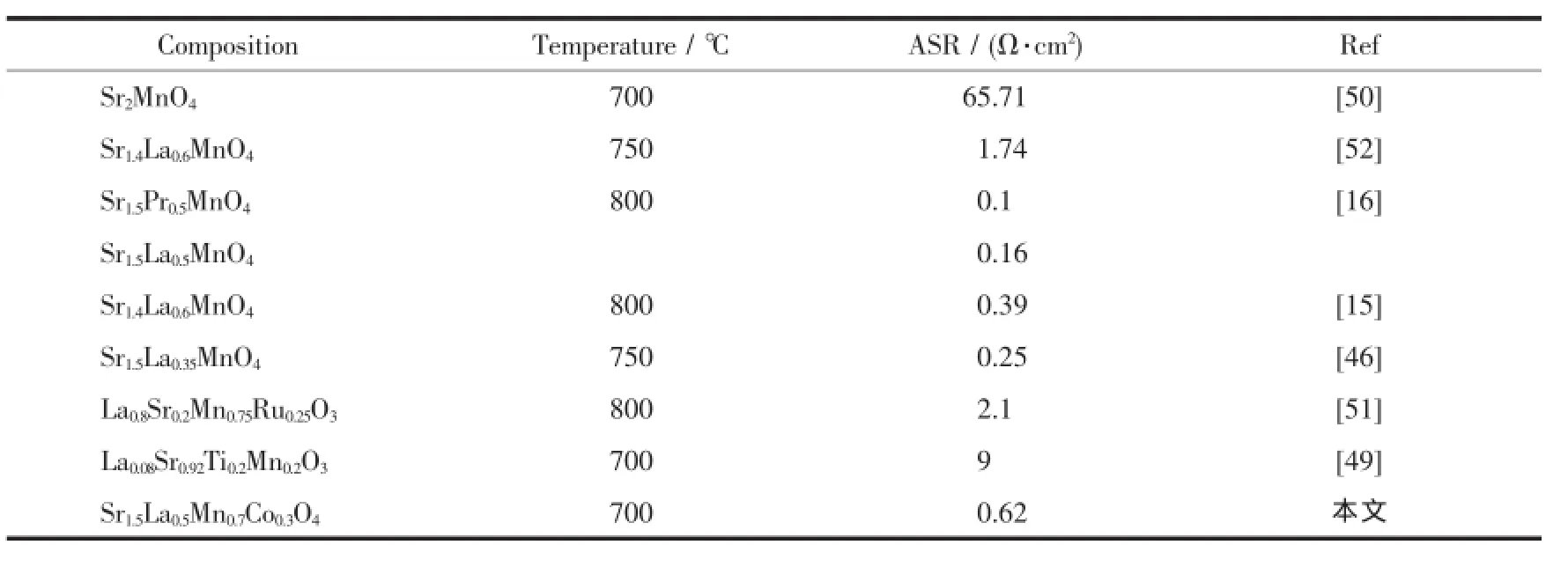
表5 部分M n系氧化物的极化电阻数据Table 5 Polarization resistance of some collected M n-based oxides
表5列出了几种锰系氧化物的极化电阻数据。对比可见,Co元素掺杂明显降低Sr2MnO4的极化电
阻值。Sr1.5La0.5Mn0.7Co0.3O4在中低温区具有较好的氧还原催化性能,是一种潜在的IT-SOFC阴极材料。但是相比于传统的钴系和镍系阴极材料,锰系材料的极化电阻仍然较高。后续工作将通过进一步的掺杂和复合来改善其电极性能。
3 结论
采用EDTA-柠檬酸法合成了K2NiF4结构纯相Sr1.5La0.5Mn1-xCoxO4(x=0.0,0.1,0.3,0.5)阴极材料。SLMCO x材料与电解质CGO之间具有良好的高温化学相容性。随着体系中Co含量的增加,材料的电导率升高,氧空位浓度增大,电极极化电阻逐渐减小。其中Sr1.5La0.5Mn0.7Co0.3O4的极化电阻值最小,700℃为0.62Ω·cm2。
[1]Kreuer K D.Annu.Rev.Mater.Res.,2003,33(1):333-359
[2]Orera A,Slater P R.Solid State Ionics,2010,181(3):110-114
[3]Brandon N P,Skinner S,Steele B C H,et al.Annu.Rev. Mater.Res.,2003,33(1):183-213
[4]Cao Y,Gu H,Chen H,et al.Int.J.Hydrogen Energy,2010, 35(11):5594-5600
[5]Atkinson A,Barnett S,Gorte R J,et al.Nat.Mater.,2004,3 (1):17-27
[6]Lynch M E,Yang L,QinW,etal.Energy Environ.Sci.,2011, 4(6):2249-2258
[7]Armstrong E N,Duncan K L,Oh D J,et al.J.Electrochem. Soc.,2011,158(5):492-499
[8]Yaremchenko A A,Kovalevsky A V,Kharton V V,et al. Solid State Ionics,2008,179(38):2181-2191
[9]Sun L P,Li Q,Huo L H,et al.J.Power Sources,2011,196 (14):5835-5839
[10]LiR K,Greaves C.J.Solid State Chem.,2000,153(1):34-40
[11]Li W,Guan B,Yan J,et al.J.Power Sources,2016,318: 178-183
[12]Zhao H,LiQ,Sun LP,et al.Sci.China Chem.,2011,54(6): 898-910
[13]Munnings C N,Skinner S J,Amow G,et al.Solid State Ionics,2006,177(19):1849-1853
[14]Broux T,Prestipino C,Bahout M,et al.Chem.Mater.,2013, 25(20):4053-4063
[15]Sun L P,Huo L H,Zhao H,et al.J.Power Sources,2008, 179(1):96-100
[16]ZHANG Li-Juan(张丽娟).Thesis for the Master of Harbin Institute of Technology(哈尔滨工业大学理学硕士学位论文).2010.
[17]Zhou J,Chen G,Wu K,et al.J.Power Sources,2014,270: 418-425
[18]Broux T,BahoutM,HernandezO,et al.Inorg.Chem.,2013, 52(2):1009-1017
[19]Shinawi H E I,Greaves C.Z.Anorg.Allg.Chem.,2009,635 (12):1856-1862
[20]Bahout M,Tonus F,Prestipino C,et al.J.Mater.Chem., 2012,22(21):10560-10570
[21]Kharton V V,Tsipis E V,Yaremchenko A A,et al.Solid State Ionics,2004,166(3):327-337
[22]Kharton V V,Yaremchenko AA.8th IntemationalSymposium on Solid Oxide Fuel(SOFC-Ⅷ).Singhal S C,Dokiya M, Ed.,New York:Pennington,2003:561-567
[23]LIQiang(李强),ZHAO Hui(赵辉),JIANG Rui(江瑞),et al.Acta Phys.-Chim.Sin.(物理化学学报),2012,28(9):2065-2070
[24]Munnings C N,Skinner S J,Amow G,et al.Solid State Ionics,2005,176(23):1895-1901
[25]JIA Li-Ping(贾丽萍).Thesis for the Master of Nanjing University of Aeronautics&Astronautics(南京航空航天大学硕士研究生学位论文).2008.
[26]Yao Y,Cai Y,Wu G,et al.J.Hazard.Mater.,2015,296: 128-137
[27]Falub M C,Tsurkan V,Neumann M,et al.Surf.Sci.,2003, 532:488-492
[28]Chen J,Wen W,Kong L,etal.Ind.Eng.Chem.Res.,2014, 53:6297-6306
[29]Galakhov V R,Ovechkina N A,Shkvarin A S,et al.Phys. Rev.B,2006,74(4):045120
[30]Galakhov V R,Karelina V V,Kellerman D G,et al.Phys. Solid State,2002,44(2):266-273
[31]Mao C,Li H,Cui F,et al.J.Cryst.Growth,1999,206(4): 308-321
[32]Van Der Heide P A W.Surf.Interface Anal.,2002,33(5): 414-425
[33]Tavares A C,Silva Pereira M I,Mendona M H,et al.J. Electroanal.Chem,1998,449(1):91-100
[34]Haenen J,VisscherW,Barendrecht E,et al.J.Electroanal. Chem.Interfacial Electrochem.,1986,208(2):297-321
[35]Vovk G,Chen X,Mims C A,et al.J.Phys.Chem.B,2005, 109(6):2445-2454
[36]Liu B,Zhang Y,Tang L,et al.Int.J.Hydrogen Energy, 2009,34(1):435-439
[37]Wang C C,O′Donnell K,Jian L,et al.J.Electrochem.Soc., 2015,162(6):507-512
[38]LICheng(李晨).Thesis for the Master of Tanjin University
of Technology(天津理工大学理学硕士学位论文).2012.
[39]Tai LW,Nasrallah M M,Anderson H U,et al.Solid State Ionics,1995,76(3):273-283
[40]Tai LW,Nasrallah M M,Anderson H U,et al.Solid State Ionics,1995,76(3):259-271
[41]Salamon M B,Jaime M.Rev.Mod.Phys.,2001,73(3):583
[42]Zhou X D,Yang J B,Thomsen E C,et al.J.Electrochem. Soc.,2006,153(12):J133-J138
[43]Kröger FA.The Chemistry of ImperfectCrystals.Amsterdam/ London:North-Holland Publishing Company,1974.
[44]Li Q,Zhao H,Huo L,et al.Electrochem.Commun.,2007,9 (7):1508-1512
[45]Li Q,Fan Y,Zhao H,et al.J.Power Sources,2007,167(1): 64-68
[46]SUN Li-Ping(孙丽萍).Thesis for theDoctorate ofHeilongjiang University(黑龙江大学博士论文).2008.
[47]Leng Y,Chan S H,Liu Q,et al.Int.J.Hydrogen Energy, 2008,33(14):3808-3817
[48]Efimov K,Halfer T,Kuhn A,et al.Chem.Mater.,2010,22 (4):1540-1544
[49]Yoon JS,Lim Y S,Choi B H,et al.Int.J.Hydrogen Energy, 2014,39:7955-7962
[50]Wang M H,Woo K D,et al.Energy Convers.Manage,2008, 49:2409-2412
[51]Lin JC,Ting F P,Lee T Y,et al.Int.J.Hydrogen Energy, 2013,38:1714-1724
[52]Jin C,Yang Z B,Zheng H H,et al.Electrochem.Commun., 2012,14:75-77
Synthesis and High Tem perature Electrochem ical Properties of Co-doped Sr1.5La0.5MnO4
FAN Yu-Hang1SUN Li-Ping1ZHAO Hui*,1HUO Li-Hua1Jean-Marc Bassat2
Aline Rougier2Sébastien Fourcade2Jean-Claude Grenier2
(1Key Laboratory of Functional Inorganic Material Chemistry,Ministry of Education,
School of Chemistry and Materials Science,Heilongjiang University,Harbin 150080,China)
(2CNRS,Universitéde Bordeaux,ICMCB,87 avenue du Dr.A.Schweitzer,F-33608 Pessac-Cedex,France)
Sr1.5La0.5Mn1-xCoxO4(SLMCO x)cathodematerials for IT-SOFCs(intermediate temperature solid oxide fuel ells)were synthesized by EDTA-citric acid method and characterized by XRD,XPS and EIS,respectively.The esults show that SLMCO x has no reaction with Ce0.9Gd0.1O1.95at 1 200℃for 12 h.Both the amount of Mn3+and Co2+in the oxide increase with the Co doping concentration;at the same time the contentof lattice oxygen reduces, nd the distortion ratio(c/a)of the lattice increases.The EIS results show that Co-doping dramatically reduces he polarization resistance(Rp)of SLMCO x cathode.The Sr1.5La0.5Mn0.7Co0.3O4has the lowest Rpof 0.62Ω·cm2at 00℃in air,which is clearly smaller than the Rpvalue of Sr1.5La0.5Mn0.7O4that measured at750℃(1.5Ω·cm2). Our results indicate that the Co doped Sr1.5La0.5Mn1-xCoxO4is potential cathodematerial for IT-SOFC.
intermediate temperature solid oxide;fuel cells(IT-SOFCs);cathodematerial
O614.81+2
A
1001-4861(2016)10-1730-09
10.11862/CJIC.2016.207
2016-01-17。收修改稿日期:2016-06-11。
国家自然科学基金(No.51302069,51372073)、高等学校博士学科点专项科研基金(No.20132301110002)和人事部留学人员科技活动择优项目(No.2014-240)资助。
*通信联系人。E-mail:zhaohui98@yahoo.com;会员登记号:S060016480P。
