无源温控包装解决方案为医疗器械冷链安全护航
2016-12-02毛盾
毛盾
对温度敏感的生化、免疫、分子诊断、基因测序等体外诊断试剂具有复杂的分子结构,在常温储存下很难保持稳定的状态,大多需要在2~8℃的温度下储存,因此其储存运输全过程需要进行冷链管理。体外诊断试剂属于医疗器械的一部分,然而当前我国医疗器械冷链管理现状并不乐观,在医疗器械的生产环节,受制于冷链包装与冷链物流成本的压力,很多企业被动选择不按冷链管理要求操作;在医疗器械的经营流通环节,受制于监管空白,代理商或经销商将体外诊断试剂的物流投递层层转包,使得冷链管理无法保障,特别是冷藏包装的温控时效、温湿度记录、日常监控记录等不完善,导致很大部分产品的存储条件不符合医疗器械说明书或者标签标示要求。
然而,医疗器械冷链管理的真正难点在于打通医疗器械流通的各个关键节点,使之共同致力于冷链各环节的温控管理。冷链管理不但对医疗器械生产端有高标准要求,对其包装、运输、储存、使用等重要环节也有非常严格的管理规范和流程标准,并受相关质量审计和法规监管。
今年3月发生的“山东疫苗事件”中的问题疫苗就在于未经严格的冷链存储运输就直接流入市场,导致疫苗失效,引起全国热议。针对该阶段医药冷链管理事故、山东疫苗事件的持续影响以及社会舆论的持续发酵,今年5月12日,国家食品药品监督管理总局(CFDA)发布了《医疗器械冷链(运输、贮存)管理指南》的征求意见稿,并在全国范围内开展了多频次的专项检查和企业自查自检。9月22日,CFDA正式发布《医疗器械冷链(运输、贮存)管理指南》的公告(2016年第154号)(以下简称“冷链新规”),对医疗器械冷链管理所涉及的人员与设施设备、验证管理、出库与运输、应急管理等环节做出具体要求。
制药企业如何应对冷链新规?
冷链新规的发布为制药企业施加了巨大的执行压力,也给监管部门带来了职能压力,但冷链新规的合规执行也淘汰了部分竞争力不强的企业,这其实也是给制药企业及代理商带来了新的发展及运营机遇。因此,制药企业需在温控技术合规达标的基础上,做好冷链物流的规划,实现相关物流的全程冷链管理。
1.企业必须做好温控设备、包装容器的设计与性能验证
冷链新规第九条再次强调了“未经验证的设施设备,不得应用于冷链管理医疗器械的运输和贮存过程。”温控方案的设计与验证需要企业组建专业工程团队或与第三方专业温控解决方案供应商合作。
2.企业需要根据自身的发货量以及配送模式选择合适的温控包装类型
目前,医疗器械的主流温控包装类型主要有无源温控包装与有源温控包装两种,有源温控冷链配送适合定点大规模配送,无源温控冷链适合分布式直达投递。按照医疗器械体外诊断行业的流通现状,如果试剂的分销量每周达到1000个包装大单元,可考虑采用有源温控冷链定点配送,但有源温控冷链配送是高值固定资产投入,企业需要拥有或租用冷库、冷藏车、冷藏箱等,需要不菲的资产支出。如果试剂的分销量每周低于500个包装大单元,则可选择无源温控冷链投递方式。
3.企业需要建立全程冷链的物流配送渠道
全程冷链对物流配送的要求较高,从单家企业来讲,要想实现多方位、门到门的配送服务,通过企业自建配送渠道是不现实,也是不经济的,企业必须借助提供完整服务的第三方物流共同配送。近两年,医疗器械冷链物流的共同配送取得较大进展,如国药、怡亚通等制药企业已经建立社会药品冷链物流业信息共享平台。
无源温控包装的优势
现阶段,医疗器械试剂生产企业普遍面临两大问题:一是试剂分发量小,无法使用有源温控冷链定点配送;二是试剂冷链配送最后一公里存在冷链盲区。也就是说,目前试剂类药品的市场占有率严重不均衡,国外巨头与国内领头企业占据了医疗器械体外诊断试剂60%以上的市场份额,剩下几千家中小企业的日均发货量不足50箱,而且终端用户分布不集中,企业无法使用有源温控包装进行定点配送。另外,在整个冷链物流过程中,第三方物流在一线城市已经能够满足全程冷藏运输的要求,但是在二、三线城市的冷藏运输中,还无法满足最后一公里运输要求。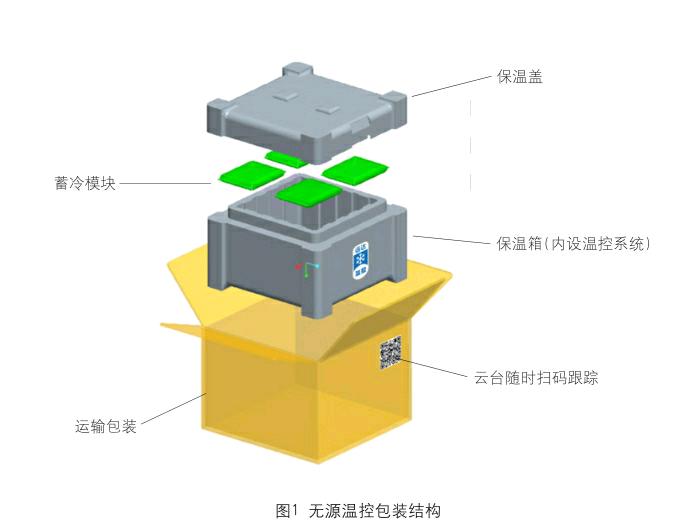
针对以上问题,无源温控包装发挥了其应用优势。无源温控包装箱内的温度场分布经过验证合格,配合一套有效的温度监测、储存、查询、报警通知系统,可解决中小试剂公司的冷链性能达标合规。我公司所使用的ONEPAC无源温控技术,具有更高效的温度绝缘特性,其聚冷强度能最大化保持长效的温控效率和抵御严酷的运输、储存环境,并能循环使用,足以应对48~72小时的冷链运输业务,无源温控包装结构如图1所示。
无源温控包装设计
1.保温材料的选择和温控时效设计
无源温控包装一般都会同客户一起来预算和评估满足温控要求的运输时效,从而帮助客户选择经济型的保温材料和长效型材料,甚至超长效型材料。目前可供无源温控包装应用的常用工程材料有聚苯乙烯、聚丙烯、聚氨酯等,也有一些超隔温材料也在逐步进入工程应用,比如真空板与气凝胶。
根据无源温控包装的尺寸和温控时效设计蓄冷配置,定制100%匹配的蓄冷相变材料。无源温控包装需要多种温区与聚冷形态的蓄冷相变材料,以实现不同的温区要求。医疗器械体外诊断试剂常用的蓄冷温区为-30~22℃,根据产品特性,其包装载体形式大致有冰袋(如图2所示)、冰盒(如图3所示)和冰板等形式,可供设计选型。
无源温控包装时效设计应通过温控包装系统热阻及蓄冷剂热交换的定量计算,建立无源温控包装温控时效的设计与配置。为设计简化,一般在设计时以温控包装内蓄冷剂的相变潜热作为冷量耗散总源,并近似地认为能力交换在温控箱中的传递过程为稳态传热过程,温控系统在一定时间内进行的热力学交换量可由傅里叶导热定律导出:
Q=KAΔT/d (公式1)
其中,Q为热量;K为导热率;A为接触面积;d为热量传递距离;ΔT为温度差。
假定温控箱内外接触面是完全光滑和平整的,所有热量全部通过热传导的方式经过材料,并到达另一端与外界环境维持能力交换。根据测试并计算出一个材料的热阻值R,计算公式如下:
R=AΔT/Q (公式2)
将公式1和公式2合并,可以得到K=d/R。因为K值相对于同一选定好的保温材料是不变的,由此可以得出热阻R值与材料厚度d成正比关系。也就说,材料越厚,热阻越大。 但很多导热材料的热阻值R,与材料厚度d并不完全成正比关系,而是会出现非线性变化。这是因为导热材料大都不是由单一成分组成,因此相关的热阻值还需由专业的仪器设备进行测定。
傅里叶导热方程式是一个完全理想化的公式,有助于我们理解导热材料的原理。但在实际应用中热阻计算是复杂的数学模型,会有很多的修正公式来完善所有环节中可能出现的问题。
选择什么样的导热材料用于无源温控包装设计,理论上来讲是一件很困难的事情,很难通过一些简单的数据来准确计算,更多的是依靠测试和数据分析,同时还要做好温控性能的验证。如果测试能达到产品要求的理想效果,就是最为合适的无源温控包装方案。建议贵重的温度敏感型药品试剂不要冒险使用温控性能不达标或者未经验证的温控包装方案。
2.案例分享
下面,以某公司委托我公司为其IVD试剂设计的无源温控包装解决方案来具体说明,其温控需求规格参数如下:蓄冷介质:UDA PCM材料;保温隔热材质:UDA-EPS;温控温区:箱内2~8℃;适用外部环境温度:30±2℃;温控时效:>48小时。
基于公式1和公式2,同时根据温控测试数据分析,为保持温控箱内2~8℃温控时效不低于48小时,将蓄冷源等量换算为标准UDA PCM冰盒6块。考虑内部冰盒的堆码方式,优选方案为4-2矩阵,同时为了热力学分布的需要,设计温控系统内部尺寸为480mm×350mm×260mm,其中内高260mm为可扩展高度,针对未来更长效的保温需求,为加高留有可置换储冰空间。
同时考虑运输过程中的缓冲与冲击,在保温系统外部设计防护结构,使用BC型瓦楞纸箱作为外部防护;考虑使用易用性,在两侧设置有提手孔,方便提用,设计效果如图4所示。
此外,按照温控设计技术要求预备包装材料,模拟运输环境下的温控方案验证,对照《医疗器械冷链(运输、贮存)管理指南》相关要求,参考ASTM D3103《运输包装件保温性能标准测试方法》和《药品冷链保温箱通用规范》相关标准进行标准温控性能验证,验证结果为标准温区内温控时效60小时,达到温控时效,预备12小时的超时效是为了应对物流配送中的签收延误。
