透明质酸在肿瘤发病机制及治疗中的研究进展(综述)
2016-11-25刘昊
刘 昊
透明质酸在肿瘤发病机制及治疗中的研究进展(综述)
刘 昊
透明质酸是细胞外基质的重要成分之一,在肿瘤的发生发展中起到关键作用。本文介绍了透明质酸的结构、合成、降解,与受体之间的相互作用,在肿瘤的发病机制中起到的作用。并且就近年来透明质酸在肿瘤的治疗中的研究进展进行综述。
透明质酸 肿瘤发生 靶向治疗
透明质酸(HA)是细胞外基质的一个重要成分,通过其合成、降解、与受体的相互作用及一系列信号通路的激活等,在肿瘤细胞增殖、侵袭、转移、血管生成等生物学行为中起到重要的作用。透明质酸作为肿瘤靶向治疗的靶点,以及作为抗肿瘤药物的载体,在肿瘤的治疗中的应用近年来也在探讨当中。
1 透明质酸的结构、代谢及其与肿瘤的关系
1.1 透明质酸的结构 透明质酸是一个带负电荷的大分子量的多聚糖,由重复的β-1,3-乙酰氨基葡萄糖-β-1,4-葡糖醛酸的双糖结构组成(Fig.1)[1],并广泛存在于结缔组织、上皮及神经组织,是细胞间的细胞外基质的重要组成成分。透明质酸的分子结构具有良好的水溶性,可以调节细胞外基质的水及渗透压[1]。在内环境中,高分子量的透明质酸(HMW)占绝大多数(0.5×106~2×106)[2]。而低分子量透明质酸(LMW)(分子量在104~0.5×106)主要在炎症反应时表达[2]。在恶性肿瘤中,LMW可刺激肿瘤血管生成,促进肿瘤微环境中的微血管结构形成[2]。另一方面,HMW在肿瘤进展中可起到保护作用,如延缓结肠肿瘤的生长[3]等。
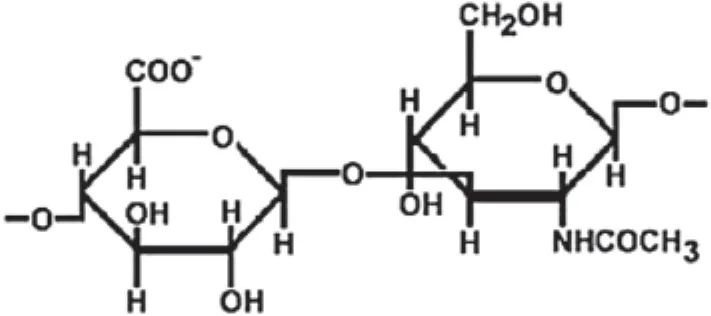
图1 透明质酸的分子结构 (Volpi N, 2010)
1.2 透明质酸合成酶及降解酶 透明质酸主要由透明质酸合成酶 (HAS)合成。透明质酸合成酶有三个异构体,HAS-1,HAS-2和HAS-3。其中,HAS-2是透明质酸合成中最重要的异构体[4]。HAS-2合成高分子量透明质酸,可调节大鼠的抗肿瘤活性[4]。也有研究表明,HAS异构体可在多种肿瘤类型中表达升高[5]。
正常情况下,透明质酸由胞吞作用清除或透明质酸降解酶(hyaluronidase, HYAL)降解。HYAL有5个同源的序列编码蛋白,分别为HYAL 1-4及PH20。其中HYAL 1-3有可测量的降解透明质酸的活性,HYAL 4主要作用于硫酸软骨素,而PH20尚未有关于透明质酸的作用的报道[6]。HYAL以及透明质酸同时过表达,与乳腺癌的侵袭和进展相关[7]。HYAL1的表达水平的升高还可发生在前列腺癌[8],卵巢癌[9],以及肺癌细胞中[10]。HYAL2被发现在恶性黑色素瘤中的表达水平升高[11]。关于HYAL 3-4在肿瘤方面的研究目前较少。
2 透明质酸的受体及其与肿瘤的关系
2.1 透明质酸的受体 透明质酸在体内的受体为透明质酸粘附分子,主要包括CD44和RHAMM等。CD44是透明质酸的主要受体,属于软骨连接蛋白家族。CD44与HA的结合是细胞特异性的,并取决于CD44的激活状态[12]。CD44在体内参与细胞粘附、细胞迁移、增殖等过程。RHAMM属于胞浆蛋白中的一个多功能家族,一般在胞内表达。胞内的RHAMM与中心体及纺锤体有关,而胞外的RHAMM可结合透明质酸[12]。RHAMM在许多肿瘤类型中表达,其过表达在恶性肿瘤中往往提示着预后不良[13]。
2.2 透明质酸与受体在肿瘤中的作用 恶性肿瘤的运动、侵袭与转移与细胞骨架、肿瘤血管生成等因素有关,这些因素都离不开细胞外基质的调节作用。透明质酸作为细胞外基质的重要成分,可通过与受体的作用影响上述过程。研究表明,透明质酸与CD44作用可影响肿瘤的生长、转移及肿瘤血管生成等[2]。透明质酸和CD44的相互作用可以通过影响G蛋白超家族的RhoGTPase(重要的可以调控细胞骨架及运动的蛋白),来调节细胞骨架的结构及细胞的运动性,从而促进肿瘤的侵袭与转移[14]。透明质酸和CD44,酪氨酸蛋白激酶受体(ErbB2),磷脂酰肌醇激酶(PI3K),埃兹蛋白组成复合体,激活ErbB2和PI3K信号通路[2],来影响肿瘤细胞的生长、凋亡及运动及肿瘤血管生成。此外,透明质酸与CD44可诱导肿瘤相关的微小RNA在恶性肿瘤中的表达,并提高肿瘤的耐药性[15]。透明质酸和RHAMM受体主要激活细胞外信号调节激酶1,2(Erk1, 2)通路,该信号通路与肿瘤细胞增殖有关[12]。透明质酸和CD44、RHAMM可以同时或分别作用来影响肿瘤细胞的生物学行为。
3 透明质酸在肿瘤治疗中的应用
3.1 透明质酸的靶向治疗 透明质酸因对肿瘤生物学行为的影响,本身可被用作靶向治疗的靶点。研究证实使用透明质酸降解酶(HYAL)治疗的癌症患者可以取得更好的临床疗效。在膀胱癌的前期临床研究中,透明质酸被HYAL降解后的产物sHA-F可以显著抑制膀胱癌细胞的增殖、侵袭及运动,促进癌细胞凋亡,以及降低透明质酸的受体水平[16]。sHA-F只作用于表达HYAL的膀胱癌细胞,对不表达HYAL的膀胱癌及正常尿路上皮细胞不起作用[16],提示其作为潜在肿瘤治疗靶点的可能性。另一项研究中,胰腺癌小鼠使用吉西他滨联合HYAL治疗,可以提高其中位生存期[17]。另外,透明质酸与受体CD44、RHAMM相互作用的信号通路也是可能的治疗靶点之一。已有研究表明,抑制透明质酸-CD44的信号通路可以增强抗肿瘤活性,使肿瘤细胞对化疗药,如阿霉素、长春花碱等更加敏感[18]。在白血病患者中使用表达RHAMM的多肽,可以激活细胞毒性免疫反应和抗肿瘤活性[19]。
3.2 透明质酸作为抗肿瘤药物的载体 因为透明质酸本身的结构,及其在细胞外基质广泛存在的特性,以及与受体的相互作用,使得透明质酸可以作为其他抗肿瘤药物的载体,有助于药物的运输,并降低毒副反应。在CD44过表达的胰腺癌中,透明质酸作为载体,与药物组合成的聚合物,作用于胰腺癌细胞,可以提高药物的细胞毒效应[20]。此外,透明质酸还可以与阿霉素[21]、顺铂[22]等多种化疗药物结合,提高药物的吸收、运输及抗肿瘤活性。另外,透明质酸可以与蛋白类药物,如细胞色素C结合,作用于乳腺癌细胞,能更好的抑制癌细胞的生长[23]。
4 展 望
透明质酸是一种大分子量的多聚糖,是细胞间的细胞外基质的重要组成成分。透明质酸通过其代谢过程,以及与受体相互作用,可以对肿瘤的运动、侵袭、转移、血管生成等过程起到重要影响。其中,透明质酸对肿瘤发病的影响的更深层次的机制还在被研究当中。透明质酸及其相关代谢酶、受体等可以作为恶性肿瘤靶向治疗的靶点。并且,透明质酸还可以作为抗肿瘤药物的载体,在恶性肿瘤的治疗中发挥重要作用。关于透明质酸在肿瘤靶向治疗中的应用,未来还需要进一步的临床试验来证实。
[1] Volpi, N.High-performance liquid chromatography and on-line mass spectrometry detection for the analysis of chondroitin sulfates/ hyaluronan disaccharides derivatized with 2-aminoacridone. Anal Biochem, 2010,397(1): 12~23.
[2] Spinelli, F.M.The immunological effect of hyaluronan in tumor angiogenesis. Clin Transl Immunology, 2015,4(12):52.
[3] Mueller, B.M., et al., Hyaluronan inhibits postchemotherapy tumor regrowth in a colon carcinoma xenograft model. Mol Cancer Ther, 2010,9(11):3024~3032.
[4] Faulkes,C.G.Molecular evolution of the hyaluronan synthase 2 gene in mammals: implications for adaptations to the subterranean niche and cancer resistance. Biol Lett, 2015,11(5):20150185.
[5] Nykopp, T.K.Hyaluronan synthases (HAS1-3) and hyaluronidases (HYAL1-2) in the accumulation of hyaluronan in endometrioid endometrial carcinoma. BMC Cancer, 2010,10:512.
[6] McAtee, C.O,J.J. Barycki, and M.A. Simpson, Emerging roles for hyaluronidase in cancer metastasis and therapy. Adv Cancer Res, 2014,123:1~34.
[7] Tan, J.X.Upregulation of HYAL1 expression in breast cancer promoted tumor cell proliferation, migration, invasion and angiogenesis. PLoS One, 2011, 6(7): 22836.
[8] Eissa, S.Detection of hyaluronidase RNA and activity in urine of schistosomal and non-schistosomal bladder cancer. Med Oncol, 2012,29(5): 3345~3351.
[9] Yoffou, P.H.Subtype specific elevated expression of hyaluronidase-1 (HYAL-1) in epithelial ovarian cancer. PLoS One, 2011,6(6): 20705.
[10] de Sa, V.K.Role of the extracellular matrix in variations of invasive pathways in lung cancers. Braz J Med Biol Res, 2013,46(1):21~31.
[11] Siiskonen, H.Inverse expression of hyaluronidase 2 and hyaluronan synthases 1-3 is associated with reduced hyaluronan content in malignant cutaneous melanoma. BMC Cancer, 2013,13:181.
[12] Misra, S.Interactions between Hyaluronan and Its Receptors (CD44, RHAMM) Regulate the Activities of Inflammation and Cancer. Front Immunol, 2015,6:201.
[13] Augustin, F.Receptor for hyaluronic acidmediated motility (RHAMM, CD168) expression isprognostically important in both nodal negative and nodal positive large cell lung cancer. J Clin Pathol, 2015,68(5):368~373.
[14] Bourguignon, L.Y.Hyaluronan-mediated CD44 activation of RhoGTPase signaling and cytoskeleton function promotes tumor progression. Semin Cancer Biol, 2008,18(4):251~259.
[15] Bourguignon, L.Y.Matrix Hyaluronan Promotes Specific MicroRNA Upregulation Leading to Drug Resistance and Tumor Progression. Int J Mol Sci, 2016,17(4):517.
[16] Jordan, A.R.Antitumor activity of sulfated hyaluronic acid fragments in pre-clinical models of bladder cancer. Oncotarget, 2016.
[17] Thompson, C.B.Enzymatic depletion of tumor hyaluronan induces antitumor responses in preclinical animal models. Mol Cancer Ther, 2010,9(11): 3052~3064.
[18] Cordo Russo, R.I.Hyaluronan oligosaccharides sensitize lymphoma resistant cell lines to vincristine by modulating P-glycoprotein activity and PI3K/Akt pathway. Int J Cancer, 2008,122(5):1012~1018.
[19] Giannopoulos, K.Peptide vaccination elicits leukemia-associated antigen-specific cytotoxic CD8+ T-cell responses in patients with chronic lymphocytic leukemia. Leukemia, 2010, 24(4):798~805.
[20] Kesharwani, P.Hyaluronic acid-conjugated polyamidoamine dendrimers for targeted delivery of 3,4-difluorobenzylidene curcumin to CD44 overexpressing pancreatic cancer cells. Colloids Surf B Biointerfaces, 2015,136:413~423.
[21] Li, K.Mulberry-like dual-drug complicated nanocarriers assembled with apogossypolone amphiphilic starch micelles and doxorubicin hyaluronic acid nanoparticles for tumor combination and targeted therapy. Biomaterials, 2015,39:131~144.
[22] Ohta, S.Production of Cisplatin-Incorporating Hyaluronan Nanogels via Chelating Ligand-Metal Coordination. Bioconjug Chem, 2016,27(3):504~508.
[23] Li, S.Redox-Sensitive and Intrinsically Fluorescent Photoclick Hyaluronic Acid Nanogels for Traceable and Targeted Delivery of Cytochrome c to Breast Tumor in Mice. ACS Appl Mater Interfaces, 2016,8(33):21155~21162.
(编审:刘付平)
安徽省立医院成功开展腹腔镜下脾切除+门奇断流术
近日,安徽省立医院普外科肝脏外科病区以马金良教授为首的治疗团队成功为一例乙肝肝硬化、门静脉高压症的患者进行了完全腹腔镜下门奇断流术(脾切除+贲门周围血管离断术)。患者,男性,40岁,系安徽省宿松县人,诊断明确,手术过程顺利,出血约100mL,术后第8天康复出院。随后,肝脏外科再接再厉又为一位门脉高压症患者成功施行了完全腹腔镜下门奇断流术,目前该患者病情稳定。
自1987年成功开展电视腹腔镜胆囊切除术以来,腹腔镜手术以切口小而视野清、术中出血少、术后疼痛轻、恢复快等“微创”优势,深得医生和患者的欢迎,很快扩展到脾脏切除,肝脏、胰腺部分切除,使外科学进入“微创外科”时代。1991年 Delaitre等成功完成了世界首例腹腔镜脾切除术,1995年Kusminsky等经手助腹腔镜行断流术治疗门脉高压取得成功,自此腹腔镜下治疗门脉高压疾病在各大医院得到开展。
由于门脉高压症患者门静脉压力高、脾脏肿大明显,解剖复杂,完全腹腔镜下门奇断流术操作难度大,风险高,要求手术者必须同时具备娴熟的开腹门奇断流的经验和精湛的腔镜技术。术中如何有效控制脾蒂出血,如何安全地进行贲门周围血管离断等,一直是限制腹腔镜门脉高压症手术的重要原因。此次完全腹腔镜下门奇断流术的开展,拓展了普外科腹腔镜下门脉高压症手术的范围,将为更多的门脉高压症患者提供一种创伤更小、术后疼痛更轻、恢复更快、住院时间更短的手术治疗方法;也代表着该院肝脏外科在腹腔镜门脉高压症的治疗中居省内领先水平。
(供稿:张传海)
Recent Advances of Hyaluronan in the Pathogenesis and Therapy of Tumors
The first Affiliated Hospital of Anhui Medical University, Hefei 230022, Anhui
LIU Hao
Hyaluronic Acid, also called hyaluronan, one of the main components of the extracellular matrix, which plays key role in the pathogenesis of tumors. In this review, the structure, synthesis, degradation of hyaluronan and its interaction with the receptors, and their functions in the pathogenesis of tumors were summarized. The recent advances of hyaluronan in the treatment of tumors were also reviewed.
Hyaluronan; Tumorigenesis; Targeted therapy
R730.5
A
1671-8054(2016)05-0030-03
安徽医科大学第一附属医院肿瘤内科 安徽合肥 230022
刘昊,女,博士,医师
2016-07-10收稿,2016-09-10修回
