MnO2/H-TiO2纳米异质阵列的调控制备及超电容特性
2016-11-22刘家琴李靖巍吴玉程
徐 娟 刘家琴 李靖巍 王 岩 吕 珺 吴玉程,*
(1合肥工业大学化学与化工学院,合肥230009;2合肥工业大学工业与装备技术研究院,合肥230009;3先进功能材料与器件安徽省重点实验室,合肥230009;4合肥工业大学材料科学与工程学院,合肥230009)
MnO2/H-TiO2纳米异质阵列的调控制备及超电容特性
徐娟1,3刘家琴2,3,*李靖巍2王岩3,4吕珺3,4吴玉程3,4,*
(1合肥工业大学化学与化工学院,合肥230009;2合肥工业大学工业与装备技术研究院,合肥230009;3先进功能材料与器件安徽省重点实验室,合肥230009;4合肥工业大学材料科学与工程学院,合肥230009)
采用目标调控的阳极氧化工艺制备了超大比表面、管与管相互分离的有序TiO2纳米管阵列(TiO2NTAs)基体,进而分别采用电化学氢化法和循环浸渍沉积法对晶化退火后的TiO2NTAs实施电化学氢化和高比电容MnO2沉积的双重功能化改性,调控构筑了一种新型MnO2/H-TiO2纳米异质阵列电极材料。利用场发射扫描电子显微镜(FESEM)、高分辨透射电子显微镜(TRTEM)、X射线衍射仪(XRD)、X光电子能谱仪(XPS)、拉曼光谱(Raman)和电化学工作站等对样品进行综合表征与超电容特性测试,结果表明:电化学氢化改性有效提高了H-TiO2NTAs的导电性和电化学特性,当电流密度为0.2 mA·cm-2时H-TiO2NTAs的面积电容达到7.5 mF·cm-2,是相同电流密度下TiO2NTAs的75倍;经过2个浸渍循环所获得的MnO2/H-TiO2NTAs-2样品在电流密度为3 mA·mg-1时比电容可达481.26 F·g-1,电流密度为5 mA·mg-1时循环充放电1000圈后比电容仅下降约11%。
TiO2纳米管阵列;氢化;MnO2;电化学;超电容特性
1 引言
超级电容器是一种新型高效的储能器件,兼有可快速充放电、长循环寿命、高能量密度、高功率密度、超低温特性好等优势,在电动汽车、通讯信息、国防科技等领域具有广阔的应用前景和发展潜力1-4。超级电容器主要由电极材料、电解质、隔膜、端板等组成,其中电极材料是决定其超电容特性的关键5-8。利用微纳技术制备高性能的电极材料成为进一步发展超级电容器的重要途径。超级电容器电极材料的发展趋势之一就是通过协同作用发挥不同纳米材料或纳米结构的功能特性如有序特性、介孔特性、大比表面积、表面官能团等制备复合电极材料,以实现电极材料在大电流密度下的高能量、高功率密度的存储能力以及长寿命循环条件下的比电容保持能力2,9-11。
将一维纳米单元按一定方式排列起来构成阵列体系,是当今纳米材料和纳米结构研究的前沿和热点,也是下一代纳米结构器件设计和制造的基础12-15。目前利用微纳技术制备高性能超级电容器电极材料的研究大多基于无序纳米材料,如何充分发掘有序纳米阵列材料的优势,成为微米、纳米技术领域关于超级电容器电极材料研究的新兴热点16-18。美国宾夕法尼亚州立大学Grimes于2008年在Nano Letters上发表论文19称:采用电化学阳极氧化法在高纯Ti片表面制得垂直有序排列的TiO2纳米管阵列,其电化学容量可达80 mF· cm-2,如果通过质子注入等途径能够有效调控TiO2纳米阵列的电子结构、电容特性,有序TiO2纳米管阵列材料将有望应用于超级电容器电极材料,由此开启了基于有序纳米阵列超级电容器电极材料的研究。加州大学Li于2012年在Nano Letters上报道了一种提高有序TiO2纳米管阵列超电容特性的有效方法:采用氢气退火工艺对Ti纤维表面阳极氧化法制备的TiO2纳米管阵列进行氢化改性,认为氢化后氧空位和纳米管表面羟基密度的增加可以显著提高H-TiO2纳米管阵列的比电容量,并且比电容抗衰减性能也有大幅度的提升,同时认为TiO2纳米管阵列是负载其他高比电容材料如MnO2等的良好载体20。2013年该课题组又发展了一种基于C纤维/H-TiO2纳米线阵列/MnO2超级电容器电极材料,其中H-TiO2@MnO2的比电容最高为449.6 F· g-1,H-TiO2@C比电容最高为253.4 F·g-121;由此可见,高比电容MnO2沉积改性可以大幅度提高HTiO2纳米线阵列的超电容性能。
本研究采用目标调控的阳极氧化工艺制备超大比表面、管与管相互分离的TiO2纳米管阵列薄膜基体;进而利用简易、绿色的电化学氢化法对晶化退火后的TiO2纳米管阵列薄膜实施氢化改性,提高TiO2纳米管阵列薄膜的电容特性和电化学性能;进一步采用循环浸渍沉积法在H-TiO2纳米管内、外表面可控负载高比电容量MnO2纳米颗粒,调控构筑一种新型MnO2/H-TiO2纳米异质阵列薄膜电极材料。不仅拓展了有序TiO2纳米管阵列应用范围,而且为基于有序纳米材料超级电容器电极材料的研究提供理论依据和技术支撑。
2 实验部分
2.1实验所用试剂
钛片(纯度99.7%,厚度0.01 mm),无水乙醇(纯度≥99.7%),丙酮(纯度≥99.5%),NH4F(纯度≥96.0%),乙二醇(纯度≥99.0%),Na2SO4(纯度≥99.0%),Mn(AC)2·4H2O(纯度≥99.0%),KMnO4(纯度≥99.5%),化学试剂均为分析纯,实验用水均为去离子水。
2.2样品制备
MnO2/H-TiO2纳米异质阵列电极材料的制备流程如图1所示,主要分为电化学阳极氧化(晶化退火)、电化学氢化改性和高比电容MnO2沉积三大主要步骤。
2.2.1超大比表面、管与管相互分离TiO2NTAs的制备
先将一定尺寸的Ti片分别在丙酮和无水乙醇中各超声清洗20 min,再用去离子水洗净干燥待用;然后将Ti片作为阳极,石墨片作为阴极,置于0.25 mol·L-1NH4F+7%(volume fraction)H2O+乙二醇电解液体系中,60 V恒压氧化6 h;阳极氧化后,将TiO2NTAs样品取出后在乙二醇中超声10-15 min去除表面絮状物质,再用去离子水清洗后60°C烘干。TiO2NTAs晶化退火采用的工艺是500°C保温2 h,升温速度为2°C·min-1。

图1 MnO2/H-TiO2NTAs复合材料制备流程Fig.1 Fabrication process of the MnO2/H-TiO2NTAs composite
2.2.2H-TiO2NTAs的制备
采用电化学氢化法对TiO2NTAs实施氢化改性,分别以晶化TiO2NTAs为阴极,石墨片为阳极,0.1 mol·L-1Na2SO4的电解液中恒压4 V氢化20 min,然后用去离子水冲洗、烘干,获得H-TiO2NTAs。值得注意的是,可以观察到大量氧空位产生所致的电致变色现象22,23,灰色TiO2NTAs经过氢化改性后转变为蓝色H-TiO2NTAs,如图1所示。
2.2.3MnO2/H-TiO2纳米异质阵列的制备
采用循环浸渍沉积工艺实现高比电容纳米MnO2在H-TiO2纳米管内、外表面的均匀负载,调控制备MnO2/H-TiO2纳米异质阵列电极材料。先分别配制0.075 mol·L-1Mn(AC)2·4H2O溶液(A)和0.05 mol·L-1KMnO4溶液(B)并放置于20°C水浴中,将H-TiO2NTAs放入A溶液中浸渍60 s后取出用去离子水冲洗,再将其放入B溶液中浸渍60 s,取出后再用去离子水冲洗。浸渍沉积反应式如下:
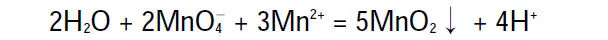
上述一个浸渍反应过程被分别循环重复1-3次,所对应样品被分别记作MnO2/H-TiO2NTAs-X (X=1,2,3);最后将样品洗涤,60°C干燥待测。
2.3表征与测试
利用场发射扫描电子显微镜(FESEM,Hitachi SU8020,操作电压5 kV)观察TiO2NTAs、H-TiO2NTAs及MnO2纳米颗粒在纳米管内外表面的负载效果,利用高分辨透射电子显微镜(HRTEM,JEOL JEM-2100F,操作电压200 kV)对样品的微观结构进行进一步的观察和异质结构的表征。利用X射线衍射仪(Rigaku D/Max-2500V)对样品进行物相分析,以Cu-Kα(λ=0.154056 nm)作为X射线激发源,扫描速率为2(°)·min-1;利用X光电子能谱仪(XPS,ESCALAB250)对样品进行成分和元素价态分析,以单色Al Kα(1486.60 eV)作为激发源,以C 1s在284.80 eV位置作为基准校正;通过显微共焦激光拉曼光谱(Raman,LabRAM HR Evolution,激发波长532 nm)分析样品的分子结构。
利用电化学工作站(上海辰华CHI760E型)三电极体系进行循环伏安(CV)特性、充放电(CD)特性测试以及电化学阻抗谱(EIS)测试。以0.5 mol·L-1Na2SO4为电解液,以所制备的目标样品、Ag/AgCl电极和铂丝分别作为工作电极、参比电极和对电极。CV测试和CD测试的电压窗口均为0-1.0 V,EIS测试频率范围为0.01 Hz-100 kHz,振幅为5 mV。采用CT2001A型蓝电电池测试系统(武汉蓝电电子股份有限公司)测试目标材料的循环稳定性。
3 结果与讨论
3.1FESEM和HRTEM分析
利用FESEM对所制备样品进行形貌表征,如图2和图3所示,结果表明:通过电化学阳极氧化法制备获得了超大比表面、管与管相互分离的TiO2NTAs(图2(a)),管径约150 nm,管壁厚度约25 nm,纳米管之间的平均间隙约10-20 nm,纳米管的相互分离和内外表面的充分裸露,为后续负载改性提供了更多的活性表面;电化学氢化改性后的H-TiO2NTAs与TiO2NTAs在微观结构和形貌上没有明显不同(图2(b));图3(a-c)分别为MnO2/ H-TiO2NTAs-1,2,3的FESEM形貌,由图可以看出,利用循环浸渍沉积工艺实现了高比电容MnO2在H-TiO2纳米管内、外表面的均匀可控负载,随着浸渍循环次数的增加,负载于TiO2NTAs内外表面的MnO2纳米颗粒数量逐渐增多,颗粒尺寸逐渐增大。经过1个浸渍循环,虽然负载于H-TiO2纳米管内外表面的MnO2纳米颗粒分布均匀弥散、尺寸细小,纳米管保持中空结构且有效内径并无明显减小,纳米管之间间隙也清晰可见,但是其整体负载量较少;经过2个浸渍循环后,MnO2纳米颗粒的负载量明显增大,并且自上而下的整个管壁的MnO2纳米颗粒负载均匀(图3(d));经过3个浸渍循环后,MnO2纳米颗粒的大量负载导致了H-TiO2纳米管内径的明显减小和纳米管间隙处的堵塞,从而会降低MnO2/H-TiO2NTAs-3的比表面积。

图2 TiO2NTAs(a)和H-TiO2NTAs(b)的FESEM形貌表征Fig.2 FESEM morphology of TiO2NTAs(a)and H-TiO2NTAs(b)

图3 MnO2/H-TiO2NTAs-1,2,3的FESEM形貌表征(a-c)和MnO2/H-TiO2NTAs-2侧面放大图(d)Fig.3 FESEM morphology of MnO2/H-TiO2NTAs-1,2,3(a-c)and enlarged side-view of MnO2/H-TiO2NTAs-2(d) Insets in(a-c)show the FESEM images of the corresponding cross-sections of samples.
采用TEM和HRTEM进一步表征和分析了MnO2H-TiO2NTAs-2的微观结构,如图4(a)所示:大量纳米颗粒均匀弥散地负载于纳米管内外表面,晶格间距为0.345 nm的晶格条纹对应锐钛矿TiO2(101)晶面(图4(b)),此外管壁附近还有大量有序的晶格条纹微区,进一步证实了纳米管表面的确负载了很多纳米颗粒。进一步对单根MnO2/HTiO2纳米管进行能量色散X射线光谱分析(图4(cf)),结果表明:MnO2/H-TiO2NTAs-2不仅含有Ti、O元素,而且含有Mn元素,并且元素分布均匀,其中O元素分布密度最大,进一步佐证了MnO2在H-TiO2纳米管表面的均匀负载。
3.2XRD分析
利用XRD对TiO2NTAs、H-TiO2NTAs和MnO2/H-TiO2NTAs-1,2,3样品分别进行了物相分析,如图5所示:所有样品在2θ=25.3°,37.9°, 48.0°和53.9°处的衍射峰分别对应于锐钛矿相TiO2NTAs的(101)、(004)、(200)和(105)晶面(JCPDS:21-1272),其它位置的衍射峰均对应于Ti基底,表明阳极氧化法制备的非晶TiO2NTAs经500°C退火后完全晶化为锐钛矿相TiO2。与锐钛矿TiO2NTAs (图5(a))相比,电化学氢化后的H-TiO2NTAs(图5 (b))和MnO2负载改性后的MnO2/H-TiO2NTAs-1,2, 3(图5(c-e))均未出现新相衍射峰,结合HRTEM有序晶格条纹像分析认为,所负载的MnO2是无定型和微晶的混合态21,24,25,因此XRD曲线中未出现明显的新相衍射峰。
3.3Raman和XPS分析
采用Raman光谱进一步深入分析了TiO2NTAs、H-TiO2NTAs和MnO2/H-TiO2NTAs-2的结构特征,如图6所示:晶化退火后的TiO2NTAs样品在145.12 cm-1(Eg)、198.40 cm-1(Eg)、397.32 cm-1(B1g)、517.28 cm-1(A1g/B1g)和639.07 cm-1(Eg)位置的拉曼峰对应于锐钛矿TiO226,27(图6(a))。与TiO2NTAs相比,H-TiO2NTAs的拉曼峰位于146.95 cm-1(Eg)、199.77 cm-1(Eg),出现明显的蓝移(即波数增大),蓝移主要是由声子限域、结构缺陷和晶粒大小所导致的。众所周知当晶粒尺寸小于10 nm或者其结构短程有序,声子限域所引起的一些缺陷将导致样品的拉曼峰出现蓝移或者加宽现象,而以上FESEM和HRTEM分析表明H-TiO2NTAs的晶粒尺寸远大于10 nm,意味着声子限域和晶粒大小对H-TiO2NTAs的拉曼峰蓝移没有影响,从而推测Eg峰的偏移是由于结构缺陷所致。TiO2NTAs的电化学氢化过程不同于氢气气氛中退火处理的氢化过程,它不仅包括水中的质子注入,而且还包括Ti基体中电子的注入28,29,电子的注入导致锐钛矿TiO中的部分八面体被还原成(O)Ti3+;质子注入致使毗连的八面体转变为(HO)Ti4+(O5),反应式如下:

图4 MnO2/H-TiO2NTAs-2的TEM和HRTEM形貌(a,b)及能量色散X射线谱图(c-f)Fig.4 TEM and HRTEM morphology(a,b)and energy dispersive X-ray spectroscopy(EDS)mapping(c-f)of MnO2/H-TiO2NTAs-2
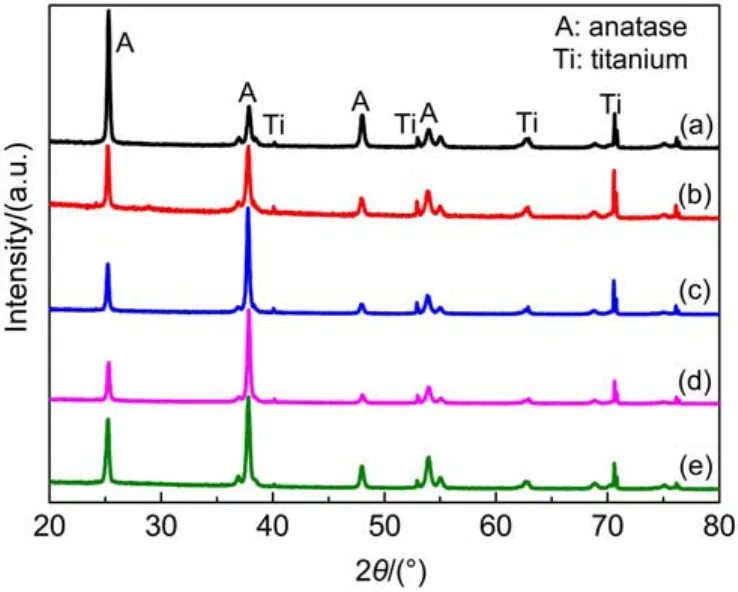
图5 TiO2NTAs(a),H-TiO2NTAs(b)和MnO2/H-TiO2NTAs-1,2,3(c-e)的XRD图Fig.5 XRD patterns of TiO2NTAs(a),H-TiO2NTAs(b) and MnO2/H-TiO2NTAs-1,2,3(c-e)
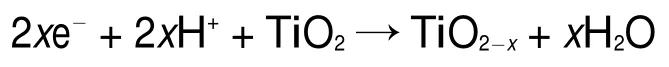
由此可知:电化学氢化处理后TiO2中的部分Ti4+被还原成Ti3+,形成了大量氧空位结构缺陷。由图6(b)也可以看出MnO2/H-TiO2NTAs-2的Eg峰呈现明显的蓝移,主要是由于负载的MnO2与TiO2的共同作用导致639.07 cm-1(Eg)(对应着TiO2的峰)被拓宽到500-700 cm-1,另外635 cm-1处的峰对应着[MnO6]八面体结构中Mn―O的对称伸缩振动30-33。
利用X光电子能谱(XPS)分析法对MnO2/HTiO2NTAs-2样品进行表面成分和元素价态分析,如图7所示,由XPS全谱(图7(a))可以看出:MnO2/ H-TiO2NTAs-2样品中含有O、Ti、Mn三种元素。由O 1s高分辨谱图(图7(b))分析,结合能为530.0 eV对应于TiO2和MnO2中的Ti―O键,结合能为531.4 eV对应于Ti―OH键;由Ti 2p高分辨谱图(图7(c))分析,结合能为458.8和464.4 eV两个特征峰分别对应于Ti 2p3/2和Ti 2p1/2,两峰之间的差值为5.6 eV,证明了锐钛矿TiO2中的Ti为+4价(Ti4+),与文献20,30,34报道一致。由Mn 2p高分辨谱图(图7 (d))分析,结合能为642.3和654.0 eV两个特征峰分别对应于Mn 2p3/2和Mn 2p1/2,两个谱峰之间的差值为11.7 eV,是典型MnO2的谱峰16,31,35。理论上在O 1s高分辨谱图(图7(b))结合能为531.4 eV处应该有偏移,在Ti 2p高分辨谱图(图7(c))中应该有Ti3+2p3/2和Ti3+2p1/2谱峰,但在图中并没有观察到20,26,可能是由于通过电化学氢化法获得的H-TiO2NTAs中Ti4+被还原成Ti3+的比例较小,因此无法有效检测到Ti 2p和O 1s结合能的偏移,但是结合Raman图谱和后续电化学性能测试结果依然可以确定HTiO2NTAs中氧空位的存在(即Ti3+的存在)。
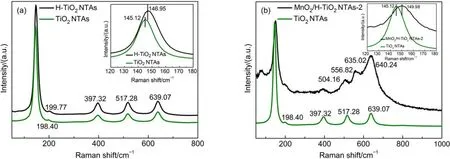
图6 TiO2NTAs和H-TiO2NTAs(a)以及TiO2NTAs和MnO2/H-TiO2NTAs-2(b)的拉曼光谱图Fig.6 Raman spectra of TiO2NTAs and H-TiO2NTAs(a)and TiO2NTAs and MnO2/H-TiO2NTAs-2(b)
3.4超电容特性分析
利用电化学工作站测试分析样品的超电容特性,其中TiO2NTAs和H-TiO2NTAs在不同扫描速率下的循环伏安曲线和不同电流密度下的充放电曲线如图8所示。TiO2NTAs的CV曲线形状接近于三角形,表明TiO2NTAs的电容特性较差,由其对应CD曲线计算可知:当电流密度为0.2 mA·cm-2时TiO2NTAs的面积电容约为0.1 mF·cm-2。H-TiO2NTAs的CV曲线随着扫描速率从10 mV·s-1增加到100 mV·s-1时均保持较好的矩形形状,表明H-TiO2NTAs具有良好的电容特性和倍率性能,由其对应的CD曲线计算可知:当电流密度为0.2 mA·cm-2时H-TiO2NTAs的面积电容达到约7.5 mF·cm-2,是相同的电流密度下TiO2NTAs比电容的75倍。进一步由图9比较可知:H-TiO2NTAs的CV曲线更接近矩形,即更接近理想电容器,H-TiO2NTAs的CD曲线充放电时间更长,且具有良好的对称性和线性,以上均说明电化学氢化改性有效提高了HTiO2NTAs的导电性和电化学特性。
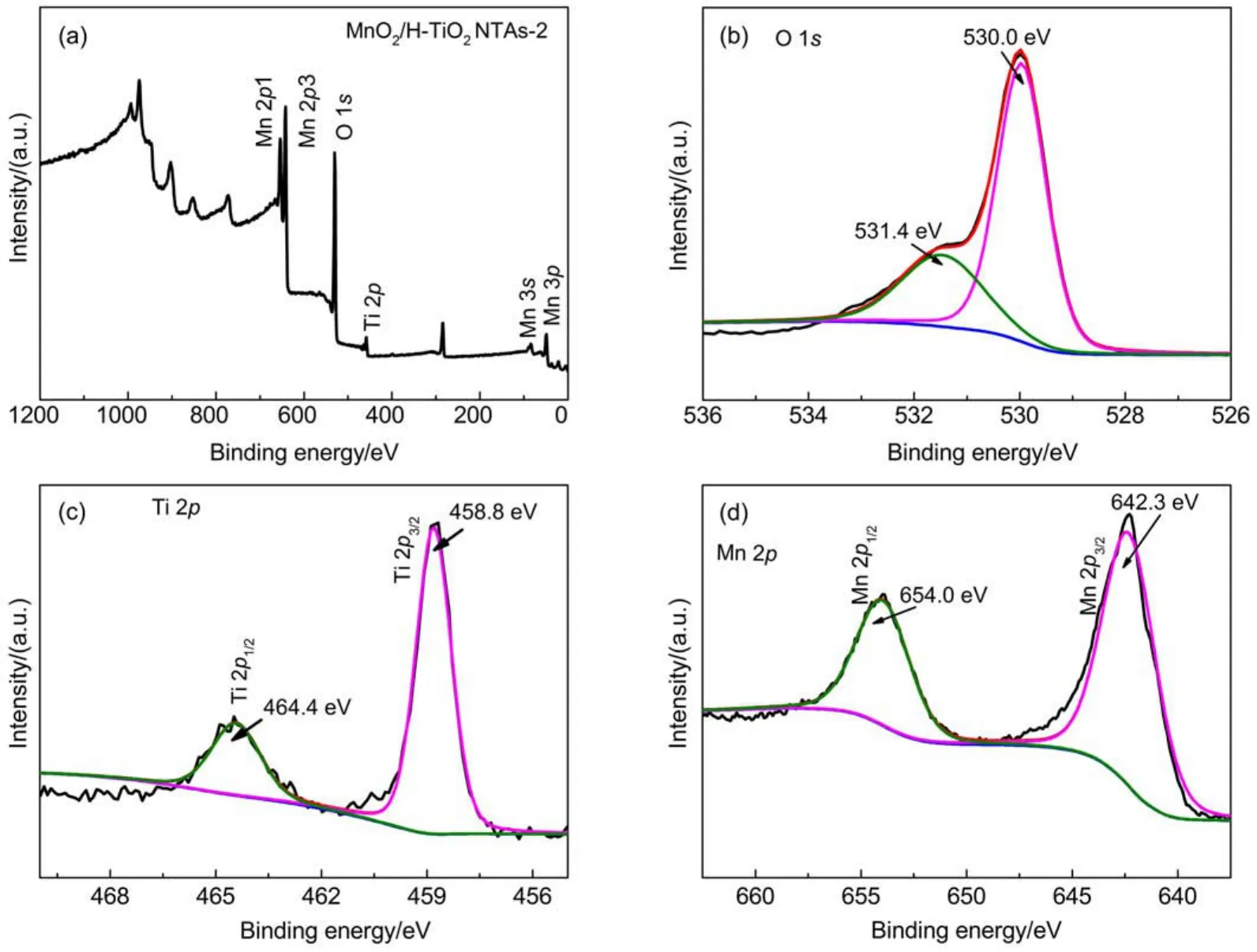
图7 MnO2/H-TiO2NTAs-2的XPS全谱图(a)以及O 1s(b),Ti 2p(c),Mn 2p(d)的XPS谱图Fig.7 XPS survey spectra of the MnO2/H-TiO2NTAs-2(a)and XPS spectra of O 1s(b),Ti 2p(c),Mn 2p(d)

图8 (a)TiO2NTAs和(c)H-TiO2NTAs在不同扫描速率下的循环伏安曲线;(b)TiO2NTAs和(d)H-TiO2NTAs在不同电流密度下的充放电曲线Fig.8 Cyclic voltammetry(CV)curves of TiO2NTAs(a)and H-TiO2NTAs(c)at different scan rates; charge-discharge(CD)curves of TiO2NTAs(b)and H-TiO2NTAs(d)at different current densities
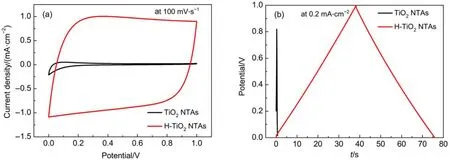
图9 (a)TiO2NTAs和H-TiO2NTAs在100 mV·s-1下的循环伏安曲线;(b)TiO2NTAs和H-TiO2NTAs在0.2 mA·cm-2下的恒电流充放电曲线Fig.9 (a)CV curves of TiO2NTAs and H-TiO2NTAs at a scan rate of 100 mV·s-1,(b)CD curves of TiO2NTAs and H-TiO2NTAs at a current density of 0.2 mA·cm-2
高比电容MnO2沉积改性后的MnO2/H-TiO2NTAs-X(X=1,2,3)在扫描速率为100 mV·s-1时的CV曲线和电流密度为1 mA·mg-1时的CD曲线如图10所示,在不同浸渍循环次数条件下,MnO2/HTiO2NTAs-X(X=1,2,3)所对应的MnO2负载量、面积负载量以及比电容大小如表1所示,分析可知:MnO2/H-TiO2NTAs-X(X=1,2,3)的MnO2负载量和比电容并不是一直随着循环浸渍次数的增加而增大。当循环次数为2次时比电容达到最大值,其原因主要是:当经过1个浸渍循环后,虽然负载于H-TiO2NTAs上的MnO2纳米颗粒分布均匀弥散、尺寸细小,但是MnO2整体负载量较少,其电容特性相对较低;随着循环次数的增加,MnO2负载量也增大,电容特性也相对提高,但是比电容与质量成正态分布,因此经过3个浸渍循环后,虽然MnO2整体负载量最大,但是MnO2/H-TiO2NTAs-3的比电容反而降低。

图10 (a)MnO2/H-TiO2NTAs-X(X=1,2,3)在扫描速率为100 mV·s-1时的循环伏安曲线,(b)MnO2/H-TiO2NTAs-X(X=1,2,3)在电流密度为1 mA·mg-1时的恒电流充放电曲线Fig.10 (a)CV curves of MnO2/H-TiO2NTAs-X(X=1,2,3)at a scan rate of 100 mV·s-1, (b)CD curves of MnO2/H-TiO2NTAs-X(X=1,2,3)at a current density of 1 mA·mg-1
进一步针对MnO2/H-TiO2NTAs-2进行了CV和CD测试,如图11所示,当扫速由30 mV·s-1逐渐增大至100 mV·s-1时,尽管其CV曲线有点偏离矩形,但是仍表现出良好的电容特性,由CD曲线计算可知,MnO2/H-TiO2NTAs-2在电流密度为3 mA· mg-1时比电容可达481.26 F·g-1。此外,随着扫描速率或者电流密度的增加,比电容逐渐减小,反之则增加,主要是由于在高扫速或者高电流密度下离子没有充分进入电极内部,导致材料的赝电容贡献很小;然而在低扫速或者低电流密度时,离子有充分时间进入电极内部,使得参与氧化还原反应的MnO2的量增加,更好地发挥了过渡金属材料的赝电容特性,因此比电容也相应增加。
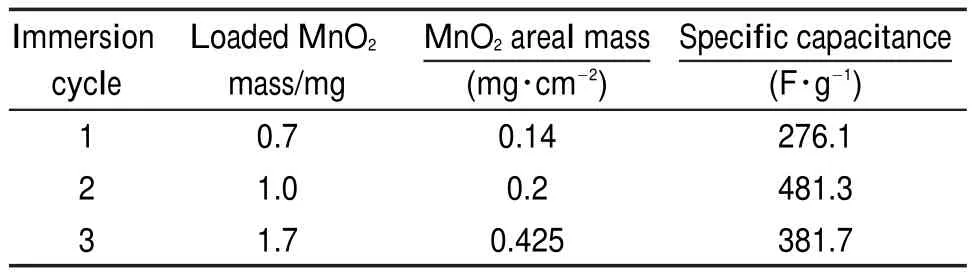
表1 浸渍循环次数与MnO2/H-TiO2NTAs-X(X=1,2,3)所对应MnO2负载量、面积负载量、比电容之间的关系Table 1 Relationship of immersion cycles with corresponding loaded MnO2mass,areal mass,and specific capacitance of MnO2/H-TiO2NTAs-X(X=1,2,3)

图11 (a)MnO2/H-TiO2NTAs-2在不同扫速下的循环伏安曲线,(b)MnO2/H-TiO2NTAs-2在不同电流密度下的充放电曲线Fig.11 (a)CV curves of MnO2/H-TiO2NTAs-2 at different scan rates,(b)CD curves of MnO2/H-TiO2NTAs-2 at different current densities
利用EIS进一步分析了TiO2NTAs、H-TiO2NTAs和MnO2/H-TiO2NTAs-2电荷储存时的动力学特征,如图12所示,与TiO2NTAs相比,H-TiO2NTAs在低频区的直线更接近90°,低频区主要是由电解质离子的扩散控制引起的,越接近90°说明扩散电阻越小,具有良好的导电性和理想的电容性能。此外,H-TiO2NTAs在高频区与X轴的交点值较小(图12(a)插图),说明H-TiO2NTAs电极材料的内阻比TiO2NTAs的内阻小,上述测试结果均表明H-TiO2NTAs具有比TiO2NTAs更高的电化学特性和电容特性。与H-TiO2NTAs相比,MnO2/HTiO2NTAs-2在低频区的直线也接近90°,说明二者的离子扩散阻力都较小;MnO2/H-TiO2NTAs-2在高频区的半圆直径小于H-TiO2NTAs的半圆直径(图12(b)插图),说明MnO2/H-TiO2NTAs-2电极材料的电荷转移电阻更小,也进一步证明了该复合电极材料具有更高的电容性能25。通过恒电流充放电测试MnO2/H-TiO2NTAs-2电极材料的循环寿命,如图13所示,当电流密度为5 mA·mg-1,电压窗口为0-1 V时,循环次数为1000圈后比电容下降了约11%,表明MnO2/H-TiO2NTAs-2电极材料具有较高的循环稳定性。

图12 TiO2NTAs和H-TiO2NTAs(a),H-TiO2NTAs和MnO2/H-TiO2NTAs-2(b)的奈奎斯特图Fig.12 Nyquist plots of the TiO2NTAs and H-TiO2NTAs(a),H-TiO2NTAs and MnO2/H-TiO2NTAs-2(b)

图13 MnO2/H-TiO2NTAs-2在电流密度为5 mA·mg-1时循环1000圈的循环稳定性Fig.13 Cycling stability of the MnO2/H-TiO2NTAs-2 at a current density of 5 mA·mg-1for 1000 cycles
4 结论
采用电化学阳极氧化法调控制备了超大比表面、管与管相互分离的TiO2NTAs基体,为后续功能化改性提供超大的活性表面和高度有序特性;进而利用简易、绿色的电化学氢化法对晶化退火后的TiO2NTAs实施氢化改性,显著提高了H-TiO2NTAs的导电性和电化学特性,当电流密度为0.2 mA·cm-2时H-TiO2NTAs的面积电容达到7.5 mF· cm-2,是相同的电流密度下TiO2NTAs的75倍;进一步采用循环浸渍沉积法在H-TiO2NTAs内、外表面可控负载高比电容MnO2纳米颗粒,可控制备了一种新型MnO2/H-TiO2纳米异质阵列电极材料,其中经过2个浸渍循环所得MnO2/H-TiO2NTAs-2在电流密度为3 mA·mg-1时比电容可达481.26 F· g-1,电流密度为5 mA·mg-1时循环充放电1000圈后比电容仅下降约11%。本研究不仅拓展了有序TiO2纳米管阵列应用领域,而且为基于有序纳米材料超级电容器电极材料的研究提供理论依据和技术支撑。
References
(1) Luo,Y.;Kong,D.;Luo,J.;Chen,S.;Zhang,D.;Qiu,K.;Qi,X.; Zhang,H.;Li,C.M.;Yu,T.RSC Adv.2013,3(34),14413. doi:10.1039/c3ra42229a
(2)Kim,B.C.;Hong,J.Y.;Wallace,G.G.;Park,H.S.Adv.EnergyMater.2015,5,1500959.doi:10.1002/aenm.201500959
(3) Kim,J.H.;Lee,S.;Choi,J.;Song,T.;Paik,U.J.Mater.Chem. A 2015,3(41),20459.doi:10.1039/c5ta06266g
(4)Ma,Y.;Chang,H.;Zhang,M.;Chen,Y.Adv.Mater.2015,27 (36),5296.doi:10.1002/adma.201501622
(5) Wang,G.;Zhang,L.;Zhang,J.Chem.Soc.Rev.2012,41(2), 797.doi:10.1039/c1cs15060j
(6) Zhi,M.;Xiang,C.;Li,J.;Li,M.;Wu,N.Nanoscale 2013,5(1), 72.doi:10.1039/c2nr32040a
(7) Titirici,M.M.;White,R.J.;Brun,N.;Budarin,V.L.;Su,D.S.; Monte,F.D.;Clarkd,J.H.;MacLachlan,M.J.Chem.Soc.Rev. 2014,25,250.doi:10.1039/C4CS00232F
(8) Dong,L.;Xu,C.;Li,Y.;Huang,Z.H.;Kang,F.;Yang,Q.H.; Zhao,X.J.Mater.Chem.A 2016,4,4659.doi:10.1039/ C5TA10582J
(9)Yuan,C.;Wu,H.B.;Xie,Y.;Lou,X.W.Angew.Chem.Int.Ed. 2013,52(6),1488.doi:10.1002/anie.201303971
(10) Achilleos,D.S.;Hatton,T.A.J.Colloid Interface Sci.2015, 447,282.doi:10.1016/j.jcis.2014.12.080
(11)Cao,X.Y.;Xing,X.;Zhang,N.;Gao,H.;Zhang,M.Y.;Shang, Y.C.;Zhang,X.T.J.Mater.Chem.A 2015,3,3785. doi:10.1039/C4TA06138A
(12) Ning,X.;Wang,X.;Yu,X.;Li,J.;Zhao,J.J.Alloy Compd. 2016,658,177.doi:10.1016/j.jallcom.2015.10.204
(13) Zhi,J.;Deng,S.;Wang,Y.;Hu,A.J.Mater.Chem.C 2015,119 (16),8530.doi:10.1021/acs.jpcc.5b01230
(14) Zhu,Q.;Hu,H.;Li,G.;Zhu,C.;Yu,Y.Electrochim.Acta 2015, 156,252.doi:10.1016/j.electacta.2015.01.023
(15) Li,Y.;Wang,H.;Jian,J.;Fan,Y.;Yu,L.;Cheng,G.;Zhou,J.; Sun,M.RSC Adv.2016,6,13957.doi:10.1039/ C5RA28077J10.1039/c5ra28077j
(16) Sun,S.;Wang,P.;Wang,S.;Wu,Q.;Fang,S.Mater.Lett.2015, 145,141.doi:10.1016/j.matlet.2015.01.061
(17) Deng,D.;Kim,B.S.;Gopiraman,M.;Kim,I.S.RSC Adv. 2015,5(99),81492.doi:10.1039/c5ra16624a
(18)Tan,D.Z.W.;Cheng,H.;Nguyen,S.T.;Duong,H.M.Mater. Technol.2014,29(A2),A107.doi:10.1179/ 1753555714y.0000000175
(19) Mor,G.K.;Varghese,O.K.;Wilke,R.H.T.;Sharma,S.; Shankar,K.;Latempa,T.J..;Choi,K.S.;Grimes,C.A.Nano Lett.2008,8(7),1906.doi:10.1021/nl500710j
(20) Lu,X.;Wang,G.;Zhai,T.;Yu,M.;Gan,J.;Tong,Y.;Li,Y. Nano Lett.2012,12(3),1690.doi:10.1021/nl300173j
(21) Lu,X.;Yu,M.;Wang,G.;Zhai,T.;Xie,S.;Ling,Y.;Tong,Y.; Li,Y.Adv.Mater.2013,25(2),267.doi:10.1002/ adma.201203410
(22) Li,Z.;Ding,Y.;Kang,W.;Li,C.;Lin,D.;Wang,X.;Chen,Z.; Wu,M.;Pan,D.Electrochim.Acta 2014,161,40.doi:10.1016/j. electacta.2014.12.132
(23) Liu,N.;Schneider,C.;Freitag,D.;Hartmann,M.;Venkatesan, U.;Muller,J.;Spiecker,E.;Schmuki,P.Nano Lett.2014,14(6), 3309.doi:10.1021/nl500710j
(24) Di,J.;Fu,X.;Zheng,H.;Jia,Y.J.Nanopart Res.2015,17(6). doi:10.1007/s11051-015-3060-z
(25) Zhou,H.;Zhang,Y.J.Power Sources 2014,272,866. doi:10.1016/j.jpowsour.2014.09.030
(26) Zhou,H.;Zhang,Y.J.Power Sources 2013,239,128. doi:10.1016/j.jpowsour.2013.03.114
(27) Wu,H.;Xu,C.;Xu,J.;Lu,L.;Fan,Z.;Chen,X.;Song,Y.;Li, D.Nanotechnology 2013,24(45),455401.doi:10.1088/0957-4484/24/45/455401
(28) Salari,M.;Konstantinov,K.;Liu,H.K.J.Mater.Chem.2011, 21(13),5128.doi:10.1039/c0jm04085a
(29)Wu,H.;Li,D.;Zhu,X.;Yang,C.;Liu,D.;Chen,X.;Song,Y.; Lu,L.Electrochim.Acta 2014,116(129).doi:10.1016/j. electacta.2013.10.092
(30) Ramadoss,A.;Kim,S.J.Int.J.Hydrog.Energy 2014,39(23), 12201.doi:10.1016/j.ijhydene.2014.05.118
(31) Zhou,D.;Lin,H.;Zhang,F.;Niu,H.;Cui,L.;Wang,Q.;Qu,F. Electrochim.Acta 2015,161,427.doi:10.1016/j. electacta.2015.02.085
(32) Li,H.;Jiang,L.;Cheng,Q.;He,Y.;Pavlinek,V.;Saha,P.;Li,C. Electrochim.Acta 2015,164,252.doi:10.1016/j. electacta.2015.02.218
(33) Liao,J.Y.;Higgins,D.;Lui,G.;Chabot,V.;Xiao,X.;Chen,Z. Nano Lett.2013,13(11),5467.doi:10.1021/nl4030159
(34)Pan,D.;Huang,H.;Wang,X.;Wang,L.;Liao,H.;Li,Z.;Wu, M.J.Mater.Chem.A 2014,2(29),11454.doi:10.1039/ c4ta01613k
(35) Sainan,Y.;Cheng,K.;Huang,J.;Ye,K.;Xu,Y.;Cao,D.;Wang, X.Z.G.Electrochim.Acta 2014,120,416.doi:10.1016/j. electacta.2013.12.088
Controlled Synthesis and Supercapacitive Performance of Heterostructured MnO2/H-TiO2Nanotube Arrays
XU Juan1,3LIU Jia-Qin2,3,*LI Jing-Wei2WANG Yan3,4LÜ Jun3,4WU Yu-Cheng3,4,*
(1School of Chemistry and Chemical Engineering,Hefei University of Technology,Hefei 230009,P.R.China;2Institute of Industry&Equipment Technology,Hefei University of Technology,Hefei 230009,P.R.China;3Key Laboratory of Advanced Functional Materials and Devices,Hefei 230009,P.R.China;4School of Materials Science and Engineering,Hefei University of Technology,Hefei 230009,P.R.China)
This study used the target-controlled anodizing process for the controllable fabrication of TiO2nanotube arrays(TiO2NTAs)film substrate with large specific surface area and well-separated nanotubes.After annealing crystallization,TiO2NTAs were successively functional modified by electrochemical hydrogenation and sequential chemical bath deposition of high specific capacitance MnO2nanoparticles onto both the outer and inner surfaces of the nanotubes,thus constructing the heterostructured MnO2/H-TiO2NTAs electrode.The as-prepared samples were fully characterized by field emission scanning electron microscopy(FESEM),highresolution transmission electron microscopy(HRTEM),X-ray diffraction(XRD),X-ray photoelectron spectroscopy (XPS),Raman spectroscopy.The supercapacitive performance and stability of the resulting samples were systematically evaluated using electrochemical workstation.The results from the current study revealed that conductivity and electrochemical properties of H-TiO2NTAs were dramatically enhanced through electrochemical hydrogenation and the specific capacitance of H-TiO2NTAs could achieve 7.5 mF·cm-2at current density of 0.2 mA·cm-2,which is almost 75 times the performance of TiO2NTAs(0.1 mF·cm-2).Furthermore,the specificcapacitance of MnO2/H-TiO2NTAs-2 could achieve 481.26 F·g-1at a current density of 3 mA·mg-1as well as outstanding long-term cycling stability with only 11%reduction of initial specific capacitance at a current density of 5 mA·mg-1after 1000 cycles.
April 12,2016;Revised:June 14,2016;Published online:June 16,2016.
s.LIU Jia-Qin,Email:jqliu@hfut.edu.cn.WU Yu-Cheng,Email:ycwu@hfut.edu.cn.
TiO2nanotubearray;Hydrogenation;MnO2;Electrochemistry;Supercapacitiveperformance
O646
10.3866/PKU.WHXB201606161
The project was supported by the National Natural Science Foundation of China(51402078),Natural Science Foundation ofAnhui Province,China (1408085QE85),and Young Scholar Enhancement Foundation(Plan B)of HFUT,China(JZ2016HGTB0711).
国家自然科学基金(51402078),安徽省自然科学基金(1408085QE85),合肥工业大学学术新人提升计划B项目(JZ2016HGTB0711)资助项目©Editorial office ofActa Physico-Chimica Sinica
