基于微流控芯片的磁性没食子酸丙酯分子印迹聚合物的制备及应用
2016-11-19江丹丹宋乃忠王皓贾琼
江丹丹 宋乃忠 王皓 贾琼


摘 要 以3(甲基丙烯酸酰氧)丙基三甲氧基硅烷修饰的Fe3O4为载体,没食子酸丙酯为模板分子,采用表面印迹技术制备了核壳结构的磁性没食子酸丙酯分子印迹聚合物(Fe3O4@SiO2MIPS),并将该磁性分子印迹聚合物作为吸附剂引入到微流控芯片中,与HPLC联用,实现对痕量酚类抗氧化剂的分离富集。采用扫描电镜、磁滞回线、热重分析、红外光谱及X射线衍射对该磁性分子印迹聚合物表征。在最佳萃取条件下(样品体积3 mL,样品溶液pH=5.0,样品流速为0.5 mL/min,洗脱液流速为0.3 mL/min),该聚合物对酚类抗氧化剂具有较强的富集作用。3种酚类抗氧化剂在10~5000 ng/mL范围内呈现良好的线性关系,线性相关系数均大于0.9901,日内和日间相对标准偏差(n=5)分别低于2.8%和3.5%。将本方法用于化妆水中酚类抗氧化剂的分析检测,加标回收率在87.9%~104.0%之间,相对标准偏差(n=3)小于3.7%。
关键词 微流控芯片;分子印迹;磁性纳米粒子;酚类抗氧化剂
1 引 言
微流控芯片是20世纪90年代迅速发展起来的一种分析技术,它主要通过微米级流路对流体进行操控达到微分析的目的[1,2]。微流控芯片装置可以实现集成化和自动化、减少试剂浪费、缩短分析时间、提高检测效率,引起了普遍的关注和兴趣。将微流控芯片用于样品前处理过程,不仅能节约试剂用量,还能达到很高的萃取效率[3],为其在分离和富集领域的应用提供了广阔的前景。
磁性纳米粒子(MNPs)具有较强的吸附能力和超顺磁性,常常在表面修饰特定的官能团实现对目标分析物的富集[4~7]。分子印迹技术是以目标分子为模板,合成对特定目标分子及其结构类似物具有特异性识别和选择性吸附的聚合物。磁性分子印迹聚合物是将磁性与分子印迹技术相结合,得到同时具有分子识别特异性和磁性分离特点的材料。磁性分子印迹聚合物不仅对印迹分子具有特异性选择,而且可以通过磁场的作用与基质快速分离,因此其作为固相萃取材料已得到广泛关注[8~10]。
食物中添加抗氧化剂能够保护食物免受氧化损伤而变质。合成酚类抗氧化剂(SPAs)是常用的抗氧化剂,包括没食子酸丙酯(PG),丁基羟基茴香醚(BHA),2,6二叔丁基对甲酚(BHT)等,其应用比天然抗氧化剂更广泛。但是,过多或长期接触酚类抗氧化剂会对人体产生不利的影响。因此,发展高选择性、低成本的材料来分离、富集和检测酚类抗氧化剂具有重要意义[11,12]。
本实验以3(甲基丙烯酸酰氧)丙基三甲氧基硅烷修饰的Fe3O4作为载体,没食子酸丙酯为模板分子,甲基丙烯酸(MAA)为功能单体,乙二醇二甲基丙烯酸酯(EDMA)为交联剂,合成了磁性没食子酸丙酯分子印迹聚合物(Fe3O4@SiO2MIPS)。用该磁性分子印迹聚合物作为吸附剂,在微流控芯片内实现酚类抗氧化剂的分离富集。本方法为食品和化妆品中酚类抗氧化剂的选择性分离富集提供了一种新型样品前处理方法。
2 实验部分
2.1 仪器与试剂
Waters 2489高效液相色谱仪(Waters,USA),配置Waters 2489紫外可见检测器;PB10 pH计(北京赛多利斯科学仪器有限公司);JJ1磁力电动搅拌器(金坛市江南仪器厂);ZK82BB真空干燥箱(上海实验仪器有限公司);722N紫外可见分光光度计(上海仪电分析仪器有限公司)。
PG、BHA、BHT标准品、甲基丙烯酸、乙二醇二甲基丙烯酸酯、偶氮二异丁腈、3(甲基丙烯酸酰氧)丙基三甲氧基硅烷、硅酸四乙酯、水合肼均购于上海阿拉丁化学试剂有限公司;FeCl3·6H2O和(NH4)2Fe(SO4)2购于上海国药集团化学试剂有限公司。甲醇、乙腈(色谱纯)购于天津市彪仕奇科技发展有限公司。
准确称取酚类抗氧化剂标准品各0.0100 g,用甲醇溶解,配制成1000 μg/mL的标准储备液,于4℃密封保存。
2.2 色谱条件
选择Symmetry C18色谱柱(4.6 mm × 75 mm,3.5 μm)为分析柱,乙腈(A)1.5%乙酸水溶液(B)作流动相,检测波长280 nm,流速1.0 mL/min,柱温25℃,进样量10 μL。采用梯度洗脱:0~4 min,90%~100% A;4~5 min,100%~90% A;5~13 min,90% A。
2.3 磁性分子印迹聚合物的制备
2.3.1 Fe3O4磁性微球的制备 Fe3O4磁性微球由共沉淀法制成[13]。准确称取10 g FeCl3·6H2O和4.2 g (NH4)2Fe(SO4)2置于含有1 mL水合肼的50 mL水溶液中,再加入10 mL氨水(27% w/v),室温下搅拌0.5 h至完全溶解,然后升温至80℃再搅拌1 h。产物用磁铁分离后,用去离子水和乙醇清洗3次,70℃真空干燥 24 h。
2.3.2 Fe3O4@SiO2的制备 Fe3O4@SiO2由溶胶凝胶法合成[14]。首先将0.2 g Fe3O4分散到60 mL乙醇和10 mL水中,超声处理15 min。加入1 mL氨水与2 mL硅酸四乙酯,溶液在室温下搅拌24 h。产物用磁铁分离后,用去离子水和乙醇清洗3次,70℃ 真空干燥 24 h。
2.3.3 Fe3O4@SiO2@MPS的制备 1.0 g Fe3O4@SiO2 分散到50 mL水中,超声处理10 min,用乙酸将溶液pH调至3.0~4.0,室温下搅拌1 h。取0.2 mL的MPS分散到50 mL乙醇中,将此溶液加入到上述溶液中,80℃下搅拌5 h[15]。产物用磁铁分离后,用去离子水和乙醇清洗3次,70℃真空干燥24 h。
2.3.4 Fe3O4@SiO2MIPs分子印迹聚合物的制备 准确称取模板分子没食子酸丙酯85 mg,功能单体MAA 346.5 mg,分散在15 mL甲苯中超声处理,混合物搅拌12 h预聚合。再向该溶液中加入Fe3O4@SiO2MPS 0.3 g,交联剂EDMA 1.5858 g,引发剂AIBN 90 mg,氮气保护下60℃反应24 h[16]。产物用甲醇/乙酸体积比9∶1的溶液洗脱模板分子,直至紫外分光光度法检测不出。产物用磁铁分离后,用去离子水和乙醇清洗3次,70℃真空干燥24 h,得到没食子酸丙酯磁性分子印迹聚合物。制备非印迹聚合物(Fe3O4@SiO2NIPs)时,除不加模板分子外,其它步骤同上。
2.4 微流控芯片制作
本实验所用的微流控芯片由上下两层聚(甲基丙烯酸甲酯)(PMMA)模块组成,下层刻有直径0.5 mm、深0.5 mm的通道作为流路,上下两层通过热粘合方法组合在一起。具体操作是:刻蚀通道后的芯片依次在乙醇、去离子水中用超声波清洗。然后将上下两层芯片的微管道对准,放入烘箱中热粘合,以5℃/30 min的速度由100℃逐步升温至120℃。
2.5 萃取过程
首先将0.3 g Fe3O4@SiO2MIPS分散到10 mL乙醇溶液中,超声处理5 min,然后将其通入到微流控芯片的通道中,利用磁铁固定在通道中,形成约10 mm的填充固定相。实验过程分3步:进样,清洗,洗脱。首先,将3 mL的样品溶液以0.5 mL/min速度流经装有Fe3O4@SiO2MIPS的芯片。然后引入去离子水清洗流路。最后,以0.3 mL/min的流速引入200 μL甲醇进行洗脱。洗脱液经0.22 μm 的滤膜过滤后取10 μL通过HPLC检测。实验示意图见图1。
图1 磁性分子印迹聚合物合成示意图
Fig.1 Preparation process of Fe3O4@SiO2molecularly imprinted polymers (MIPS)
3 结果与讨论
3.1 磁性分子印迹聚合物的表征
3.1.1 扫描电镜 Fe3O4和Fe3O4@SiO2MIPs的形貌和大小通过SEM表征。由图2A可以看到,Fe3O4呈现规则的球状结构。从图2B可以看出,Fe3O4包裹印迹聚合物后有效的降低了Fe3O4微球之间的磁性偶极吸引,
图2 Fe3O4(A)和Fe3O4@SiO2MIPs(B)的SEM图
Fig.2 SEM images of Fe3O4 (A) and Fe3O4@SiO2MIPs (B)
使Fe3O4@SiO2MIPs的分散性更好。同时可以看出,Fe3O4@SiO2MIPs表面凹凸不平,说明存在大量空穴,有利于对模板分子的吸附。
3.1.2 红外光谱 由图3A(a~d)看出Fe3O4的FeO基团的弯曲振动引起的特征吸收峰出现在580 cm
Symbolm@@ 1处。从图3A(b)观察到,在Fe3O4硅烷化后,SiOSi不对称伸缩振动的特征峰出现在1080 cm
Symbolm@@ 1处,SiO弯曲振动的特征峰出现在799 cm
Symbolm@@ 1处,这说明SiO2成功地包裹到了Fe3O4磁性微球的表面上。观察图3A(c)和图3A(d),在1730 cm
Symbolm@@ 1处均出现了CO的特征吸收峰,这证实了MPS的成功修饰。图3A(d)出现的2975 cm
Symbolm@@ 1处的吸收峰归属于EDMA中CH芳香伸缩振动,1390 cm
Symbolm@@ 1处的吸收峰归属于EDMA中CH对称弯曲振动峰。以上这些特征吸收峰的出现说明成功地制备了磁性分子印迹聚合物。
3.1.3 热重分析 由图3B看出,曲线分为3段区间,0~400℃的失重是由于Fe3O4@SiO2MIPs表面乙醇分子的挥发;400℃~600℃的失重是由于包裹Fe3O4@SiO2MIPs的有机化合物的挥发;600℃以后曲线趋于平稳,说明Fe3O4表面修饰的有机化合物已经完全分解。
图3 (A)Fe3O4(a),Fe3O4@SiO2(b),Fe3O4@SiO2@MPS(c)和Fe3O4@SiO2MIPs(d)的红外吸收图谱;(B)Fe3O4@SiO2MIPs的TGA图
Fig.3 (A) FTIR spectra of Fe3O4 (a), Fe3O4@SiO2(b), Fe3O4@SiO2@MPS (c) and Fe3O4@SiO2MIPs (d); (B) TGA curve of Fe3O4@SiO2MIPs
3.2 实验参数的优化
3.2.1 试液pH值的优化 本实验研究了样品pH在2.0~10.0范围内对吸附效率的影响(图5A),结果表明,3种抗氧化剂的峰面积均在pH为5.0时达到最大值。可能的原因是:包覆在Fe3O4@SiO2MIPs外层的甲基丙烯酸表面存在COOH,当pH小于5.0时,随着pH的下降,甲基丙烯酸与抗氧化剂之间的氢键作用逐渐减小,所以吸附效率减低。而pH过高也不利于吸附,所以本实验选择的最佳pH值为5.0。
3.2.2 样品流速的优化 在0.1~0.8 mL/min范围内考察样品流速的影响,如图5B所示,在0.1~0.5 mL/min范围内,峰面积随着样品流速的增加而增大,但当样品流速大于0.5 mL/min时,峰面积逐渐减小。这说明过高的样品流速不利于吸附剂对样品的吸附,所以,本实验选择样品流速为0.5 mL/min。
3.2.3 洗脱液流速的优化 选择甲醇作为洗脱液,同时还考察了洗脱液流速对萃取效果的影响,结果如图5C所示。当洗脱液的流速为0.1~0.3 mL/min时,峰面积逐渐变大,当继续增大洗脱液的流速时,由于洗脱液与吸附剂的接触时间变短,影响洗脱效率导致峰面积减小。最终,选择0.3 mL/min作为洗脱液流速。
图5 (A)样品pH值,(B)样品流速和(C)洗脱液流速的条件优化实验
Fig.5 Effects of experimental conditions: (A) Sample pH; (B) Sample flow rate; (C) Eluent flow rate
3.3 方法评价
3.3.1 方法学考察 在上述优化的实验条件下(样品体积3 mL,样品流速0.5 mL/min,洗脱液流速0.3 mL/min, 样品pH值5.0),进一步考察了线性范围、检出限、定量限、日内、日间精密度,结果见表1,3种酚类抗氧化剂的线性相关系数(R2)均高于0.9901。慕尼黑上海分析生化展(analytica China)
展会时间:2016年10月10~12日
展会地点:上海新国际博览中心N1、N2、N3馆
展会网址:www.ac.cn
展会周期:两年一届
会展主办方: 德国慕尼黑国际博览集团 慕尼黑展览(上海)有限公司
展出时间:2016年10月10日~12日
展会描述:
慕尼黑上海分析生化展(analytica China)是分析和生化技术领域的国际性博览会,专门面向飞速发展的中国市场。凭借着analytica 的国际品牌,analytica China 吸引了来自全球主要工业国家的分析、诊断、实验室技术和生化技术领域的厂商。继2002年首次成功举办以来,analytica China 已经成为亚洲最大的分析、实验室技术和生化技术领域的专业博览会,每两年举办一次,是业内领军企业全面展示最新技术、产品和解决方案的最佳平台,这也是该展会能够吸引越来越多展商和观众的关键所在。同期举办的analytica China国际研讨会与研习班也是业内人士关注的焦点,其聚焦整个行业的发展,是科学技术和行业技术相互传递的理想平台。
第八届慕尼黑上海分析生化展(analytica China 2016)将于2016年10月10-12日在上海新国际博览中心拉开帷幕。展会将推出四大展区,包括生物技术、生命科学与诊断展区;分析与质量控制展区;实验室装备与技术展区;食品安全装备与技术主题展区。展区分布进一步细化,旨在为行业企业与用户提供一个更广泛、更深入交流与合作的良好平台。
高水平学术研讨会和研习班一直是慕尼黑上海分析生化展亮点之一!除以往倍受好评的上海国际食品安全研讨会、“组学与个性化治疗”专题研讨会、LSAC 生命科技论坛等之外,2016年还将在原有培训班的基础上,新增更多生物医药、实验室技术等系列培训班,紧扣飞速发展的中国市场,促进产、学、研各环节紧密连接, 更好的服务于展商与观众。
3.3.2 印迹聚合物与非印迹聚合物吸附性能对比 本实验对比了经过印迹聚合物(Fe3O4@SiO2MIPs)富集HPLC分析的3种抗氧化剂得到的峰面积及经过非印迹聚合物(Fe3O4@SiO2NIPs)富集HPLC分析的3种酚抗氧化剂得到的峰面积,如图6所示,可以看出经过印迹聚合物富集的抗氧化剂得到的峰面积响应值明显高于后者,同时也可以看出印迹聚合物对印迹分子没食子酸丙酯有很高的选择性。
3.4 实际样品分析
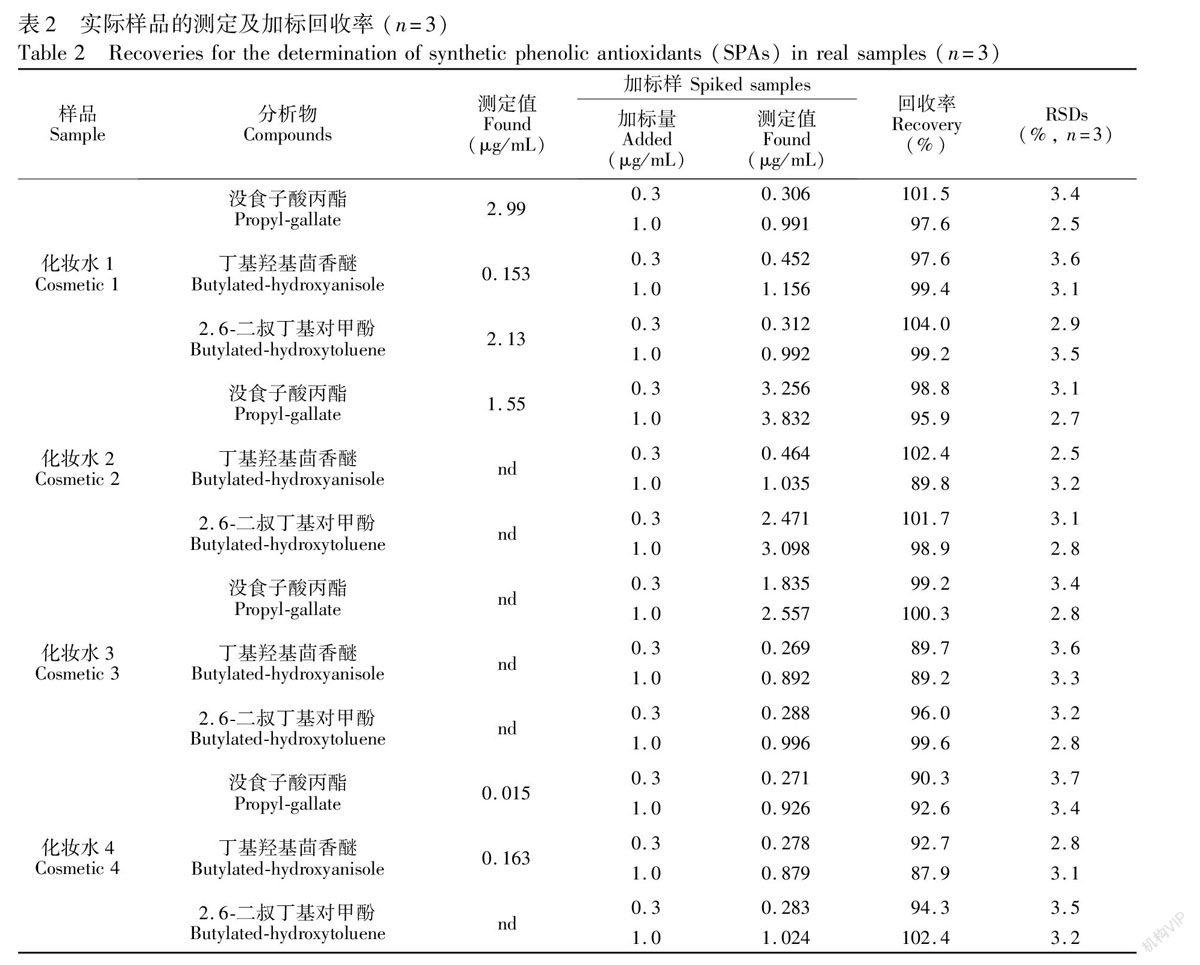
本实验检测的4种化妆水均购于当地超市,取3 mL化妆水经过0.45 μm的滤膜过滤后储存置4℃的冰箱中。这4种化妆水中均被加入不同浓度的标准溶液来进行测定,结果见图7和表2,所得的回收率在87.9%~104.0%范围内。结果表明,该方法能够适用于化妆水抗氧化剂含量的检测,有效地避免
了基质的影响。
4 结 论
本实验以没食子酸丙酯为模板分子,甲基丙烯酸(MAA)为功能单体,乙二醇二甲基丙烯酸酯(EDMA)为交联剂,成功地合成了一种新型的磁性印迹聚合物(Fe3O4@SiO2MIPs),并应用于微流控芯片中,与液相色谱联用,检测了化妆水中的酚类抗氧化剂的含量。结果表明,此吸附剂对化妆水中的酚类抗氧化剂有特异的吸附性能,3种物质检出限分别为8, 22和31 ng/mL,在10~5000 ng/mL范围内,3种物质均具有良好的线性关系(R2>0.9901)。
References
1 Waters L C, Jacobson S C, Kroutchinina N, Khandurina J, Foote R S, Ramsey J M. Anal. Chem., 1998, 70(1): 158-162
2 Zhang J L, Chen G, Tian M M, Li R G, Quan X J, Jia Q. Talanta, 2013, 115: 801-805
3 Gao D, Liu J J, Wei H B, Li H F, Guo G S, Lin J M. Anal. Chim. Acta, 2010, 665: 7-14
4 Chia H Y, Shu H C, Jue L H. J. Chromatogr. A, 2012, 1224: 70-78
5 LIAN LiLi, GUO TingXiu, WU YuQing, JIN Li, LOU DaWei, SUN DaZhi. Chinese J. Anal. Chem., 2015, 43(12): 1876-1881
连丽丽, 郭亭秀, 吴玉清, 金 丽, 娄大伟, 孙大志. 分析化学, 2015, 43(12): 1876-1881
6 CHEN Shuai, YAO JianLin, GUO QingHua, GU RenAo. Spectroscopy and Spectral Analysis, 2011, 31(12): 3169-3174
陈 帅, 姚建林, 郭清华, 顾仁敖. 光谱学与光谱分析, 2011, 31(12): 3169-3174
7 LI YaZhen, LI ZhaoQian, ZHU HuaLing, WANG WeiPing. Chinese J. Anal. Chem., 2015, 43(12): 1882-1887
李亚珍, 李兆乾, 朱华玲, 王卫平. 分析化学, 2015, 43(12): 1882-1887
8 Li X J, Zhang B L, Li W, Lei X F, Fan X L, Tian L, Zhang H P, Zhang Q Y. Biosens. Bioelectron., 2014, 51: 261-267
9 ZHU LiLi, CAO YuHua, CAO GuangQun. Chinese J. Anal. Chem., 2013, 41(11): 1724-1728
朱丽丽, 曹玉华, 曹光群. 分析化学, 2013, 41(11): 1724-1728
10 Li Y X, Bin Q, Lin Z Y, Chen Y T, Yang H H, Cai Z W, Chen G N. Chem. Commun., 2015, 51: 202-205
11 Zhou S Y, Li Z, Lv X J, Hu B, Jia Q. Analyst, 2015, 140: 5944-5952
12 Zhao P N, Hao J C. Food. Chem., 2013, 139: 1001-1007
13 Sun S, Chen L Z, Shi H J, Li Y J, He X W. J. Electroanal. Chem., 2014, 734: 18-24
14 Wan W, Han Q, Zhang X Q, Xie Y M, Sun J P, Ding M Y. Chem. Commun., 2015, 51: 3541-3544
15 Tian M M, Feng W, Ye J J, Jia Q. Anal. Methods, 2013, 5: 3984-3991
16 Wang S, Li Y, Ding M J, Wu X L, Du S H. J. Chromatogr. B, 2011, 879: 2595-2600
17 Zhang S X, Niu H Y, Zhang Y Y. J. Chromatogr. B, 2012, 1238: 38-45
