HPLC法同时测定精制冠心颗粒中5种成分的含量Δ
2016-11-19付连浩张熙洁刘晓红唐山市工人医院河北唐山063000
姜 晖,王 玉,付连浩,张熙洁,刘晓红(唐山市工人医院,河北唐山 063000)
HPLC法同时测定精制冠心颗粒中5种成分的含量Δ
姜 晖*,王 玉,付连浩,张熙洁,刘晓红#(唐山市工人医院,河北唐山 063000)
目的:建立同时测定精制冠心颗粒中丹参素、丹酚酸B、原儿茶醛、芍药苷和阿魏酸含量的方法。方法:采用高效液相色谱法。色谱柱为Zorbax Eclipse XDB-C18,流动相为乙腈-甲醇-0.5%磷酸(梯度洗脱),流速为1.0 ml/min,检测波长为280 nm(丹参素、原儿茶醛、丹酚酸B)、230 nm(芍药苷)、320 nm(阿魏酸),柱温为30℃,进样量为1.0 μl。结果:丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸检测质量浓度线性范围分别为1.19~478.34 μg/ml(r=0.999 9)、0.11~44.93 μg/ml(r=0.999 9)、7.49~995.20 μg/ml(r=0.999 7)、0.95~379.39 μg/ml(r=0.999 9)、0.01~3.12 μg/ml(r=0.999 5);定量限分别为1.91、0.36、150.00、2.74、0.10 ng,检测限分别为0.96、0.10、45.00、1.52、0.03 ng;精密度、稳定性、重复性试验的RSD<2%;加样回收率分别为98.06%~99.47%(RSD= 0.52%,n=6)、98.01%~99.49%(RSD=0.70%,n=6)、98.44%~99.45%(RSD=0.37%,n=6)、96.94%~100.71%(RSD= 1.27%,n=6)、95.44%~100.44%(RSD=1.90%,n=6)。结论:该方法操作简单、结果准确,适用于同时测定精制冠心颗粒中丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸的含量。
含量测定;高效液相色谱法;丹参素;原儿茶醛;丹酚酸B;芍药苷;阿魏酸
精制冠心颗粒收载于2015年版《中国药典》(一部)[1],由丹参、赤芍、川芎、红花、降香5味中药材组成。丹参为该方君药,辅以川芎、红花、赤芍,佐以降香,用于气滞血瘀、胸痹、心痛、舌赤瘀斑、脉弦等证;可用于治疗冠心病、心绞痛、心肌梗塞等疾病[2]。其中,丹参可用于胸肋胁痛、风湿痹痛、症瘕结块、疮疡肿痛、跌仆伤痛、月经不调、经闭痛经、产后瘀痛等证;赤芍中的芍药苷可用于治疗冠心病、增强体质与免疫功能、抗炎止咳、祛痰平喘等,尤其是针对老年慢性呼吸道疾病的治疗可作辅助药物;川芎中含有的阿魏酸具有抗血小板聚集、增强前列腺素活性、镇痛、缓解血管痉挛等作用,是生产用于治疗心脑血管疾病及白细胞减少症药品的基本原料。精制冠心颗粒作为中药复方制剂,其成分复杂,药理作用是多种药理成分共同作用的结果,然而药典标准及相关的文献仅考察了其中少数成分的含量[3-7],因此笔者采用高效液相色谱法(HPLC)同时测定丹参中的活性成分[8]丹参素、原儿茶醛、丹酚酸B,赤芍[9]中的活性成分芍药苷以及川芎中的活性成分阿魏酸[10-13],以期为精制冠心颗粒的质量控制提供参考。
1 材料
1.1 仪器
1200型HPLC仪,包括G1311A型四元泵、G1322A型脱气机、G1316A型柱温箱、G1329A型自动进样器、G1315D型二极管阵列检测器(美国Agilent公司);ELITE-TEST型真空抽滤泵(大连依利特分析仪器有限公司);CP225D型分析天平(德国Sartorius公司);80-2型离心沉淀机(上海手术器械厂);FS-150型超声波提取器(上海生析超声仪器有限公司,功率:300 W,频率:20 kHz)。
1.2 药品与试剂
精制冠心颗粒(陕西汉唐制药有限公司,批号:131001、120801、120501,规格:13 g/袋;吉林益民堂制药有限公司,批号:20130502,规格:13 g/袋;广州白云山奇星药业有限公司,批号:121124,规格:13 g/袋);丹参素钠对照品(批号:110855-200507,纯度:98%)、原儿茶醛对照品(批号:110810-200205,纯度>98%)、丹酚酸B对照品(批号:111562-201212,纯度≥98%)、芍药苷对照品(批号:110736-200423,纯度>98%)和阿魏酸对照品(批号:0773-9910,纯度>98%)均购自中国食品药品检定研究院;丹参免煎颗粒(批号:1306761)、川芎免煎颗粒(批号:1305807)、红花免煎颗粒(批号:1305725)、降香免煎颗粒(批号:1208734)、赤芍免煎颗粒(批号:6053132)均购自广东一方制药有限公司;乙腈、甲醇为色谱纯,磷酸、冰乙酸、甲酸、无水乙醇和乙醚均为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:Zorbax Eclipse XDB-C18(150 mm×4.6 mm,5 μm);流动相为乙腈(A)-甲醇(B)-0.5%磷酸(C),梯度洗脱(洗脱程序见表1);流速:1.0 ml/min;检测波长:280 nm(丹参素、原儿茶醛、丹酚酸B)、230 nm(芍药苷)、320 nm(阿魏酸);柱温:30℃;进样量10 μl。

表1 梯度洗脱程序Tab 1 Conditions of gradient elution
2.2 溶液的制备
2.2.1 混合对照品溶液 精密称取丹参素钠对照品13.250 mg(相当于丹参素11.958 mg),置于5 ml量瓶中;原儿茶醛对照品5.616 mg,置于25 ml量瓶中;丹酚酸B对照品14.976 mg,置于1 ml量瓶中;芍药苷对照品18.970 mg,置于10 ml量瓶中;阿魏酸对照品0.780 mg,置于50 ml量瓶中,分别加甲醇溶解并定容,制成丹参素、原儿茶醛、丹酚酸B、芍药苷、阿魏酸的质量浓度分别为2 650.00、224.64、14 976.00、1 897.00、15.60 μg/ml的单一对照品贮备液。分别精密吸取上述单一对照品贮备液各1 ml,置于5 ml量瓶中,摇匀,即得丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸的质量浓度分别为478.34、44.93、2 995.20、379.40、3.12 μg/ml的混合对照品贮备液;再精密吸取上述混合对照品贮备液1 ml,置于5 ml量瓶中,加3 ml甲醇稀释,即得丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸的质量浓度分别为119.58、11.23、748.80、94.85、0.80 μg/ml的混合对照品溶液。2.2.2 供试品溶液 取样品0.7 g,精密称定,置于10 ml量瓶中,加9 ml水溶解,超声处理30 min,冷却至室温后加水定容,以半径5 cm、1 500 r/min离心30 min,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性对照溶液 用免煎颗粒代替丹参、川芎、红花、降香、赤芍药材,按样品的制备工艺和配方比例制备阴性对照品,再按“2.2.2”项下方法制备阴性对照溶液,即得。
2.3 系统适用性试验
精密量取“2.2”项下混合对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,各成分均能达到基线分离,分离度>1.5;各成分的理论板数以芍药苷峰计>4 000,保留时间为18.5 min。结果表明,其他成分对测定无干扰。

图1 高效液相色谱图A.混合对照品;B.供试品;C.缺丹参的阴性对照;D.缺赤芍的阴性对照;E.缺川芎的阴性对照;1.丹参素;2.原儿茶醛;3.芍药苷;4.阿魏酸;5.丹酚酸BA.mixed reference substances;B.test sample;C.negative control without Salvia miltiorrhiza;D.negative control without Radix panoniae;E. negative controlwithoutLigusticum chuanxiong;1.danshensu;2. protocatechuic aldehyde;3.peoniflorin;4.ferulic acid;5.salvianolic acid B
2.4 线性关系考察
分别精密吸取“2.2.1”项下混合对照品贮备液2.5、5.0、7.5、10.0、12.5、15.0 μl,用甲醇倍比稀释,制成系列线性溶液。精密量取上述系列线性溶液各10 μl,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,μg/ml)为横坐标、峰面积(y)为纵坐标进行线性回归,得回归方程与线性范围见表2。

表2 回归方程与线性范围Tab 2 Regression equations and linear ranges
2.5 定量限与检测限考察
取“2.2.1”项下混合对照品溶液适量,等倍逐步稀释,按“2.1”项下色谱条件进样测定,当信噪比为10∶1时,得定量限(LOQ);当信噪比为3∶1时,得检测限(LOD),结果见表3。

表3 定量限与检测限测定结果Tab 3 Determination results of detection limit and quantitation limit
2.6 精密度试验
精密吸取“2.2.1”项下混合对照品溶液10 μl,按“2.1”项下色谱条件进样测定,记录峰面积。结果,丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸峰面积的RSD分别为1.40%、1.86%、1.71%、0.91%、1.94%(n=6),表明仪器精密度良好。
2.7 稳定性试验
精密吸取“2.2.2”项下供试品溶液(批号:131001)10 μl,分别于室温下放置0、2、4、6、8、12、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸峰面积的RSD分别为1.17%、1.09%、0.83%、0.86%、1.53%(n=7),表明供试品溶液在室温下24 h内稳定性良好。
2.8 重复性试验
取同一批(批号:131001)样品适量,精密称定,按“2.2.2”项下方法平行制备6份供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积。结果丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸峰面积的RSD分别为1.66%、1.72%、1.31%、1.94%、1.96%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
取样品(批号:131001)适量,共6份,每份约0.35 g,精密称定,分别加入低、中、高质量的丹参素、丹酚酸B、原儿茶醛、芍药苷、阿魏酸对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表4。

表4 加样回收率试验结果(n=6)Tab 4 Results of recovery tests(n=6)
2.10 样品含量测定
分别取5批样品各适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算样品中丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸的含量,结果见表5。
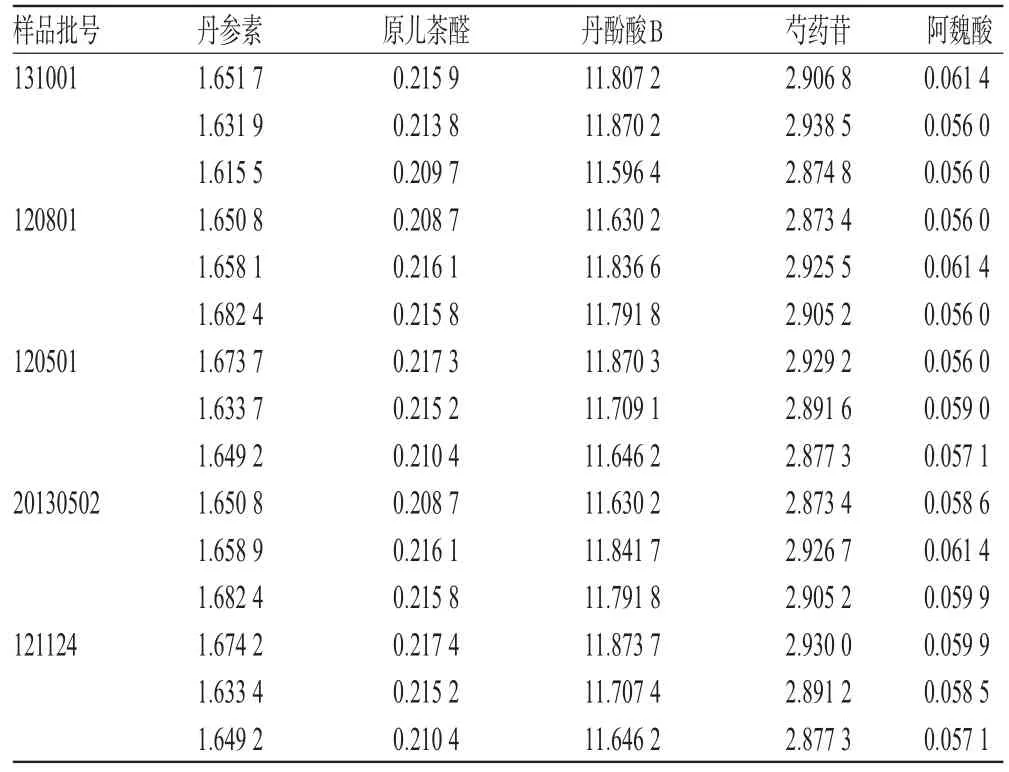
表5 样品含量测定结果(n=3,mg/g)Tab 5 Results of contents determination of samples(n=3,mg/g)
3 讨论
3.1 提取方式的选择
本试验对样品进行前处理时比较了索氏提取和超声提取两种方法,在相同的提取时间下索氏提取的提取率与超声提取无明显的区别,但索氏提取不如超声提取简单、方便、安全,因此本试验选用超声提取对样品进行前处理。
本试验还考察了超声提取时间(10、20、30、40、50、60 min)。结果,丹参素、原儿茶醛、芍药苷、阿魏酸在30 min时提取率相对较大;而丹酚酸B在40 min时的提取率相对较大,故本试验综合考虑5种成分的提取率,超声时间选择30 min。
3.2 阴性对照品的制备
本试验用免煎颗粒按照2015年版《中国药典》(一部)中精制冠心颗粒的制备工艺和配方比例来制作阴性对照品,用免煎颗粒制作的阴性对照品的HPLC图谱与生产工艺的阴性对照图谱相比,虽有所差异,但对本试验中要测的5种成分影响不大,鉴于有些阴性对照品不容易找到,而且按照该药的处方工艺制备阴性对照品程序比较烦琐、所用设备不齐全等,且用免煎颗粒制作阴性对照品方法简单也不影响试验结果,故本试验用免煎颗粒制作阴性对照品。
综上所述,本方法操作简单、结果准确,适用于同时测定精制冠心颗粒中丹参素、原儿茶醛、丹酚酸B、芍药苷和阿魏酸的含量。
[1]国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:1 700.
[2]Zhang H,Yu C,Jia JY,et al.Contents of four active components in differern commercia crude drugs and preparations of Danshen Salvia miltiorrhiza[J].Acta Pharmacol Sin,2002,23(12):110.
[3]Yuan JC,Yin YQ,Shen ZB,et al.Simultaneous determination of danshensu,protocatechuic aldehyde,caffeic acid,rosmarinci acid,salvianolic acid B,and salvianolic acid A in Xiandan Injection by HPLC[J].Chin Tradit HerbalDrugs,2009(40):128.
[4]阎便杰,李彤晖,刘珍.HPLC法测定精制冠心颗粒中原儿茶醛的含量[J].陕西中医,2005,26(4):376.
[5]黄海欣.HPLC法测定精制冠心颗粒中丹酚酸B的含量[J].中国药师,2009,12(11):1 665.
[6]王俊杰,刘弘,于天杰,等.HPLC法同时测定精制冠心颗粒中芍药苷与丹酚酸B含量[J].中国药师,2013,16(8):1 175.
[7]王新立,张越华.HPLC法测定精制冠心颗粒中芍药苷的含量[J].陕西中医,2007,28(5):601.
[8]姜晖,张丽英,王绍志,等.HPLC法测定消渴平片中5种成分[J].中草药,2015,46(4):530.
[9]姜晖,王绍志,张熙洁,等.HPLC法同时测定利脑心胶囊中6种成分的含量[J].中国药房,2015,26(3):374.
[10]付连浩,张熙洁,王绍志,等.多波长RP-HPLC法同时测定参芍口服液中5种成分的含量[J].中国药房,2015,26(24):3 423.
[11]冀兰鑫,黄浩,姜民,等.HPLC测定血必净注射液内11种主要成分[J].中国中药杂志,2010,35(18):2 395.
[12]马彬峡,陈恒冲,吴春高,等.RP-HPLC法同时测定乐脉颗粒中丹参素、原儿茶醛、芍药苷和阿魏酸的含量[J].药物分析杂志,2009,29(7):1 122.
[13]陈斌,叶隽,纪峰,等.高效液相色谱法同时测定脑血栓片中丹参素、原儿茶醛、芍药苷、阿魏酸和丹酚酸B的含量[J].药物分析杂志,2007,27(12):1 891.
Simultaneous Determination of Five Components in Jingzhi Guanxin Granule by HPLC
JIANG Hui,WANG Yu,FU Lianhao,ZHANG Xijie,LIU Xiaohong(Tangshan Worker’s Hospital,Hebei Tangshan 063000,China)
OBJECTIVE:To establish a method for simultaneous determination of danshensu,salvianolic acid B,protocatechuic aldehyde,paeoniflorin and ferulic acid in Jingzhi guanxin granule.METHODS:HPLC was performed on the column of Zorbax Eclipse XDB-C18with mobile phase of acetonitrile-methanol-0.5%H3PO4(gradient elution)at a flow rate of 1.0 ml/min,the detection wavelength was 280 nm(for danshensu,protocatechuic aldehyde,salvianolic acid B),230 nm(for ferulic acid)and 320 nm(for paeoniflorin),column temperature was 30℃,injection volume was 10 μl.RESULTS:The linear range was 1.19-478.34 μg/ml for danshensu(r=0.999 9),0.11-44.93 μg/ml for protocatechuic aldehyde(r=0.999 9),7.49-995.20 μg/ml for salvianolic acid B(r=0.999 7),0.95-379.39 μg/ml for paeoniflorin(r=0.999 9)and 0.01-3.12 μg/ml for ferulic acid(r=0.999 5);the limits of quantitation were 1.91 ng,0.36 ng,150.00 ng,2.74 ng and 0.10 ng,limit of detection were 0.96 ng,0.10 ng,45.00 ng,1.52 ng and 0.03 ng;RSDs of precision,stability and reproducibility tests were lower than 2%;recoveries were 98.06%-99.47%(RSD= 0.52%,n=6),98.01%-99.49%(RSD=0.70%,n=6),98.44%-99.45%(RSD=0.37%,n=6),96.94%-100.71%(RSD= 1.27%,n=6)and 95.44%-100.44%(RSD=1.90%,n=6).CONCLUSIONS:The method is simple and accurate,and suitable for the simultaneous determination of danshensu,salvianolic acid B,protocatechuic aldehyde,paeoniflorin and ferulic acid in Jingzhi guanxin granule.
Content determination;HPLC;Danshensu;Protocatechuic aldehyde;Salvianolic acid B;Paeoniflorin;Ferulic acid
R917
A
1001-0408(2016)30-4261-04
2015-10-30
2016-07-19)
(编辑:刘 柳)
河北省自然科学基金资助项目(No.C2011105042)
*副主任药师,硕士研究生。研究方向:药理学、临床药学、药物分析学。电话:0315-3722840。E-mail:jianghui910@163.com
#通信作者:主任药师,博士研究生。研究方向:药理学、临床药学、药物分析学。电话:0315-3722435。E-mail:13930520000@163. com
DOI 10.6039/j.issn.1001-0408.2016.30.27
