HPLC法同时测定参菊洗剂中4种成分的含量Δ
2016-11-19张广求黄冈市中心医院药剂科湖北黄冈438000
谭 璐,张广求,刘 文(黄冈市中心医院药剂科,湖北黄冈 438000)
HPLC法同时测定参菊洗剂中4种成分的含量Δ
谭 璐*,张广求#,刘 文(黄冈市中心医院药剂科,湖北黄冈 438000)
目的:建立同时测定参菊洗剂中苦参碱、蒙花苷、盐酸小檗碱和蛇床子素含量的方法。方法:采用高效液相色谱法。色谱柱为Dionex C18,流动相为乙腈-0.1%三乙胺水溶液(用磷酸调节pH至7.2)(梯度洗脱),流速为1.0 ml/min,检测波长为210 nm,柱温为30℃,进样量为20 μl。结果:苦参碱、蒙花苷、盐酸小檗碱和蛇床子素检测进样量线性范围分别为1.400~8.400 μg(r=0.999 4)、0.152~0.912 μg(r=0.999 6)、0.248~1.488 μg(r=0.999 9)、0.128~0.768 μg(r=0.999 4);定量限分别为84.85、3.15、15.03、7.76 ng,检测限分别为24.13、0.89、4.27、2.20 ng;精密度、稳定性、重复性试验的RSD<2%;加样回收率分别为96.29%~99.06%(RSD=1.10%,n=9)、96.49%~98.27%(RSD=0.69%,n=9)、99.26%~101.13%(RSD=0.62%,n=9)、96.27%~98.64%(RSD=0.89%,n=9)。结论:该方法操作简便、结果准确、重复性好,可用于同时测定参菊洗剂中苦参碱、蒙花苷、盐酸小檗碱和蛇床子素的含量。
参菊洗剂;苦参碱;蒙花苷;盐酸小檗碱;蛇床子素;高效液相色谱法;含量测定
参菊洗剂是黄冈市中心医院自主研制并在临床应用多年的中药制剂(批准文号:鄂药制字Z20110230),由苦参、野菊花、黄柏、蛇床子等12味中药材组成,具有消炎、止痒、除秽、杀菌等功效,可用于细菌性、真菌性、滴虫性阴道炎及多种皮肤瘙痒症,疗效较好[1]。方中苦参为君药,野菊花、黄柏、蛇床子为主要药材。苦参具有抗滴虫作用,对痢疾杆菌、大肠杆菌及金黄色葡萄球菌均有明显的抑制作用;野菊花对金黄色葡萄球菌、痢疾杆菌、大肠埃希菌及多种致病性杆菌、皮肤真菌均有一定抗菌作用;黄柏有杀灭阴道滴虫作用,对金黄色葡萄球菌、白色葡萄球菌、枯草芽孢杆菌、大肠埃希菌、铜绿假单胞菌和多种致病性皮肤真菌均有抑制作用;蛇床子有抗滴虫作用,对絮状表皮癣菌、石膏样小芽胞菌、羊毛状小芽胞菌有抑制作用[2]。参菊洗剂收录于2011年版《湖北省医疗机构制剂规范》中,该制剂规范只采用薄层色谱法对苦参、野菊花、黄柏、蛇床子进行定性鉴别,而没有对其进行含量测定。因此,本研究采用高效液相色谱法(HPLC)建立了同时测定参菊洗剂中苦参、野菊花、黄柏、蛇床子中的有效成分苦参碱、蒙花苷、盐酸小檗碱和蛇床子素含量的方法,以期为更好地控制该制剂的质量提供参考。
1 材料
1.1 仪器
Ultimate 3000型HPLC仪,包括Ultimate 3000泵、Ultimate 3000紫外检测器、UltiMate 3000 WPS自动进样器、Chromeleon高效液相数据处理系统(美国Dionex公司);FA1604型万分之一电子天平(上海越平科学仪器有限公司);pHs-3C型pH计(杭州奥立龙仪器有限公司)。
1.2 药品与试剂
参菊洗剂(黄冈市中心医院自制,批号:141105、141201、150209,规格:500 ml/瓶);苦参碱对照品(批号:110805-200508,纯度:99.80%)、蒙花苷对照品(批号:111528-201308,纯度:99.50%)、盐酸小檗碱对照品(批号:110713-201212,纯度:99.00%)、蛇床子素对照品(批号:110822-201308,纯度:99.00%)均购自中国食品药品检定研究院;甲醇、乙腈为色谱纯,乙酸乙酯、三乙胺、磷酸、氨水均为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件
色谱柱:Dionex C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%三乙胺水溶液(用磷酸调节pH至7.2)(B),梯度洗脱(洗脱程序见表1);流速:1.0 ml/min;检测波长:210 nm;柱温:30℃;进样量:20 μl。
2.2 溶液的制备
2.2.1 混合对照品溶液 分别精密称取苦参碱对照品0.017 5 g、蒙花苷对照品0.001 9 g、盐酸小檗碱对照品0.003 1 g、蛇床子素对照品0.001 6 g,置于同一25 ml量瓶中,加甲醇溶解并定容,摇匀,制成质量浓度分别为700、76、124、64 μg/ml的混合对照品溶液。

表1 梯度洗脱程序Tab 1 Conditions of gradient elution
2.2.2 供试品溶液 精密量取样品5 ml,置于分液漏斗中,用氨水调节pH至9.3,加乙酸乙酯置于分液漏斗中,振摇提取3次,每次20 ml,合并乙酸乙酯提取液,挥干,残渣加甲醇溶解并定容至10 ml量瓶中,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按样品的处方比例和制备工艺,分别制备不含苦参、野菊花、黄柏和蛇床子的阴性样品,然后按“2.2.2”项下方法制备阴性对照溶液。
2.3 系统适用性试验
取“2.2”项下混合对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,各成分均能达到基线分离,分离度>1.5;理论板数以苦参碱峰计>2 000,保留时间为20 min。结果表明,其他成分对测定无干扰。
2.4 线性关系考察
分别精密量取“2.2.1”项下混合对照品溶液1、2、3、4、5、6 ml,分别置于10 ml量瓶中,加甲醇定容,制成系列线性溶液。取上述溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分进样量(x,μg)为横坐标、峰面积(y)为纵坐标进行线性回归,得苦参碱、蒙花苷、盐酸小檗碱和蛇床子素的回归方程与线性范围,见表2。
2.5 定量限与检测限考察
取“2.2.1”项下混合对照品溶液适量,等倍逐步稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10∶1时,得定量限(LOQ);当信噪比为3∶1时,得检测限(LOD),结果见表3。
2.6 精密度试验
取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。结果,苦参碱、蒙花苷、盐酸小檗碱和蛇床子素峰面积的RSD分别为0.41%、0.37%、0.58%、0.66%(n=6),表明仪器精密度良好。
2.7 稳定性试验
取“2.2.2”项下供试品溶液适量,分别于室温下放置0、2、4、6、8、10、12 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,苦参碱、蒙花苷、盐酸小檗碱和蛇床子素峰面积的RSD分别为0.89%、0.77%、1.15%、1.23%(n=7),表明供试品溶液在室温下12 h内稳定性良好。

图1 高效液相色谱图A.混合对照品;B.供试品;C.缺苦参的阴性对照;D.缺野菊花的阴性对照;E.缺黄柏的阴性对照;F.缺蛇床子的阴性对照;1.苦参碱;2.蒙花苷;3.盐酸小檗碱;4.蛇床子素Fig 1 HPLC chromatogramsA.mixed reference substance;B.test sample;C.negative control without Sophora flavescens;D.negative control without Chrysanthemum indicm;E.negative control without Phellodendron chinese;F.negative control without Cnidium monnieri;1.matrine;2.linarin;3.berberine hydrochloride;4.osthole

表2 回归方程与线性范围Tab 2 Regression equations and linear ranges

表3 定量限与检测限测定结果Tab 3 Determination results of quantitation limit and detection limit
2.8 重复性试验
取同一批样品(批号:150209)适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积。结果,苦参碱、蒙花苷、盐酸小檗碱和蛇床子素的平均含量分别为297.76、10.88、47.33、11.06 μg/ml;RSD分别为0.69%、0.85%、1.00%、0.91%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
精密量取已知含量的样品(批号:141105)适量,共9份,分别加入低、中、高质量的苦参碱、蒙花苷、盐酸小檗碱和蛇床子素对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表4。
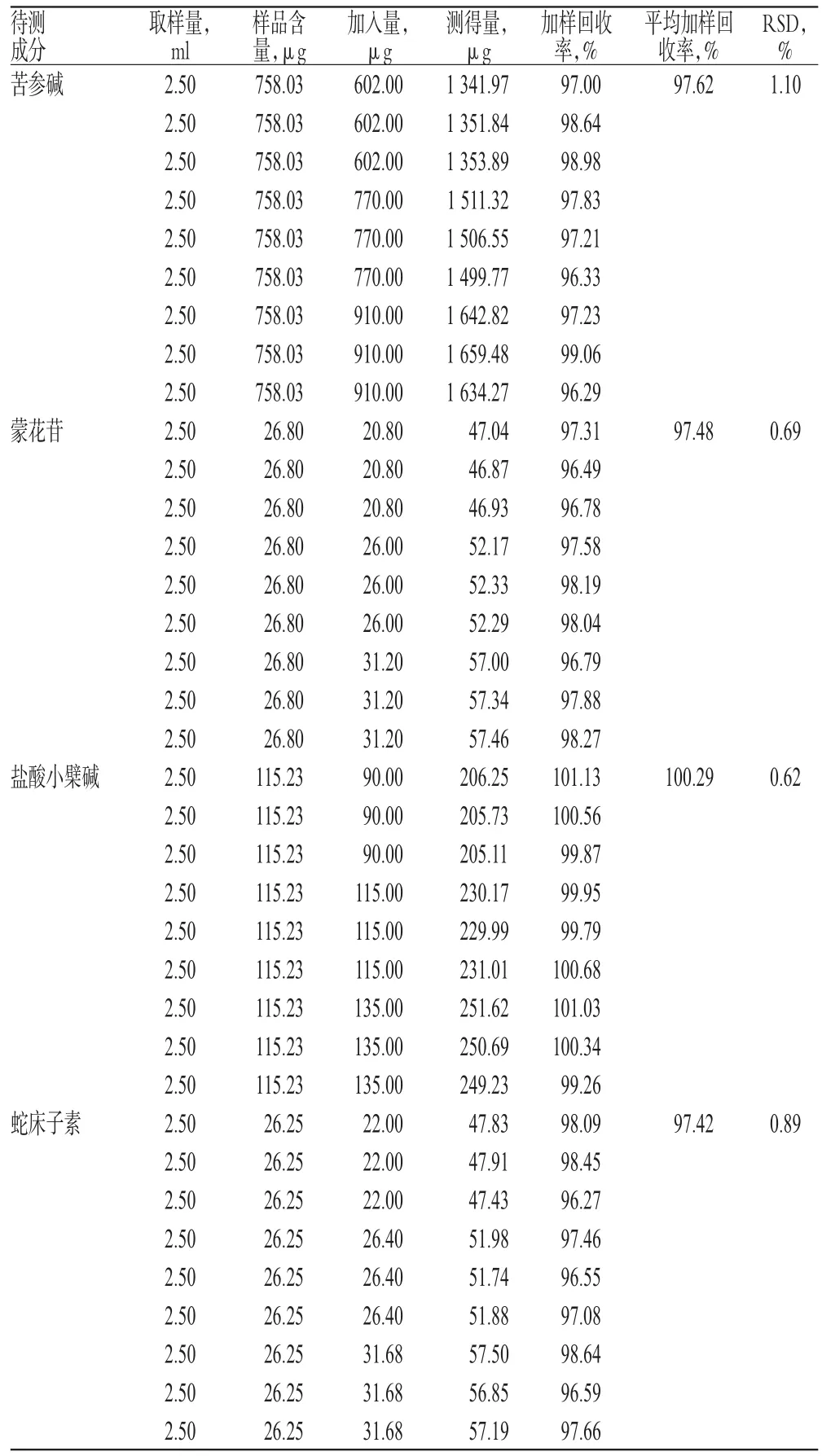
表4 加样回收率试验结果(n=9)Tab 4 Results of recovery tests(n=9)
2.10 样品含量测定
取3批样品各适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算苦参碱、蒙花苷、盐酸小檗碱和蛇床子素的含量,结果见表5。

表5 样品含量测定结果(n=3,μg/g)Tab 5 Results of contents determination of samples(n=3,μg/g)
3 讨论
3.1 测定波长的选择
苦参碱的检测波长主要为210[3]、220[4-5]、230 nm[6]等,蒙花苷的检测波长为268、334 nm[7],盐酸小檗碱的检测波长为228、264、346 nm[8],蛇床子素的检测波长为206[9]、322 nm[10]。笔者尝试在不同检测波长处测定参菊洗剂中4种待测成分,结果在210 nm波长处,4种成分均有较好的响应值,且其他杂质干扰较小,故本试验选择210 nm为检测波长。
3.2 提取溶剂的考察
预试验时,笔者考察了甲醇、乙醚、乙酸乙酯作为提取溶剂。结果,相同提取条件下,乙酸乙酯提取率最高,故本试验选择乙酸乙酯作为提取溶剂。为确定最佳提取溶剂体积和提取次数,笔者选用乙酸乙酯30、20、15 ml/次分别振摇提取3次或者4次,以峰面积比较提取效果。结果,乙酸乙酯20 ml/次振摇提取3次即可有效提取出样品中4种待测成分,故本试验选择乙酸乙酯的提取体积为20 ml/次,提取次数为3次。
3.3 流动相的选择
笔者参考相关文献[11-15],考察了乙腈-不同浓度磷酸溶液、乙腈-0.05 mol/L磷酸二氢钾水溶液和乙腈-0.1%三乙胺水溶液(磷酸调节不同pH)等不同流动相进行等度和梯度洗脱。结果,以乙腈-0.1%三乙胺水溶液(磷酸调节pH至7.2)梯度洗脱效果最佳,各色谱峰峰形、分离度均较好且基线较平稳。因此,本试验选择乙腈-0.1%三乙胺水溶液(磷酸调节pH至7.2)为流动相,洗脱方式为梯度洗脱。
综上所述,本方法简便、准确,重复性好,可用于同时测定参菊洗剂中苦参碱、蒙花苷、盐酸小檗碱和蛇床子素的含量。
[1]刘文,谭璐,张广求,等.参菊洗剂治疗阴道炎的疗效观察[J].临床合理用药杂志,2015,8(9):21.
[2]张广求,刘文,谭璐,等.参菊洗剂体外抑菌作用[J].医药导报,2015,34(8):1 032.
[3]李翔,刘皈阳,马建丽,等.HPLC法测定扁咽口服液中苦参碱的含量[J].解放军药学学报,2014,30(6):532.
[4]国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:202-203.
[5]侯杰荣,柯发敏,侯思奎.HPLC法同时测定苦参中3种生物碱的含量[J].中药材,2014,37(2):273.
[6]王慧,毛春芹,周渊,等.HPLC法同时测定舒乐洗剂中苦参碱和小檗碱[J].中国实验方剂学杂志,2014,20(12):88.
[7]王伯涛,王峰,张同波,等.反相高效液相色谱法测定野菊花中蒙花苷的含量[J].时珍国医国药,2009,20(1):166.
[8]徐璐扬,李中东,刘庆丰,等.HPLC测定三黄汤中4种成分含量[J].中国现代应用药学,2011,28(12):1 135.
[9]杨娟,黄敬群.除湿止汗散的制备及质量控制[J].中国医院药学杂志,2011,31(2):154.
[10]黄良永,郑江萍,甘春英.独活药材及其配方颗粒中蛇床子素的含量比较[J].医药导报,2010,29(1):90.
[11]胡军林,谭静玲,费毅琴,等.高效液相色谱法同时测定一清颗粒中3种原小檗碱型生物碱的含量[J].中国医院药学杂志,2014,34(1):50.
[12]唐春丽,陆石英,覃文慧,等.多波长HPLC法同时测定清胃黄连片中4种成分的含量[J].中药材,2014,37(6):1 062.
[13] 孙艳涛.HPLC法同时测定安脑丸中栀子苷、盐酸小檗碱和黄芩苷的含量[J].中国药房,2016,27(3):389.
[14]韩永成,龚海燕,刘伟,等.UPLC同时测定野菊花中蒙花苷和绿原酸含量[J].中国实验方剂学杂志,2013,19(20):88.
[15]李义敏,张巧艳,秦路平,等.HPLC法测定蛇床子中3种香豆素类成分的含量[J].中药材,2015,38(7):1 441.
Simultaneous Determination of Four Components in Shenju Lotion by HPLC
TAN Lu,ZHANG Guangqiu,LIU Wen(Dept.of Pharmacy,Huanggang Central Hospital,Hubei Huanggang 438000,China)
OBJECTIVE:To establish a method for simultaneous determination of matrine,linarin,berberine hydrochloride and osthole in Shenju lotion.METHODS:HPLC was performed on the column of Dionex C18with mobile phase of acetonitrle-0.1%triethylamine(pH was adjusted to 7.2 with phosphoric)(gradient elution)at a flow rate of 1.0 ml/min,detection wavelength was 210 nm,column temperature was 30℃,and injection volume was 20 μl.RESULTS:The linear range was 1.400-8.400 μg for matrine(r=0.999 4),0.152-0.912 μg for linarin(r=0.999 6),0.248-1.488 μg for berberine hydrochloride(r=0.999 9)and 0.128-0.768 μg for osthole(r=0.999 4);limit of quantitation was 84.85,3.15,15.03,7.76 ng,limit of detection was 24.13,0.89,4.27,2.20 ng;RSDs of precision,stability and reproducibility tests were lower than 2%;recoveries were 96.29%-99.06%(RSD=1.10%,n=9),96.49%-98.27%(RSD=0.69%,n=9),99.26%-101.13%(RSD=0.62%,n=9)and 96.27%-98.64%(RSD=0.89%,n=9).CONCLUSIONS:The method is simple,accurate and reproducible,and can be used for the simultaneous determination of matrine,linarin,berberine hydrochloride and osthole in Shenju lotion.
Shenju lotion;Matrine;Linarin;Berberine hydrochloride;Osthole;HPLC;Content determination
R282.71;R927.2
A
1001-0408(2016)30-4257-04
2015-11-27
2016-08-13)
(编辑:刘 柳)
黄冈市科技计划项目(No.黄科〔字2013〕76号)
*主管药师,硕士。研究方向:医院药学、药物分析。电话:0713-8625312。E-mail:tanlu05@126.com
#通信作者:副主任药师。研究方向:医院药学、药物分析。E-mail:ccnpa@163.com
DOI 10.6039/j.issn.1001-0408.2016.30.26
