“一锅法”水热制备CuS/C复合材料及其在超级电容器中的应用
2016-11-18赵双生应宗荣杨佳佳凡川
赵双生,应宗荣,杨佳佳,凡川
“一锅法”水热制备CuS/C复合材料及其在超级电容器中的应用
赵双生,应宗荣,杨佳佳,凡川
(南京理工大学化工学院,江苏南京210094)
采用三水合硝酸铜为铜源、硫脲为硫源、D-葡萄糖酸钠为络合剂,发展了简单的“一锅法”水热直接一步合成CuS/C复合材料。采用X射线衍射仪(XRD)、激光显微拉曼光谱仪(Raman)、扫描电子显微镜(SEM)和有机元素分析仪对复合材料组成、结构及形貌进行表征。研究发现,样品主要由花状CuS球组成,同时含有质量分数约为6%的光滑炭球,CuS球表面分布有花瓣状褶皱,形成的大量孔道有利于离子传输,并增大活性物质与电解液的接触面积。研究表明,在1 A·g-1电流密度下,比电容高达719 F·g-1,与不加络合剂制备得到的CuS(382 F·g-1)相比,比电容显著提高,并且在充放电1000次后比电容保持在80%左右,显示出良好的循环稳 定性。
“一锅法”;水热;硫化铜;碳;复合材料;电化学;超级电容器
引 言
近年来,锂离子电池和超级电容器等新型储电装置受到人们的广泛关注[1]。超级电容器具有能量密度高、功率密度高、使用时间长和充放电时间短等特点,引起研究者们的极大兴趣[2]。超级电容器按储能机理可分为双电层电容器和法拉第赝电容器。电极材料是超级电容器的核心[3]。双电层电容主要来源于碳基材料,如碳纤维、碳纳米管、石墨烯、活性炭等,循环稳定性好但比电容相对较低。法拉第赝电容材料有导电聚合物和过渡金属的氧化物、氢氧化物、硫化物等,比电容高但循环稳定性较差[4]。因此,通过碳基材料与赝电容材料复合以改善综合电化学性能,目前已成为电极材料研究的重要趋势。
过渡金属通常具有多种价态,是其作为赝电容电极材料的理论前提[5],如MnO2[6]、CoOOH[7]、Ni3S2[8]、CuS[9]等。其中,过渡金属硫化物[10]制备成本低、导电性好、物理化学性质优异,有较高的理论比电容,近来受到普遍关注。特别是,硫化铜作为硫族过渡金属化合物,其3d电子使其具有较宽的禁带(1.2~2.4 eV),能形成一系列非化学计量的化合物,如CuS、Cu1.39S、Cu1.6S、Cu7S4、Cu9S5、Cu2S等[5],因此成为近年的研究热点之一。Wang等[5]以乙二胺作为双齿配体采用水热法制备出了无规片状、六角片状、海星状和雪花状的硫化铜,表现出较好的电化学性能。Huang等[11]水热时加入表面活性剂制备出了不同厚度片状堆积的硫化铜,比电容最高达378.9 F·g-1。Peng等[12]利用乙二醇作溶剂时制备得到表面布满片状分支的球状硫化铜,比电容为475 F·g-1,而利用丙三醇作溶剂时制备的花状硫化铜,比电容达597 F·g-1。
CuS和碳材料复合近年来已有部分报道,如Huang等将CuS负载在多壁碳纳米管上[13],他们还将乙炔黑插入到硫化铜片层之间制备得到了CuS/乙炔黑复合材料[14]。但是,目前CuS和碳材料复合都是采用与现有碳材料进行复合,直接通过“一锅法”一步制备CuS/C复合材料还未见有报道。本文采用三水合硝酸铜为铜源、硫脲为硫源、D-葡萄糖酸钠为络合剂,通过水热法合成CuS,却意外发现,不仅制备得到新颖结构的球花状CuS,还同时生成了一定量的炭球,即“一锅”直接合成得到了CuS/C复合材料。所制备的CuS/C复合材料在1 A·g-1电流密度下比电容高达719 F·g-1,远高于不加络合剂制备的CuS的比电容(382 F·g-1)和大部分现有资料报道的CuS的比电容数值,显示出“一锅法”合成CuS/C复合材料具有明显的优越性。尽管由于CuS熔点低(220℃)且熔点附近会发生分解,制得的CuS/C复合材料不能高温热处理将无定形炭转化成结晶性炭来进一步改善电化学性能,但是本文“一锅法”的思想,将打开一步法直接合成过渡金属化合物/碳复合材料的新思路,特别是为能进行高温碳化处理的高熔点过渡金属化合物/碳复合材料提供了新的技术途径。
1 实验部分
1.1 试剂
所有化学试剂,包括三水合硝酸铜、硫脲、D-葡萄糖酸钠、氢氧化钾等,均为分析纯。
1.2 样品材料的制备
称取0.242 g三水合硝酸铜溶于60 ml去离子水中,再加入0.218 g D-葡萄糖酸钠(D-葡萄糖酸钠与三水合硝酸铜的摩尔比为1:1),搅拌至溶液均匀,后加入0.153 g硫脲,继续搅拌形成均一溶液。转移至100 ml高压反应釜中在150℃反应24 h,然后自然冷却至室温,离心分离出黑色沉淀物,水洗,醇洗,在60℃真空干燥12 h,即得到CuS/C复合材料。不加D-葡萄糖酸钠,其余条件同前,水热制得纯CuS样品作对比样。
1.3 工作电极的制备
1.4 测试仪器及方法
采用D8 Advance X射线衍射仪(Bruker AXS GmbH,Germany)表征晶相结构(靶材为Cu靶,工作电压40 kV,工作电流40 mA,2为10°~80°);采用Elementar Vario MICRO(德国)有机元素分析仪测试碳含量;采用激光共聚焦显微拉曼光谱仪(英国雷尼绍公司)进行拉曼分析;采用S-4800Ⅱ场发射扫描电子显微镜(Hitachi High-Technologies Corporation,Japan)表征表面形貌。
采用Autolab电化学工作站(瑞士万通中国有限公司)测试电化学性能。采用三电极工作体系,以铂片电极为对电极,饱和甘汞电极(SCE)为参比电极。测试项目包括循环伏安测试(CV)、恒流充放电测试(GCD)和交流阻抗测试(EIS)。所有的电化学测试均在6 mol·L-1的KOH电解液中进行,循环伏安的电位范围为-1.4~0.25 V,恒流充放电的电位范围为-1.1~0.25 V。
2 结果与讨论
2.1 微观结构分析
图1(a)为在纯水中制备的CuS的SEM图。从图中可以看出,CuS呈片状并且无规团聚成块状和棒状。这可能是因为纯水中较低的沸点、黏度和热导率导致铜离子具有较高的扩散速率,因此晶核更容易聚集并且无规生长[12,15]。图1(b)~(d)为加入D-葡萄糖酸钠后的SEM图。从图(b)、(c)中可以看出,CuS呈球花状,这是因为加入D-葡萄糖酸钠后,其会与体系中的自由铜离子形成络合体系并且达到平衡状态。此时体系中仍然有很少量的自由铜离子,在水热过程中,该部分自由铜离子会优先反应生成CuS,随反应的进行,铜离子不断被消耗,络合平衡向离解方向移动,保证水热反应继续进行,直至铜离子完全反应生成CuS,因此D-葡萄糖酸钠的加入影响了最终产物的形貌走向,即被络合的铜离子由于受到来自络合剂的络合作用在成核、生长过程中受到调控从而形成了球花形貌。从图(d)中可以看出,球花状CuS表面的花瓣状褶皱的平均宽度在50 nm左右。从图1(e)、(f)可以看出最终产物中球花状的CuS占大多数,此外还有少量的光滑球体和极少量的无规堆积体,光滑球体是D-葡萄糖酸钠在水热过程中生成的炭球,其量少是因为在生成CuS的水热条件(150℃)下转化率低(葡萄糖水热制备炭球的反应温度通常为160~200℃)[16]。而无规堆积体可能是反应后期被D-葡萄糖酸阴离子所络合稳定的少量络合铜离子反应所生成的CuS。图1(g)、(h)为图(f)中001和002区域的EDX谱图。001区域为光滑炭球和球花状CuS,002区域为光滑炭球和无规堆积体。由谱图可知,两区域都主要由Cu、S和C 3种元素组成,Cu和S的原子数之比接近1:1,这与CuS的分子式相符。C的含量较少,为了进一步确定C含量,对CuS/C复合材料进行了元素分析。元素分析结果表明,C的含量为6.1%,进一步佐证炭球的存在。
图2分别为CuS/C、CuS和纯炭球的XRD谱图。前两者谱图中在10.807°、27.681°、29.277°、31.784°、32.852°、38.835°、47.941°、52.714°和59.345° 处出现明显的衍射峰,分别对应于(002)、(100)、(101)、(102)、(103)、(105)、(107)、(108)和(203)等晶面。与标准卡片JCPDS 06-0464比对后,可确定样品为六方晶系CuS(晶胞参数为37.92 nm,163.44 nm,90°,120°)。上述衍射峰峰形尖锐,表明CuS/C和CuS样品结晶完善程度较高。根据CuS/C复合材料在47.941°处的最强峰,采用Scherrer公式/cos可计算出其CuS晶粒尺寸0.29 nm。但是,并没有发现碳的衍射峰,说明通过本文方法水热制得的CuS/C复合材料的碳为无定形炭。为了确认这一点,图3显示了按相同条件水热制得的纯炭球,可见纯炭球在26°左右出现一个非常宽的弥散峰,强度非常弱,确实为无定形结构。由于CuS/C复合物的碳含量不高,以至于在其XRD谱图中看不到与碳相对应的衍射弥散峰。
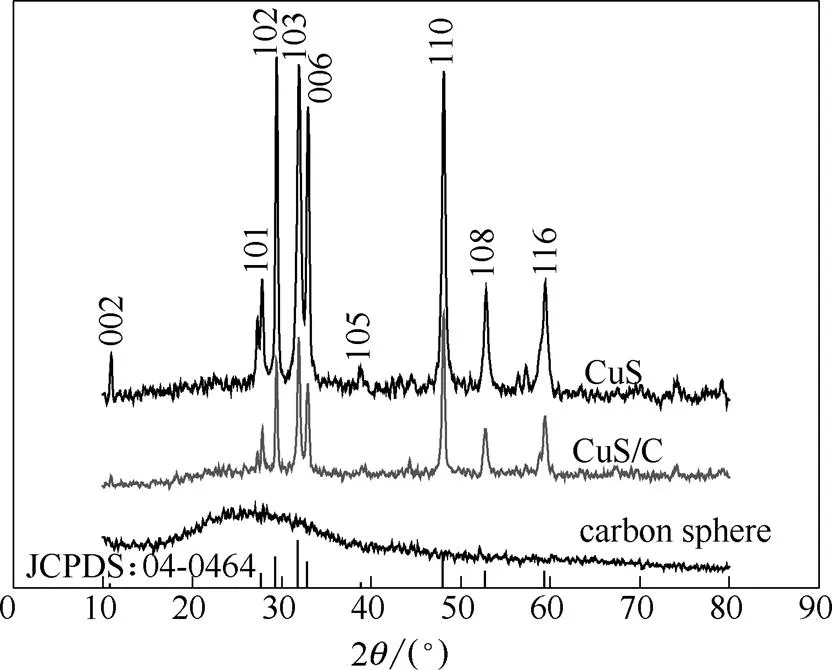
图2 CuS/C、CuS及纯碳球的XRD谱图
图3为CuS/C、CuS和纯炭球的拉曼谱图。前两者在474 cm-1处出现尖峰,为单晶CuS的特征峰,该峰可用S-2的SS键伸展模型来解释[5]。而CuS/C的拉曼谱图在1360、1578 cm−1处出现两特征峰,为炭球的两个特征峰。前者为D峰,表征碳材料石墨结构缺陷的sp3杂化键;后者为G峰,表征碳材料中与结构完整程度相关的sp2杂化键。D峰与G峰的峰强的相对大小反映碳材料的石墨化程度和完整性[17],CuS/C复合材料中炭球组分的D值明显小于G值,表明CuS/C复合材料中炭球组分为无定形结构,这与XRD分析相吻合。
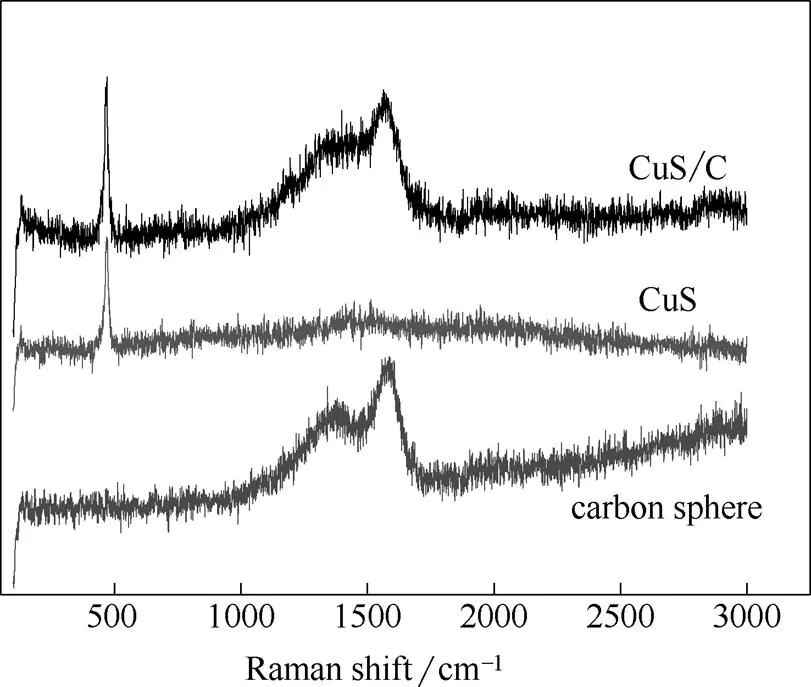
图3 CuS/C、CuS及纯炭球的Raman谱图
2.2 电化学性能分析
图4(a)分别为CuS/C和CuS循环伏安对比,扫速为50 mV·s-1,电位窗口为-1.4~0.25 V。从图中可以明显看出两对氧化还原峰,表明活性材料的电容主要来自于电极材料和电解质界面间发生的氧化还原反应。在0 V/-1.15 V处的一对氧化还原峰可能是CuS和CuSOH之间的可逆转化所致,反应式为:CuS+OH-CuSOH+e[18],这与CoS和CoSOH之间的可逆转化相似[19]。另一对氧化还原峰出现在-0.3 V/-0.6 V处,这可能与Cu0/Cu+之间的可逆转化有关,反应式为:Cu0Cu++e[20]。图中CuS/C复合材料的面积明显大于在纯水中制备的CuS的面积,表明前者的比电容优于后者。恒流充放电测试是表征活性材料电化学电容性能的有力手段。图4(b)为恒流充放电曲线,计算得到CuS/C复合材料的比电容为719 F·g-1,而在没有加络合剂的情况下制备的CuS的比电容仅为382 F·g-1。这是因为,与在纯水中水热生成的无规堆积CuS微粒相比,采用D-葡萄糖酸钠为络合剂制备的球花状CuS表面分布有大量的花瓣状褶皱,花瓣状褶皱之间会形成大量孔道,这些孔道更利于离子的传输,并且凸起的褶皱和大量的孔道都将增加活性物质与电解质之间的接触面积,极大促进离子在活性物质和电解质之间的扩散[11]。此外,复合材料中的炭球可能会提供双电层电容,同时由葡萄糖酸钠合成得到的炭球表面具有羟基、羧基等含氧官能团[21],能够提供部分赝电容。上述因素的综合使得CuS/C复合材料具有较大的比电容。
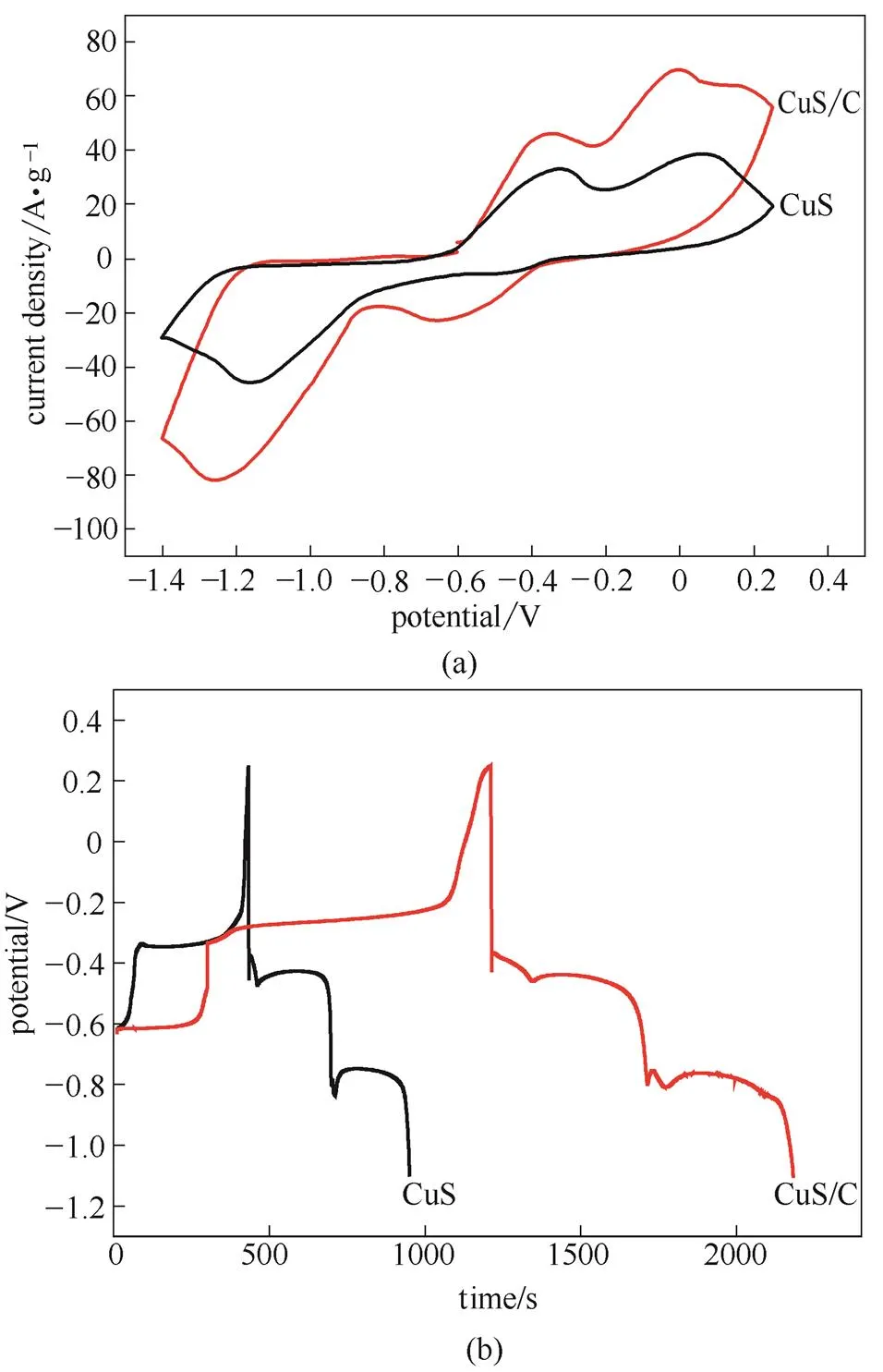
图4 CuS/C和CuS在扫速50 mV·s-1下的CV曲线对比 (a)及在电流密度1 A·g-1的恒流充放电对比(b)
图5(a)为CuS/C复合材料在不同扫速下的循环伏安图。随着扫速从5 mV·s-1增大到50 mV·s-1,CV曲线的面积和峰电流都相应增大,并且氧化峰向正极方向偏移,还原峰向负极方向偏移。但是即使在较高扫速下,从CV图中仍可以看出有明显的氧化还原峰,说明CuS/C复合材料具有较好的可逆性[16]。随着扫速的增加,CV曲线的面积随之增大,但比电容却在降低。图5(b)为CuS/C复合材料在不同电流密度下的恒流充放电曲线。当电流密度为1、2、3、5和7 A·g-1时,对应的比电容分别为719、567、500、453和423 F·g-1。可见,随着电流密度的增大,比电容逐渐减小,如图5(c)所示。当电流密度增大到7 A·g-1时,比电容与1 A·g-1时相比的保持率为59%,说明所制备的CuS/C复合材料具有较好的倍率性能。
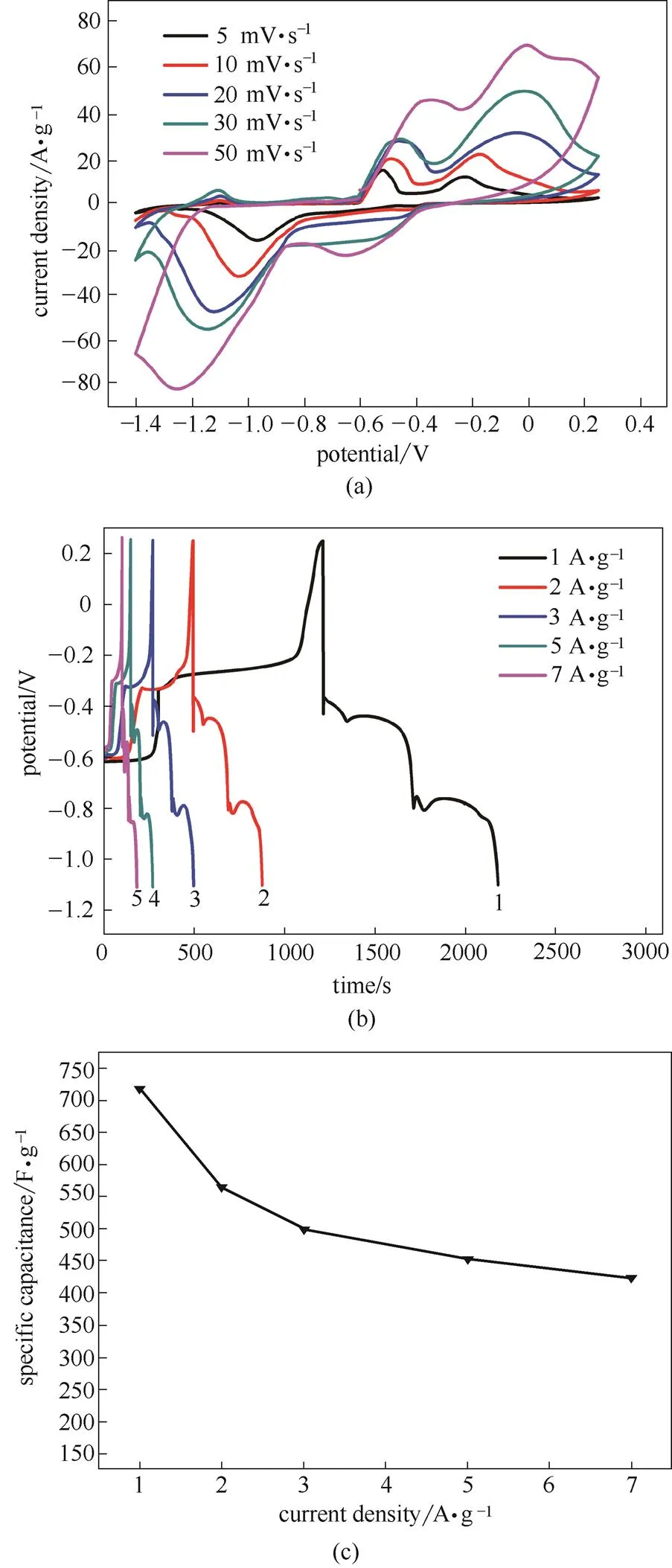
图5 CuS/C复合材料的CV曲线图(a)、恒流充放电图(b)和比电容对电流密度的变化图(c)
交流阻抗测试是表征超级电容器电极材料的另一基本手段。图6为CuS/C复合材料的交流阻抗(EIS)图,频率范围为10-2~105Hz。在最高频区,散点与实轴的截距代表组合电阻s,是电极材料内阻、电解质中的离子电阻及电极与集流体之间的接触电阻之和。由图计算可知,所制备的材料的s较小,为1.20 Ω。而在高频区,散点呈现出半圆形,半圆的直径等于活性物质在反应过程中的电荷转移电阻ct,通过拟合得出其值为6.41 Ω。在低频区,散点呈45°直线形,代表Warburg电阻,由离子在电极和电解质之间的界面上扩散和转移的频率相关所致[13]。
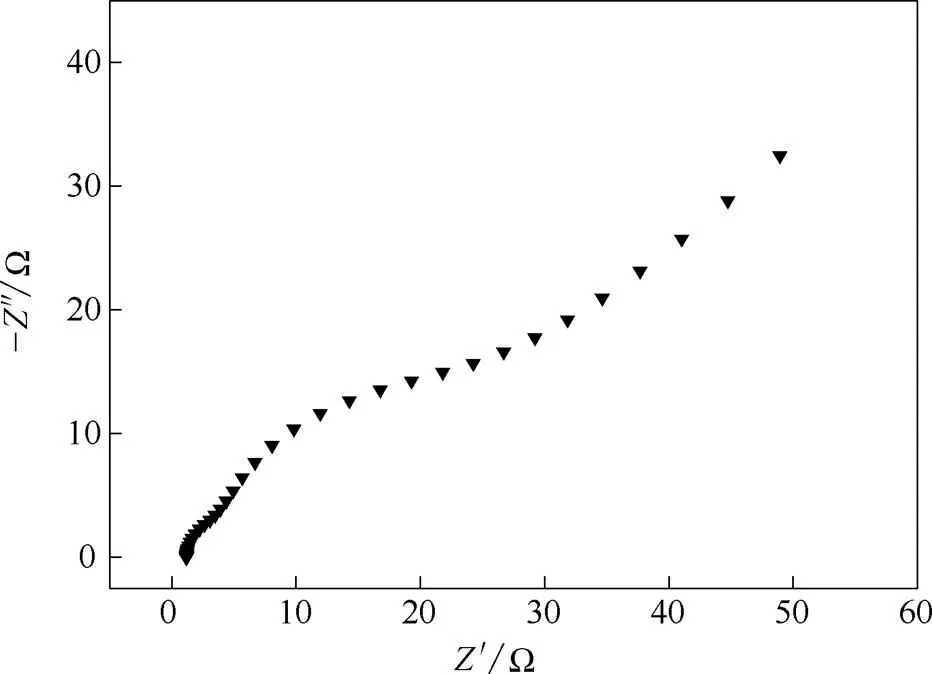
图6 CuS/C复合材料的交流阻抗图
图7为CuS/C复合材料的循环稳定性图,电流密度为1 A·g-1。可以看出,在循环100圈后,活性物质的比电容有所下降。随着循环的继续进行,比电容略有回升并趋于稳定。在循环1000圈后,比电容的保持率为80%左右,显示出CuS/C复合材料较好的循环稳定性。
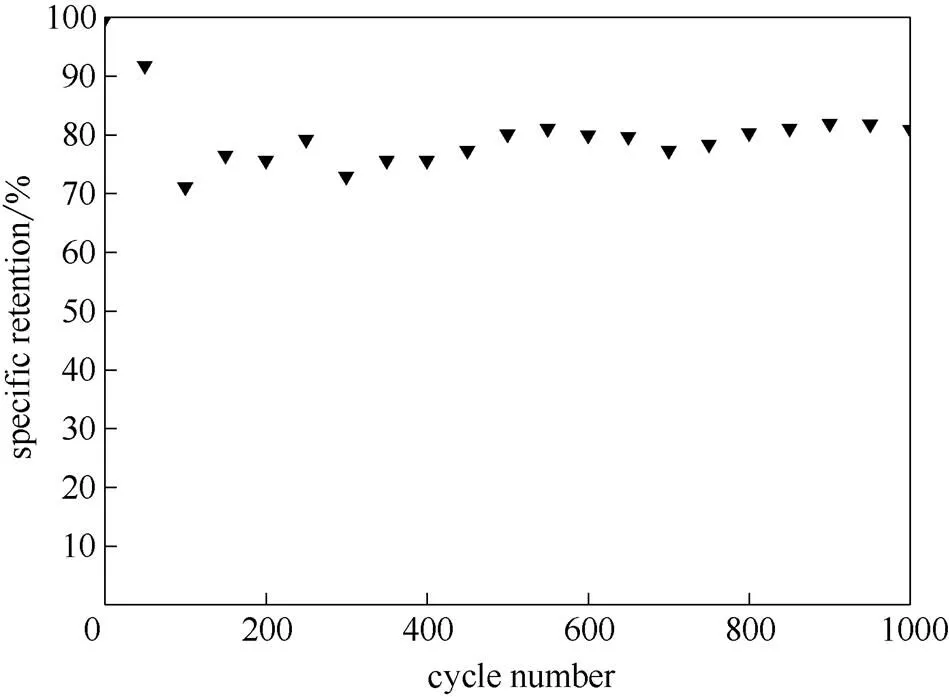
图7 CuS/C复合材料的比电容保持率随循环次数的变化散点图
3 结 论
(1)采用D-葡萄糖酸钠为络合剂,利用其对铜离子的络合作用来调控产物的形貌,从而生成新颖的球花状CuS,并且反应过程中部分D-葡萄糖酸钠转化成炭球,以致通过简单的“一锅法”水热直接一步合成球花状CuS与少量光滑炭球组成的CuS/C复合材料。
(2)复合材料中CuS呈球花状,表面大量凸起的花瓣状褶皱及褶皱间存在的孔道极大增加了活性物质CuS与电解质之间的接触面积,并且有利于离子的传输,同时无定形炭球对复合材料的比电容可能也有贡献。CuS/C复合材料比电容高,循环稳定性较好,显示出较为优异的电化学性能。
References
[1] 李吉, 魏彤, 闫俊, 等. 石墨烯纳米片/CoS2复合材料的制备及其在超级电容器中的应用 [J]. 化工学报, 2014, 65 (7): 2849-2854. LI J, WEI T, YAN J,. Preparation of graphene nanosheet/CoS2composite and its application in supercapacitors [J].CIESC Journal, 2014, 65 (7): 2849-2854.
[2] LÜ Q Y, WANG S, SUN H Y,. Solid-state thin-film supercapacitors with ultrafast charge/discharge based on N-doped-carbon-tubes/ Au-nanoparticles-doped-MnO2nanocomposites [J]. Nano Letters, 2016, 16: 40-47.
[3] JIANG Z, LU W J, LI Z P,. Synthesis of amorphous cobalt sulfide polyhedral nanocages for high performance supercapacitors [J]. Journal of Materials Chemistry A, 2014, 23 (2): 8603-8606.
[4] YU W D, LIN W R, SHAO X F,. High performance supercapacitor based on Ni3S2/carbon nanofibers and carbon nanofibers electrodes derived from bacterial cellulose [J]. Journal of Power Sources,2014, 272: 137-143.
[5] WANG Y, LIU F Y, JI Y,. Controllable synthesis of various kinds of copper sulfides (CuS, Cu7S4, Cu9S5) for high-performance supercapacitors [J]. Dalton Transactions, 2015, 44 (22): 10431-10437.
[6] QU Q T, ZHANG P, WANG B,. Electrochemical performance of MnO2nanorods in neutral aqueous electrolytes as a cathode for asymmetric supercapacitors [J]. Journal of Physical Chemistry C, 2009, 113: 14020-14027.
[7] ZHU L, WU W Y, ZHU Y S,. Composite of CoOOH nanoplates with multiwalled carbon nanotubes as superior cathode material for supercapacitors [J]. Journal of Physical Chemistry C, 2015, 119: 7069-7075.
[8] ZHANG Z, HUANG Z Y, REN L,. One-pot synthesis of hierarchically nanostructured Ni3S2dendrites as active materials for supercapacitors [J]. Electrochimica Acta, 2014, 149: 316-323.
[9] HSU Y K, CHEN Y C, LIN Y G. Synthesis of copper sulfide nanowire arrays for high-performance supercapacitors [J]. Electrochimica Acta, 2014, 139: 401-497.
[10] RAJ C J, KIM B C, CHO W J,. Electrochemical capacitor behavior of copper sulfide (CuS) nanoplatelets [J]. Journal of Alloys and Compounds, 2014, 586: 191-196.
[11] HUANG K J, ZHANG J Z, FAN Y. One-step solvothermal synthesis of different morphologies CuS nanosheets compared as supercapacitor electrode materials [J]. Journal of Alloys and Compounds, 2015, 625: 158-163.
[12] PENG H, MA G F, MU J J,. Controllable synthesis of CuS with hierarchical structuresa surfactant-free method for high-performance supercapacitors [J]. Materials Letters, 2014, 122: 25-28.
[13] HUANG K J, ZHANG J Z, XING K. One-step synthesis of layered CuS/multi-walled carbon nanotube nanocomposites for supercapacitor electrode material with ultrahigh specific capacitance [J]. Electrochimica Acta, 2014, 149: 28-33.
[14] HUANG K J, ZHANG J Z, JIA Y L,. Acetylene black incorporated layered copper sulfide nanosheets for high-performance supercapacitor [J]. Journal of Alloys and Compounds, 2015, 641: 119-126.
[15] LI F, KONG T, BI W T,. Synthesis and optical properties of CuS nanoplate-based architectures by a solvothermal method [J]. Applied Surface Science, 2009, 255 (12): 6285-6289.
[16] 魏静, 褚云, 蒋国明, 等. 水热碳化法制备碳微球 [J]. 功能材料, 2014, 45 (z2): 136-143. WEI J, CHU Y, JIANG G M,. Preparation for carbon microspheres by hydrothermal carbonization process [J]. Journal of Functional Materials, 2014, 45 (z2): 136-143.
[17] ZHENG M T, LIU Y L, XIAO Y,. An easy catalyst-free hydrothermal method to prepare monodisperse carbon microspheres on a large scale [J]. Journal of Physcial Chemistry C, 2009, 113 (19): 8455-8459.
[18] QIAN L, TIAN X Q, YANG L,. High specific capacitance of CuS nanotubes in redox active polysulfide electrolyte [J]. RSC Advances, 2013, 3 (6): 1703-1708.
[19] CHEN Y H, DAVOISNE C, TARASCON J M,. Growth of single-crystal copper sulfide thin filmselectrodeposition in ionic liquid media for lithium ion batteries [J]. Journal of Materials Chemistry, 2012, 22: 5295-5299.
[20] PILYTE S, VALIULIEN G, ŽIELIEN A,. Study of interaction of ZnS coatings with Cu(Ⅰ) and Cu(Ⅱ) by cyclic voltammetry [J]. Journal of Electroanalytical Chemistry, 1997, 436 (1/2): 127.
[21] SUN X M, LI Y D. Colloidal carbon spheres and their core /shell structures with noble-metal nanoparticles [J]. Angewandte Chemie (International Edition), 2004, 43 (5): 597-601.
One-pot hydrothermal synthesis of CuS/C composite and its application in supercapacitors
ZHAO Shuangsheng, YING Zongrong, YANG Jiajia, FAN Chuan
(School of Chemical Engineering, Nanjing University of Science and Technology, Nanjing 210094, Jiangsu, China)
In this work, a simple one-pot hydrothermal method was developed to synthetize CuS/C composite in one-step by using copper nitrate trihydrate (Cu(NO3)2·3H2O) as copper source, thiourea as sulfur source and D-glucose sodium as complexing agent. The composition, microstructure and morphology of the CuS/C composite were characterized by X ray diffraction (XRD), Raman spectroscopy, organic element analyzer and scanning electron microscopy (SEM). It was found that the as-synthesized composite was mainly composed of novel petaloid CuS microspheres, which provided many paths for ion diffusion and increased specific area with about 6% of amorphous carbon microspheres (mass fraction). The composite exhibited a maximum specific capacitance of up to 719 F·g-1at 1 A·g-1, while the specific capacitance was 382F·g-1at 1 A·g-1for CuSprepared without using complexing agent. The long-term constant current charge-discharge test showed that the CuS/C composite exhibited excellent long cycle life with capacitance retention of 80% after 1000 cycles at 1 A·g-1. Although due to low melting point (220℃) of CuS, heat treatment at high temperature cannot be employed to transform the amorphous carbon microspheres into crystalline carbon for further improving the electrochemical properties, the one-pot hydrothermal method was likely to open a new way for directly synthetizing transition metal compounds/carbon composite materials by a one-step process, especially for transition metal compounds with high melting point/carbon composites with the possibility of carbonization treatment at high temperature.
one-pot process; hydrothermal; CuS; carbon; composite; electrochemistry; supercapacitor
2016-05-03.
10.11949/j.issn.0438-1157.20160588
TB 34
A
0438—1157(2016)11—4892—07
赵双生(1991—),男,硕士研究生。
2016-05-03收到初稿,2016-06-07收到修改稿。
联系人:应宗荣。
YING Zongrong, zrying@njust.edu.cn
