气泡液膜界面法制备纳米级碳酸氢钠
2016-11-16伍文宗
伍文宗,孙 鹏,石 璞
(湖南工业大学 包装新材料与技术重点实验室,湖南 株洲 412007)
气泡液膜界面法制备纳米级碳酸氢钠
伍文宗,孙鹏,石璞
(湖南工业大学 包装新材料与技术重点实验室,湖南 株洲 412007)
采用气泡液膜界面法制备了纳米级碳酸氢钠NaHCO3粒子。通过单一变量法实验确定,当将100 mL蒸馏水、10 g NaHCO3、12 g纳米SiO2、6 mL增稠剂和8 mL发泡剂混匀,并通过搅拌,可制备出优质的纳米级NaHCO3。在制备的大量高质量气泡液膜中,不仅NaHCO3溶于该薄液膜中,且液膜内还有大量更小的气泡。将该薄液膜干燥时,NaHCO3在气泡液膜界面上结晶析出,液膜中间的气泡阻碍了NaHCO3粒子的长大,因此很容易获得小粒径的粒子。微观分析结果表明,制备的NaHCO3粒子为宽约80 nm、长约280 nm的片状,明显小于市售NaHCO3粒子尺寸的5~100m。
气泡;液膜;纳米级NaHCO3;纳米SiO2
1 背景知识
碳酸氢钠NaHCO3俗称小苏打,它是一种较为重要的无机化工产品。由于市场竞争的日趋激烈,有些应用领域对NaHCO3的品质要求越来越高,例如高分子发泡材料领域。目前,在高分子发泡材料领域中使用最多的发泡剂为偶氮二甲酰胺(azodicar-bonamide,AC),它具有产气量大、所得发泡材料力学性能较好等优点,但是同时存在发泡材料易有异味和微弱的毒性物质残留、发泡制品的表面泛黄和喷霜[1]、AC分解时产生的NH3及分解残渣可能引发模具污染[2]等缺陷。而NaHCO3作为一种无机型发泡剂,具有无毒、分解时吸热、产物CO2在聚合物中易溶解扩散等优点。因此,在发泡剂领域,尤其是在需要注意安全(如需要与食品或者人体接触)的领域中,NaHCO3发挥着重要作用。
国内外目前普遍采用Na2CO3和CO2反应制取NaHCO3,其主要的制备方法有气-固相法和气-液相法。NaHCO3结晶时,由于晶体极快速地生长,因此易产生大颗粒产品,尽管生产者可对产品进行机械法细化,但产品的绝大部分颗粒粒径仍只能达到60~100目[3]。使用大粒径NaHCO3为发泡剂时,只能获得大孔径的发泡材料。泡孔越大,发泡材料的力学性能、缓冲性能和隔热性能等均越差。因此,将NaHCO3的粒径缩小为纳米级对基体材料的发泡具重要作用。纳米粒子因具有表面效应、体积效应及尺寸效应等特性,故能给予纳米粒子更强的化学活性和催化效应[4]。将发泡剂制备成纳米粒子,然后与基体材料进行发泡,将会得到性能优越的微孔发泡材料。而由于微孔发泡材料中的微孔尺寸比聚合物材料内部的缺陷尺寸小,因此发泡后的发泡材料密度会下降,但其力学性能下降很少,也有些指标(如冲击强度等)会得到大幅度提高[5-7],且聚合物的导热系数会大幅度降低[8],因而能提高发泡材料的保温、隔热、隔音效果[9],这些特性均有极高的应用价值。
获得粒径较小的NaHCO3并非易事,且近年来关于NaHCO3粒度细化方面的研究报道不仅较少,同时存在一定的缺陷。如李懋强[10]利用溶液喷雾蒸发工艺制备了NaHCO3粉料,所制备的粉料呈球形,粒度较小,粉料直径为0.8~20.0m,其中直径小于10m 的颗粒约占总颗粒数的92%。但是此法在喷雾蒸发过程中,部分NaHCO3粒子会因为温度过高而分解为Na2CO3,导致所得产品不纯。张玉倩等[11]采用直接冷冻、真空蒸发冷冻和喷雾冷冻3种冷冻干燥法制备了超细NaHCO3粉料,其中以喷雾冷冻干燥法的制备效果最好,粉料粒度为2.26m。尽管此法可制得粒径较小的NaHCO3粒子,但其需要经过预冻和冷冻干燥等步骤,因而设备投入较大,能耗较高。因此,需要寻找一种能耗较少、工艺较为简便的新方法来制备出粒径更小的NaHCO3粒子。
近年来,有研究者使用气泡液膜界面法制备了纳米级粒子,但相关研究较少。杨第伦等[12-14]提出了气泡液膜法,它通过原料与沉降剂在液相中进行反应而获得纳米级粒子。首先,在反应装置中,全部反应液被气泡分割成液膜,形成纳米反应环境或微米反应环境,生成水难溶性或水不溶性氢氧化物、氧化物或盐的纳米粒子;然后,用相应的表面活性剂对这些纳米粒子进行原位包覆,制得纳米粒子或纳米胶囊粒子。如他们使用这种方法,制得了粒径为30~ 50 nm的Mg(OH)2胶囊粒子疏松型块体[14]。
本文拟通过气泡液膜界面法制备纳米级粒径的NaHCO3粒子。其基本原理如下:在NaHCO3溶液中加入泡沫强度高的发泡剂,搅拌后产生大量气泡液膜,NaHCO3在液膜界面上结晶,由于液膜很薄,且液膜内有很多更小的气泡存在,其能阻碍NaHCO3晶体的生长,因此达到了减小NaHCO3粒度的目的。实验结果表明,此法确实可行,且其设备简单、操作方便、方法新颖。将所制备的NaHCO3粒子作为发泡剂,有望制备出性能优良的微孔发泡材料。
2 实验部分
2.1试剂与仪器
主要试剂:碳酸氢钠,分析纯,天津市福晨化学试剂厂;纳米SiO2,SP1,浙江弘晟材料科技股份有限公司;水性聚氨酯触变增稠剂,XH-0766,东莞新骅新材料科技有限公司;发泡剂,ZC-D60,市售;蒸馏水,自制。
主要仪器:Leica DM2500P偏光显微镜(带热台),德国徕卡公司;Phenom G2 pro台式扫描电子显微镜(scanning electron microscope,SEM),荷兰Phenomworld BV;Titan G2 60-300物镜球差校正场发射透射电镜(transmission electron microscope,TEM),美国FEI公司;Q20差示扫描量热仪(differential scanning calorimetry,DSC),美国TA公司。
2.2NaHCO3粒子的制备
首先,取一定量市售NaHCO3和蒸馏水,并将NaHCO3溶于蒸馏水中制备出NaHCO3溶液;然后,取一定量SiO2,并将其加入制备的NaHCO3溶液中,用搅拌器搅拌至其分布均匀;接下来向混合溶液中加入一定量的增稠剂;待溶液再次分布均匀后,加入适量的发泡剂,搅拌至气泡稳定存在;再将这些稳定的气泡平铺在托盘上,置于50 ℃烘箱中干燥12 h。最后,将所得干燥后的产物稍加研磨,即可得纳米级粒径的NaHCO3粒子。
2.3测试与表征
1)偏光显微镜观测。对所得样品进行偏光显微镜观测的操作如下:首先,取少量样品,并将其平铺在载玻片上;然后将载玻片置于显微镜热台,于常温下观察、拍照记录;再设定程序进行升温处理,以10 ℃/min的升温速率将温度升至50 ℃,并在50 ℃恒温条件下观察气泡破裂和NaHCO3结晶情况,且用软件拍照记录。
2)SEM观测。使用Phenom G2 pro台式SEM,观察所选用的普通NaHCO3粒子的形态。
3)TEM观测。取少量样品,并将其加入无水乙醇中,超声分散30 min;然后将分散后的样品溶液滴于样品台上,待干燥后置于TEM上观察样品粒子的形态。
4)DSC测试。对市售NaHCO3和自制细化后的NaHCO3进行DSC测定,测定过程中,以10 ℃/min的升温速率,将其从20 ℃升温至200 ℃,且整个操作在氮气流保护下进行。
3 结果与讨论
3.1市售NaHCO3的结晶观察
图1所示为不同处理条件下的市售NaHCO3粒子在偏光显微镜下观测到的图片。

图1 不同处理NaHCO3粒子的偏光显微镜图片Fig.1 POM images of different processed commercial NaHCO3particles
图1a所示为将市售NaHCO3溶于水,并且在50 ℃温度条件下干燥后的偏光显微镜图片,由该图可以看出:在此处理条件下,NaHCO3晶体能长得很大,晶体尺寸约为50~150m不等;并且在观察过程中发现,它从开始结晶到完成结晶仅需要2~3 s,NaHCO3晶体长大的速度非常快,这是制备细微NaHCO3粒子的最大难点。
图1b所示为将市售NaHCO3晶体,经过充分研磨之后,分散于无水乙醇中,并超声分散30 min后观测到的偏光显微镜观测图片。由该图片中可以看出,机械研磨处理在一定程度上使NaHCO3的粒度减小了,但是还有相当多的粒子尺寸仍然为50m左右,这一结果说明,机械研磨很难从根本上减小粒子的尺寸。因而,要从根本上解决NaHCO3颗粒大小的问题,必须找到一种新的方法,使其晶体在长大的过程中受到抑制。
3.2纳米NaHCO3制备条件探索
本研究中,课题组探索纳米NaHCO3制备条件的思路为:首先试图在NaHCO3溶液体系中引入一些稳定的、细微的空气气泡,然后当NaHCO3颗粒在这些气泡的液膜上结晶长大时,空气气泡所形成的空间间隔便可以有效地阻止NaHCO3晶体的长大和合并,这样,NaHCO3的生长就会被抑制。反应体系中引入的气泡粒径越小、气泡数量越多、气泡强度越大、气泡在受热时的强度越高,则隔离抑制NaHCO3粒子长大的能力越强,从理论上来说,所制备出的NaHCO3粒子的尺寸将会越小。由此可见,获得高质量的气泡是制备纳米NaHCO3粒子的关键技术。而要获得高质量的气泡,则需要控制好反应溶液的黏度和液膜强度。而纳米SiO2的用量、增稠剂的用量和发泡剂的用量是反应溶液黏度和液膜强度的主要影响因素。因此,接下来采用单一变量法对这几个主要影响因素进行探索。经过前期的实验,课题组发现以上3个影响因素重要性大小的顺序依次为:SiO2的用量>增稠剂的用量>发泡剂的用量。故后续将按此顺序进行实验研究,以获得各原材料的较优配比。
3.2.1纳米SiO2添加量的影响
纳米SiO2具有触变作用,其在低剪切作用或静置条件下能使反应体系的黏度增大,并可以增加液膜强度,尤其是增加升温干燥时的液膜强度。这一点对于制备纳米NaHCO3特别重要,这是因为,常温下一般能较容易获得好的气泡,但是加热后,气泡极易破裂。课题组在实验过程中发现,当此反应体系中不加入纳米SiO2时,无论怎么改变其它几个条件,气泡在干燥过程中几乎全部破裂,最后仅能得到粗NaHCO3粒子,由此可见,SiO2在此反应体系中具有重要的作用。
为了确定反应体系中较为适宜的SiO2添加量,在保持其余各材料用量不变的情况下,即选取蒸馏水的用量为100 mL,NaHCO3的用量为10 g,增稠剂的用量为4 mL,发泡剂的用量为12 mL,仅改变纳米SiO2的添加质量,依次设定为4, 6, 8, 10, 12, 14 g,在相同的反应条件下,分别制备出相应的NaHCO3粒子,然后用偏光显微镜观察所得各产物气泡的稳定性。将不同SiO2添加量下所制备的产物在50 ℃温度条件下干燥后,所观测到的NaHCO3气泡粒子的部分偏光显微镜图片如图2所示。


图2 不同SiO2添加量下粒子的偏光显微镜图片Fig.2 POM images of Nano-SiO2particles under different addition amounts
从图2a中可以看出:当体系中仅加入4 g纳米SiO2时,干燥后的气泡破裂程度较大。当加入6~10 g纳米SiO2时,气泡破裂情况明显好转,如图b所示为当纳米SiO2的添加量为8 g时所得样品干燥后的泡孔情况,这说明适量的纳米SiO2起到了稳固气泡的效果。当加入12 g纳米SiO2时(见图c),破泡的情况也会出现,但比较少,大部分小气泡保留在体系当中,基本满足要求。多次实验的结果表明,以上规律的重现性较好。
将添加12 g SiO2样品的偏光显微图片局部进行放大(见图2d)还可以看出,在干燥情况下其实还有很多更微小的气泡存在(如图中圈出区域),说明加入12 g纳米SiO2后存在2种粒径分布。这些气泡阻隔了NaHCO3晶体的生长,且还能够获得大量高强度的小气泡,因此,气泡尺寸较小,数量较大。而当纳米SiO2的添加量为14 g时,气泡的效果改观不大(图略)。因此,确定纳米SiO2在此反应体系中的较适用量为12 g。
3.2.2增稠剂的影响
增稠剂可以调节溶液的黏度,因而在搅拌条件下,可获得不同品质的气泡。已有研究表明,添加适量的增稠剂可以在常温下获得泡孔直径小、大小均匀的高质量液膜气泡。
确定纳米SiO2的用量为12 g,蒸馏水的用量为100 mL,NaHCO3的用量为10 g,发泡剂的用量为12 mL,仅改变增稠剂的添加量,从2~10 mL依次加大,进行实验,制备出系列样品,并且用偏光显微镜观察常温下各制品气泡液膜的质量。总体说来,增稠剂可以大大改善常温下溶液的气泡质量,当仅加入少量的增稠剂(2~4 mL,图略)就有改善效果。而当增稠剂的添加量为6 mL时,气泡的效果较为理想,其泡沫形态如图3所示。

图3 添加6 mL增稠剂的NaHCO3样品泡沫形态Fig.3 Morphological features of the sample with the addition of 6 mL thickening agent
由图3可以看出,在大气泡液膜上面还存在一些更小的气泡,且它们能够稳定存在。正是因为这些更小气泡的存在,阻碍了NaHCO3结晶过程中晶体的进一步长大;并且气泡均匀程度比添加2~4 mL增稠剂时要好。这是因为,加入聚氨酯类增稠剂后,溶液的黏度增大,液体的表面张力更适合形成稳定的小气泡。
Ⅱ类海风锋7次个例的合成地面要素场(图9a)显示,与Ⅰ类海风锋过程相比,Ⅱ类海风锋的温压风场配置中,沿岸的温度锋区等温线更为密集,海风锋强度从苏北至苏南逐渐变强。
当增稠剂的用量增加到8 mL和10 mL时(图略),所得图片相较于添加6 mL时的差别不大,说明改性效果变化不大。为了节约成本,确定增稠剂的添加量为6 mL为佳。
3.2.3发泡剂用量的影响
所选用的ZC-D60发泡剂是一种新型环保高效的水性发泡剂。它所形成的气泡液膜十分坚韧、富有弹性,受外力压迫后,可立即恢复原状,不易破裂,并且泡径较小。
确定纳米SiO2的用量为12 g,蒸馏水的用量为100 mL,NaHCO3的用量为10 g,增稠剂的用量为6 mL,仅改变发泡剂的用量,设定为6~14 mL依次增大,进行试验,制备出系列样品,并用偏光显微镜观察常温下各样品气泡液膜的形态。图4所示为实验所得部分气泡液膜的电镜图片。


图4 不同发泡剂添加量下气泡液膜的电镜图片Fig.4 POM images of the bubble liquid membranes with different additive amounts of foaming agent
从图4中可以看出,即使发泡剂的添加量很少,也会产生很多高质量的气泡(见图4a),这一结果说明,所选用发泡剂的起泡能力非常强,当其用量较少时即产生了大量的气泡。当发泡剂的添加量为8 mL时,可发现气泡的质量比添加6 mL时的更好(见图4b),表明此添加量下的起泡效果较好。随着发泡剂用量的进一步增加,即发泡剂的添加量大于8 mL时,反应体系中部分气泡的泡径反而增大(见图4c,其为发泡剂的添加量为10 mL时的气泡形态),且发泡剂添加量越大,此现象越明显,当发泡剂的添加量为14 mL时,气泡孔径大小极不均匀(图略)。出现这一现象可能的原因是:在过量的发泡剂作用下,产生过量的小气泡,这些高表面能的小气泡互相挤压破裂,最终形成过大的气泡。利用偏光显微镜观察可以得知,当发泡剂用量为8 mL时,其气泡大小较其它几组均匀,质量最好,由此得出本实验条件下,发泡剂的添加量以8 mL为宜。
3.3NaHCO3粒子的微观分析
图5所示为市售NaHCO3的SEM照片以及前述经单一因素实验确定的较佳制备条件下制备并细化后NaHCO3粒子的TEM照片。

图5 不同NaHCO3粒子在SEM和TEM下的图片Fig.5 SEM and TEM images of different NaHCO3particles
从图5a中可以看出,市售NaHCO3颗粒较大,且大小极不均匀,颗粒尺寸为5~100m不等,且大粒子居多,较小粒子黏覆在大粒子表面。
3.4NaHCO3的热性能分析
本研究制得的NaHCO3微粒主要被用于高分子发泡材料当中,因此对其进行热性能分析必不可少。本研究采用差示扫描量热仪对其分解温度进行表征,所得结果如图6所示。
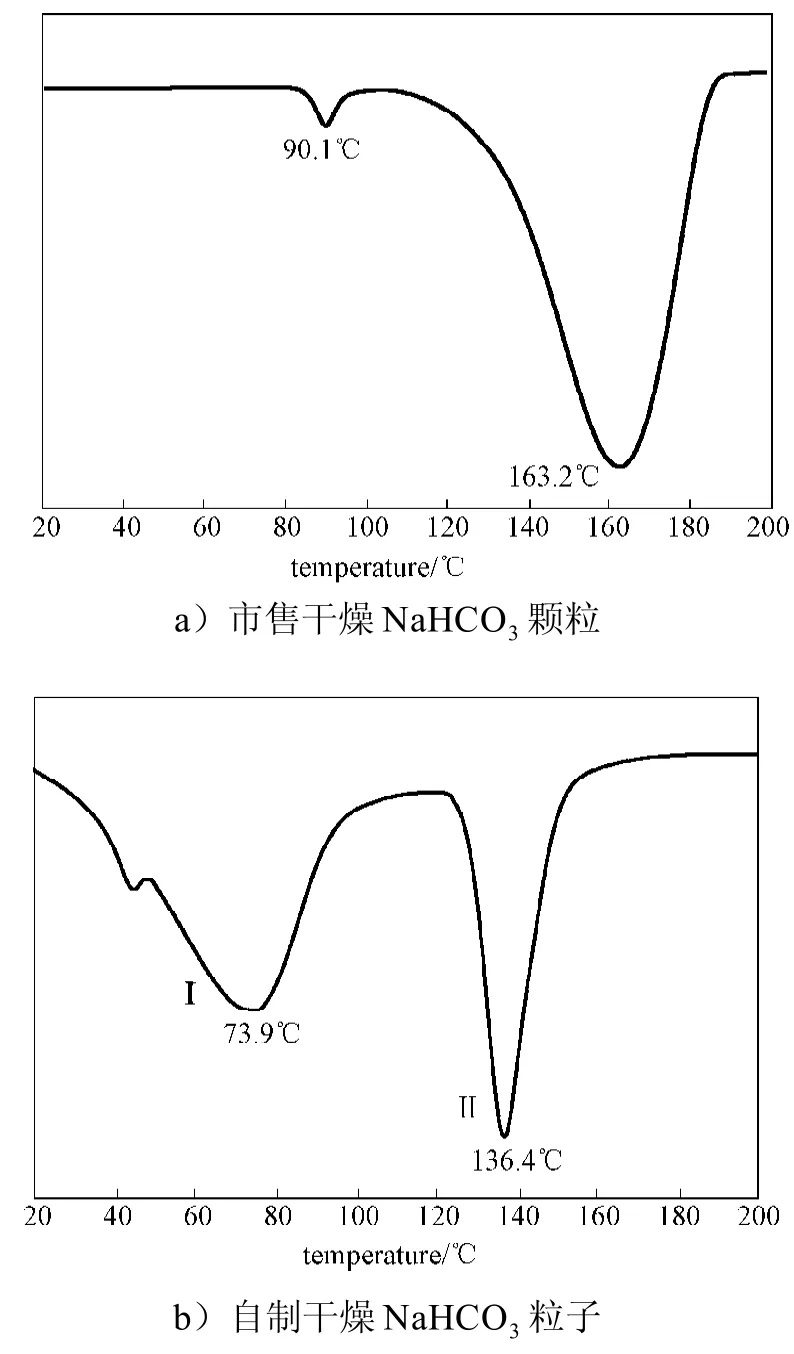
图6 不同NaHCO3粒子的DSC曲线Fig.6 DSC curves of different NaHCO3particles
从图6a中可以看出,市售NaHCO3中含有少量的水,当其加热到90.1 ℃时,因失水形成了一个小的吸热峰;第二个峰为NaHCO3分解时的吸热峰,非常宽,约110~180 ℃,这说明市售NaHCO3粒径分布范围较广;且在163.2 ℃时分解最快。
从图6b中可以看出,自制NaHCO3粒子的DSC曲线有2个明显的、有一定间距的分解吸热峰,这一结果揭示了本法合成的NaHCO3粒子尺寸可能有2种不同的尺度范围,这可能与制备过程中气泡的二重结构有关(见图2c和2d)。分解的温度都远小于市售NaHCO3的分解温度。这是由于当材料的粒径变为纳米材料后,分解温度会变低。所得结果进一步证实了本法所合成的NaHCO3粒径已大为减小,这与TEM测试结果相吻合。
4 结论
本文通过气泡液膜界面法制备了纳米级粒径的NaHCO3粒子,可得到如下结论:
1)使用100 mL蒸馏水、10 g NaHCO3、12 g纳米SiO2、6 mL增稠剂和8 mL发泡剂,通过搅拌,可获得大量的高质量气泡液膜。微观分析结果表明,此条件下制备的NaHCO3粒子为宽约80 nm、长约280 nm的片状,明显小于市售NaHCO3粒子尺寸的5~100m。
2)NaHCO3只能在气泡液体表面上结晶,气泡液膜上产生小气泡也能够限制NaHCO3晶体的生长。将气泡液膜充分干燥后稍加研磨,即可以获得纳米级的NaHCO3粒子。
总体说来,通过气泡液膜界面法制备纳米级粒子是一种低成本制备纳米级NaHCO3的方法。实验结果表明,此法确实可行,且其设备简单、操作方便、方法新颖。将所制备的NaHCO3粒子作为发泡剂,有望制备出性能优良的微孔发泡材料。
[1]陈立军,陈焕钦.AC发泡剂的制备工艺及微细化途径[J].化工新型材料,2005,33(1):52-54,60.CHEN Lijun,CHEN Huanqin.Preparation Technique and Minification Pathway of AC Blowing Agent[J].New Chemical Materials, 2005,33(1):52-54,60.
[2]何继敏,王苏平,顾淑云.新型聚合物发泡材料及技术[M].北京:化学工业出版社, 2009:25-34.HE Jimin,WANG Suping,GU Shuyun.New Polymer Foam Materials and Technology[M].Beijing:Chemical Industry Press,2009:25-34.
[3]顾德平.小苏打制造方法[J].广西化工,1986(2):14-22.GU Deping.Manufacturing Methods of NaHCO3[J].Guangxi Chemical,1986(2):14-22.
[4]张立德,牟季美.纳米材料与纳米结构[M].北京:科学出版社, 2001:14-15.ZHANG Lide,MOU Jimei.Nano Materials and Nano Structure[M].Beijing:Science Press,2001:14-15.
[5]RACHTANAPUN P,SELKE S E M,MATUANA L M.Relationship Between Cell Morphology and Impact Strength of Microcellular Foamed High-Density Polyethylene/ Polypropylene Blends[J].Polymer Engineering & Science,2004,44(8):1551-1560.
[6]MATUANA L M,PARK C B.Cell Morphology and Property Relationships of Microcellular Foamed PVC/ Wood-Fiber Composites[J].Polymer Engineering & Science, 1998, 38(11):1862-1872.
[7]WALDMAN F A.The Processing of Microcellular Foam[D].Massachusetts:Massachusetts Institute of Technolgy,1982.
[8]REGLERO RUIZ J,SAIZ-ARROYO C,DUMON M,et al.Prouction,Cellular Structure and Thermal Conductivity of Microcellular (Methylmethacrylate)-(Butyl Acrylate)- (Methylmethacrylate) Triblock Copolymers[J].Polymer International,2011,60(1):146-152.
[9]YUAN Mingjun,TURNG Lihsheng,GONG Shaoqin.Study of Injection Molded Microcellular Polyamide-6 Nanocomposites[J].Polymer Engineering and Science,2004,44(4):673-686.
[10]李懋强.溶液喷雾蒸发制备碳酸氢钠球形颗粒细粉的研究[J].过程工程学报,2004,8(4):247-251.LI Maoqiang.Preparation of Spherical NaHCO3Paticles with Spray Evaporation Process[J].The Chinese Journal of Process Engineering,2004,8(4):247-251.
[11]张玉倩,潘仁明.冷冻干燥法制备超细碳酸氢钠的工艺研究[D].南京:南京理工大学, 2010.ZHANG Yuqian,PAN Renming.Freeze-Drying Preparation of Ultrafine Technology Research of NaHCO3[D].Nanjing:Nanjing University of Science and Technology,2010.
[12]杨第伦,李宗葆.一种制造纳米粒子的气泡液膜法:中国,1803272A[P].2005-12-02.YANG Dilun,LI Zongbao.A Manufacturing Nanoparticles Bubble Liquid Membrane Method:CN,1803272A[P].2005-12-02.
[13]杨第伦,李宗葆.气泡液膜法制备纳米碳酸钙纳米粒子材料:中国,101117232A[P].2008-02-06.YANG Dilun,LI Zongbao.Nano Calcium Carbonate Nanoparticles Prepared by Utilizing the Bubble Liquid Membrane Method:CN,101117232A[P].2008-02-06.
[14]杨第伦,李宗葆,曾能.氢氧化镁疏松型纳米粒子块体阻燃剂的制造方法:中国,200510033253.X[P].2005-02-23.YANG Dilun,LI Zongbao,ZENG Neng.Flame Retardant Type Magnesium Hydroxide Loose Nanoparticles Block Manufacturing Method:CN,200510033253.X[P].2005-02-23.
(责任编辑:廖友媛)
Preparation of Nano-Sized Sodium Bicarbonate Utilizing Bubble Liquid Membrane Interfaces
WU Wenzong,SUN Peng,SHI Pu
(Key Laboratory of New Packaging Materials and Technology, Hunan University of Technology, Zhuzhou Hunan 412007, China)
Nano-sized sodium bicarbonate (NaHCO3) will be prepared by utilizing the method of bubble liquid membrane interfaces.Nano-sized sodium bicarbonate (NaHCO3) of high quality will be successfully produced with 100 mL distilled water, 10 g NaHCO3, 12 g nano-SiO2, 6 mL thickener and 8 mL foaming agent blended evenly and mixed together.NaHCO3is soluble in the high-quality prepared bubble liquid membranes, where more smaller bubbles are formed in large quantity.The separation by crystallization of NaHCO3is achieved at the interface of drying thin liquid membranes.The smaller bubbles between the liquid membranes hinder the growth of NaHCO3, thus making it easy to obtain particles of even smaller sizes.The microscopic analysis results show that the prepared NaHCO3particles, 80 nm in width and 280 nm in length, are much smaller than those commercial NaHCO3particles of 5 to 100m in size.
liquid membrane;nano-sized sodium bicarbonate;Nano-SiO2
O611.65
A
1673-9833(2016)04-0041-07
10.3969/j.issn.1673-9833.2016.04.009
2016-04-06
国家自然科学基金资助项目(11372108),湖南省自然科学基金资助项目(14JJ5021 ),湖南省高校创新平台开放基金资助项目(14K032,13K098),湖南省研究生科研创新计划基金资助项目(CX2015B561)
伍文宗(1989-),男,湖南永州人,湖南工业大学硕士生,主要研究方向为高分子材料加工与改性,E-mail:911588945@qq.com
石璞(1976-),男,安徽安庆人,湖南工业大学副教授,主要从事高分子材料改性研究及实验室管理工作,E-mail:739603197@qq.com
