玫瑰与烟草间作对烟叶蛋白质影响的生物信息学分析
2016-11-16徐洁余萍董超朱海滨张静杨义罗云姚春馨陶南丁玉梅王耀进周晓罡
徐洁,余萍,董超,朱海滨,张静,杨义,罗云,姚春馨,陶南,丁玉梅,王耀进,周晓罡
1红云红河烟草(集团)有限责任公司,云南 昆明 650202;
2云南省农业科学院生物技术与种质资源研究所,云南 昆明650223;
3云南省农业生物技术重点实验室,云南 昆明 650223;
4农业部西南作物基因资源与种质创制重点实验室,云南 昆明 650023;
5石林耀奇农产品开发有限公司
玫瑰与烟草间作对烟叶蛋白质影响的生物信息学分析
徐洁1,余萍2,3,4,董超1,朱海滨1,张静1,杨义1,罗云1,姚春馨2,3,4,陶南2,3,4,丁玉梅2,3,4,王耀进5,周晓罡2,3,4
1红云红河烟草(集团)有限责任公司,云南 昆明 650202;
2云南省农业科学院生物技术与种质资源研究所,云南 昆明650223;
3云南省农业生物技术重点实验室,云南 昆明 650223;
4农业部西南作物基因资源与种质创制重点实验室,云南 昆明 650023;
5石林耀奇农产品开发有限公司
本试验应用蛋白质双向电泳及质谱技术,对单作和与玫瑰间作的K326叶片蛋白质进行分离鉴定。利用Plant-mPLoc、Gene Ontolog、KOBAS、STRING对所鉴定蛋白进行生物信息学分析。在每份样品分离到的400左右个蛋白质中,MALDI-TOF/TOF MS法成功鉴定了20个差异蛋白质,生物信息学分析表明其中80%定位于叶绿体,主要参与光合作用和碳代谢,参与的生物过程主要是细胞过程、细胞成分组织或生物起源、生物调控、代谢过程和定位。研究表明,玫瑰散发的香气物质一方面促进烟草产生防卫反应蛋白的表达来加强其自身的抗病性,另一方面降低烟草的光合作用,抑制烤烟的生长发育。
玫瑰;烤烟;间作;生物信息学
烟草是我国重要的经济作物,K326是我国种植面积最大的烤烟品种,玫瑰是古老的天然香料植物,玫瑰花香主要包含醇类、萜烯类和酯类等挥发性有机物。这些挥发性有机物在植物之间信息交流中发挥重要作用[1-2]。黎华寿等[3]研究表明,香茅草挥发物对玉米和稗草幼苗的生物量、根长及苗高产生显著抑制作用。山艾树的枝叶被剪去后会散发某些化合物增强相邻烟草的抗病性[4]。应用蛋白质组学技术研究植物受生物和非生物胁迫后蛋白质变化已成为研究的热点。近几年也有不少烟草蛋白质组学的研究,但主要集中在烟草低氮[5]、紫外线[6]、低温[7]、高盐[8]和病原菌[9]等非生物和生物胁迫后响应的研究。对于烟草受某些植物产生的挥发性有机化合物影响的蛋白质组学研究还未见报道。本研究采用双向电泳联合质谱技术,对烟草单作和烟草与玫瑰间作的烟叶蛋白质进行比较分析,并应用生物信息学分析软件对差异表达蛋白进行亚细胞定位预测、功能分类、代谢途径分析及蛋白质间互作网络分析,旨在探讨挥发性有机化合物是否对烟草的抗病性及生长发育产生影响。
1 材料与方法
1.1 材料
试验地设在云南石林烟庄,属亚热带季风气候。供试烟草品种为K326;玫瑰品种为墨红。试验地总面积为5040 m2,平均分为2块地,一块地种植烟草21行;另一块地玫瑰与烟草间作,烟草7行,玫瑰14行,行距均为1.2 m,株距均为50 cm,烟草和玫瑰分别于2012年5月和2011年12月移栽。2012年8月5点取样法采集2块地团棵期烟株中上部上数第4片烟叶叶尖,每块地的5份叶尖混合作为1份样品,置-80℃冰箱备用。
1.2 蛋白质提取
称取1.0 g烟草叶片。参照Su等[10]方法提取叶片总蛋白质。 Bradford法测定蛋白质浓度[11]。
1.3 双向电泳
每根IPG胶条的上样量为600 µg,溶解在500µL的水化液(7 M尿素,2 M硫脲,4%CHAPS,65 mM DTT,0.2% IPG)中在IPGphorII中进行等电聚焦。其聚焦程序:250 V 30 min,500 V 30 min,1000 V 30 min,8000 V 4 h,8000 V 65000 Vh。待等电聚焦结束,把IPG胶条分别放在平衡液1(6 M 尿素,2% SDS,50 mM Tris-HCl pH 8.8,20% 甘油,2% DTT)和平衡液2(6 M 尿素,2% SDS,50 mM Tris-HCl pH 8.8,20% 甘油,2.5% 碘乙酰胺)中先后各平衡15 min。平衡结束后将胶条转移至含12.5%的聚丙烯酰胺上进行第二向电泳。胶条用考马斯亮蓝G-250染色。
1.4 凝胶图谱分析及差异点的确定
脱色后的凝胶用UMAX Power Look扫描仪扫描,分辨率设置为300 dpi的灰度模式。使用Image Master 5.0软件进行图谱分析。以其中一块以单作烟草为样品的电泳图谱为参考胶,其余5块均与其进行自动匹配分析蛋白点之间的差异。参数设定为Smooth 2,Min Area 5,Saliency30。筛选3次试验中选取处理组与对照组相对丰度(vol%)大于2倍改变的点为差异表达蛋白质点(包括有无蛋白),挖取并质谱检测。
1.5 MALDI-TOF/TOF MS分析及数据库检索
将所挖取的蛋白质斑点脱色、酶解、酶解产物的抽提和脱盐,利用ABI公司的4800 Proteomics Analyzer MALDI-TOF/TOF仪器进行分析,将质谱仪分析获得的质谱PMF图谱、二级质谱图,通过 Mascot搜 索 引 擎(http∶//matrixsciece.com) 进行蛋白质检索。检索的数据库为NCBInr(NCBINational center for biotechnology information),物种为Viridplantae(绿色植物)。
1.6 差异表达蛋白亚细胞定位的预测
利用植物蛋白亚细胞定位在线预测软件PlantmPLoc[12](http∶//www.csbio.sjtu.edu.cn/ bioinf/plantmulti/)进行差异表达蛋白的亚细胞定位预测。
1.7 GO注释
按 照 Gene Ontology(http∶//geneontology.org/)基因功能分类体系,对所有鉴定出的差异蛋白进行GO功能注释分析,并对三个本体(Ontology):生物过程(Biological Process)、细胞位置(Cellular Component)和分子功能(Molecular Function)中所涉及的GO条目进行统计分析。
1.8 差异表达蛋白的代谢途径分析
利用生物信息学在线工具KOBAS 2.0软件[13](http∶//kobas.cbi.pku.edu.cn/home.do)对差异表达蛋白进行代谢途径分析。
1.9 差异表达蛋白的相互作用网络分析
采 用 STRING 数 据 库[14](http∶//www.string-db.org/)对受玫瑰花花香影响的烟草差异蛋白进行蛋白-蛋白相互作用网络分析,构建差异表达蛋白间的互作网络图。
2 结果
2.1 烟草叶片蛋白质2D图谱
选用pH 4~7范围,24 cm的IPG胶条,对烟叶的总蛋白质提取样重复双向电泳,一次同时电泳6块胶,得到分辨率和重复性均较好的6张2-DE图谱(图1)。利用ImageMaster 5.0软件对6张图谱进行分析,通过图谱比较分析发现,每张凝胶上都可检测到400左右个可重复清晰的蛋白点,其中有26个蛋白点的表达丰度在处理与对照间存在显著差异且分离清晰。
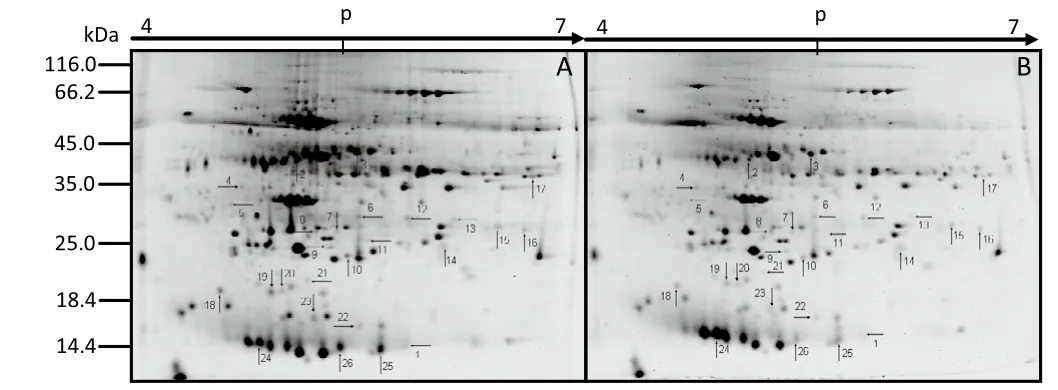
图1 烟草叶片总蛋白质的双向电泳图谱Fig.1 2-DE maps of tobacco leaf proteins
2.2 差异表达蛋白点的质谱鉴定
26个差异蛋白质点经串联质谱鉴定,除了6个蛋白点( spot3,5,8,19,22和24)未检测成功外,共有20个差异蛋白点成功鉴定,在成功鉴定的差异蛋白中共包括 17个下调蛋白,2个上调蛋白,1个蛋白的表达量消失。其中2个上调蛋白分别为4号β-1,3-葡聚糖酶(PR2)和14号24K类萌发素蛋白(germin-like protein, GLP),该2种蛋白在间作玫瑰的烟草叶片中表达量上升(表1)。
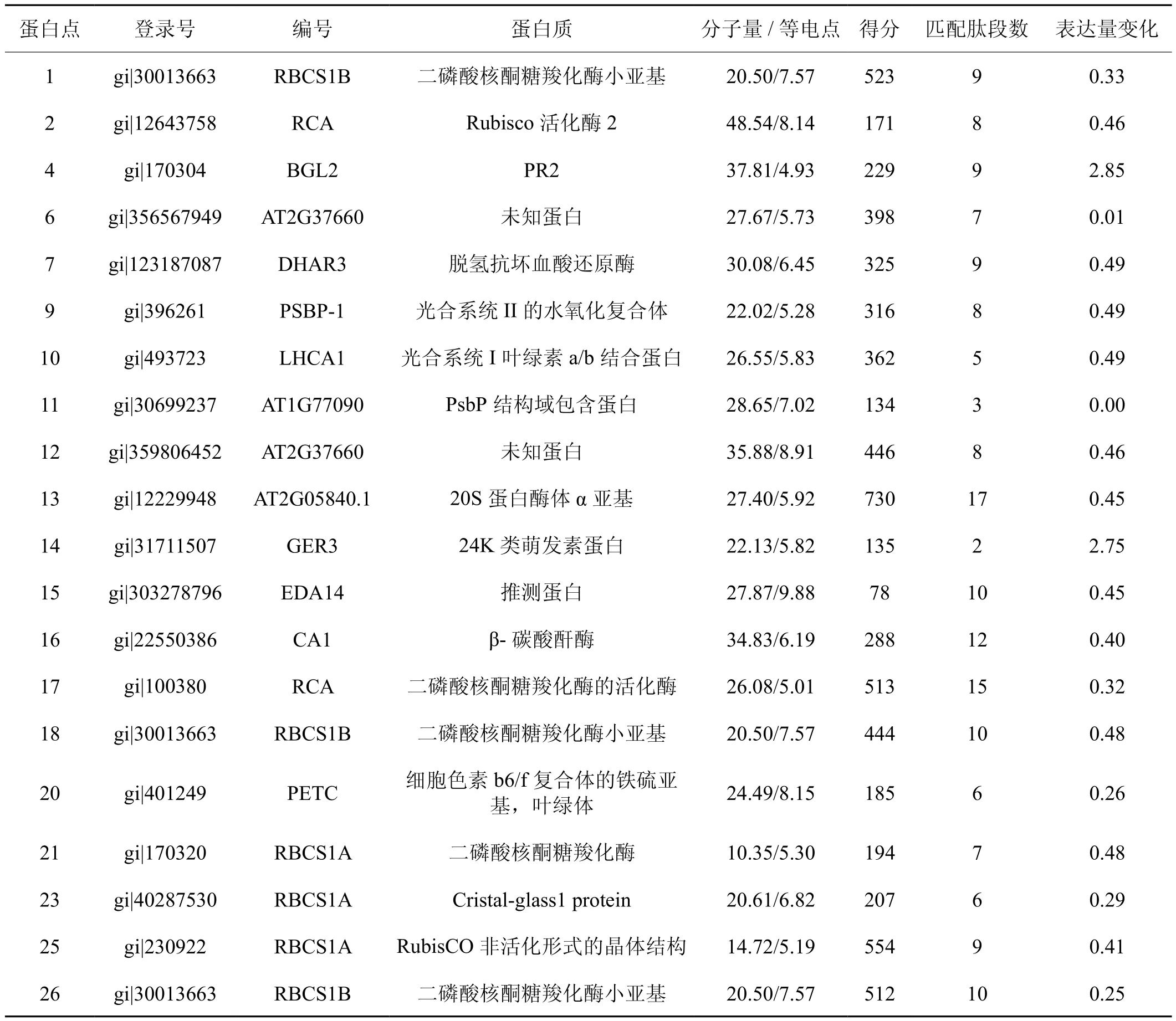
表1 差异蛋白质点的鉴定结果Tab.1 Different espression spots identified by MALDI-TOF/TOF MS
2.3 差异表达蛋白亚细胞定位的预测
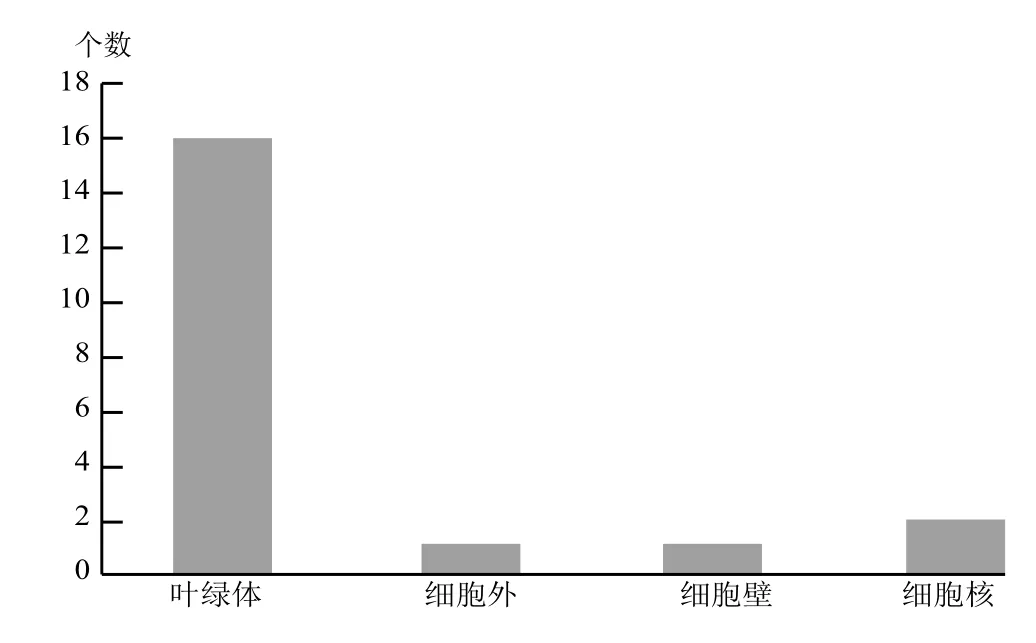
图2 差异表达蛋白点的亚细胞定位分析Fig.2 Subcelluar location of differently expressed proteins
由图2可看出,20个蛋白质定位在细胞的4个部位,其中在细胞壁和胞外区的蛋白质各仅有1个,分别为14号蛋白和4号蛋白;细胞核上的2个,分别为13号、15号蛋白;其余16个蛋白均定位在叶绿体上,比例高达80%。
2.4 差异表达蛋白的GO注释
为明确差异表达蛋白的功能,利用GO功能分类系统对20个鉴定的差异蛋白进行生物过程、分子功能和细胞位置分类(图3)。这20个蛋白主要参与生物过程中的细胞过程(18%)、细胞成分组织或生物起源(13%)、生物调控(12%)、代谢过程(12%)和定位(10%)。分子功能中的链接(52%)和催化活性(29%)。细胞位置中的细胞(29%)、细胞器(19%)、部分细胞(19%)、部分细胞器(10%)和胞外区(12%)。
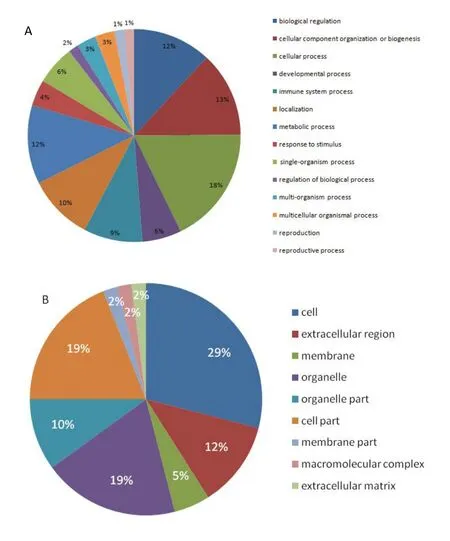
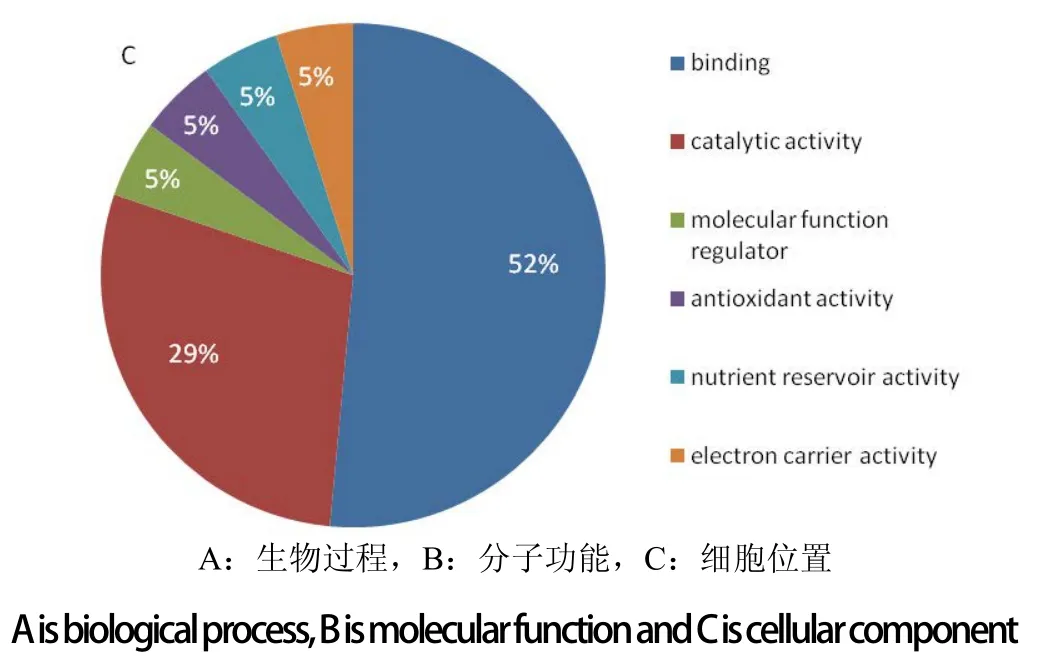
图3 差异表达蛋白的GO注释Fig.3 GO analysis of differently expressed proteins
2.5 KOBAS分析差异表达蛋白的代谢途径
为了解差异表达蛋白参与的代谢途径,用KOBAS 2.0软件对20个差异表达蛋白进行分析,以确定它们属于哪一类生化代谢途径(表2)。KOBAS 2.0分析把20个差异表达蛋白定位于8个代谢途径。其中25号、26号、21号、23号、18号和1号6个蛋白既可能参与二羧酸代谢也可能参与碳代谢。9号、20号蛋白参与光合作用,其中9号蛋白是光系统II放氧复合体的外周蛋白PsbP,20号蛋白是细胞色素b/f复合物中的PetC蛋白。光合作用天线蛋白,氮代谢和蛋白酶体各一个蛋白。依此推测与玫瑰间作可能影响烟叶细胞中碳代谢和光合作用的相关蛋白。
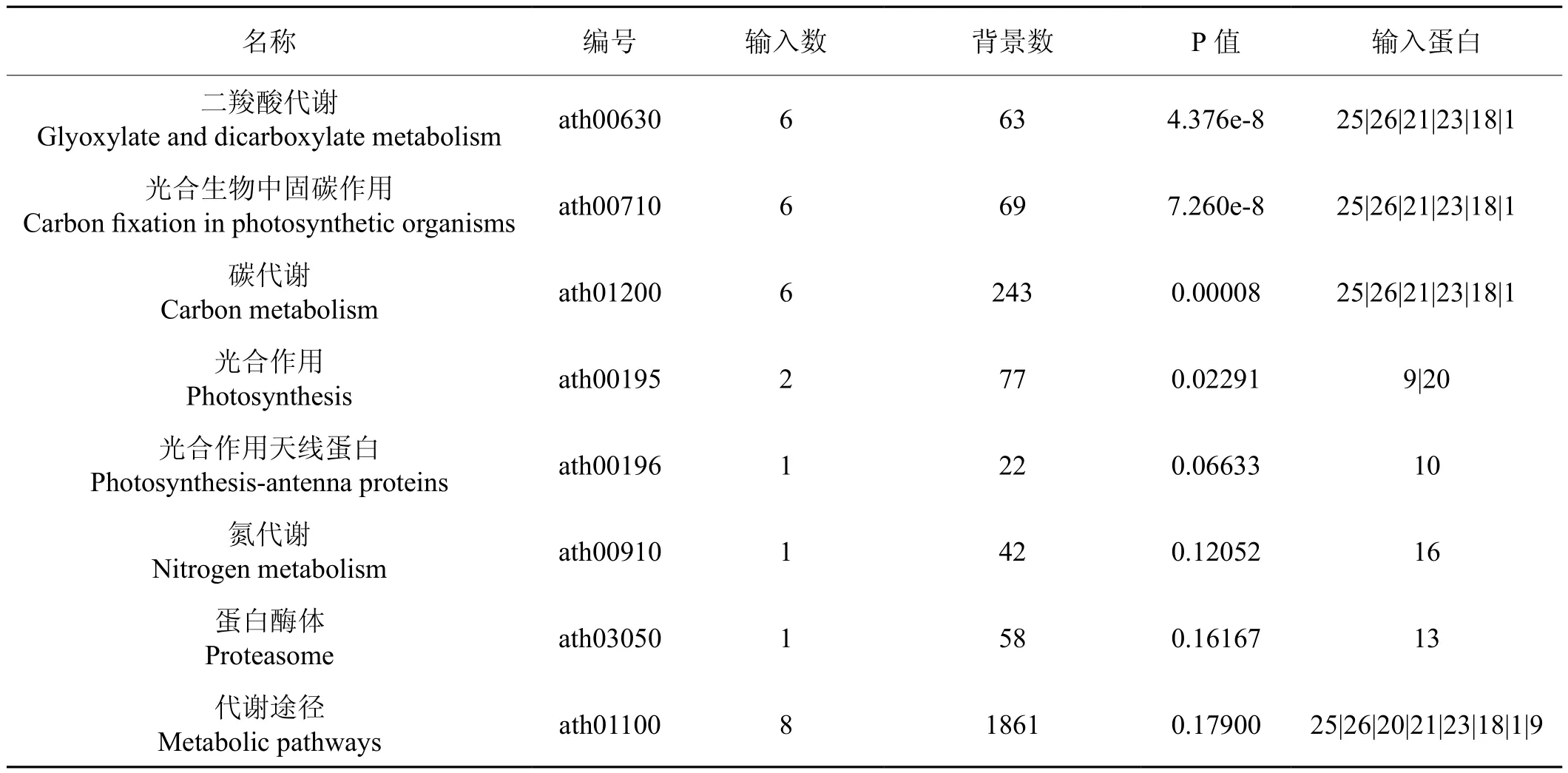
表2 差异蛋白参与的代谢途径Tab.2 Metabolic pathways of differently expressed proteins
2.6 蛋白-蛋白相互作用网络图谱
通过STRING在线分析数据库对20个差异表达蛋白进行蛋白质-蛋白质相互作用网络分析(图4),从图4可以看出,这些蛋白之间有密切的作用关系,构成结构复杂的差异表达蛋白相互作用网络。聚类分析结果发现20个差异表达蛋白可分为4类(图5)。1号、18号、26号蛋白同为RBCS1B,21号、23号、25号蛋白同为RBCS1A, RCA蛋白与AT2G05840.1蛋白聚为一类,共同参与1,5二磷酸核酮糖转化为磷酸乙醇酸的反应。蛋白PETC、AT2G37660、AT1G77090聚为一类,说明AT2G37660未知蛋白可能是参与光合作用反应相关蛋白。蛋白DHAR3、PSBP-1、LHCA1聚为一类。剩下的GER3、CA1、BGL2和EDA14为一类,说明EDA14推测蛋白与抗病蛋白在功能上紧密相关,这一预测结果还需进一步试验验证。
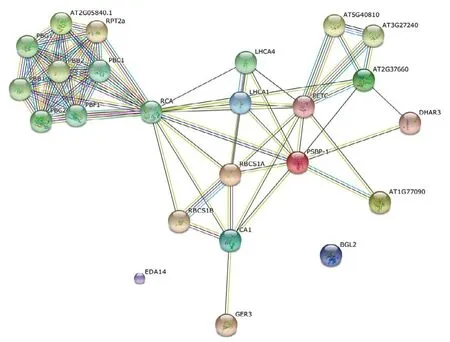
图4 差异表达蛋白的蛋白—蛋白相互作用网络图Fig.4 Protein-protein interaction network of the differentially expressed proteins
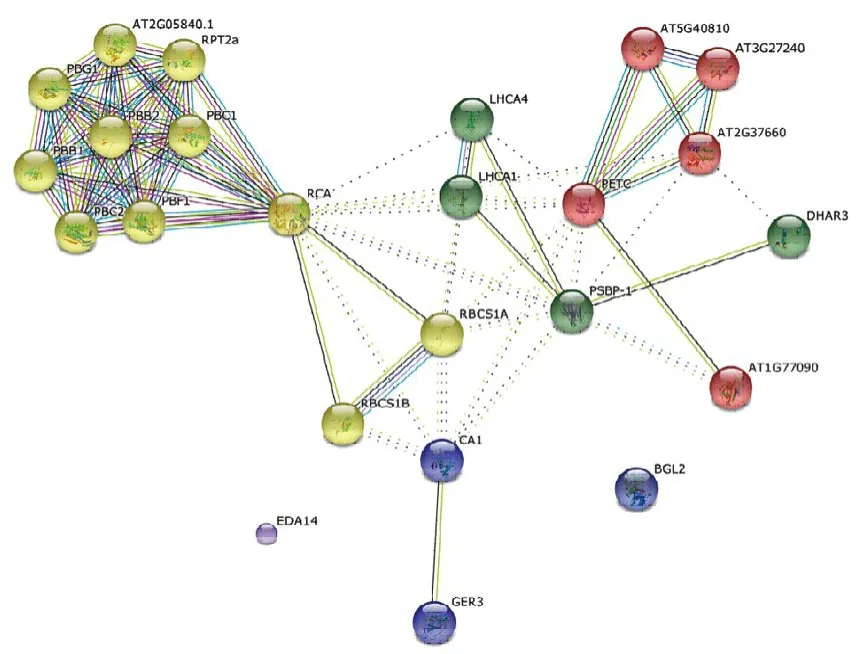
图5 差异表达蛋白的聚类互作网络图Fig.5 Clustering network map of the differentially expressed proteins
3 讨论
植物挥发性有机化合物是通过植物体内的次生代谢途径合成的低沸点、易挥发的小分子化合物,其含量低但化学活性很高,在调节植物的生长、发育和环境胁迫等方面具有重要作用[15-17]。
3.1 防卫反应
防卫反应在抗病机制中起最终作用,防卫反应蛋白具有普遍性,一般是受诱导表达。PR2(点4)是植物病程相关蛋白中的一个重要类群,可由一些特定化合物,例如水杨酸(SA)[18]、茉莉酸(JA)[19]、β-氨基丁酸(BABA)[20]等化学因子诱导产生,在植物抗病过程中担任重要角色。因PR2可以水解真菌细胞壁的主要成分β-1,3-葡聚糖,水解过程释放的寡糖可作为植物多种抗病反应的激发因子,诱导植物的防卫反应[21],PR2是植物的典型抗性标志。Yoshikawa等[22]把大豆的β-1,3-葡聚糖酶基因导入烟草可提高转化烟草对赤星病和黑胫病病菌的抗性。类萌发素蛋白(点14)是一类含有cupins结构域的糖蛋白,在植物生长发育及抗性等方面起着重要作用[23]。有些GLP还具有草酸氧化酶或超氧化物歧化酶活性,促使植物细胞壁更为致密和坚固[24]。具有OXO活性的GLP编码基因导入烟草中,可增强烟草对核盘菌的抗性。本研究中,PR2和GLP在间作玫瑰的烟草叶片中上调表达,说明玫瑰花香释放的醇类、萜烯类和酯类等挥发性有机化合物质可能作为化学诱导因子促使烟草产生防卫反应蛋白,这些蛋白可能通过对自身和病原菌细胞壁的作用产生抗性。
3.2 光合作用
光合作用类蛋白质RubisCO是卡尔文循环的关键酶,既参与光合作用又参与光呼吸作用,是所有光合生物进行光合碳同化的关键酶,将CO2还原成有机碳的限速酶。烟草 RubisCO小亚基由细胞核基因组编码,然后通过叶绿体膜上的ATP泵进入叶绿体,其表达量可调节大亚基翻译的起始[25]。RubisCO 活化酶(RCA)是一种核基因编码的叶绿体蛋白,具有ATP酶活性和活化RubisCO的功能。当RCA水平下降时,可促进PSI的环式电子流、类囊体腔的酸化和能量耗散,以缓解碳同化下降导致激发能过剩[26]。这两种酶的表达量在间作烟草叶片中下调,说明挥发性有机物影响光合作用中的碳同化可能使植物生长发育所需要的碳源下降,从而对烟草的生长产生影响。叶绿素a/b结合蛋白(点10)能够迅速把光能传到光系统Ⅰ和Ⅱ的反应中心,引起光化学反应,将光能转化为化学能,是光合系统中重要的功能蛋白[27]。碳酸酐酶(carbonic anhydrase,CA)虽然在生物学功能分类中归于气孔运动调控类蛋白,但碳酸酐酶(点16)是一种含Zn2+的与光合作用密切相关的酶,其活性与光合速率和叶肉导度相关,在CO2传导和运输中起着重要作用[28]。植物的光合速率和CO2的运输传递等间接调控气孔运动。本研究中光合作用相关蛋白的表达量在间作玫瑰的烟草叶片中表达量下调,说明玫瑰释放的挥发物中的某种或某些物质通过影响CO2的传导、运输、还原反应以及电子传递等直接或间接的影响烟草的光合作用,从而影响烟草的生长发育。
植物间可由某些挥发物进行“信息交流”,这些挥发物可能作为化感物质影响植物生长发育。化感物质可引起叶片中叶绿素含量的降低,造成植物光合作用的下降[29]。
4 结论
本研究表明,玫瑰散发的香气物质可能通过促进烟草中PR2和24K类萌发素蛋白等防卫反应蛋白的表达来加强其自身的抗病性,该结论还需进一步试验验证。另外对烟草的光合作用也会产生一定的影响,玫瑰香气使烟草的光合作用降低,而光合作用受抑制可能对烟株生长发育产生抑制作用,是否影响烟叶的品质还有待进一步研究。本试验为大田试验,对于单作与间作玫瑰K326之间检测到的蛋白质点差异如此之大的原因可能是地下营养的竞争,可能是地上光照的竞争,也可能是地上挥发性有机化合物的作用,探明到底是单方面原因还是多方面原因相互作用还有待进一步设计室内盆栽试验进行验证。
[1]Ueda H, Kikuta Y, Matsuda K. Plant communication mediated by individual or blended VOCs[J]. Plant Signaling& Behavior, 2012, 7(2)∶222-226.
[2]Das A, Lee S H, Hyun T K, et al. Plant volatiles as method of communication. Plant Biotechnol Rep, 2012,
[3]黎华寿,黄京华,张修玉,等. 香茅天然挥发物的化感作用及其化学成分分析[J]. 应用生态学报, 2005,16(4)∶763-767.
LI Huashou, HUANG Jinghua, ZHANG Xiuyu, et al.Allelopathic effects of Cymbopogon citratu volatile and its chemical components[J]. Chinese Journal of Applied Ecology, 2005, 16(4)∶763-767. Karban R, Baldwin I T,Baxter K J, et al. Communication between plants∶ induced resistance in wild tobacco plants following clipping of neighboring sagebrush[J]. Oecologia, 2000, 125∶66-71.
[4]梁景霞. 烟草种质ISSR标记及对氮素响应的生理遗传与差异蛋白质组学研究 [D]. 福州:福建农林大学,2008.
LIANG Jingxia. ISSR analysis of tobacco germplasm and physiological genetics and differential proteomics in response to nitrogen nutrition[D]. Fuzhou∶ Fujian Agriculture and Forestry University, 2008.
[5]陈宗瑜,毕婷,吴潇潇. 滤减 UV-B 辐射对烤烟蛋白质组变化的影响[J]. 生态学杂志, 2012, 31(5)∶1129-1135.
CHEN Zongyu, BI Ting, WU Xiaoxiao. Effects of reduced UV-B radiation on the variation of flue-cured tobacco proteome[J]. Chinese Journal of Ecology, 2012, 31(5)∶1129-1135.
[6]JIN Yan, ZHANG Caohao, YANG Hui, et al. Proteomic analysis of cold stress responses in tobacco seedlings[J].African Journal of Biotechnology, 2011, 10(82)∶ 18991-19004.
[7]Razavizadeh R, Ehsanpour A A, Ahsan N, et al. Proteome analysis of tobacco leaves under salt stress[J]. Peptides,2009, 30∶1651-1659.
[8]Pineda M, Sajnani C, Baron M. Changes induced by the Pepper mild mottle tobamovirus on the chloroplast proteome of Nicotiana benthamiana[J]. Photosynth Res,2010, 103∶ 31-45.
[9]苏源,余萍,孔垂思,等. 玉米幼苗根、茎、叶总蛋白质双向电泳方法的优化[J]. 西南农业学报, 2012,25(6)∶2033-2036.
SU Yuan, YU Ping, KONG Chuisi, et al. Optimization of two-dimensional electrophoresis for total proteins in maize seedling roots and stems leaves[J]. Southwest China Journal of Agricultural Sciences, 2012, 25(6)∶2033-2036.
[10] Bradford M M. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye bingding[J]. Analytical Biochemistry, 1976, 76(1-2)∶248-254.
[11] Chou K C and Shen H B. Plant-mPLoc∶ a top-down strategy to augment the power for predicting plant protein subcellular localization[J]. PLoS ONE, 2010, 5∶ e11335.
[12] Xie C, Mao X, Huang J, et al. KOBAS 2.0∶ a web server for annotation and identification of enriched pathways and diseases[J]. Nucleic Acids Research, 2011, 39∶W316-W322.
[13] Szklarczyk D, Franceschini A, Wyder S, et al. STRING v10∶ protein-protein interaction networks, integrated over the tree of life[J]. Nucleic Acids Res, 2015, 43∶ D447-52.
[14] Theis N, Lerdan M. The ecology and evolution of plant secondary etabolites[J]. Plant Sci., 2003, 164(3)∶ 92-102.
[15] 孔垂华,徐涛,胡飞,等. 环境胁迫下植物化感作用及其诱导机制[J]. 生态学报, 2000, 20(5)∶849-854.
KONG Chuihua, XU Tao, HU Fei, et al. Allelopathy under environmental stress and its induced mechanism[J]. Acta Ecologica Sinica, 2000, 20(5)∶849-854.
[16] Dudareva N, Pichersky E, Gershenzon J. Bioehemistry of Plant Volatilesl [J]. Plant Physiology, 2004, 135∶1893-1902.
[17] Alexander J, Enyedi A J, Nasser Y, et al.Localization,conjugation,and function of salicylic acid in tobacco during the hypersensitive reaction to tobacco mosaic virus[J]. PNAS, 1992, 89∶2480-2484.
[18] 牛吉山,刘靖,倪永静,等. 茉莉酸对PR-1、PR-2、PR-5和Ta-JA2基因表达以及小麦白粉病抗性的诱导[J].植物病理学报, 2011, 41(3)∶270-277.
NIU Jishan, LIU Jing, NI Yongjing, et al. Induction of PR-1,PR-2,PR-5,Ta-JA2 and wheat powdery mildew resistance in response to MeJA treatment[J]. Acta Phytopathologica Sinica, 2011,41(3)∶270-277.
[19] Siegrist J, Orober M, Buchenauer H. β-Aminobutyric acidmediated enhancement of resistance in tobacco to tobacco mosaic virus depends on the accumulation of salicylic acid[J]. Physiological and Molecular Plant Pathology, 2000,56∶95-106.
[20] Selitrennikoff C P. Antifungal proteins[J]. Apple Environ Microbiol, 2001, 67∶2883-2894.
[21] Yoshikawa M, Tsuda M, Takeuchi Y. Resistance to fungal diseases in transgenic tobacco plants experessing the phytodexin elicitor releasing factor, β-1,3-endoglucanase,from soybean[J].Naturwiss, 1993, 80(9)∶417-420.
[22] Breen J, Bellgard M. Germin-like proteins (GLPs)in cereal genomes∶ gene clustering and dynamic roles in plant defence. Funct Integr Genomics, 2010, 10∶ 463-476.
[23] Caliskan M, Turet M, Cuming A C. Formation of wheat(Triticum aestivum L.)embryogenic callus involves peroxide-generating germin-like oxalate oxidase. Planta,2004, 219∶ 132-140.
[24] Rodermel S, Haley J, Jiang C Z, et al. A mechanism for intergenomic in tegration abundance of ribulose bisphosphate carboxylase small-subunit protein in fluencies the translation of the large-subunit mRNA. Proc Natl Acad Sci USA, 1996, 93(9)∶3881-3885.
[25] Essemine J, Govindachary S, Ammar S, et al. Functional aspects of the photosynthetic light reactions in heat stressed Arabidopsis deficient in digalactosyl-diacylglycerol. Journal of Plant Physiology, 2011, 168(13)∶1526-1533.
[26] Xia Y, Ning Z, Bai G, et al. Allelic variations of a light harvesting chlorophyll a/b-binding protein gene (Lhcb1)associated with agronomic traits in barley. PLoS One, 2012,7∶ e37573.
[27]江力, 张荣铣. 烟草叶片CO2 传导与碳同化参数的研究[J]. 合肥工业大学学报, 2001, 24(4)∶598-601.JIANG Li, ZHANG Rongxian. On the parameters of the conduction of CO2and carbon assimilation in tobacco leaves[J]. Journal of Hefei University of Technology, 2001,24(4)∶598-601.Baziramakwnga R, Leroux G D, Smand R R. Effects of benzoic and cinnamic acia on growth, mineral cornpposition and chilorophyll content of soybean[J]. J Chem Ecol, 1995,20∶2821-2833.
Bioinformatics analysis of protein in leaf of tobacco intercropped with rose plant
XU Jie1, YU Ping2,3,4, DONG Chao1, ZHU Haibin1, ZHANG Jing1, YANG Yi1, LUO Yun1, YAO Chunxin2,3,4, TAO Nan2,3,4,DING Yumei2,3,4,WANG Yaojin5,ZHOU Xiaogang2,3,4
1 Hongyun-Honghe Tobacco (Group)Ltd. Co, Kunming 650202, China;
2 Biotechnology and Genetic Germplasm Institute, Yunnan Academy of Agricultural Sciences, Kunming 650223, China;
3 Kunming University Life science and technology department, Kunming 650223, China;
4 Key Laboratory of Agricultural Biotechnology of Yunnan Province, Kunming 650223, China;
5 Yaoqi Agricultural Development Ltd. Co, Kunming 652200, China
Leaf proteins of tobacco cultivar K326 from monoculture and intercropping with roses were isolated and identified by using two-dimensional electrophoresis and mass spectrometry. Bioinformatics analysis identified protein using Plant-mPLoc, Gene ontology,KOBAS, STRING. 400 proteins were isolated in each sample. 20 proteins were identified by MALDI-TOF/TOF MS. Bioinformatics analysis showed that 80% of them were located in chloroplast. They were mainly involved in photosynthesis and carbon metabolism. They were also involved in biological processes such as cellular process, cellular component organization or biogenesis, biological regulation,metabolic process and localization. Flavoring substances from roses can strengthen tobacco resistance to diseases by improving defense responses protein expression on one hand, and reduce tobacco photosynthesis, thus suppressing tobacco growth on the other hand.
rose;flue-cured tobacco;intercropping;bioinformatics
徐洁,余萍,董超,等. 玫瑰与烟草间作对烟叶蛋白质影响的生物信息学分析[J]. 中国烟草学报,2016,22(5)
应用生物多样性理论提升烟叶品质的技术研究(2015YL07)
徐 洁(1966—), 博士,高级农艺师,主要从事烟草原料研究, Email:1262254015@qq.com
周晓罡(1974—), 研究方向:植物分子生物学,Email:zxg88@163.com
2015-12-30
:XU Jie, YU Ping, DONG Chao, et al. Bioinformatics analysis of protein in leaf of tobacco intercropped with rose plant [J]. Acta Tabacaria Sinica, 2016, 22(5)
