莫西沙星相关性肝损害及血细胞减少的自动监测研究
2016-11-11贾王平郭代红王啸宇解放军总医院药品供应中心北京100853
贾王平,郭代红,朱 曼,寇 炜,王啸宇(解放军总医院药品供应中心,北京 100853)
莫西沙星相关性肝损害及血细胞减少的自动监测研究
贾王平,郭代红,朱曼,寇炜,王啸宇(解放军总医院药品供应中心,北京 100853)
目的:利用“住院患者ADE主动监测与智能评估警示系统”分析莫西沙星致肝损害和血细胞减少的发生规律。方法:借助系统回顾性调取我院2016年1 - 6月期间使用莫西沙星的住院患者病历,设置“肝功能”“血小板”“血红蛋白”“白细胞”四个模块的事件配置器参数,分析系统阳性报警病例及各ADR发生率,并对莫西沙星致肝损害的相关因素进行分析。结果:2263例次莫西沙星用药患者的自动监测,每个模块平均用时约10 min;经临床药师再评估,四个模块阳性报警率分别为54.55%、47.06%、52.94%、47.62%;ADR发生率分别为4.70%、0.54%、3.26%、0.98%。莫西沙星致肝损害在老年患者与非老年患者中无统计学差异,但男性患者比女性患者更容易发生肝损害。结论:专项软件系统可以实现莫西沙星相关性肝损害和血细胞减少等多个ADR的自动监测,筛选速度快,准确率较高;且能够初步预测ADR发生特征和相关因素,有助于降低临床用药风险。
莫西沙星;肝损害;血细胞减少;药品不良反应;自动监测
盐酸莫西沙星属于第四代氟喹诺酮类广谱抗菌药物,临床上主要用于治疗成人(≥18岁)上呼吸道和下呼吸道感染以及皮肤和软组织感染等。随着莫西沙星在临床上的广泛应用,相关的药品不良反应(ADR)报道也不断增多;常见ADR有头痛、头晕、恶心、呕吐、转氨酶升高等;少见ADR有血小板减少症、贫血、白细胞减少症、中性粒细胞减少症等。我院自主研发的医疗机构药品不良事件主动监测与智能评估警示系统(简称“系统”),可以实现药品不良事件(ADE)自动识别和辅助评估[1-2]。本研究拟借助该系统,开展对住院患者莫西沙星致相关性肝损害、血小板减少、贫血、白细胞减少等多个ADR的自动监测研究,并初步探索莫西沙星致肝损害的相关因素。
1 资料与方法
1.1研究对象
1.2四个模块自动监测的事件配置器参数设置
参照国家药品不良反应监测中心的《药品不良反应术语使用指南》(征求意见稿)[3],在“肝功能”“血小板”“血红蛋白”“白细胞”事件配置器母版的基础上,根据莫西沙星发生相应ADR的特点调整参数,包括入选标准、排除标准、筛选标准和严重程度分级。
1.2.1病例入选标准 四个事件配置器入选标准相同,均为经静脉途径使用盐酸莫西沙星氯化钠注射液(拜复乐,简称莫西沙星)。
1.2.2病例排除标准 四个事件配置器均排除检验
指标缺失,其他排除条件详见表1。
1.2.3病例筛选标准 见表2。
1.2.4严重程度分级肝损害严重程度分级如下:轻度肝损害:ALT异常伴21 μmol·L-1< TB ≤105 μmol·L-1;病人无症状或仅有轻微症状。重度肝损害:ALT ≥ 400 IU·L-1,伴105 μmol·L-1< TB ≤ 210 μmol·L-1,病人出现明显肝损害症状和体征。肝衰竭:(1)胆红素平均每天上升17 μmol·L-1或总数大于10倍正常值上限;(2)凝血酶原活动度< 40%;(3)症状进行性加重,极度乏力、厌食、呕吐;(4)出现各种严重并发症,包括腹水、上消化道出血、肝性脑病、肝肾综合征等。(1)(2)为必须条件。血细胞严重程度分级详见表3,其中3级以上属于严重ADR。
一场大战惊动了钱镇长。他终于出来了。镇长把保安拉开,训斥道:你是保安,不是保乱,怎么连这点规矩都不懂!钱镇长拉起地上的人,这才看清,原来是牛皮糖。牛皮爹,是您啊。怎么跑到这里来闹场火呢。
1.3评价内容
基于系统的自动监测结果,由两名临床药师分别对自动监测筛查出的报警病例进行人工评价,最终确定阳性病例,分析系统四个模块的阳性报警率及ADR发生率,并对莫西沙星致肝损害的相关因素进行分析。
1.4统计学处理
采用Microsoft Excel 2013对数据进行整理;采用SPSS 22.0统计学软件,对计数变量采用χ2检验,检验水准α = 0.05。
2 结果
2.1肝损害病例自动筛查及再评价结果
系统用时612 s完成莫西沙星用药患者2136例、2263例次的肝损害自动监测工作。其中系统自动排除475例次(如指标缺失、诊断混杂等),入选筛查1788例次(男性1024例次,女性764例次),报警154例次。最终经临床药师人工评价阳性为84例次,阳性报警率为54.55%,ADR发生率为4.70%,其中8例轻度肝损害,无重度肝损伤、肝衰竭病例。

表1 病例排除标准Tab 1 The exclusion standard of cases

表2 病例筛选标准Tab 2 The selected standard of cases

表3 血细胞减少严重程度分级Tab 3 The severity classification of hypocytosis
2.2血细胞减少病例自动筛查及再评价结果
血细胞减少分为“血小板”“血红蛋白”“白细胞”三个监测模块,系统自动监测用时分别为612 s、550 s、630 s。自动筛查及再评价结果详见表4,严重程度分级详见表5。
2.3莫西沙星致肝损害的相关因素分析
对莫西沙星致肝损害的年龄、性别两个因素进行统计学分析,结果显示男女患者间存在有统计学意义的差异(P = 0.014),但在老年患者与非老年患者间无统计学差异(P > 0.05)。详见表6。
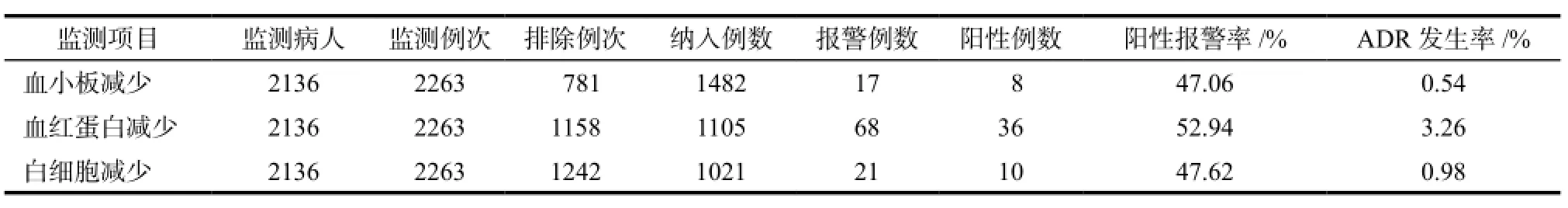
表4 血细胞减少自动筛查及再评价结果Tab 4 The re-evaluation result of hypocytosis caused by moxifloxacin
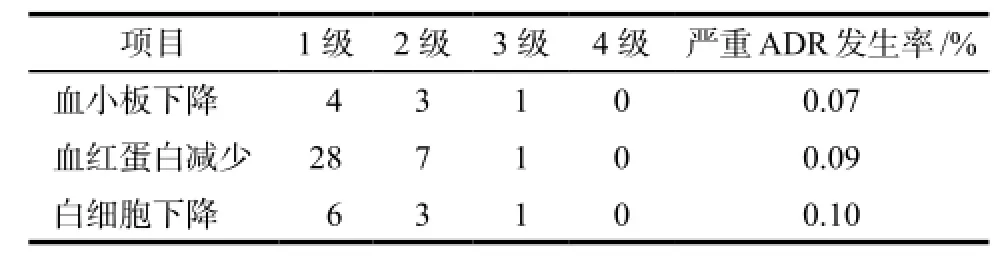
表5 血细胞减少严重程度分级结果Tab 5 The severity classification result of hypocytosis
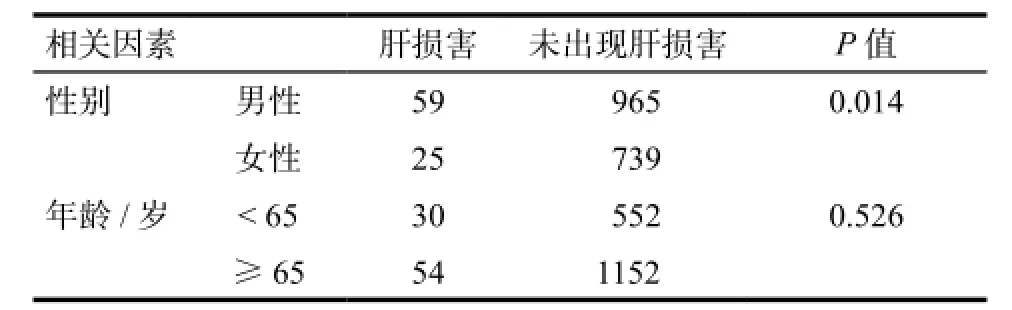
表6 莫西沙星致肝损害的影响因素分析Tab 6 Analysis of related factors about hepatic impairment caused by moxifloxacin
3 讨论
3.1系统监测效能分析
记录2263例次患者的自动监测与智能评估的过程,“肝功能”“血小板”“血红蛋白”“白细胞”每个模块用时均在10 min左右,阳性报警率分别为54.55%、47.06%、52.94%、47.62%。相比人工筛查节省了大量的时间人力,具有极高的监测效率;同时系统也具备有较高的报警准确率,可有效发现ADR。系统自动报警病例经临床药师再评估后,判定为可能无关与无法评价的病例中,大多是因为患者病情进展复杂,且合并重症感染、多重用药等,而无法准确判断为莫西沙星关联性ADR。此外四个模块均是基于触发器原理的量化指标推算,尚无法“关联”识别电子病历中诸如“极度乏力、厌食、呕吐”等文本描述,对重度肝损害与肝衰竭中的症状与体征描述的判断尚有赖于人工甄别。
3.2系统监测结果分析
莫西沙星说明书中肝损害发生率范围在0.1% ~1%。国外文献研究表明[4-5],莫西沙星的相关性肝损害发生率为0.1% ~ 7.3%。本研究结果显示,莫西沙星相关性肝损害的发生率为4.70%,明显高于说明书的发生率,但在已报道的发生率范围内。另外目前肝功能异常、肝损害的排除标准及筛选标准不统一,可能也是差异产生的原因之一。
莫西沙星说明书中记载贫血、白细胞减少症、血小板减少症三种ADR发生率范围均在0.1% ~ 1%。本研究结果显示,白细胞减少的发生率为0.98%,血小板减少的发生率为0.54%,与说明书的发生率相似,也与国外报道类似[5]。但贫血的发生率3.26%,高于说明书的发生率,也高于国外报道的贫血发生率1.1%[5]。分析原因可能是由于研究中36例阳性病例中老年人占2/3,老年患者多有基础疾病,身体弱,营养差,更容易出现贫血。也不排除真实世界中莫西沙星致贫血发生率确实较高,有待大样本深入研究加以验证。
3.3莫西沙星相关性肝损害的危险因素分析
莫西沙星药品说明书中提示老年人使用莫西沙星不必要调整用药剂量。国外文献报道莫西沙星导致的ADR在≤65岁、65 ~ 74岁、≥75岁三个不同年龄段无统计学意义差异[6]。本研究对莫西沙星致肝损害的年龄因素进行的统计学分析亦为同样结论,可能与莫西沙星的药代动力学不受年龄的影响相关[7];但对莫西沙星致肝损害的性别因素进行的统计学分析显示,男性患者较女性患者更容易出现肝损害,分析可能与男性患者生活习惯不规律、饮食偏好、饮酒较多等,导致肝功能状态不良以及脂肪肝有关,原因尚需进一步证实。
总之,借助专项软件系统实施莫西沙星相关性肝损害、血小板减少、贫血、白细胞减少等多个ADR的自动监测,病例筛选速度快、报警准确率高,数据回溯性好,能够深化分析性别和年龄等因素相关性,有助于ADR的早期发现。但系统的改进升级需要与时俱进。2016年5月FDA发布信息,氟喹诺酮类药物可能致残及并发多种永久性严重ADR,这些ADR包括肌腱炎、肌腱断裂、重症肌无力恶化等[8]。而针对性开发能够“关联”识别这些文本与词集的功能,将会进一步拓展系统自动监测的范围。
[1] 陈超,郭代红,刘皈阳,等.医疗机构药品不良反应监测的优化实践[J].中国药物警戒,2010,7(3):164-168.
[2] 陈超,郭代红,薛万国,等.住院患者药品不良事件主动监测与评估警示系统的研发[J].中国药物警戒,2013,10(7):411-414,418.
[3] 国家药品不良反应监测中心.药品不良反应术语使用指南(征求意见稿)[S].监测与评价综[2016]77号.
[4] Tulkens PM, Arvis P, Kruesmann F. Moxifloxacin safety: an analysis of 14 years of clinical data[J]. Drugs R D, 2012, 12(2): 71-100.
[5] Moxifloxacin hydrochloride injection, solution[EB/OL].[2016-07-01]. https://dailymed.nlm.nih.gov/dailymed/drugInfo. cfm?setid=a4e28b09-714b-46e7-b4e6-0163cad78fc5.
[6] Andriole VT, Haverstock DC, Choudhri SH. Retrospective analysis of the safety profile of oral moxifloxacin in elderly patients enrolled in clinical trials[J]. Drug Saf, 2005, 28(5): 443-452.
[7] Stahlmann R, Lode H. Safety considerations of fluoroquinolones in the elderly: an update[J]. Drugs Aging, 2010, 27(3): 193-209.
[8] FDA Drug Safety Communication: FDA updates warnings for oral and injectable fluoroquinolone antibiotics due to disabling side effects[EB/OL].[2016-07-01]. http://www.fda.gov/Drugs/ DrugSafety/ucm511530.htm.
The automatic surveillance of moxifloxacin-related hepatic impairment and hypocytosis cases
JIA Wang-ping, GUO Dai-hong, ZHU Man, KOU Wei, WANG Xiao-yu(Department of Pharmaceutical Care, PLA General Hospital, Beijing 100853, China)
Objective: To analyze the regularity of hepatic impairment and hypocytosis caused by moxifloxacin using inpatient's active monitoring and assessment system of adverse drug events. Methods: The data of hospitalized patients in our hospital from January to June in 2016 were extracted and analyzed retrospectively. Event configuration parameters for liver function,blood platelet, hemoglobin, white blood cell were set, and positive warning rate, incidence rate of adverse drug reactions were analyzed. Related factors of hepatic impairment and hypocytosis caused by moxifloxacin were analyzed. Results: A total of 2263 cases using moxifloxacin were automatically monitored, and the runtime of this system was about 10 minutes every model. After manual re-evaluation by clinical pharmacists, the positive predictive value of liver function, blood platelet, hemoglobin, white blood cell was 54.55%, 47.06%, 52.94%, 47.62% respectively, and the incidence rate of them was 4.70%, 0.54%, 3.26%, 0.98% respectively. There was no significant difference in incidence of hepatic impairment caused by moxifloxacin between elderly patients and non-older patients in this study, but male patients are more vulnerable to hepatic impairment caused by moxifloxacin than female patients. Conclusion: The automatic surveillance of hepatic impairment and hypocytosis caused by moxifloxacin can be realized by this system with high speed and accuracy. It also can be used for predicting the characteristics and related factors of adverse drug reaction of moxifloxacin, which can help to reduce the risk of clinical medication.
Moxifloxacin; Hepatic impairment; Hypocytosis; Adverse drug reaction; Automatic surveillance
R969.4
A
1672 - 8157(2016)05 - 0306 - 04
2014年全军后勤科研重点项目(BWS14R039)
郭代红,女,主任药师,硕士生导师,研究方向:临床药学与药物警戒。E-mail:guodh301@163.com
贾王平,男,药师,硕士研究生,主要从事临床药学工作。E-mail:18519196066@163.com
(2016-07-05
2016-07-20)
2014年全军后勤科研重点项目(BWS14R039)
郭代红,女,主任药师,硕士生导师,研究方向:临床药学与药物警戒。E-mail:guodh301@163.com
赵粟裕,男,药师,主要从事临床药学工作。E-mail:406805595@qq.com
