槐耳联合顺铂体外诱导肝癌细胞HepG2自噬的实验研究
2016-09-22谢龙腾邱国仕蒋永生翁家武马军柯婷婷
谢龙腾,邱国仕,蒋永生,翁家武,马军,柯婷婷
槐耳联合顺铂体外诱导肝癌细胞HepG2自噬的实验研究
谢龙腾,邱国仕,蒋永生,翁家武,马军,柯婷婷
目的观察槐耳联合顺铂是否能诱导HepG2细胞自噬及探讨其对自噬相关蛋白表达的影响。方法采用体外细胞培养方法,分别用槐耳浸膏、顺铂及槐耳浸膏联合顺铂干预HepG2细胞。用MTT法检测细胞活性;光学显微镜观察HepG2细胞自噬的形态学改变;Western blot检测自噬相关蛋白P53、P-Akt、Akt表达的影响。结果光学显微镜下可观察到药物组细胞的形态改变;MTT实验显示槐耳及顺铂均可抑制HepG2细胞的生长,呈时间及浓度依赖性;各药物组细胞P-Akt蛋白表达水平下降,Akt和P53表达升高。结论槐耳给药可能是通过抑制PI3K/Akt信号通路激活肝癌HepG2自噬。
肝肿瘤;HepG2;癌细胞细胞自噬;槐耳;顺铂
原发性肝癌,特别是肝细胞性肝癌(以下简称肝癌),是最常见的恶性肿瘤之一,绝大部分中晚期肝癌患者缺乏有效的治疗措施;而且,对肝癌采取包括中药在内的综合治疗的疗效明显优于单一化疗药物的治疗。槐耳是我国重要的药用抗肿瘤真菌.其主要成分是槐耳多糖蛋白(PS-T),临床研究表明槐耳对肝癌有独特的疗效[1],对其机制研究较多的是诱导肿瘤细胞的凋亡。顺铂为临床一线化疗药,因其单药大剂量应用可引起不可逆性肾功能损害及严重的胃肠道反应,因此目前临床主张联合用药[2]。自噬是指真核生物在一些应激状态下的一种细胞自我消化过程的一系列生化过程[3]。作为细胞程序性死亡的重要方式之一,越来越多的证据表明自噬在肿瘤细胞的生长和抗肿瘤药物的疗效上扮演着重要的角色[4]。本实验以肝癌细胞HepG2为研究对象,旨在通过槐耳联合顺铂激活肝癌细胞 HepG2的自噬作用及其对相关蛋白P53、P-Akt、Akt表达的影响,探讨其对PI3K/Akt信号传导通路的影响。现将结果报道如下。
1 资料与方法
1.1材料槐耳颗粒(江苏启东盖天力药物有限公司);小牛血清(美国Gibco公司);四甲基偶氮唑盐(MTT,sigma公司);RPMI-1640干粉(美国 Gibco公司);P-AKT(Abcam公司);AKT antibody(Abcam公司),P53单克隆抗体(Abcam公司);HRP标记的羊抗兔IgG (Stanta Cruz公司);-actin(Cell Signaling公司)。
1.2仪器CO2培养箱(HERAEUS);酶标仪(美国Bio-Rad公司);电泳槽(美国Bio-Rad公司);CKX41型倒置显微镜(OLYMPUS);流式细胞仪(美国BD公司)。
1.3细胞培养人肝癌细胞株HepG2购自中国医学科学院细胞中心。细胞用含10%小牛血清、100U/ml青霉素、100 g/ml链霉素的RPMI1640培养液,于37℃、5%CO2条件下培养;以0.25%胰蛋白酶(含0.02%EDTA)消化,按实验所需细胞密度接种,所有实验均在细胞对数生长期进行。
1.4MTT法测定
1.4.1不同浓度的槐耳及顺铂单独作用对MGC803增殖的影响取对数生长期的肝癌HepG2细胞消化后,接种于96孔培养板中,每孔200l含有4×103个细胞,培养24 h后,分别设槐耳组、顺铂组、空白对照组,每组6复孔。药物组加不同浓度的槐耳使其终浓度分别为 2、 4、6、8 mg/ml;顺铂使其终浓度分别为10、20、30、40g/ml,空白对照组为不加药物的培养基。置37℃,5%CO2培养箱中分别培养24h和48h后弃上清液,期间在倒置显微镜下观察细胞形态的改变,并摄影。之后用磷酸盐缓冲液(PBS)清洗3次,然后每孔加MTT 20 l,继续培养4 h后取出,吸弃培养基,每孔加 150l DMSO,置微量振荡仪上振荡10 min,于酶标仪490nm处测定其OD值,以正常组OD值为对照,计算各孔细胞抑制率(%)=(1-各孔OD值/正常组OD值均数)×100%。
1.4.2槐耳与顺铂联合给药不同时间对MGC803细胞增殖的影响取对数生长期的HepG2细胞消化后,制成4×103个/ml细胞混悬液,接种于96孔培养板中,每孔200l,正常培养24 h后,加入槐耳(4 mg/ml)+顺铂(10 g/ml)分别干预24 h。分别设空白对照组、联合给药组(4 mg/ml槐耳+10 g/ml顺铂)。其余实验步骤同步骤1.4.1。
1.5Western blot法检测 MMP-2蛋白的表达将处于对数生长期的HepG2细胞于6孔板中,培养过夜,待其贴壁后,分为3组,分别为空白组,槐耳组(4 mg/ml)和联合给药组即槐耳(4mg/ml)+顺铂(10g/ml)。24 h后提取各组细胞总蛋白,BCA法定量后,SDS-PAGE电泳,转膜,封闭液室温封闭2 h,加入一抗(1∶500),4℃孵育过夜,洗膜后加入二抗室温孵育2 h,滴加ECL液冲洗显色检测相应蛋白条带并拍照。同时以 -actin作为内参照,比较确定P53,P-Akt和Akt的相对表达水平。
1.6统计方法采用SPSS 11.0统计软件进行统计学分析,计量资料采用均数±标准差表示,两组比较采用检验。<0.05为差异有统计学意义。
2 结果
2.1倒置显微镜下细胞形态学改变倒置显微镜下观察发现,正常细胞生长状况良好,细胞胞体饱满,随着槐耳浓度的增加及作用时间延长细胞数逐渐减少,部分细胞变圆,胞体变小,部分细胞破裂;大半细胞出现碎裂、脱落并漂浮于培养基中,呈坏死状。见封三彩图1。
2.2不同浓度槐耳、顺铂对HepG2细胞的生长抑制作用槐耳、顺铂均可抑制HepG2细胞的增殖,且均呈时间、剂量依赖性,当药物干预48 h后,槐耳浓度达到8 mg/ml时,HepG2细胞存活率仅为21.9%.;顺铂达到40.0g/ml,存活率为25.1%,对HepG2细胞的抑制程度达到最大。 24 h、48 h槐耳组OD值与空白组比较差异均有统计学意义(≥3.41,均<0.05)。见表1~2。
2.3槐耳与顺铂联合干预不同时间对MGC803细胞存活率的影响槐耳+顺铂组 24 hMGC803细胞存活率为52.2%,48 h存活率为40.5%;24 h、48 h槐耳组、顺铂组、槐耳+顺铂组OD值与空白组比较差异均有统计学意义(≥3.43,均<0.05)。见表3。
2.4槐耳对肝癌HepG2细胞中蛋白表达的影响经槐耳处理的HepG2细胞,P53和Akt蛋白表达水平明显高于正常对照组,P-Akt表达低于正常组,且联合顺铂给药后这种差异更大,见图1。
3 讨论
自噬是真核细胞所共有的一种通过降解细胞内过多或异常物质以维持其正常功能的一种高度保守的生物学行为,能为细胞提供营养物质和能量,缓解应激压力[5]。自噬作为细胞的一种适应性应答,对肿瘤具有双重的作用。一方面,自噬可以通过维持细胞内稳态,抑制癌基因的激活,防止肿瘤的发生[6]。另一方面,自噬通过再循环作用,为癌细胞的生存提供营养物质,从而维持癌细胞的存活[7]。槐耳是一种药用真菌,槐耳菌质的提取物,主要的抗癌活性成分为槐耳多糖,具有扶正与抗癌的双重功能,多项基础试验研究证明,该药具有抑制肿瘤细胞生长、诱导肿瘤细胞凋亡、诱导机体产生多种细胞因子、提高机体免疫力等作用。目前已用于临床,治疗肝癌、乳腺癌、肺癌及胃癌等均有独特的疗效[8-11],磷脂酰肌醇3-激酶(PI3K)家族成员属于原癌基因,是细胞内重要的信号传导分子,参与调控细胞的增殖、分化与凋亡等一系列的生理过程,Akt是一种分子量约为57 kD的丝氨酸/苏氨酸激酶,是PI3K信号通路的主要下游效应分子之一。在许多恶性肿瘤中,PI3K/Akt信号通路参与细胞生长、肿瘤形成及侵袭、肿瘤药物疗效等方面的调控[12]。如 -榄香烯作用于胃癌SGC-7901细胞[13]和肺癌NSCLCA549细胞[14]均可通过抑制此通路而促进相应的细胞自噬。此外还有许多中药成分均可激活细胞自噬通过抑制PI3K/Akt信号通路:槲皮素也对胃癌MNK28细胞[15];白芦藜醇对白血病TALL细胞[16];麦冬皂苷B对肺癌H15/ H460细胞[17]等。
本研究发现,槐耳对肝癌HepG2细胞的增殖有显著的抑制作用。通过MTT结果可发现槐耳在体外联合顺铂与单独使用槐耳或顺铂相比对 HepG2具有更强的抗肿瘤细胞增殖作用,显微镜下的实验结果结果也证实槐耳联合顺铂对细胞的抑制作用更强,因而联合用药组显示出了更明显的优势。在 Western Blotting的结果中发现,相对于空白实验组,单用槐耳组和槐耳联合顺铂组均可上调P53、T-Akt蛋白的表达量,下调PAkt蛋白的表达量;槐耳联合顺铂给药可以通过上调P53、T-Akt及下调P-Akt促进细胞自噬。说明槐耳联合给药可能是通过抑制 PI3K/Akt信号通路激活肝癌HepG2自噬。
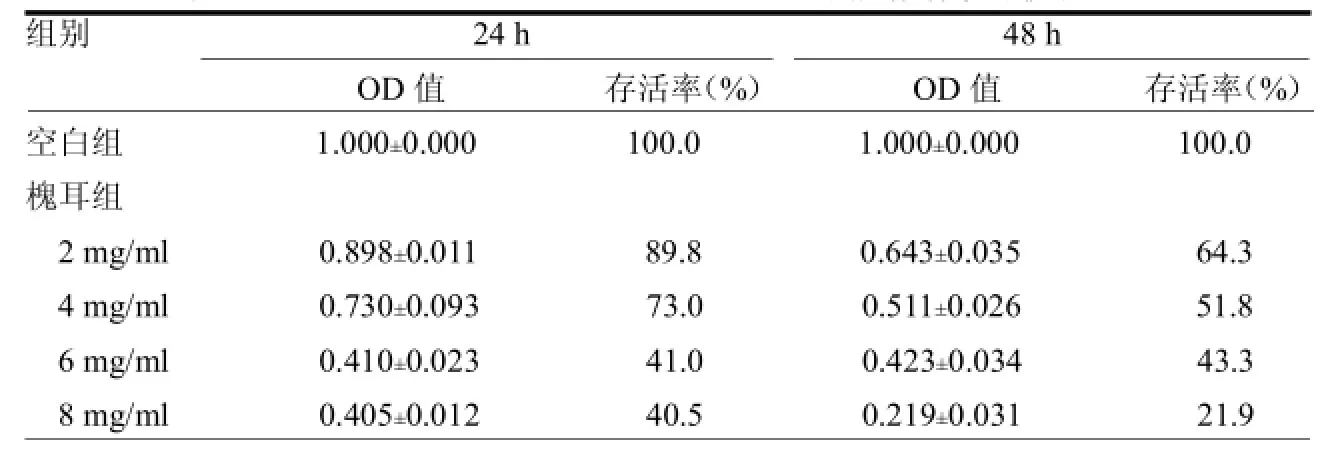
表1 不同浓度槐耳作用不同时间对HepG2细胞存活率的影响( =6)
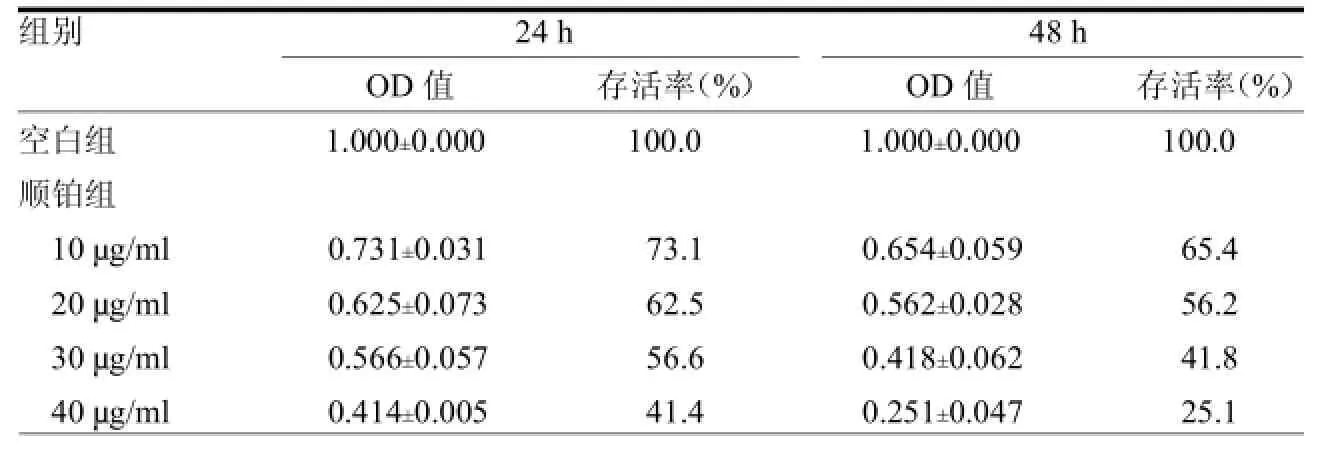
表2 不同浓度顺铂作用不同时间对HepG2细胞存活率的影响( =6)
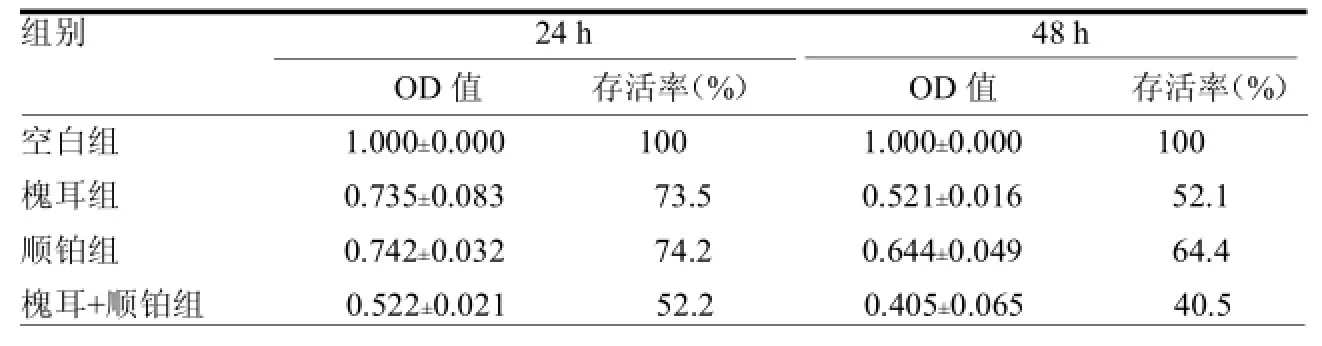
表3 槐耳与顺铂联合干预不同时间对MGC803细胞存活率的影响( =6)
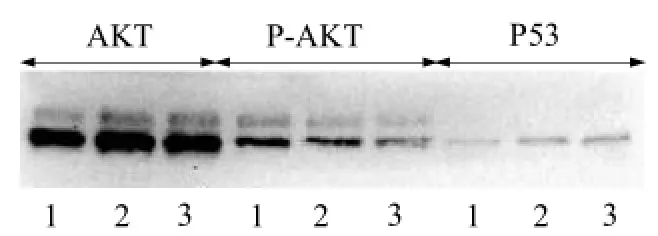
图1 Western blot法检测组别处理肝癌HepG2细胞24h后P53P-Akt和Akt蛋白的表达情况
综上所述,而槐耳作为一种新型抗肿瘤药物,可以激活肝癌细胞自噬,其途径可能是抑制 PI3K/Akt信号通路。两者联合使用可增加抗肿瘤活性,这也为临床治疗恶性肿瘤提供新的策略。
致谢我院作为温州医科大学非直管附属医院,非常感谢温州医科大学药学院的各位老师在本论文的完成过程中给予的各种帮助,使本实验可以在温州医科大学和浙江省生物技术工程制药重点实验室开展实验。
[1]吴晖.槐耳颗粒联合化疗栓塞术治疗原发性肝癌96例[J].中国药业,2014,23 (3):16-18.
[2]云春林,牛慧云,宋田霞.顺铂的临床应用[J].包头医学,2013,37(4):194-196.
[3]He LQ,Lu JH,Yue ZY.Autophagy in ageing and ageing-associated diseases.Acta Pharmacol Sin,2013,34(5):605-611.
[4]Gozuacik D,Kimchi A.Autophagy as a cell death and tumor suppressor mechanism.Oncogene,2004,23(16):2891-2906.
[5]Lozy F,Karantza V.Autophagy and can cer cell metabolism[J].Semin Cell Dev Biol,2012,23(4):395-401.
[6]Levine B,Mizushima N,Virgin HW. Autophagy in immunity and infl ammation[J].Nature,2011,469(7330):323-335.
[7]White E.Deconvoluting the context-dependent role for autophagy in cancer[J]. Nat Rev Cancer,2012,12(6):401-410.
[8]张光军,郑起,袁周,等.槐耳清膏诱导人肝癌细胞MHCC97H凋亡[J].肿瘤学杂志.2010,16(4):281-284.
[9]Zhang N,Kong XL,Yan S,et al.Huaier aqueous extract inhibits proliferation of breast cancercellsbyinducingapoptosis[J]. Cancer Sci.2010,101(11);2375-2383.
[10]沈泽天,武新虎,李兵,等.槐耳颗粒联合同步放化疗治疗局部晚期直肠癌的临床研究[J].现代肿瘤医学,2014,22(5): 1114-1117.
[11]刘聪,孙秀华.槐耳颗粒对30例晚期胃癌患者T细胞亚群的影响[J].医学综述, 2013,19(7):292-1293.
[12]Faried LS,Faried A,Kanuma T,et al.Expression of anactivatedmammalian target of rapamycin in adenocarcinoma of the cervix:A potential biomarker and moleculartarget therapy[J].MolCarcinog,2008,47 (6):446-457.
[13]Liu J,Zhang Y,Qu J,et al.-Elemene-induced autophagy protects human gastric cancer cells from undergoing apoptosis[J]. BMC Cancer,2011,11(1):183-193.
[14]Liu J,Hu X J,Jin B,et al.-Elemene induces apoptosis as well asprotectiveautophagy in human non-small-cell lung cancer A549 cells[J].J Pharm Pharmacol, 2012,64(1):146-153.
[15]WangK,LiuR,LiJ,MaoJ,etal.Quercetin induces protective autophagy in gastric cancer cells:involvement of Akt-mTOR and hypoxia-induced factor 1-mediated signaling[J].Autophagy,2011,7(9):966-978.
[16]Ge J,Liu Y,Li Q,et al.Resveratrol induces apoptosis and autophagy in T-cell acutelymphoblasticleukemiacellsbyinhibiting Akt/mTOR and activating p38-MAPK[J]..BiomedEnviron Sci,2013,26 (11):902-911.
[17]Chen M,Du Y,Qui M,et al.Ophiopogonin B-induced autophagy in non-small cell lungcancercellsviainhibitionofthePI3K/ Akt signaling pathway[J].Oncol Rep, 2013,29(2):430-436.
10.3969/j.issn.1671-0800.2016.05.020
R735.7
A
1671-0800(2016)05-0601-03
2016-02-15
(本文编辑:姜晓庆)
浙江省医药卫生一般研究计划(2016KYB275),象山县科技计划项目(2015C6005)
315700浙江省象山,象山县第一人民医院
蒋永生,Email: xsyykjk@126.com
