壳聚糖与顺铂分子的相互作用及对顺铂分子的保护机理研究
2016-09-15孙文晶赵江浩
孙文晶,赵江浩
(1.广东医科大学 中美肿瘤研究所,东莞 广东 523808;2.广东医科大学附属医院神经内科,湛江 广东 524001)
壳聚糖与顺铂分子的相互作用及对顺铂分子的保护机理研究
孙文晶1,赵江浩2*
(1.广东医科大学 中美肿瘤研究所,东莞 广东 523808;2.广东医科大学附属医院神经内科,湛江 广东 524001)
使用密度泛函方法,研究了壳聚糖与顺铂的分子电子结构以及壳聚糖-顺铂相互作用。结果表明,壳聚糖分子中的C-O-C和-OH结构非常容易给出电子,并与顺铂中的N-H部位发生氢键相互作用。而顺铂在壳聚糖内部吸附时,体系更加稳定。由于顺铂与壳聚糖主要通过氢键作用,因此很容易在环境pH值改变时,导致氢键裂解,从而释放顺铂分子,达到可控释放的目地。
壳聚糖;顺铂;密度泛函方法
顺铂属于细胞周期非特异性药物,可以抑制细胞DNA的复制过程,并对细胞膜上的结构造成损害[1]。因此,其常被用来作为临床的抗癌药物。但是顺铂对癌细胞无选择性,即其对正常细胞和癌细胞均具有毒负作用,对人体的消化道、肾毒性具有严重的影响[2]。
因此,如何控制顺铂在人体中的释放,并可靶向输送顺铂到特定的器官、组织等,实现可控释放,以达到减少对正常组及器官的毒负作用,增强抗癌效果已经成为近几年新药物研究的热点。
壳聚糖是一种天然的、可生物降解的高分子材料[3]。其具有降低胆固醇、促进伤口愈合等效果。并且其来源广泛,价格低廉,也有一定的抗癌效果。其多枝状的结构可以形成自聚合的微球,因此,很适合作为一种缓释材料,用于包裹顺铂,以达到可控负载和释放的目的[4]。
然而,很少有报道研究了壳聚糖与顺铂的分子作用方式。本工作拟从分子的角度,通过密度泛函方法考察壳聚糖和顺铂分子的相互作用机制。
2 计算细节
计算基于Accelrys公司的Material studio 的Dmol3模块来完成所有的工作。采用使用广义梯度近似的泛函和基组,对进行了分子结构的全优化和电子性质的计算。 体系采用自旋极化的方法。能量收敛精度设置为10-5a.u. 吸附能Eb=E(cp-CHI)-E(CHI)- E(cp)
3 结果与讨论
图1a展示了顺铂的分子结构图。Pt形成了一个四配位的结构,其中Pt-Cl键长为2.39 Å,Pt-N键长为2.21 Å。这就导致顺铂分子是较为平面结构的构型。壳聚糖分子(图b),从图中可以观察到,壳聚糖分子结构单元易形成分子内的氢键。这主要是因为壳聚糖分子中包括的大量的-OH 结构,易发生氢键相互作用。
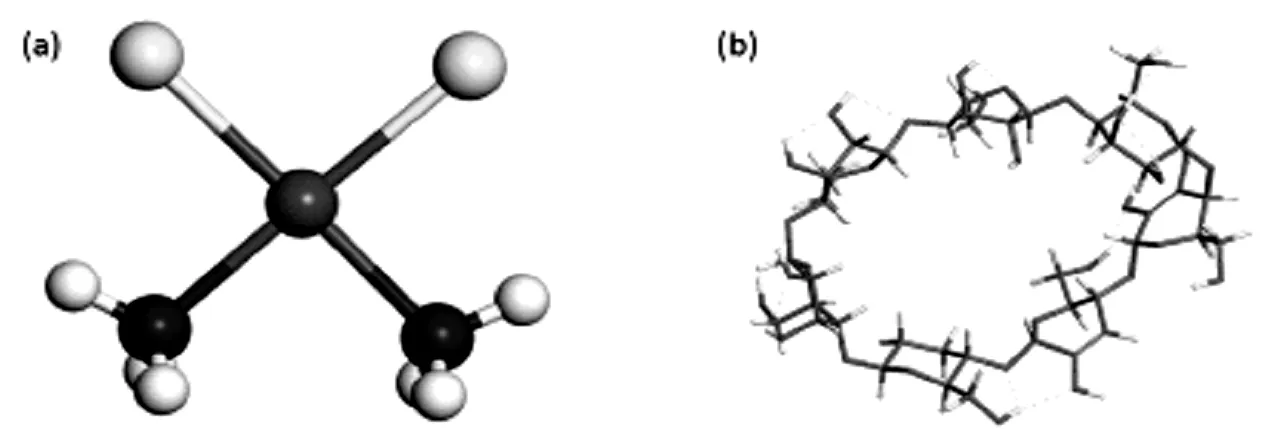
图1 (a) 顺铂的分子结构图; (b) 壳聚糖的分子结构图
Fig.1 The molecular structure of (a) cis-platimum; (b) chitosan

图2 顺铂分子的HOMO(a)和LUMO(b)轨道分布图;壳聚糖分子的HOMO(c)和LUMO(d)轨道分布图
图2 展示了两个分子的前线轨道分布图。从图中我们可以观测到,顺铂的HOMO轨道主要分布在Pt原子和Cl原子。其LUMO轨道主要分布在Pt, Cl, N 原子上。而壳聚糖分子的HOMO轨道主要分布在C-OH,-OH,及C-O-C上。而LUMO轨道主要分布在临近的C-OH,-OH,及C-O-C。说明这些位点最容易在反应时发生反应。
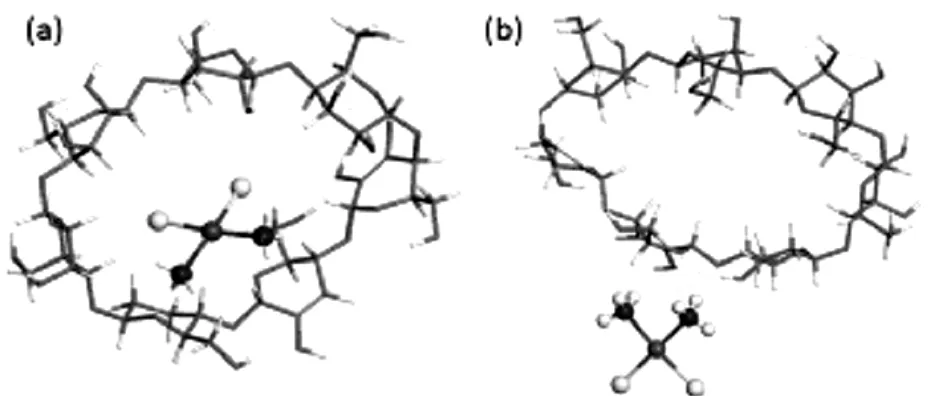
图3 (a)顺铂分子在壳聚糖分子内部吸附;(b)顺铂分子在壳聚糖分子外部吸附
图3 a 和b 分别展示了顺铂分子在壳聚糖外部和内部的相互作用。这两种作用的吸附能分别为25.6 kcal/mol 及17.8 kcal/mol. 这说明当顺铂吸附在壳聚糖环状的内部结构时,比在外部吸附稳定。从图中我们可以观测到,顺铂与壳聚糖发生的作用主要是通过两种氢键作用:N-H…O及 N-H…C。其中C和O元素是壳聚糖的组成原子。而此类的氢键,在非常容易受到环境pH值的影响,从而发生断裂。根据文献报道,癌瘤内外及癌细胞外的pH值范围在8.0-8.5之间,高于正常细胞外的pH值(7.1-7.6)[5]。这就说明,当环境的pH值改变时,将影响氢键的断裂,从而实现释放药物的目的。
4 结论
本文使用密度泛函方法,从分子角度考察了抗癌药物顺铂分子及壳聚糖的相互作用。结果表明,顺铂在壳聚糖内部吸附时的结构比在外部吸附的结构更加稳定。而顺铂与壳聚糖的主要通过氢键发生作用,因此,可以达到保护和输送顺铂的目的。当环境的pH值发生改变时,就会促进氢键的断裂,从而达到药物释放的目的。
[1]Rijt S V, Zutphen S V, Dulk H D, et al. Structure-activity relationship studies for three new asymmetric cis-platinum(II) aminoethanol-based complexes[J].Inorg Chim Acta, 2006, 359 (12), 4125-4129.
[2]Shi Y, Koneru B, Redfearn W,et al. Platinum(IV) cisplatin derivative trans, cis, cis-bis(heptanoato)amine(cyclohexylamine)dichloridoplatinum(IV) has an enhanced therapeutic index compared to cisplatin for the treatment of non-small cell lung cancer[J].Inorg Chim Acta ,2014, 423: 215-219.
[3] Juárez A R, Anota E C, Cocoletzi H H,et al. Adsorption of chitosan on BN nanotubes: A DFT investigation[J]. Appli Surf Sci, 2013, 268:259-264.
[4] Oberhauser W, Stampfl T, Bachmann C,et al. Palladium(II), platinum(II), and platinum(IV) complexes containing trans-1,2-bis(diphenylphosphino)ethene or cis,trans,cis-1,2,3,4-tetrakis(diphenylphosphino)cyclobutane: complete X-ray structural characterization of binuclear compounds[J]. Polyhedron ,2000, 19 (8), 913-923.
[5] 牛振明.人体癌瘤pH值的测试及其意义[J]. 中外健康文摘, 2012, 09(26): 447-448.
(本文文献格式:孙文晶,赵江浩.壳聚糖与顺铂分子的相互作用及对顺铂分子的保护机理研究[J].山东化工,2016,45(14):9-10.)
A DFT Study of Chitosan- cis-platinum Interactions and the Protection Mechanism of Chitosan on Cis-platinum
SunWenjing1,ZhaoJianghao2
(1.China-America Cancer Research Institute, Guangdong Medical University, Dongguan 523808, China; 2.Department of Neurology, Affiliated Hospital of Guangdong Medical University, Zhanjiang 524001, China.)
In this study, the DFT methods were applied to study the molecular structure of chitosan (CHI) and cis-platinum (cp) as well as the CHI-cp interactions. The results show that the C-O-C and -OH groups in CHI are very easy to apply electrons, and could interact with the N-H in cp with hydrogen bonds. ChI-cp complexes are more stable when it adsorb in inner sites of CHI. Because the hydrogen interactions between CHI-cp, the bonds are easy to broke, leading the leaching of the cp molecular, when the pH values changes.
chitosan; cis-platinum; DFT
2016-07-04
国家自然基金(21406039)
孙文晶(1984—),女,青海省海西州蒙古族藏族自治州人,助理研究员,博士。研究方向:计算化学;通讯作者:赵江浩(1984-),陕西省韩城市人,医师,博士。研究方向:分子生物学。
TQ460.6
A
1008-021X(2016)14-0009-02
