BCBP 与牛血清白蛋白相互作用热力学
2016-09-09郭清莲何欢潘凌立刘义
郭清莲 何欢 潘凌立 刘义
(1武汉大学中南医院检验科,武汉430071;2武汉大学化学与分子科学学院,武汉430072;3鄂东医疗集团黄石市中心医院(湖北理工学院附属医院)急诊科,湖北黄石435002)
BCBP 与牛血清白蛋白相互作用热力学
郭清莲1,*何欢2潘凌立3刘义2
(1武汉大学中南医院检验科,武汉430071;2武汉大学化学与分子科学学院,武汉430072;3鄂东医疗集团黄石市中心医院(湖北理工学院附属医院)急诊科,湖北黄石435002)
塞来昔布衍生物是一类应用非常广泛的治疗急慢性炎症的新型非甾体抗炎药。本文综合利用荧光光谱、紫外吸收光谱、圆二色谱和分子模拟等方法,研究了塞来昔布衍生物1-苯磺酰胺-3-羧基-5-苯基吡唑(BCBP)与牛血清白蛋白(BSA)相互作用的热力学行为。荧光光谱和紫外吸收光谱的分析表明:BCBP能有效猝灭BSA的内源荧光,猝灭机制为静态猝灭。通过所获取的相互作用热力学参数,可知两者之间的相互作用是一个吉布斯自由能降低的自发过程,且二者之间的主要作用力为氢键和范德华力。圆二色谱的分析发现BCBP引起BSA的构象发生改变,其α-螺旋含量降低,无规卷曲含量升高。分子对接的结果与实验结果相符。
塞来昔布衍生物;牛血清白蛋白;相互作用;热力学参数
1 引言
炎症是机体对感染的一种防御机制,主要表现为红肿、疼痛等1。疾病的产生往往伴随着炎症,抗炎药则在治疗疾病和恢复健康过程中起着至关重要的作用。选择性环氧合酶2(COX-2)抑制剂是一类应用非常广泛的治疗急慢性炎症的新型非甾体抗炎药(NSAIDs),具有很好的抗炎活性和较小的胃肠道不良反应2,3。塞来昔布是第一个上市的选择性COX-2抑制剂,为1,5-二芳基-3-取代的吡唑衍生物,能够有效地治疗各种急性疼痛和各种关节炎伴发的慢性疼痛4,5。
尽管传统的非甾体抗炎药具有良好的抗炎活性,临床研究表明塞来昔布等选择性COX-2抑制剂具有中风和心肌梗死的风险5,6。发现新型的、毒副作用较低的COX-2抑制剂是当今的研究热点,而基于塞来昔布结构进行改造是其中一种重要的途径7,8。大量的构效关系研究9-11显示,吡唑类化合物母核的1,3,5位取代对非甾体抗炎药(NIAIDs)的选择性非常关键,而4位取代将会使其对COX-2的选择性下降。Abdellatif等7,11通过大鼠足跖肿胀法评估了塞来昔布衍生物的抗炎症活性,发现C-3位羧基取代的塞来昔布系列衍生物具有良好的体内抗炎症活性,其中BCBP(1-苯磺酰胺-3-羧基-5-苯基吡唑,图1)的口服给药半数抑制剂量为104.4 mg∙kg-1。Abdellatif等11进一步将BCBP与NO释放基团通过共价键连接,发现其抗炎症活性提高,心血管副作用降低。
血清白蛋白(SA)是血液中最丰富的载体蛋白,对于药物在生物体内的运输有着重要的生理作用,许多生物活性物质,如代谢物、医药及其他有机物,与血清白蛋白的亲和性,影响它们在体内的分布和新陈代谢12-14。研究血清蛋白与药物的作用有助于了解药物的体内运输性质,对药物化学和药物分子设计具有重要的意义15,16。考虑到抗炎药物的活性与重要的医疗价值,研究其与蛋白质的相互作用,有助于在分子水平上认识抗炎药物与蛋白质的作用机理和规律,为药物分子的设计、修饰与筛选提供有益的启发与指导。
目前,塞来昔布与生物大分子相互作用引起了较多研究人员的关注,但对于塞来昔布衍生物的相关报道较少。Masomeh等17通过多种光谱手段以及差示扫描量热法,研究发现塞来昔布能够有效的与人碳酸酐酶II结合并抑制其活性,这种结合对碳酸酐酶II结构的影响不大,氢键和疏水作用对塞来昔布-碳酸酐酶II复合物的形成起关键作用。Neelam和Sonu18通过荧光光谱的手段,研究了塞来昔布与人血清白蛋白(HSA)的相互作用,结果表明塞来昔布结合在Site II位点,结合自由能为-27.92 kJ∙mol-1。Pereira-Leite等19在模拟生理条件下(4-羟乙基哌嗪乙磺酸、醋酸钠缓冲溶液,离子强度为0.1 mol∙L-1)研究了塞来昔布与磷脂膜的相互作用,发现在pH=5.0条件下(炎症细胞pH),塞来昔布结合在磷脂膜内部;而在pH=7.4条件下(血浆pH),塞来昔布主要结合在磷脂膜表面。研究塞来昔布衍生物与蛋白质的相互作用,对于了解其在体内的运输过程以及作用机制,对发现和设计新型低毒副作用COX-2抑制剂具有重要意义。
本文选择牛血清白蛋白(BSA)作为模型蛋白,利用多种光谱手段和分子模拟的方法,研究了牛血清白蛋白与BCBP的相互作用机制,获取了两者相互作用的系列热力学参数、结合位点和作用力类型等,并研究了BCBP对牛血清白蛋白的构象的影响。
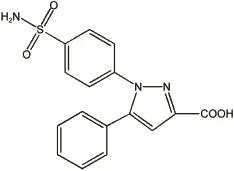
图1 塞来昔布衍生物1-苯磺酰胺-3-羧基-5-苯基吡唑(BCBP)结构Fig.1 Structure of celecoxib derivatives 1-benzenesulfonamides-3-carboxyl-5-phenyl pyrazole(BCBP)
2 实验部分
2.1试剂与仪器
带恒温系统的F-2500荧光光度计(日本日立公司);TU-1901紫外可见分光光度计(北京普析通用仪器有限公司);Jasco J-810圆二色光谱仪(日本Jasco公司)。
牛血清白蛋白等均为Sigma公司产品;NaCl、KCl、Na2HPO4、KH2PO4等均为分析纯;实验用水为三次亚沸水;BSA等溶液均用pH=7.4的磷酸盐缓冲溶液(PBS)配成。
2.2荧光光谱
荧光猝灭光谱:选定激发波长为λex=280 nm,发射狭缝分别为2.5和5.0 nm,测得研究体系的荧光光谱。在模拟人体生理条件下,测定加入不同量的BCBP时BSA的荧光发射光谱,记录温度在298、304、310 K下,波长290-510 nm范围内的荧光发射光谱。
2.3紫外吸收光谱
紫外-可见吸收光谱:测定各BCBP、BSA以及BCBP与BSA物质的量之比为1:1的溶液吸收光谱,波长范围350-200 nm。
2.4圆二色(CD)谱
持续氮气流条件下,室温时波长范围为200-260 nm内样品的CD光谱。比色皿的光路长为0.1 cm,扫描速度200 nm∙min-1。在相同实验条件下,缓冲溶液作为空白,从样品光谱图中扣除,实验的结果由SELCON 3.0软件进行处理。
2.5分子对接模拟
BSA的晶体结构来自于数据库Protein Data Bank(PDB),本实验选择了蛋白编号为3v03的晶体结构数据20,原始晶体结构数据经去水、加氢、加电荷处理。BCBP三维结构由软件Sybyl 8.1构建,并用最小能量法进行优化。
3 结果与讨论
3.1荧光猝灭机制及猝灭常数
任何能够通过相互作用(如:激发态反应,分子重排,能量转移,形成基态复合物及碰撞猝灭等)使荧光物质荧光强度下降的现象,都可称为荧光猝灭作用21。图2给出了pH=7.4时在不同浓度BCBP作用下的BSA的荧光猝灭光谱。可以看出,随着BCBP的不断加入,其浓度增大,BSA的荧光强度逐渐降低,但最大发射波长并没有明显的移动,表明BCBP可以有效猝灭BSA的内源荧光。
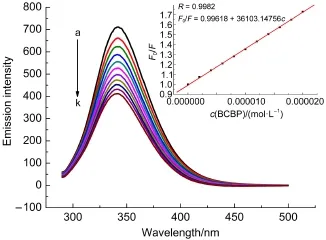
图2 加入不同浓度BCBP之后BSA的荧光光谱Fig.2 Emission spectra of BSAin presence of various concentrations of BCBPc(BSA)=2.0×10-6mol∙L-1;106c(BCBP)/(mol∙L-1),a-k:0.0,2.0,4.0,6.0,8.0,10.0,12.0,14.0,16.0,18.0,20.0,respectively. F0:fluorescenceintensityof 2.0×10-6mol∙L-1BSAsolution;F:fluorescenceintensityof BSAsolutioninthepresenceof variousconcentrationsof BCBP
通常,荧光猝灭过程被认为是猝灭剂和荧光团之间的碰撞过程或者是二者之间形成了复合物,即动态猝灭或者是静态猝灭22,23。不同的猝灭机制,可以根据温度对结合常数和粘度的影响及测定荧光寿命的方法,来加以区分。
为了判断上述体系的猝灭机制,对猝灭过程的荧光实验结果,按照Stern-Volmer方程24进行处理:
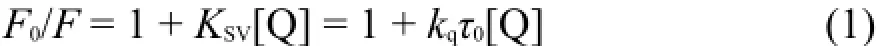
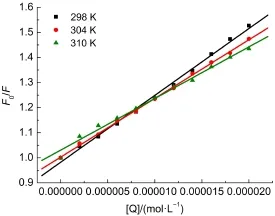
图3 不同温度下药物BCBP与BSA作用的Stern-Volmer关系图Fig.3Stern-Volmer plots for the quenching of BSAby BCBPat different temperatures
式(1)中F0和F分别表示不存在和存在猝灭剂时荧光物质的荧光强度;KSV表示Stern-Volmer猝灭常数;[Q]表示猝灭剂的浓度;kq表示生物大分子的猝灭速率常数;τ0表示不存在猝灭剂时生物大分子的平均荧光寿命。
一般情况下,对于静态猝灭,猝灭常数Ksv随着温度的升高而减小;相反地,对于动态猝灭,猝灭常数Ksv随着温度的升高而增大25,26。
图3为在研究浓度范围内,不同温度下药物BCBP猝灭BSA荧光的Stern-Volmer关系图。从图中可以看出,在pH=7.4时,直线斜率在一定温度范围内随着温度升高呈明显下降趋势。计算各个温度下的猝灭常数列于表1,表中数据显示,温度升高猝灭常数呈规律性减小,表明药物BCBP对BSA的荧光猝灭机理为静态猝灭。
在式(1)中,KSV=kqτ0,生物大分子的荧光平均寿命τ0为10-8s,kq可以通过式(1)计算得到,列在表1中。由上述的分析结果可知:KSV的值随着温度的升高而减小,且kq值远大于生物大分子的最大碰撞猝灭速率常数(2.0×1010L∙mol-1∙s-1),可以判断上述实验中的荧光猝灭是由于形成了复合物的静态猝灭过程。

表1 pH=7.4时不同温度下药物BCBP对BSA作用的Stern-Volmer猝灭常数Table 1Stern-Volmer quenching constants for the interaction of BCBPwith BSAat different temperatures and pH=7.4
为了进一步验证BCBP对BSA的静态猝灭机理,实验设计了BSA与BCBP作用的紫外吸收光谱。由于静态猝灭是由于药物与BSA形成了基态复合物,因而对于BSA的紫外吸收光谱会发生一定的改变。图4为T=298 K,pH=7.4时,2.0× 10-6mol∙L-1的BSA溶液的紫外吸收(曲线a)、药物BCBP与BSA的物质的量之比为1:1的混合物溶液的紫外吸收(曲线b)、药物BCBP与BSA的物质的量之比为1:1的混合物溶液与同等浓度药物的紫外吸收差谱(曲线c)以及药物自身的紫外吸收(曲线d)。从图4中可以看出,在200-300 nm之间,曲线a和c出现了较明显的差异,说明此时有新物质生成,可以推测这是由于药物BCBP与BSA形成了基态复合物所致。此结果进一步证明了该体系的猝灭机理为静态猝灭。
3.2相互作用的热力学参数和主要作用力
对于静态猝灭,其荧光猝灭数据可用修正的Stern-Volmer方程(即Lehrer方程)进行处理27:
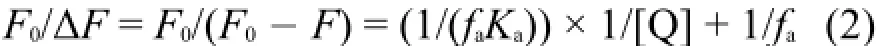
式(2)中fa为蛋白质(荧光基团)可接近猝灭剂的部分(分数);Ka为有效猝灭常数,可用作结合常数;ΔF为加入猝灭剂前后荧光强度的变化。以F0/ΔF 对1/[Q]作图(图5),即可求得蛋白质与药物BCBP的结合常数Ka。分别在298、304及310 K三个温度下,固定BSA的浓度进行荧光滴定,根据方程(2)拟合计算结合常数,列于表2。
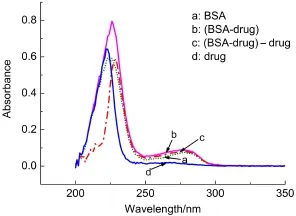
图4 298K时BCBP对BSA紫外吸收光谱的影响Fig.4UV-Vis spectra of interaction of BSAand BCBPat 298 K drug:BCBP

图5 不同温度下药物BCBP与BSA作用的修正Stern-Volmer曲线Fig.5Modified Stern-Volmer plots for the quenching of BSAby BCBPat different temperatures ΔF:F0substractthefluorescenceintensityofBSAsolutioninthe presenceofvariousconcentrationsof BCBP
药物小分子与蛋白质等生物大分子之间的相互作用,通常包括静电作用力、疏水作用力、氢键、范德华力和空间位阻排斥力等28。根据相互作用的热力学参数,可以近似判断活性小分子与生物大分子之间的主要作用力类型。
若在研究的温度范围内,反应的焓变没有明显变化,视为常数,利用vanʹt Hoff方程,可以计算相互作用的焓变ΔH和熵变ΔS,进而得到不同温度下反应的自由能变化ΔG。

表2 不同温度下药物BCBP对BSA作用的结合常数及热力学参数Table 2Binding constants and thermodynamic parameters of BCBP-BSAsystem at different temperatures
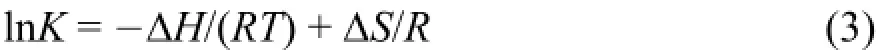
式(3)中K为对应温度下的结合常数,R为摩尔气体常数。以lnK对1/T作图,由斜率与截距分别可以计算出焓变ΔH和熵变ΔS,再由下式计算出反应的自由能变:

根据关系式(3)作图(图6),并计算出BCBP与BSA相互作用的热力学参数,结果列于表2。结果表明此过程为焓驱动的自发过程,但负熵变对此过程较为不利。另外,根据ΔH和ΔS均小于0,我们可以推测,BCBP与BSA之间的作用力主要是氢键和范德华力29。
3.3BCBP对血清白蛋白二级结构的影响
圆二色谱在研究蛋白质结构方面具有独特的优势,不仅可以在接近生理条件下对蛋白质进行低浓度、无损伤的分析,为蛋白质的构象变化提供相关信息,而且还可以定量推算出其分子中α-螺旋、β-折叠以及无规则卷曲的含量等30。因此该方法在蛋白质结构分析中发挥着重要作用,成为解析蛋白质构象变化的最理想、最常用的方法之一。为了考察BCBP对血清白蛋白二级结构的影响,实验设计并测试了不同浓度BCBP与BSA相互作用的CD谱。
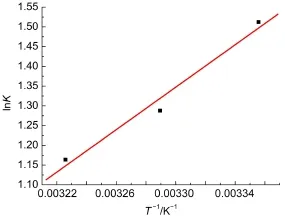
图6 药物BCBP与BSA相互作用的Vanʹt Hoff关系图Fig.6Vanʹt Hoff plot for the interaction of BSAand BCBP
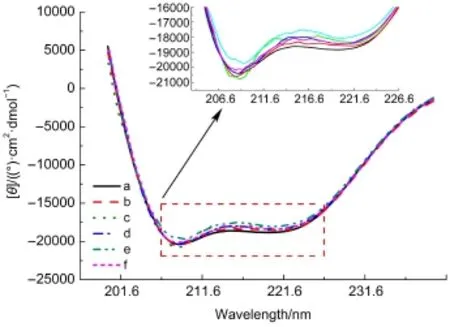
图7 BCBP与BSA作用的圆二色谱Fig.7CD spectra of BCBP-BSAsystemFrom a to f,[BCBP]:[BSA]=0:1,0.5:1,1:1,2:1,5:1,10:1,respectively.color online
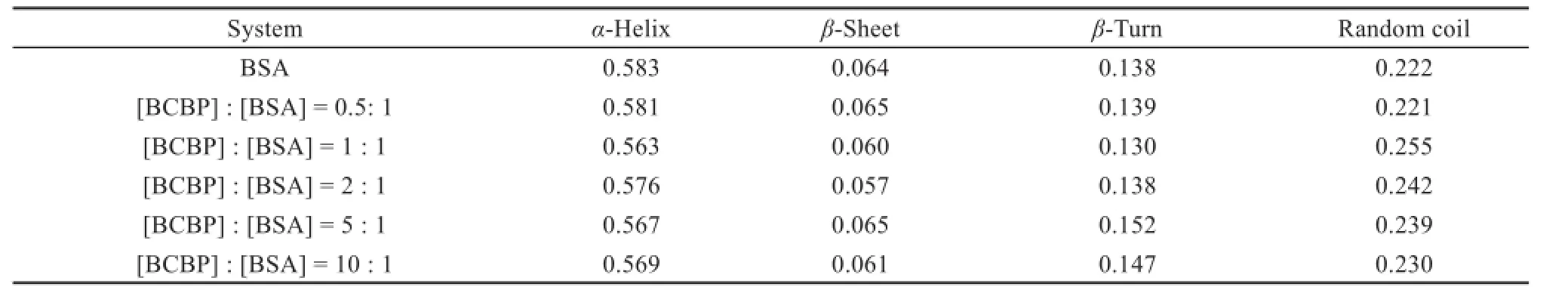
表3 BSA二级结构在不同浓度BCBP作用下的变化Table 3Change of secondary structures of BSAunder the action of different concentrations of BCBP
如图7所示,随着BCBP浓度的增加(图7中a-f),BSA分子典型二级结构的208和222 nm处负的椭圆峰变化不明显。当加入BCBP时,BSA的负椭圆率峰较未加药物前总体趋势是降低的,说明BCBP的加入使BSA的分子结构发生了变化,其α-螺旋含量有所减少,肽链结构有所伸展。利用程序SELCON 3.0,可以方便地计算出蛋白质各二级结构的百分比,如表3所示,在BCBP与BSA的摩尔比为1:1时,体系(在实验浓度范围内)负椭圆率峰最小,α-螺旋度最低。
3.4BCBP与牛血清白蛋白结合距离
荧光共振能量转移理论(FRET)被称作“光谱尺”,广泛应用于研究生物体系或大分子体系与其它分子间相互作用的结合距离31。当蛋白质与药物分子的光谱特性符合能量转移条件时,它们之间就可能发生有效的能量转移,反映在荧光光谱上是蛋白质的荧光被部分猝灭,猝灭程度取决于蛋白质(供体)与猝灭剂(受体)间的距离及能量转移效率32,并有:

式(5)中E是供体-受体间能量转移效率;F和F0分别为存在和不存在能量受体时,供体的荧光发射强度;R为供体与受体之间的真实距离,R0是转移效率为50%时的临界距离,其值可由下式求得:

式(6)中K2为偶极空间取向因子,n为介质的折射指数,ϕ为给体的荧光量子产率,J为给体的荧光发射光谱与受体吸收光谱间的光谱重叠积分,即:

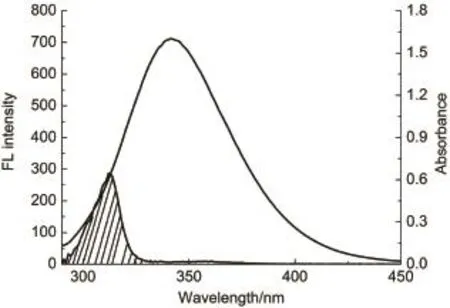
图8 BCBP与BSA的荧光光谱和吸收光谱重叠图Fig.8Overlapping of the fluorescence spectra of BSA with the absorption spectra of BCBP c(BSA)=c(BCBP)=1.0×10-5mol∙L-1

图9 (a)BCBP与BSA对接模型;(b)BCBP周围0.5 nm范围内的氨基酸残基Fig.9(a)Docking model of BCBPand BSA;(b)amino acid residues around BCBPin 0.5 nm
式(7)中,F(λ)为荧光授体在波长λ处的荧光强度,ε(λ)为受体在波长λ处的摩尔吸光系数。图8为BCBP与BSA的物质的量之比为1:1时,BCBP的吸收光谱与BSA的重叠图。将图中的光谱重叠部分按式(7)积分,即可求算出J为8.180×10-17cm3∙L∙mol-1。在上述实验体系中,取向因子K2取供体和受体各向随机分布的平均值2/3,折射指数n取水和有机物的平均值1.36,色氨酸的量子产率为ϕ=0.1533,将这些数值带入式(6)和(7)中,即可求出临界距离R0为1.69 nm,根据据R0的值,由式(5)计算得BSA内色氨酸残基与已结合的BCBP分子间距离R为2.60 nm。
3.5分子模拟
大量的研究工作表明:大多数药物分子与血清白蛋白的作用位置,位于由亚结构域II A和亚结构域III A的疏水腔内,即site I和site II34。BCBP 和BSA分子对接结果的最佳构象见图9(a),可以看出:BCBP和BSA的作用区域更趋于位于site II,即布洛芬位点。在0.5 nm范围内,BCBP周围的氨基酸残基主要有13个,如图9(b)所示:LEU386、ILE387、GLN389、PHE402、LEU406、TYR410、LYS413、ARG444、THR448、LEU452、ARG484、PHE487、SER488。此外,BCBP分子磺胺基上的―NH2与ILE387主链上的O原子形成了氢键(图9 (b)黑色虚线),这有助于BCBP在BSA疏水腔中稳定存在,这也与前面热力学数据分析的结果相符合。进一步计算发现,BCBP与BSA发光残基TRP213的距离(质心间距)为2.43 nm,与前面利用荧光共振能量转移理论计算出的结果R=2.60 nm非常接近,说明了计算结果的准确性。
4 结论
在模拟人生理条件下,采用光谱和分子对接法,研究了BCBP与BSA相互作用的热力学行为。由变温滴定实验可知,Stern-Volmer猝灭常数KSV随着温度的升高而减小,BSA的吸收光谱也在BCBP加入之后发生变化,说明BCBP对BSA的猝灭是生成了复合物的静态猝灭过程。在获取的热力学参数中,焓变和熵变均为负值,说明BCBP与BSA之间相互作用力类型主要是氢键和范德华力。CD光谱的结果表明BCBP与BSA的结合会引起BSA构象发生一定的改变,但不显著。通过荧光共振能量转移理论,计算出了BCBP与BSA色氨酸的距离约为2.60 nm。分子对接结果与实验结果相一致。与塞来昔布相比,BCBP与血清白蛋白的结合自由能更低,结合常数相对较小,表明羧基的引入降低了其与血清白蛋白的结合能力,这可能有利于其在体内的快速结合和释放。同时,BCBP与塞来昔布均结合在血清白蛋白的site II位点,结合的作用力类型也一致,表明C-3位羧基取代对其结合模式影响不大。这些研究结果为了解塞来昔布衍生物在体内的运输过程以及作用机制,提供了一些重要的理论信息,对发现和设计新型低毒副作用COX-2抑制剂,也具有重要的意义。
References
(1)Zheng,H.Pharmaceutical Chemistry,4th ed.;Peopleʹs Medical Publishing House:Beijing,2000.[郑虎.药物化学(第四版).北京:人民卫生出版社,2000.]
(2)Asit,K.C.;Sanjeev,K.G.;Raj,K.;Hashim,F.M.;Pradeep,S. Curr.Med.Chem.2016,23(42),0929.
(3)Guo,L.Z.;Ren,J.M.Pain Clin.J.2008,4(6),445.[郭立志,任进民.实用疼痛学杂志,2008,4(6),445.]
(4)Delyth,C.;Karen,L.G.Drugs 2000,59,957.doi:10.2165/ 00003495-200059040-00017
(5)Meng,M.;Liu,L.C.;Ge,B.;Tang,H.;Wu,Y.Q.;Xu,Y.Chin. J.Evid.-Based Med.2011,11(5),560.[孟敏,刘丽春,葛斌,汤浩,吴玉琼,徐杨.中国循证医学杂志,2011,11(5),560.]
(6)Ricciotti,E.;Grosser,T.;Grant,G.R.;Liu,S.L.;Lawson,J.A.;Assoian,R.;FitzGerald,G.A.Arterioscl.Throm.Vas.2015,35 (Suppl 1),A238.
(7)Abdellatif,K.R.A.;Chowdhury,M.A.;Velázquez,C.A.; Huang,Z.J.;Dong,Y.;Das,D.;Yu,G.;Suresh,M.R.;Knaus,E.E.Bioorg.Med.Chem.Lett.2010,20(15),4544. doi:10.1016/j.bmcl.2010.06.022
(8)Lee,Y.;Jung,E.H.;Kim,H.;Yoon,J.H.;Kim,D.D.;Jung,Y. J.Pharm.Invest.2012,42(3),115.doi:10.1007/s40005-012-0018-3
(9)Abdellatif,K.R.A.;Dong,Y.;Chen,Q.H.;Chowdhury,M.A.;Knaus,E.E.Bioorg.Med.Chem.2007,15(21),6796. doi:10.1016/j.bmc.2007.07.021
(10)Ranatunge,R.R.;Augustyniak,M.;Bandarage,U.K.;Earl,R. A.;Ellis,J.L.;Garvey,D.S.;Janero,D.R.;Letts,L.G.;Martino,A.M.;Murty,M.G.;Richardson,S.K.;Schroeder,J. D.;Shumway,M.J.;Tam,S.W.;Trocha,A.M.;Young,D.V.J. Med.Chem.2004,47(9),2180.doi:10.1021/jm030276s
(11)Abdellatif,K.R.A.;Abdelgawad,M.A.;Elshemy,H.A.H.;Alsayed,S.S.;Kamel,G.Arch.Pharm.Res.2015,38,1932. doi:10.1007/s12272-015-0606-7
(12)He,W.Y.;Yao,X.J.;Hua,Y.J.;Huang,G.L.;Wu,X.L.;Li,X. B.;Han,C.R.;Song,X.P.Acta Phys.-Chim.Sin.2014,30(11),2142.[何文英,姚小军,华英杰,黄国雷,吴秀丽,李小宝,韩长日,宋小平.物理化学学报,2014,30(11),2142.]doi:10.3866/ PKU.WHXB201409253
(13)Bekale,L.;Agudelo,D.;Tajmir-Riahi,H.A.Colloid Surface B 2015,130,141.doi:10.1016/j.colsurfb.2015.03.045
(14)Zhang,J.;Wang,X.J.;Yan,Y.J.;Xiang,W.S.J.Agri.Food Chem.2011,59(13),7506.doi:10.1021/jf2005194
(15)Zhivkova,Z.D.Curr.Pharm.Design 2015,21(14),1817.doi: 10.2174/1381612821666150302113710
(16)Banker,M.J.;Clark,T.H.Curr.Drug Metab.2008,9,854.doi: 10.2174/138920008786485065
(17)Masomeh,M.;Sirous,G.;Reza,K.J.Photochem.Photobiol.B 2009,97,161.doi:10.1016/j.jphotobiol.2009.09.005
(18)Neelam,S.;Sonu,B.Pharm.Res.2006,54,77.doi:10.1016/j. phrs.2006.02.008
(19)Pereira-Leite,C.;Nunes,C.;Lima,J.L.F.C.;Salette,R.;Marlene,L.J.Phys.Chem.B 2012,116(46),13608. doi:10.1021/jp304037v
(20)Majorek,K.A.;Porebski,P.J.;Dayal,A.;Zimmerman,M.D.;Jablonska,K.;Stewart,A.J.;Chruszcz,M.;Minor,W.Mol. Immunol.2012,52,174.doi:10.1016/j.molimm.2012.05.011
(21)Hemmateenejad,B.;Yousefinejad,S.J.Mol.Struct.2013,1037,317.doi:10.1016/j.molstruc.2013.01.009
(22)Li,D.W.;He,H.;Lin,B.B.;Xu,Z.Q.;Jiang,F.L.;Liu,Y. RSC Adv.2014,4(8),3913.doi:10.1039/C3RA46172F
(23)Peng,L.P.;Nagarajan,S.;Rasheed,S.;Zhou,C.H.Med.Chem. Comm.2015,6(1),222.doi:10.1039/C4MD00281D
(24)Zaidi,N.;Ahmad,E.;Rehan,M.;Rabbani,G.;Ajmal,M.R.;Zaidi,Y.;Subbarao,N.;Khan,R.H.J.Phys.Chem.B 2013,117,2595.doi:10.1021/jp3069877
(25)Ma,X.;Yan,J.;Wang,Q.;Wu,D.;Li,H.Int.J.Bio.Macromol. 2015,77,280.doi:10.1016/j.ijbiomac.2015.03.052
(26)Huang,S.;Qiu,H.;Lu,S.;Zhu,F.;Xiao,Q.J.Hazard.Mater. 2015,285,18.doi:10.1016/j.jhazmat.2014.11.019
(27)Chaturvedi,S.K.;Ahmad,E.;Khan,J.M.;Alam,P.;Ishtikhar,M.;Khan,R.H.Mol.Bio.Syst.2015,11(1),307.doi:10.1039/ c4mb00548a
(28)Banerjee,M.;Chakrabarti,A.;Basu,S.Dyes Pigments 2013,97 (3),446.doi:10.1016/j.dyepig.2013.01.005
(29)Ross,P.D.;Subramanian,S.Biochemistry 1981,20(11),3096. doi:10.1021/bi00514a017
(30)Louis-Jeune,C.;Andrade-Navarro,M.A.;Perez-Iratxeta,C. Proteins 2012,80(2),374.doi:10.1002/prot.v80.2
(31)Mohammadi,F.;Moeeni,M.Mater.Sci.Engin.C 2015,50,358.doi:10.1016/j.msec.2015.02.007
(32)Stauffer S.R.;Hartwig J.F.J.Am.Chem.Soc.2003,125,6977. doi:10.1021/ja034161p
(33)Cyril,L.;Earl,J.K.;Sperry,W.M.BiochemistsʹHandbook;E. &F.N.Spon:London,1961.
(34)Tian,F.F.;Jiang,F.L.;Han,X.L.;Xiang,C.;Ge,Y.S.;Li,J. H.;Zhang,Y.;Li,R.;Ding,X.L.;Liu,Y.J.Phys.Chem.B 2010,114,14842.doi:10.1021/jp105766n
Thermodynamics of the lnteraction of BCBP with Bovine Serum Albumin
GUO Qing-Lian1,*HE Huan2PAN Ling-Li3LIU Yi2
(1Department of Clinical Laboratory,Zhongnan Hospital,Wuhan University,Wuhan 430071,P.R.China;2College of Chemistry and Molecular Sciences,Wuhan University,Wuhan 430072,P.R.China;3Department of Emergency,Huangshi Central Hospital (Affiliated Hospital of Hubei Polytechnic University),Edong Healthcare Group,Huangshi 435002,Hubei Province,P.R.China)
Celecoxib derivatives are widely used,non-steroidal,anti-inflammatory drugs for the treatment of acute or chronic inflammation.Under simulated physiological conditions,we used fluorescence and ultraviolet absorption spectroscopy,circular dichroism,and methods of molecular simulation to study the thermodynamics of the interaction between the celecoxib derivative 1-benzenesulfonamides-3-carboxyl-5-phenyl pyrazole (BCBP)and bovine serum albumin(BSA).The fluorescence quenching of BSAby BCBP was a static process,which was confirmed by the UV-Vis absorption spectra.The calculated enthalpy(ΔH)and entropy(ΔS)changes implied that hydrogen bonds and van der Waals forces played a predominant role in the binding process.The circular dichroism demonstrated that the secondary structure of BSA changed after its interaction with BCBP,causing the α-helix content to decrease,accompanied by an increase in an unordered structure.Molecular docking results confirmed the experimental results.
Celecoxib derivative;Bovine serum albumin;Interaction;Thermodynamics parameter
January 14,2016;Revised:March 8,2016;Published on Web:March 9,2016.
O642
[Article]10.3866/PKU.WHXB201603093www.whxb.pku.edu.cn
*Corresponding author.Email:yunjiang716@hotmail.com.
The project was supported by the Key Project of Health and Family Planning Commission of Hubei Province,China(WJ2015MB097)and Wuhan Yellow Crane Talents Program for Science and Technology,China(2014[10]).
湖北省卫生计生委重点项目(WJ2015MB097)和武汉黄鹤英才(科技)计划(2014[10])资助
©Editorial office ofActa Physico-Chimica Sinica
